一种乳腺癌多维度免疫压力CRISPR文库筛选方法
文献发布时间:2023-06-19 18:30:43
技术领域
本发明涉及肿瘤治疗领域,具体涉及一种乳腺癌多维度免疫压力CRISPR文库筛选方法。
背景技术
肿瘤治疗中最为关注的是肿瘤免疫治疗,其中最成功的是免疫检查点阻断治疗。然而,免疫检查点的阻断不能在大多数患者中实现持续的临床反应,肿瘤细胞可以表达更多其他的基因来调节它们对肿瘤免疫的逃避或抵抗,因此需要探索肿瘤免疫过程中其他的免疫治疗靶点以及治疗策略。
三阴性乳腺癌(TNBC)因其缺乏有效的治疗靶点,是当今乳腺癌治疗的难点之一。免疫治疗作为TNBC的新型疗法已展示出良好的应用前景,但同时其也存在着靶点单一、疗效局限等挑战。虽然免疫治疗药物在三阴性乳腺癌领域获批,但目前仍有许多亟待解决的临床问题。例如PD-L1的表达虽然已作为预测免疫检查点抑制剂疗效的生物标志物,但在常规临床试验中仍存在担忧:PD-L1是一个动态标记物,表达可能随时间而变化;一些PD-L1检测阳性的患者可能对治疗无反应,而其他检测阴性的患者可能仍有反应。此外,靶向PD-1/PD-L1的单药治疗在乳腺癌中疗效欠佳,可能提示乳腺癌中存在其他关键分子介导免疫逃逸。
因此,临床上需要发现三阴性乳腺癌特异性的新型肿瘤免疫靶点,开发针对性的靶向疗策略,才有希望在三阴性乳腺癌的免疫治疗上取得更大突破。通过构建不同的CRISPR-Cas9文库高通量文库筛选平台,可以在系统和全面地筛选肿瘤免疫相关的基因,充分挖掘肿瘤治疗的潜在靶点。
发明内容
为克服上述问题,本发明利用多维度免疫压力小鼠模型开展两轮CRISPR文库筛选,主要利用正常(Balb/c,免疫系统完整)以及各类免疫缺陷小鼠(NPG,T细胞、B细胞、NK细胞缺失;CB-17Scid,T细胞、B细胞缺失;Balb/c-nude小鼠,T细胞缺失)不用的免疫微环境对于移植性肿瘤(导入MiTCL文库的4T1细胞)的不同免疫压力,筛选发现能够调控肿瘤免疫逃逸的关键分子。
具体地,本发明第一方面提供了sgRNA文库,所述sgRNA文库为MiTCL-L和/或MiTCL-S;所述MiTCL-L包含靶向选自表1中2796个基因的sgRNA,所述MiTCL-S包含靶向选自表2中273个基因的sgRNA。
在某些实施方式中,所述MiTCL-L的靶标序列选自表1。
在某些实施方式中,所述MiTCL-S的靶标序列选自选自表2。
本发明第二方面提供了本发明第一方面所述的sgRNA文库在筛选肿瘤免疫相关的基因中的应用。
本发明第三方面提供了本发明第一方面所述的sgRNA文库在制备筛选肿瘤免疫相关的基因的试剂盒中的应用。
本发明第四方面提供了一种乳腺癌多维度免疫压力CRISPR文库筛选方法,所述方法包括如下步骤:a)MiTCL-L质粒文库的构建;b)利用MiTCL-L文库进行首轮基于不同免疫压力小鼠模型的CRISPR筛选;c)利用生物信息学分析MiTCL-L免疫文库筛选结果,鉴定出三阴性乳腺癌免疫逃逸和免疫监视相关的候选基因;d)根据MiTCL-L文库筛选结果,进行次轮筛选MiTCL-S质粒文库的制备;e)基于MiTCL-S文库的次轮免疫筛选;f)利用生物信息学分析MiTCL-S免疫文库筛选结果,鉴定出免疫逃逸相关基因。
在某些实施方式中,所述步骤a)MiTCL-L质粒文库的构建使用本发明第一方面所述的MiTCL-L sgRNA文库。
在某些实施方式中,所述步骤a)中sgRNA与lentiGuide-Puro质粒连接、扩增构成MiTCL-L质粒文库。
在某些实施方式中,所述步骤b)中,在4T1细胞中用慢病毒导入Cas9基因,筛选阳性细胞后再导入慢病毒包装的MiTCL-L文库,再筛选得到阳性的混合文库细胞;将阳性的混合文库细胞分成9份:3份细胞为第0天的基准细胞,立即抽取基因组DNA;3份细胞接种免疫完善的Balb/c小鼠,3份细胞接种免疫重度缺陷的NPG小鼠。
在某些实施方式中,所述步骤c)中,利用基准细胞的DNA和移植瘤的DNA,采用巢式PCR的方案进行扩增、纯化和测序,采用MAGeCK算法,计算和比较了注射前的基线细胞和收集的肿瘤组织细胞的sgRNA的分布,计算每个基因在肿瘤组织细胞相较于基线细胞细胞的β值;经MAGeCK算法中的最大似然值估计法(maximum likelihood estimation,MLE)模块计算得到每个基因的β值,并计算每个基因在Balb/c对比NPG筛选中的δ值;根据β值和δ值鉴定出一批三阴性乳腺癌免疫逃逸和免疫监视相关的候选基因。
在某些实施方式中,所述步骤d)中,MiTCL-S质粒文库的构建使用本发明第一方面所述的MiTCL-S sgRNA文库。
在某些实施方式中,所述步骤e)中,选用四种具有不同免疫缺陷的小鼠,注射感染MiTCL-S文库的4T1-Cas9细胞构建乳腺癌移植瘤模型,观察肿瘤生长并提取肿瘤组织基因组DNA进行二代测序。
在某些实施方式中,所述步骤f)包括对二代测序结果进行MAGeCK算法分析,计算出(1)T、B、NK细胞筛选,(2)T、B细胞筛选,(3)T细胞筛选,(4)B细胞筛选,(5)B、NK细胞筛选和(6)NK细胞筛选共6种不同免疫压力筛选下的MiTCL-S文库中各基因的δ值,并利用FUSCC中TNBC队列的转录组数据对MiTCL-S文库基因在TNBC肿瘤组织中基因的表达情况进行分析,综合δ值和转录组数据筛选出TNBC中的免疫逃逸相关基因。
本发明的有益效果在于:
本项目构建了两套CRISPR文库(MiTCL-L,2796基因;MiTCL-S,273基因),采用多种不同免疫缺陷小鼠进行高通量筛选,能够发现TNBC微环境中发挥免疫逃逸的关键基因。该项方法筛选发现的候选基因中包括了已经证实的免疫异质性明星基因LAG3和CD38,证实了筛选平台的可靠性。
本项目CRISPR文库筛选手段揭示了调控肿瘤免疫逃逸的关键分子,为发现新型免疫治疗靶标奠定了重要的理论和实验基础,有利于三阴性乳腺癌免疫治疗上的突破。
附图说明
通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更显著:
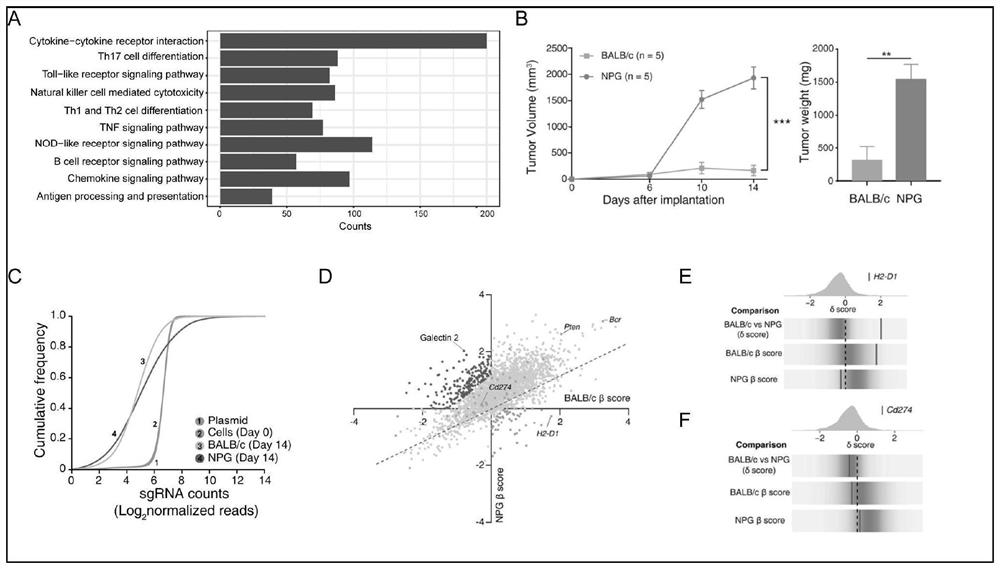
图1显示基于免疫压力模型的CRISPR文库初轮筛选结果。(A)靶向2796个小鼠免疫相关基因的MiTCL-L文库的基因功能分布;(B)导入MiTCL-L文库的4T1-Cas9细胞的小鼠肿瘤生长曲线以及肿瘤重量;(C)不同样本中MiTCL-L文库sgRNA的累计分布曲线;(D)文库基因β值分布散点图;(E和F)H2-D1(E)和Cd274(F)不同免疫压力筛选下的β值。
图2显示基于免疫压力模型的CRISPR次轮筛选结果(A和B)导入MiTCL-S文库的4T1-Cas9细胞的四种小鼠移植瘤生长曲线;(C)不同样本中MiTCL-S文库的sgRNA的累计分布曲线;(D)不同样本件的Spearman相关性显示组间异质性良好;(E)不同样本中MiTCL-S文库的sgRNA的分布箱式图。
图3多维度免疫压力小鼠模型下CRISPR文库筛选的比对表。
图4显示基于免疫压力模型的CRISPR次轮筛选结果(A-F)6种不同免疫筛选压力下MiTCL-S文库富集比对的δ值与TNBC转录组表达差异散点图;(G)6种免疫筛选压力共性差异变化基因的δ值,深色代表δ>0,浅色代表δ<0。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例的附图,对本发明实施例的技术方案进行清楚、完整地描述。显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于所描述的本发明的实施例,本领域普通技术人员在无需创造性劳动的前提下所获得的所有其它实施例,都属于本发明保护的范围。
除非另作定义,此处使用的技术术语或者科学术语应当为本发明所属领域内具有一般技能的人士所理解的通常意义。
以下结合具体实施例对本发明的一种乳腺癌多维度免疫压力CRISPR文库筛选方法进行阐述。
实施例1基于不同免疫压力小鼠模型,建立针对小鼠免疫基因的CRISPR文库筛选平台(MiTCL-L)
1.1构建靶向2796个小鼠免疫相关的MiTCL-L文库
从小鼠基因组信息库(Mouse Genome Informatics,MGI)中挑选与人类疾病相关且和免疫系统有关联的基因,并从中筛选到2796个基因,构成Mouse immune TargetingCRISPR Library-Large(MiTCL-L)靶向小鼠免疫基因的CRISPR文库,文库的基因主要富集于细胞因子及受体通路、Toll-样受体通路、NK细胞、T细胞、B细胞以及抗原呈递通路等(图1A)。随后参考Addgene(http://www.addgene.org/)上John&David的小鼠CRISPR敲除文库(Pooled Library#73632,#73633,#73633-LV)为本研究选定的2796个基因每个基因匹配4条sgRNA,共计11184条sgRNA构成MiTCL-L免疫文库(表1),另外设置未靶向任何基因的阴性对照sgRNA。通过定制含有sgRNA特异性20bp靶向序列的DNA寡核苷酸混合文库,将目的序列通过Gibson Ligation方式将sgRNA序列插入到lentiGuide-Puro质粒后进行电转扩增(BioRad公司GenePulser Xcell电转仪),以200
1.2利用MiTCL-L文库进行首轮基于不同免疫压力小鼠模型的CRISPR筛选
首轮筛选采用的小鼠乳腺肿瘤4T1细胞,4T1细胞来源于BalB-c小鼠的乳腺肿瘤,因此具备在BalB-c小鼠自发性成瘤的特征。本项目采用的小鼠为(1)BalB-c小鼠:具备完整的免疫系统,具有T细胞、B细胞、NK细胞以及其他免疫细胞(例如单核细胞、中性粒细胞等);(2)NPG小鼠(NOD-PrkdcscidII2rgnull):该小鼠的建立通过小鼠胚胎干细胞上的基因同源重组技术,建立C57B/6小鼠来源的ES细胞的Il2rg(Interleukin-2receptor gamma chain)基因敲除细胞系,并获得Il2rg基因敲除小鼠。其重要特征为小鼠的T细胞缺失、B缺失、NK细胞的活性缺失,对于外援性细胞或者组织几乎没有排斥反应。
首先利用293T细胞以及包装质粒PAX2(Addgene,35002)、PMD2.G(Addgene,12259)进行慢病毒包装,收集病毒后进行滴度测定。在4T1细胞中分别用慢病毒以低MOI分别导入Cas9基因,以blasticidin筛选到阳性细胞,然后以离心感染法(MOI=0.5)导入MiTCL-L文库病毒并以puromicin筛选5天得到阳性的混合文库基线细胞。将阳性的混合克隆细胞分成9份:3份细胞为第0天的基准细胞(baseline cells),立即抽取基因组DNA;3份细胞接种选用免疫完善的Balb/c小鼠,3份细胞接种免疫重度缺陷的NPG小鼠,肿瘤的生长时间约为4周。借助小鼠的体内环境,进行体内筛选。
结果显示,免疫完善的Balb/c小鼠的肿瘤生长速度明显慢于免疫重度缺陷NPG小鼠(图1B),并且实验结束对肿瘤组织进行称重,同样发现Balb/c小鼠的肿瘤肿瘤小于NPG小鼠(图1B)。以上结果提示,完整的免疫系统对肿瘤生长有抑制作用,当免疫系统缺陷时,肿瘤生长迅速。
1.3利用生物信息学分析MiTCL-L免疫文库筛选结果
利用基准细胞的DNA和移植瘤的DNA,采用巢式PCR(Nesting PCR)的方案进行扩增、纯化和测序,针对每个sgRNA的测序覆盖深度为500×。针对CRISPR-Cas9基因文库筛选的数据,首先对文库筛选的质量进行分析。illumina平台生成的原始FASTQ文件经过Geneious 7.0(Biomatters Inc,Auckland)分析后可以得到每个样本所对应的每个sgRNA的reads数。利用累积分布函数对于基准细胞和移植瘤样本的sgRNA的分布进行了分析,发现基准细胞中sgRNA均一性良好,移植瘤样本中出现了sgRNA的差异性丢失/扩增(图1C),说明有些sgRNA出现丢失,而有些出现明显富集。为了进一步分析筛选哪些sgRNA对细胞的影响,采用MAGeCK算法,计算和比较了注射前的基线细胞和收集的肿瘤组织细胞的sgRNA的分布,计算每个基因在肿瘤组织细胞相较于基线细胞细胞的β值。经MAGeCK算法中的最大似然值估计法(maximumlikelihood estimation,MLE)模块计算得到每个基因的β值,并计算每个基因在Balb/c对比NPG筛选中的δ值。β>0代表筛选后该基因对应的sgRNA分布增加,β<0则代表减少,β绝对值越大意味着在该种免疫压力筛选下该基因越重要(图1D)。基于Balb/c小鼠和NPG小鼠的β的比较,第一象限中的基因为在免疫系统健全(Balb/c小鼠)和严重免疫缺陷(NPG小鼠)的微环境中都促进肿瘤生长,在第三象限中的基因则参与了肿瘤生长抑制(图1D)。位于第二、四象限的基因则通过免疫环境对肿瘤生长产生影响,其中位于第四象限的基因参与了免疫逃逸;位于第二象限的基因参与了免疫监视(图1D)。进一步比较了在基因在Balb/c小鼠和NPG小鼠中的β值,计算得到δ值(δ=β免疫缺陷低-β免疫缺陷高),用δ值来展示基因对于肿瘤免疫逃逸和免疫监视的影响。δ>0代表筛选后该基因参与免疫监视,如H2-D1(MHC-Ⅰ)(图1E);δ<0,代表筛选后该基因参与免疫逃逸,Cd274(PD-L1),能够与PD-1结合抑制T细胞的激活(图1F)。
通过首轮基于不同免疫压力小鼠模型的MiTCL-L文库筛选,可以鉴定出一批三阴性乳腺癌免疫逃逸和免疫监视相关的候选基因,之后围绕该免疫基因集开展次轮MiTCL-S文库筛选。
实施例2建立针对靶向重点免疫基因的MiTCL-S文库
2.1次轮筛选MiTCL-S文库的制备
根据MiTCL-L文库筛选结果,经MAGeCK算法中的最大似然值估计法(maximumlikelihood estimation,MLE)模块计算得到每个基因的β值,并计算每个基因在Balb/c对比NPG筛选中的δ值。根据δ值挑选δ>0和δ<0的前8%基因,以及中间部分基因作为阳性对照,共计273个基因,作为为Mouse immune Targeting CRISPR Library-Small(MiTCL-S)文库的靶向基因。随后为每个靶点基因匹配10条sgRNA,共计2730条sgRNA,组成MiTCL-S文库(表2)。同时设置未靶向任何基因的阴性对照sgRNA。文库的构建方法同MiTCL-L类似。
2.2基于MiTCL-S文库的次轮免疫筛选
在次轮研究中选用四种具有不同免疫缺陷的小鼠,按免疫力从低到高排序为:NOD-PrkdcscidII2rgnull(T细胞、B细胞、NK细胞缺失)<CB-17Scid(T细胞、B细胞缺失)<Balb/c-nude(T细胞缺失)<Balb/c(免疫系统完整),利用这些小鼠具有不同的免疫特征进行筛选,从而发现关键肿瘤免疫调控因子。与第一轮筛选方法一致,向乳房垫原位注射感染MiTCL-S文库的4T1-Cas9细胞构建乳腺癌移植瘤模型,观察肿瘤生长(图2A和图2B)并提取肿瘤组织基因组DNA进行二代测序。
2.3利用生物信息学分析MiTCL-S免疫文库筛选结果
为了探究MiTCL-S文库在不同免疫压力筛选下的变化,比较不同样本(质粒、基准细胞、移植瘤组织)中检测到的sgRNA的数量变化。利用累积分布函数对于基准细胞和移植瘤样本的sgRNA的分布进行了分析,发现移植瘤样本中出现了sgRNA的差异性丢失(图2C)。利用Spearman相关性分析发现基准细胞(baseline cells)的重复性良好,移植瘤样本(Xenograft tumors)之间的差异性较大(图2D);利用箱式图也可以发现部分sgRNA在成瘤的过程中出现了丢失,提示这些sgRNA靶向的基因可能是在三阴性乳腺癌演进过程中关键的基因(图2E)。
进一步对二代测序结果进行MAGeCK算法分析,将四组小鼠进行两两比较(免疫力较强的定为干预组,免疫力较弱的定为对照组),利用四种不同小鼠之间的比对,可进行不同的免疫压力筛选(图3):(1)T、B、NK细胞筛选;(2)T、B细胞筛选;(3)T细胞筛选;(4)B细胞筛选;(5)B、NK细胞筛选;(6)NK细胞筛选。MAGeCK算法计算出6种不同免疫压力筛选下的MiTCL-S文库中各基因的δ值,并利用FUSCC中TNBC队列的转录组数据对MiTCL-S文库基因在TNBC肿瘤组织中基因的表达情况进行分析(图4A-F)。基因δ<0代表基因调控肿瘤细胞参与了免疫逃逸,结合了三阴性乳腺癌转录组数据综合分析。根据δ值和FUSCC转录组分析结果发现,在6种免疫筛选压力下,有不少δ<0的基因在肿瘤组织表达较癌旁组织增多(癌与癌旁相比,log2 FoldChange>0.5)(图4A-F中深色点表示)。通过6种免疫筛选压力差异基因取交集分析,发现共有11个基因在六种不同的免疫筛选压力下δ<0,且在肿瘤组织普遍表达较高(图4G),提示这些基因可能与TNBC中的免疫逃逸相关。
11个筛选出候选基因中,淋巴细胞活化基因-3(LAG3)对于免疫的负向调控作用已经被广泛的报道。LAG3是蛋白质Ig超家族的成员,属于1型跨膜蛋白,在活化的人NK细胞、T细胞、活化的B细胞和浆细胞样树突细胞上表达。LAG3与MHC II类结合,亲和力比与CD4高100倍,LAG3在T细胞增殖和活化中起负调节作用。靶向LAG3成为肿瘤治疗的一个新型的策略,靶向LAG3能够激活效应T细胞和抑制Treg抑制活性,所以这种具有双重作用机制的LAG3成为检查点抑制的重要靶点。目前,LAG3的抑制剂联合紫杉醇已经在转移性乳腺癌的一线治疗临床试验中证实有效。另外一个被筛选出的著名基因为CD38(Cluster ofDifferentiation 38),CD38是位于细胞表面的重要的代谢酶,CD38的酶活性表现为催化NAD+转化为ADPR、cADPR、NAM等代谢物,它的产物在免疫调节的过程中发挥了重要的功能。CD38在非实体瘤,尤其是多发性骨髓瘤(multiple myeloma,MM)中表达量很高,这使得CD38成为了多发性骨髓瘤、CLL等非实体瘤靶向治疗的良好靶点之一。强生公司研发了CD38介导性、溶细胞性抗体药物,具有广谱杀伤活性,可靶向结合多发性骨髓瘤及多种实体瘤细胞表面高度表达的跨膜胞外酶CD38分子,诱导肿瘤细胞的快速死亡。
以上发现提示基于多维度免疫压力小鼠模型的CRIPSR筛选能够有效筛选出与三阴性乳腺癌免疫调控密切相关的关键调控因子。
以上显示和描述了本发明的基本原理和主要特征和本发明的优点,对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。不应将权利要求中的任何附图标记视为限制所涉及的权利要求。
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这中叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
