一种可抑制冠状病毒3CL蛋白酶活性的化合物、制备方法及其应用
文献发布时间:2024-04-18 20:01:55
技术领域
本发明涉及一种3CL蛋白酶抑制剂,具体涉及一种抑制冠状病毒3CL蛋白酶活性的化合物、制备方法及其应用。
背景技术
冠状病毒以新冠病毒SARS-CoV-2为例,其入侵宿主细胞原理是作为具有包膜的单正链RNA病毒,其基因组内包含大约三万个核苷酸。在进入宿主细胞后,它会分解释放出病毒RNA,病毒RNA借由宿主细胞中的核糖体翻译成为两条多聚蛋白pp1a和pp1ab,这两条多聚蛋白就像是整盒包装的拼图,还不能发挥作用,需要在3CL蛋白酶和PL蛋白酶作用下拆装重组,以形成具有功能的结构蛋白。在这个过程中,3CL蛋白酶负责多聚蛋白11个位点的切割,以便产生对病毒生存、繁殖非常重要的结构蛋白,因此又被称为主蛋白酶(M pro)。因此,可以通过抑制3CL蛋白酶的活性,从而干扰病毒复制过程,起到抗病毒的作用。并且,由于人体中原本缺乏3CL蛋白酶的同源物,因此,在抑制3CL蛋白酶的活性过程中,药物副作用能够被更大程度地降低。因此,3CL蛋白酶的抑制剂被大家公认为最有潜力的抗冠状病毒药物。CN112574104A公开了一种用于SARS-CoV-2靶点Mpro抑制剂的乙酰胺类化合物,但是所述化合物的IC
发明内容
有鉴于此,本发明的目的在于提供一种新型的可抑制冠状病毒3CL蛋白酶活性的化合物、制备方法及其应用,对冠状病毒的3CL蛋白水解酶具有强抑制活性,且对宿主细胞的毒性小。
本发明的可抑制冠状病毒3CL蛋白酶活性的化合物,所述化合物为1,3-氧硫杂环戊基嘧啶酮类磷酸酯衍生物;
进一步,所述化合物的结构式为:
进一步,所述所述化合物的结构式为:
进一步,所述所述化合物的结构式为:
本发明还可抑制冠状病毒3CL蛋白酶活性的化合物的制备方法,包括以下步骤:将拉米呋啶与磷酸衍生物酯化反应制得。
本发明还公开一种可抑制冠状病毒3CL蛋白酶活性的化合物在制备预防和/或治疗冠状病毒所致疾病的药物中的应用。
本发明还公开了可抑制冠状病毒3CL蛋白酶活性的化合物在制备抑制新型冠状病毒2019-nCoV 3CL蛋白水解酶的药物中的应用。
本发明的有益效果是:本发明公开的可抑制冠状病毒3CL蛋白酶活性的化合物、制备方法及其应用,经体外酶抑制活性实验研究表明,该类化合物对冠状病毒的3CL蛋白水解酶有强抑制活性;经体外抗病毒活性实验及细胞水平毒性研究表明,部分化合物对冠状病毒有较强的生长抑制活性,且对宿主细胞的毒性小。本发明的可抑制冠状病毒3CL蛋白酶活性的化合物的制备方法简单,原料易得,收率较高。
附图说明
下面结合附图和实施例对本发明作进一步描述:
图1为可抑制冠状病毒3CL蛋白酶活性的化合物(Ⅰ)的体外抗新型冠状病毒活性测试结果;
图2为可抑制冠状病毒3CL蛋白酶活性的化合物(Ⅱ)的体外抗新型冠状病毒活性测试结果;
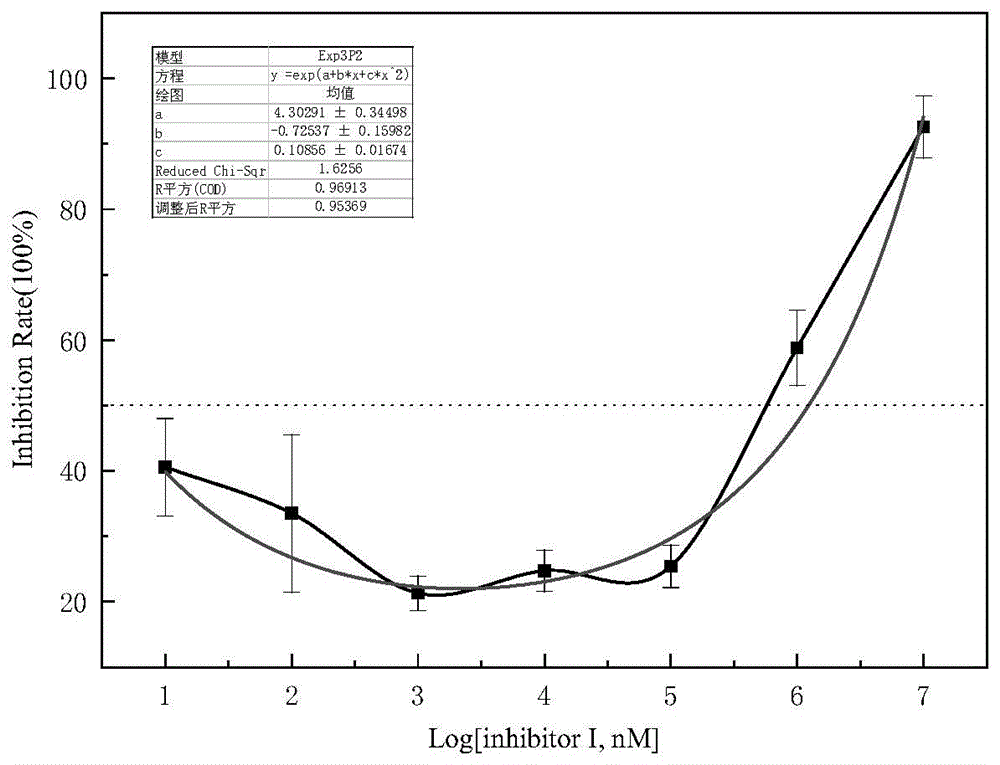
图3为双硫仑抑制曲线;
图4为氯喹抑制曲线。
具体实施方式
实施例一
本实施例的可抑制冠状病毒3CL蛋白酶活性的化合物结构式为:
其制备方法为:
S1,将拉米呋啶溶解在二氯甲烷和N-甲基咪唑的溶液中,向其中滴加氯磷酸二乙酯(1mmol),反应温度保持在-10℃。混合搅拌经TLC检测确定拉米呋啶完全消耗。然后用饱和的碳酸氢钠溶液中止反应,分离混合物,二氯甲烷萃取水相层用。合并有机相经盐水洗涤,经过硫酸钠干燥、过滤和真空浓缩。粗产物经过硅胶柱层析纯化得到粗产物。
S2,将所得粗产物(1.1mmol)溶解在二氯甲烷中,加入四甲基溴化硅,在25℃下搅拌过夜。反应混合物蒸发至干燥,残渣重新溶解于甲醇中,加入水。随后,溶剂被蒸发至干燥,粗产物溶解于水中,并在0℃下用氢氧化铵调节pH至10,碱性溶液经过柱层析得到最终产物。
1
其合成路线如下:
实施例二
本实施例的可抑制冠状病毒3CL蛋白酶活性的化合物结构式为:
其制备方法为:
S1,将苯二氯磷酸酯(10mmol)溶解在二氯甲烷中,并在冰浴中氮气保护下搅拌。一次性加入-(S)2-乙基丁基-丙氨酸酯盐酸盐(10mmol),滴加三乙胺,在0℃下搅拌1小时,然后加入对硝基酚(10mmol)和三乙胺。随后在室温下搅拌反应混合物16小时,用二氯甲烷稀释并用饱和碳酸氢钠溶液洗涤,有机相经过无水硫酸钠干燥,减压浓缩,通过柱层析纯化得到中间体。
S2,将拉米呋啶(0.051mmol)溶解在DMF(1mL)中,并在氮气氛下搅拌。将对硝基酚磷酰胺(0.077mmol)溶解在DMF(0.5mL),滴加叔丁基氯化镁(THF)。搅拌2小时,用乙酸乙酯稀释并用饱和的碳酸氢钠溶液洗涤,用饱和的氯化钠溶液洗涤并用无水硫酸钠干燥有机物,减压浓缩。通过柱层析纯化得到产物。
1
其合成路线为:
实施例三
本实施例的可抑制冠状病毒3CL蛋白酶活性的化合物结构式为:
其制备方法为:
S1,将苯二氯磷酸酯(10mmol)溶解在二氯甲烷中,并在冰浴中氮气保护下搅拌。一次性加入-(R)2-乙基丁基-丙氨酸酯盐酸盐(10mmol),滴加三乙胺,在0℃下搅拌1小时,然后加入对硝基酚(10mmol)和三乙胺。随后在室温下搅拌反应混合物16小时,用二氯甲烷稀释并用饱和碳酸氢钠溶液洗涤,有机相经过无水硫酸钠干燥,减压浓缩,通过柱层析纯化得到中间体。
S2,将拉米呋啶(0.051mmol)溶解在DMF(1mL)中,并在氮气氛下搅拌。将对硝基酚磷酰胺(0.077mmol)溶解在DMF(0.5mL),滴加叔丁基氯化镁(THF)。搅拌2小时,用乙酸乙酯稀释并用饱和的碳酸氢钠溶液洗涤,用饱和的氯化钠溶液洗涤并用无水硫酸钠干燥有机物,减压浓缩。通过柱层析纯化得到产物。
实施例四
将上述实施例1和2的两种可抑制冠状病毒3CL蛋白酶活性的化合物用于2019-nCoV新型冠状病毒的3CL蛋白水解酶活性抑制测定:
采用现有的测定方法(如申请号202111555106.4)进行化合物的酶抑制活性测定:以荧光标记的多肽为底物通过酶动力学方法测定3CL酶的催化活性及初始速度。在化合物的酶抑制活性测定中,孵育体系含有3CL蛋白酶(50nM),荧光标记多肽(160uM)浓度。根据加入抑制剂后酶催化底物水解的初始速度变化率,计算不同浓度下待测物的酶抑制率。所有实验均重复3次,并通过Origin软件计算待测物抑制酶的IC
在酶抑制活性实验中,测定结果如表1所示:
实施例五
将上述实施例1和2的化合物用于对新型冠状病毒3CL酶的抑制活性测定:
1、Reaction Buffer配制:20mM HEPES,pH=7.0
2、酶液配制:50nM 3CL蛋白酶溶液:2uL 3CL(30uM)和2uL DTT(1M)溶液混匀后冰上放置3分钟,然后加入1.2mL Reaction Buffer以及2uL的DTT溶液。
3、化合物抑制率测定:
a.将3CL蛋白酶溶液与探针溶液孵育,并加入Zn
b.将3CL蛋白酶溶液先与抑制剂于反应缓冲液中预孵育20分钟,然后加入优化浓度的探针溶液和Zn
c.将步骤b中不同浓度的抑制剂溶液直接与探针溶液和Zn
d.将前三步算出的荧光积分面积代入以下公式:
抑制率=(不加抑制剂时的光谱积分面积-加抑制剂后的光谱积分面积)/(不加抑制剂时的光谱积分面积-背景光谱积分面积)*100%
计算得到抑制剂对3CL蛋白酶的抑制率,从而进行筛选和IC
(图3,图4)。
综上所述,本发明根据目前国内外对冠状病毒特别是以2019-nCoV冠状病毒为例的研究现状,以其3CL蛋白水解酶为药物作用靶点,通过化学方法合成1,3-氧硫杂环戊基嘧啶酮磷酸酯衍生物,所制备的化合物利用我们前期开发的3CL蛋白酶活性荧光探针进行检测筛选(申请号202111555106.4)。
筛选结果表明:在体外实验中,所合成的1,3-氧硫杂环戊基嘧啶酮磷酸酯衍生物对3CL蛋白水解酶显示了非常强的抑制活性。化合物IC
此外,本发明的1,3-氧硫杂环戊基嘧啶酮磷酸酯类化合物结构明确,其制备方法简便、收率较高。以该类化合物为新药候选物,开发高效低毒的抗冠状病毒的外用制剂、口服制剂及注射剂等药物具有良好的应用前景。
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
