一种乳腺癌化疗药物耐药相关的靶点及其应用
文献发布时间:2023-06-19 18:53:06
技术领域
本发明属于生物医药技术领域,尤其涉及一种乳腺癌化疗药物耐药相关的靶点及其应用。
背景技术
乳腺癌(BC)是当今世界最常见的恶性肿瘤之一。据2022年全球癌症统计数据显示,女性乳腺癌占所有癌症发病病例的三分之一,且发病率逐年上升。目前乳腺癌的治疗采用手术切除联合化疗药物。作为乳腺癌化疗的经典药物,顺铂通过与肿瘤细胞的DNA结合,形成铂-DNA加合物,损伤肿瘤细胞的DNA并抑制DNA的复制过程,使其发生凋亡,从而抑制肿瘤的发生和发展。但铂类药物具有固有耐药性和获得性耐药性,长期使用顺铂会出现乳腺癌细胞耐药,并导致化疗效果不佳。因此,需要确定新的治疗靶点并提出新的治疗策略,以提高乳腺癌患者对顺铂化疗治疗的敏感性。
根据过去的文献报道,乳腺癌细胞顺铂耐药的机制有:药物外排增加、药物摄取减少、细胞内解毒作用增强、DNA修复增加、加合物形成减少、抗凋亡信号转导增加以及代偿信号通路的激活等。
目前,有研究报道RRS1与肿瘤的发生发展有关。人源RRS1蛋白由365个氨基酸残基组成,主要定位在核仁和内质网中。在有丝分裂间期调节染色体排列和纺锤体的组装。在肿瘤细胞中表达升高,促进细胞的增殖和转移。此外,在亨廷顿病中RRS1与3D3/lyric共同作用参与内质网应激反应。但RRS1在乳腺癌细胞顺铂耐药中的研究尚未见报道。因此,解析RRS1在乳腺癌顺铂耐药中的机制有助于确定新的治疗靶点,对乳腺癌患者尤其是化疗效果较差患者的治疗具有重要的意义。
发明内容
本发明实施例的目的在于提供一种乳腺癌化疗药物耐药相关的靶点及其应用,旨在解决上述背景技术中提出的问题。
本发明实施例是这样实现的,一种乳腺癌化疗药物耐药相关的靶点,所述靶点为人源RRS1蛋白,所述人源RRS1蛋白与乳腺癌细胞具有相关性的验证方法包括以下步骤:
步骤1、乳腺癌细胞和乳腺癌顺铂耐药细胞中RRS1、AEG-1、ABCG2和 MDR1蛋白表达:
采用Western blot检测乳腺癌细胞和乳腺癌顺铂耐药细胞中RRS1、AEG-1、ABCG2和 MDR1蛋白的表达;
步骤2、顺铂处理诱导RRS1蛋白表达:
步骤2.1、使用1.501μg/ml顺铂处理乳腺癌细胞12 h,使用western blot和RT-qPCR检测RRS1蛋白和mRNA的表达;
步骤2.2、使用乳腺癌细胞构建裸鼠皮下增殖瘤模型,待小鼠生长一个月后,脱颈处死小鼠,取出肿瘤,RT-qPCR和 Western blot检测 RRS1的表达;
步骤3、敲减RRS1来验证乳腺癌顺铂耐药细胞对顺铂的敏感性:
采用RNA干扰技术敲减乳腺癌顺铂耐药细胞中RRS1基因的表达,采用Westernblot检测细胞中耐药蛋白ABCG2和 MDR1蛋白的表达,采用CCK8检测乳腺癌顺铂耐药细胞的IC
步骤4、验证敲降RRS1减低乳腺癌顺铂耐药细胞的增殖能力,诱导细胞周期阻滞和凋亡:
采用流式细胞术检测敲降RRS1基因后,检测乳腺癌顺铂耐药细胞的周期分布,使用Annexin V-APC/PI双染试剂盒检测细胞的凋亡能力,采用CCK8连续5天检测细胞的增殖情况;再通过Western blot检测增殖相关信号通路蛋白;
步骤5、验证AEG-1参与 RRS1介导乳腺癌细胞顺铂耐药:
通过网络数据库筛选得到与RRS1相关的互作蛋白AEG-1,通过RT-qPCR检测敲降RRS1后AEG-1的mRNA表达水平,结果表明mRNA无明显变化,但利用Western blot检测AEG-1蛋白水平的表达发现,敲降RRS1基因后,AEG-1的蛋白水平明显降低;
在乳腺癌顺铂耐药细胞中使用AEG-1抗体进行COIP实验,结果表明AEG-1与RRS1和MDR1均有相互作用;
步骤6、验证RRS1对AEG-1的含量的影响方式:
步骤6.1、使用蛋白质合成抑制剂环己酰亚胺(CHX)对 AEG-1蛋白的稳定性进行检测;
步骤6.2、在乳腺癌顺铂耐药细胞中过表达RRS1后再次使用CHX处理细胞,发现AEG-1蛋白水平无明显变化,随后使用蛋白酶体抑制剂 MG132处理细胞,结果发现相较于未使用MG132处理的细胞,AEG-1的蛋白水平升高,并且过表达RRS1后AEG-1蛋白水平升高更明显;
步骤6.3、使用泛素化抗体对AEG-1的泛素化水平进行检测,结果表明过表达RRS1能够降低AEG-1的泛素化水平。
进一步的技术方案,在所述步骤2.2中,裸鼠皮下增殖瘤模型的构建步骤如下:
将乳腺癌细胞接种至裸鼠腋下,并每日观察肿瘤生长状况,待肿瘤体积达到 100mm
本发明实施例的另一目的在于,一种乳腺癌化疗药物耐药相关的靶点在制备抗乳腺癌药物的制备中的应用。
本发明实施例提供的一种乳腺癌化疗药物耐药相关的靶点及其应用,系统性的验证了人源RRS1蛋白在促进乳腺癌细胞的顺铂耐药的作用原理,发现:
1、乳腺癌顺铂耐药细胞中RRS1、AEG-1、ABCG2和 MDR1蛋白表达明显高于MCF-7细胞,并且加入顺铂处理乳腺癌细胞后,RRS1蛋白的含量明显增加。在乳腺癌异种移植瘤模型中,注射顺铂30天后发现,肿瘤体积相比生理盐水对照组明显小很多,且RRS1表达显著增加;
2、敲降RRS1蛋白增加了乳腺癌顺铂耐药细胞对顺铂的敏感性,且乳腺癌顺铂耐药细胞的增殖能力明显降低,细胞凋亡明显增加,AEG-1、MDR1、ABCG2、p-ERK及凋亡抑制蛋白Bcl-2的含量明显下降。说明RRS1的表达与乳腺癌细胞顺铂耐药有关,减少RRS1的表达能够增强乳腺癌细胞对顺铂的敏感性。
3、敲降RRS1减少了AEG-1的蛋白水平,对mRNA水平无明显影响,而过表达RRS1使AEG-1的蛋白水平增加,使用放线菌酮(CHX)处理乳腺癌顺铂耐药细胞导致AEG-1蛋白发生降解,而过表达RRS1明显延长了AEG-1蛋白的半衰期。随后使用蛋白酶体抑制剂MG132处理细胞发现AEG-1的蛋白水平显著增加。此外,过表达RRS1减少了AEG-1的泛素化水平。这说明RRS1通过干扰 AEG-1的泛素化和蛋白酶体降解来减少乳腺癌顺铂耐药细胞中 AEG-1的降解,稳定AEG-1的蛋白水平。
通过解析RRS1在乳腺癌顺铂耐药中的机制有助于确定新的治疗靶点,对乳腺癌患者尤其是化疗效果较差患者的治疗具有重要的意义。
附图说明
图1是WB检测MCF-7和MCF-7/DDP细胞中RRS1、AEG-1、ABCG2和 MDR1蛋白表达结果示意图;
图2是顺铂(DDP)处理MCF-7细胞后RRS1蛋白及mRNA表达结果示意图;
图3是顺铂对MCF-7异种移植瘤模型的治疗结果(A),以及顺铂治疗导致RRS1蛋白(B)和mRNA(C)表达增加示意图;
图4 为敲降RRS1蛋白减少了耐药相关蛋白的表达(A),增加了MCF-7/DDP对顺铂的敏感性(B)示意图;
图5为敲降RRS1蛋白导致MCF-7/DDP细胞凋亡增加(A),细胞周期阻滞(B)示意图;
图6为敲降导致MCF-7/DDP细胞增殖能力下降(A),增殖相关信号通路蛋白和凋亡抑制蛋白表达减少、促凋亡蛋白表达增加(B、C、D)示意图;
图7为敲降RRS1对AEG-1的mRNA水平无明显影响(A),但减少了AEG-1的蛋白水平(B)示意图;
图8为COIP证实AEG-1与RRS1和MDR1有相互作用示意图;
图9为使用CHX(A)和MG132(B)处理MCF-7/DDP细胞,检测RRS1对AEG-1蛋白半衰期的影响示意图;
图10为过表达RRS1蛋白减少了AEG-1蛋白的泛素化降解示意图;
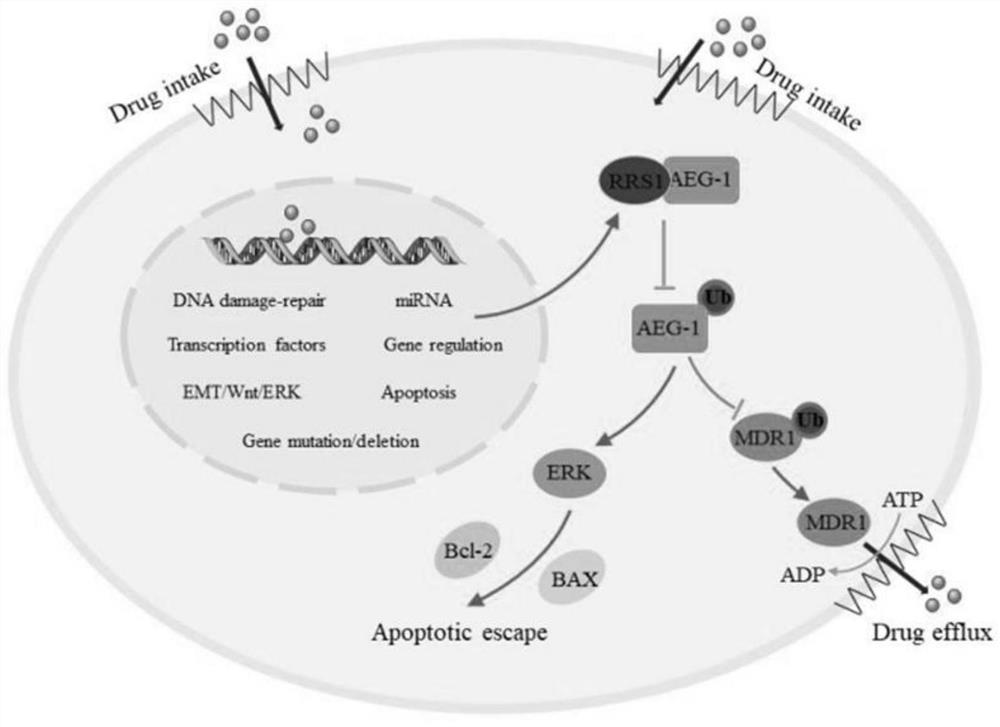
图11为本发明的RRS1通过AEG-1调控乳腺癌细胞顺铂耐药的机制图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
以下结合具体实施例对本发明的具体实现进行详细描述。
为本发明一个实施例提供的一种乳腺癌化疗药物耐药相关的靶点,所述靶点为人源RRS1蛋白,所述人源RRS1蛋白与乳腺癌细胞具有相关性的验证方法包括以下步骤(在该验证方法中,选用具有代表性的乳腺癌细胞MCF-7,以及乳腺癌顺铂耐药细胞MCF-7/DDP作为实验对象进行实验验证,采用如下的步骤可对已知的各种乳腺癌细胞及其耐药细胞进行实验,用以验证):
步骤1、MCF-7和MCF-7/DDP细胞中RRS1、AEG-1、ABCG2和 MDR1蛋白表达:
采用Western blot检测MCF-7和MCF-7/DDP细胞中RRS1、AEG-1、ABCG2和 MDR1蛋白的表达,结果表示,与MCF-7相比,MCF-7/DDP细胞中RRS1、AEG-1、ABCG2和 MDR1蛋白表达均明显升高(如图1所示)。
步骤2、顺铂处理诱导RRS1蛋白表达:
步骤2.1、使用1.501μg/ml顺铂处理MCF-7细胞12 h,使用western blot和RT-qPCR检测RRS1蛋白和mRNA的表达,结果表示MCF-7中RRS1的蛋白水平和mRNA水平均明显升高(如图2所示);
步骤2.2、使用MCF-7构建裸鼠皮下增殖瘤模型,将MCF-7细胞接种至裸鼠腋下,并每日观察肿瘤生长状况,待肿瘤体积达到 100 mm
结果表明,顺铂处理组肿瘤体积明显小于生理盐水组;且与生理盐水组相比,顺铂处理组 RRS1表达量明显增加,表明RRS1与顺铂化疗有关。(如图3所示)
步骤3、敲减RRS1来验证MCF-7/DDP细胞对顺铂的敏感性:
采用RNA干扰技术敲减MCF-7/DDP细胞中RRS1基因的表达,采用Western blot检测细胞中耐药蛋白ABCG2和 MDR1蛋白的表达,结果表明敲降RRS1基因后MDR1和 ABCG2的表达量显著降低。采用CCK8检测MCF-7/DDP的IC
这表明RRS1在乳腺癌细胞的顺铂耐药进程中发挥重要作用,敲降 RRS1基因导致乳腺癌细胞的顺铂敏感性增强。
步骤4、验证敲降RRS1减低MCF-7/DDP细胞的增殖能力,诱导细胞周期阻滞和凋亡:
采用流式细胞术检测敲降RRS1基因后MCF-7/DDP细胞的周期分布,结果显示细胞周期被明显阻滞在G1期;使用Annexin V-APC/PI双染试剂盒检测细胞的凋亡能力,结果表明敲降RRS1基因后,细胞凋亡明显高于未敲降组。采用CCK8连续5天检测细胞的增殖情况,结果显示敲降RRS1基因后,MCF-7/DDP细胞的增殖能力明显降低(如图5所示)。
此外,Western blot检测增殖相关信号通路蛋白,结果表明,敲降RRS1基因导致p-ERK和凋亡抑制蛋白Bcl-2的蛋白水平下降,促凋亡蛋白BAX的蛋白水平上升,Bcl-2/BAX比值降低(如图6所示)。
以上结果表明RRS1影响乳腺癌细胞的增殖、周期分布、细胞凋亡以及药物外排蛋白的表达,敲降RRS1增强了MCF-7/DDP细胞的顺铂敏感性。
步骤5、验证AEG-1参与 RRS1介导 MCF-7细胞顺铂耐药:
通过网络数据库筛选得到与RRS1相关的互作蛋白AEG-1。通过RT-qPCR检测敲降RRS1后AEG-1的mRNA表达水平,结果表明mRNA无明显变化,但利用Western blot检测AEG-1蛋白水平的表达发现,敲降RRS1基因后,AEG-1的蛋白水平明显降低(如图7所示)。因此RRS1是通过翻译后修饰途径影响AEG-1的蛋白水平。在MCF-7/DDP细胞中使用AEG-1抗体进行COIP实验,结果表明AEG-1与RRS1和MDR1均有相互作用(如图8所示)。
这说明AEG-1参与 RRS1介导 MCF-7细胞顺铂耐药。
步骤6、验证RRS1对AEG-1的含量的影响方式:
使用蛋白质合成抑制剂环己酰亚胺(CHX)对 AEG-1蛋白的稳定性进行了检测,发现AEG-1蛋白水平随时间增加逐渐降低。在MCF-7/DDP细胞中过表达RRS1后再次使用CHX处理细胞,发现AEG-1蛋白水平无明显变化(如图9所示)。随后,使用蛋白酶体抑制剂 MG132处理细胞,结果发现相较于未使用MG132处理的细胞,AEG-1的蛋白水平升高,并且过表达RRS1后AEG-1蛋白水平升高更明显(如图9所示)。使用泛素化抗体对AEG-1的泛素化水平进行检测,结果表明过表达RRS1能够降低AEG-1的泛素化水平(如图10所示)。
这说明RRS1通过干扰 AEG-1的泛素化和蛋白酶体降解来减少 MCF-7/DDP细胞中AEG-1的降解,稳定AEG-1的蛋白水平。
通过上述方法可知,RRS1通过抑制 AEG-1的泛素化和蛋白酶体降解增加 AEG-1的蛋白含量,一方面通过升高 MDR1,使药物外排增加;另一方面,通过调控 ERK/Bcl-2/BAX信号通路,引起细胞凋亡抵抗,共同促进乳腺癌细胞的顺铂耐药(如图11所示)。
因此可将人源RRS1蛋白应用于抗乳腺癌药物的制备中。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 与结直肠癌化疗药物耐药相关的靶点及应用
- 一种与乳腺癌多西紫杉醇耐药相关的microRNA分子及其应用
