一种人工心脏瓣膜支架
文献发布时间:2023-06-19 19:00:17
技术领域
本申请涉及但不限于医疗器械技术领域,尤其涉及一种人工心脏瓣膜支架。
背景技术
介入手术是治疗各种心血管相关疾病的可选方案,心血管相关疾病包括心脏瓣膜疾病。生物体如人体内的原生瓣膜(如主动脉瓣,肺动脉瓣,房室瓣等)对血液循环系统的运作起到至关重要的作用,如果患有先天或后天瓣膜疾病,例如主动脉二尖瓣或瓣膜钙化,可能导致瓣膜不能正常开闭,则会增加心脏负荷且影响对其他器官的供血。经导管瓣膜置换术(Transcatheter Valve Therapies,TVR)是一种针对心脏瓣膜疾病的治疗手段,通过导丝引导,将支架送至瓣膜区域并撑开原生瓣膜,由支架上带有的人工瓣膜代替原生瓣膜进行工作。这种方式避免了外科开胸手术,降低了治疗过程的创伤性,对一些年纪大或体力较弱的病人也适用。
人工瓣膜植入后,瓣膜跨壁压和瓣膜流量是主要监测的生理参数。传统监测方案中,瓣膜流量通过超声检查进行测量,瓣膜跨壁压则需要用压力导丝进行测量;两者都需要专业的测量设备和操作人员,需要病人到医院进行测量;且适用压力导丝测量跨壁压的耗时较长。可见,目前亟需对监测瓣膜跨壁压和瓣膜流量的设备进行改进。
发明内容
本申请实施例提供一种人工心脏瓣膜支架,以解决相关技术中监测瓣膜跨壁压和瓣膜流量的方式耗时较长,且操作复杂的问题。
本申请实施例的技术方案是这样实现的:
本申请实施例提供一种人工心脏瓣膜支架,所述人工心脏瓣膜支架包括:主体区段,所述主体区段包括由多个金属支杆交错连接而成的内网结构,所述内网结构由多个单元格沿周向和轴向排列而成;
其中,所述主体区段的流出端设置有用于检测主动脉静压的第一无源无线传感器;和/或所述主体区段的侧壁设置有用于检测心室静压的第二无源无线传感器;
所述主体区段的流入端设置有平台结构,所述平台结构伸向所述人工心脏瓣膜支架的内部,所述平台结构与径向平行,所述平台结构设置有用于检测心室总压的第三无源无线传感器。
本申请提供的人工心脏瓣膜支架,该人工心脏瓣膜支架包括:主体区段,主体区段包括由多个金属支杆交错连接而成的内网结构,内网结构由多个单元格沿周向和轴向排列而成;其中,主体区段的流出端设置有用于检测主动脉静压的第一无源无线传感器;主体区段的侧壁设置有用于检测心室静压的第二无源无线传感器;主动脉内部静压和心室静压的差值为跨壁压;主体区段的流入端设置有平台结构,平台结构伸向人工心脏瓣膜支架的内部,平台结构与径向平行,平台结构设置有用于检测心室总压的第三无源无线传感器;心室总压和心室静压的差值为心室动压,心室动压用于转换为流量;可见,本申请提供的人工心脏瓣膜支架,在人工心脏瓣膜支架上搭载多个传感器以测量瓣膜跨壁压和瓣膜流量,电路设计简单,省略了电源电线等装置,减少了植入物的体积和数量,提高安全性和适用性,同时对跨壁压和流量进行实时监测,获得的参数可辅助医生监测病人状态,可提前发现问题及进行干预。
附图说明
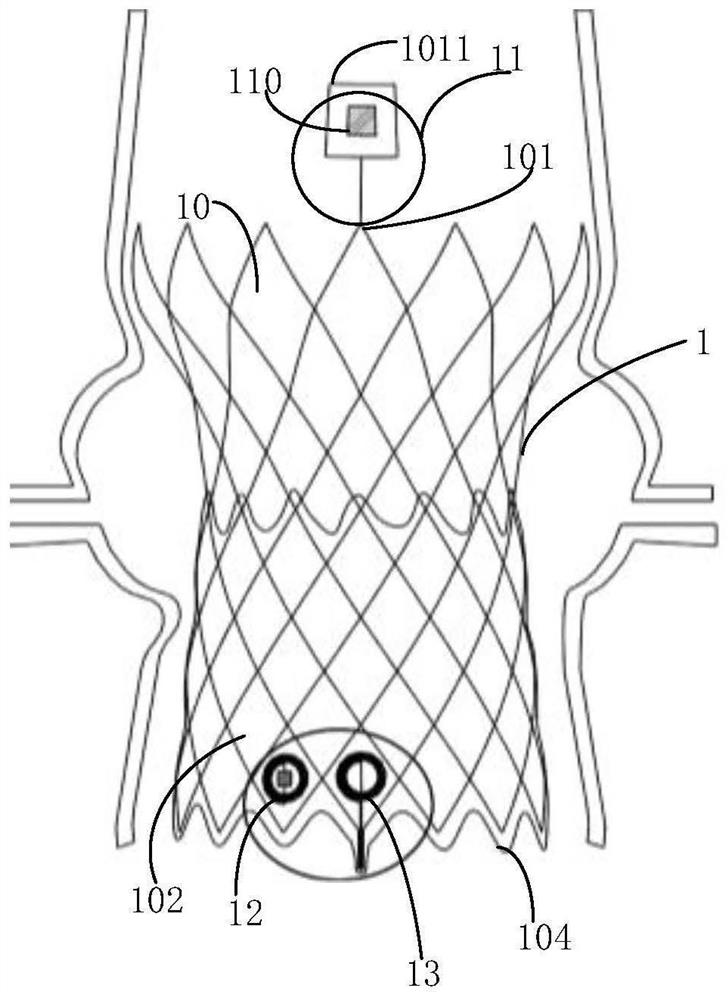
图1为本申请实施例提供的人工心脏瓣膜支架的结构示意图;
图2为本申请实施例提供的主体区段的流入端的部分区段的结构示意图;
图3为本申请实施例提供的人工心脏瓣膜支架上搭载传感器的结构示意图;
图4为本申请实施例提供的主体区段和裙边区段的结构示意图;
图5为本申请实施例提供的平台结构底部设置有第二无源无线传感器的结构示意图;
图6为本申请实施例提供的第二电容式传感器的结构示意图;
图7为本申请实施例提供的电容式传感器的构造剖面图;
图8为本申请实施例提供的电阻式传感器的构造剖面图;
图9为本申请实施例提供的植入支架后,通过第一外部天线对传感器的参数进行测量的电路结构示意图;
图10为本申请实施例提供的输入阻抗辐角随频率变化的曲线图示意图;
图11为本申请实施例提供的植入支架后,通过第二外部天线和第三外部天线对传感器的参数进行测量的电路结构示意图;
图12为本申请实施例提供的第二外部天线的功率随频率的变化曲线示意图;
图13为本申请实施例提供的多个传感器共同工作的情况下,信号分析系统得到的辐角曲线和功率曲线示意图;
图14为本申请实施例提供的两种电感的绕线方式的示意图;
图15为本申请实施例提供的支架放置在心窦附近,两个传感器分别测量心室和主动脉的压力的示意图。
具体实施方式
应理解,说明书通篇中提到的“本申请实施例”或“前述实施例”意味着与实施例有关的特定特征、结构或特性包括在本申请的至少一个实施例中。因此,在整个说明书各处出现的“本申请实施例中”或“在前述实施例中”未必一定指相同的实施例。此外,这些特定的特征、结构或特性可以任意适合的方式结合在一个或多个实施例中。在本申请的各种实施例中,上述各过程的序号的大小并不意味着执行顺序的先后,各过程的执行顺序应以其功能和内在逻辑确定,而不应对本申请实施例的实施过程构成任何限定。上述本申请实施例序号仅仅为了描述,不代表实施例的优劣。
为了使本申请的目的、技术方案和优点更加清楚,下面将结合附图对本申请作进一步地详细描述,所描述的实施例不应视为对本申请的限制,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本申请保护的范围。
除非另有定义,本文所使用的所有的技术和科学术语与属于本申请的技术领域的技术人员通常理解的含义相同。本文中所使用的术语只是为了描述本申请实施例的目的,不是旨在限制本申请。
本申请实施例中,根据心室舒张状态时的血流方向,限定人工心脏瓣膜支架及其各部件、人工心脏瓣膜及其各部件的“流入端”和“流出端”,其中“流入端”指靠近血液流入侧或者靠近心室侧的一端;“流出端”是指靠近血液流出侧或靠近主动脉侧的一端。“轴向”是指平行于流出端中心与流入端中心的连线的方向。“径向”是指垂直于或者大致垂直于轴向的方向。“周向”是指环绕轴向的方向。
人工心脏瓣膜支架具有径向压缩后的输送状态和径向展开后的自然状态。在输送状态下,通过外力对人工心脏瓣膜支架进行径向压缩,使其能压缩装入径向尺寸较小的鞘管内,从而通过输送装置输送至心脏处。在自然状态下,人工心脏瓣膜支架不受外力作用,径向自然展开,本申请中如无特殊说明,所阐述的均为人工心脏瓣膜支架在自然状态下的结构特征。
本申请实施例提供一种人工心脏瓣膜支架,参见图1、图2和图3所示,该人工心脏瓣膜支架1包括:
主体区段10,主体区段包括由多个金属支杆交错连接而成的内网结构,内网结构由多个单元格沿周向和轴向排列而成;
示例性的,参见图1所示,图1为人工心脏瓣膜支架1的正视图,人工心脏瓣膜支架1的形状,一般可以简化为类似图1的形状。人工心脏瓣膜支架1径向自然展开,其花纹由多个金属支杆交错连接形成四边形单元格,多个单元格沿周向和轴向排列形成内网结构;示例性的,单元格又称网格,与菱形相似,沿着轴向方向,同一侧的网格边长是相等的,而不同侧的网格边长有差异;沿着周向的四边形网格形状相同;主体区段10的一些区域有镂空的部分,其位于主动脉一侧;镂空或增加该区域网格长度的目的是为了防止对冠脉介入手术造成阻碍。
其中,主体区段的流出端101设置有用于检测主动脉静压的第一无源无线传感器11;主体区段的侧壁102设置有用于检测心室静压的第二无源无线传感器12。
本申请中在主体区段10的一些区域有镂空的部分的情况下,第二无源无线传感器12尽量避免放置在大网格或镂空区域,而是放置在靠近主体区段的流入端104的网格区域,以免对冠脉介入手术造成影响。需要说明的是,第一无源无线传感器11设置在主体区段的流出端101,第二无源无线传感器12设置在主体区段的侧壁102,第一无源无线传感器11和第二无源无线传感器12均与轴向平行。
参见图2所示,图2中的A为人工心脏瓣膜支架1的主体区段中,靠近主体区段的流入端的部分区段的侧视图,图2中的B为人工心脏瓣膜支架1的主体区段中,靠近主体区段的流入端的部分区段的仰视图,如图2所示主体区段的流入端104设置有平台结构105,平台结构105伸向人工心脏瓣膜支架的内部,平台结构105与径向平行;结合图2和图5所示,平台结构105设置有用于检测心室总压的第三无源无线传感器13的第三电容式传感器130,第三电容式传感器130通过导线107与人工心脏瓣膜支架单一单元格内部的电感线圈连接。
介入手术是治疗各种心血管相关疾病的可选方案,心血管相关疾病包括心脏瓣膜疾病。生物体如人体内的原生瓣膜(如主动脉瓣,肺动脉瓣,房室瓣等)对血液循环系统的运作起到至关重要的作用,如果患有先天或后天瓣膜疾病,例如主动脉二尖瓣或瓣膜钙化,可能导致瓣膜不能正常开闭,则会增加心脏负荷且影响对其他器官的供血。经导管瓣膜置换术(Transcatheter Valve Therapies,TVR)是一种针对心脏瓣膜疾病的治疗手段,通过导丝引导,将支架送至瓣膜区域并撑开原生瓣膜,由支架上带有的人工瓣膜代替原生瓣膜进行工作。这种方式避免了外科开胸手术,降低了治疗过程的创伤性,对一些年纪大或体力较弱的病人也适用。
人工瓣膜植入后,瓣膜跨壁压和瓣膜流量是主要监测的生理参数。传统监测方案中,瓣膜流量通过超声检查进行测量,瓣膜跨壁压则需要用压力导丝进行测量;两者都需要专业的测量设备和操作人员,需要病人到医院进行测量;且适用压力导丝测量跨壁压的耗时较长和经济成本较高。
本申请实施例中,本申请提供的人工心脏瓣膜支架,在单个人工心脏瓣膜支架上搭载多个无源无线传感器,可测量人工心脏瓣膜使用过程中瓣膜跨壁压和瓣膜流量;例如,上述第一无源无线传感器11用于检测主动脉静压,第二无源无线传感器12用于检测心室静压,主动脉内部静压和心室静压的差值为跨壁压;第三无源无线传感器13用于检测心室总压,心室总压和心室静压的差值为心室动压,心室动压用于转换为流量;本申请提供的第一无源无线传感器11、第二无源无线传感器12和第三无源无线传感器13,在较小的程度内影响人工心脏瓣膜支架的原有外形和功能,此外,还可以在人工心脏瓣膜支架上搭载多个传感器以测量瓣膜跨壁压或瓣膜流量。可见,本申请提供的人工心脏瓣膜支架,电路设计简单,省略了电源电线等装置,减少了植入物的体积和数量,提高安全性和适用性,同时对跨壁压和流量进行实时监测,获得的参数可辅助医生监测病人状态,可提前发现问题及进行干预。
上述的第一无源无线传感器11、第二无源无线传感器12和第三无源无线传感器13均包括基于谐振电路设计原理设计的电路,本申请所采用的谐振电路结构简单,在谐振电路上搭载电容式传感器或电阻式传感器,即可组成一个带传感器的简易天线,使用射频(radio frequency,RF)天线可与该简易天线通信,通过测量简易天线的共振频率或带宽,可获得谐振电路中传感器的电容值或电阻值,从而反推物理值且达到测量瓣膜跨壁压、瓣膜流量的目的。
本申请其他实施例中,在第一种可实现的方案中,参见图1所示,主体区段的流出端101具有固定结构1011,固定结构1011与轴向平行,固定结构1011设置有第一无源无线传感器11包括的第一电容式传感器110。
这里,以第一电容式传感器110设置在主体区段的流出端101为例,可选地,主体区段的流出端101设置有固定结构1011,固定结构1011设置有第一电容式传感器110,由于金属支架本身带有电感和电阻,以此支架本体与第一电容式传感器110共同组成第一无源无线传感器的一个测量电路;此时,第一电容式传感器110可以通过激光焊接或导电环氧树脂粘合剂等方式固定在固定结构1011上,从而形成一个RLC串联谐振电路。
需要说明的是,参见图1所示,在固定结构1011设置有第一电容式传感器110,第一电容式传感器110和支架本体组成第一无源无线传感器11的同时,还需要在主体区段的侧壁102上设置第二无源无线传感器12。固定结构1011用于将人工心脏瓣膜支架固定在输送系统上,控制人工心脏瓣膜支架的释放。人工心脏瓣膜支架可以是镍钛诺合金制作的自膨胀支架。
本申请其他实施例中,图1中第二无源无线传感器12具有第一串联谐振电路,第一串联谐振电路包括在多个单元格的单一单元格内,参见图3所示,由第二电容式传感器120和导线(图3中在单元格内缠绕的线和/或在单元格的支架上缠绕的线都是导线)连接形成的电路。也就是说,组成第二无源无线传感器12的第一串联谐振电路可以设置在多个单元格的单一单元格内。
本申请其他实施例中,参见图4所示,人工心脏瓣膜支架1还包括:
裙边区段30,包覆在主体区段10的径向内外侧,且裙边区段30位于主体区段的流出端101和主体区段的流入端104之间;示例性的,图4中裙边区段30位于主体区段的底部,底部是指靠近主体区段的流入端104的方位。参见图4所示,主体区段10的一些区域有镂空的部分108,其位于主动脉一侧;镂空或增加该区域网格长度的目的是为了防止对冠脉介入手术造成阻碍。
针对不同人工心脏瓣膜支架设计,镂空的部分108的位置可能有所变化;人工心脏瓣膜支架会的支架底部包覆一层裙边区段30,在本申请中,裙边区段30既可用作防止周漏,又可用作固定传感器;裙边区段30特指由裙边覆盖的区域。
在第二种可实现的方案中,提供了单一单元格内设置第一串联谐振电路的一种方案,图3中的第一种第一串联谐振电路201被固定在图4所示的裙边区段30上,如图3所示,第一种第一串联谐振电路201的结构为:单一单元格内导线环绕或缠绕形成电感,且在导线环绕的中间区域设置有第二电容式传感器120,导线的两端分别与第二电容式传感器120的电极连接,结合导线本身的电阻,形成RLC串联电路;该方案中,可以通过调整电感环绕的半径,圈数等参数来调节电感值,从而调节RLC串联电路的工作频率范围。
本申请其他实施例中,在第三种可实现的方案中,提供了单一单元格内设置第一串联谐振电路的另一种方案,图3中的第二种第一串联谐振电路202、第三种第一串联谐振电路203、第四种第一串联谐振电路204的结构为:导线缠绕在单一单元格的至少一条支撑杆上形成螺旋电感线圈,或者,导线在一个单元格内形成多匝环形线圈电感,导线的两端分别与第二电容式传感器120的电极连接。其中,图3中的第二种第一串联谐振电路202的结构为:导线缠绕在单一单元格的一条支撑杆上形成电感线圈,导线的两端分别与第二电容式传感器120的电极连接。图3中的第三种第一串联谐振电路203的结构为:导线缠绕在单一单元格的二条支撑杆上形成电感线圈,导线的两端分别与第二电容式传感器120的电极连接。图3中的第四种第一串联谐振电路204的结构为:导线缠绕在单一单元格的三条支撑杆上形成电感线圈,导线的两端分别与第二电容式传感器120的电极连接。可见,在第三种可实现的方案中,在一个网格内,导线缠绕网格边界,即人工心脏瓣膜支架的支撑杆,形成线圈。导线的两端分别与第二电容式传感器120的电极相连接,结合导线本身的电阻,形成RLC串联电路。需要说明的是,在实际应用中,根据所需电感值大小,可选择缠绕1到3条支撑杆;另外,该方案中,可以通过调整导线缠绕圈数,螺距等参数,调整电感值,从而调节RLC串联电路的工作频率范围。
本申请其他实施例中,图1中第二无源无线传感器12具有第一串联谐振电路,第一串联谐振电路设置在相邻两个单元格内,参见图3所示,第一无源无线传感器具有第一串联谐振电路,第一串联谐振电路包括在多个单元格的相邻的两个单元格内。
进一步地,本申请其他实施例中,在第四种可实现的方案中,提供了相邻两个单元格内设置第一串联谐振电路的一种方案,图3中的第五种第一串联谐振电路205的结构为:导线环绕设置在相邻的两个单元格中的一个单元格内,第二电容式传感器120设置在相邻的两个单元格中的另一个单元格内,导线的两端分别与第二电容式传感器120的电极连接。参见图3中的第五种第一串联谐振电路205所示,RLC串联电路放置在人工心脏瓣膜支架的底部区域,第二电容式传感器120放置在与导线环绕形成的线圈所在网格的相邻的另一个网格内。
进一步地,本申请其他实施例中,在第五种可实现的方案中,提供了相邻两个单元格内设置第一串联谐振电路的一种方案,图3中的第六种第一串联谐振电路206的结构为:导线缠绕在相邻的两个单元格同一侧的支撑杆上形成两个电感线圈,两个电感线圈的一端通过电阻式传感器22连接,两个电感线圈的另一端通过定值电容23连接。参见图3中的第六种第一串联谐振电路206所示,RLC串联电路放置在人工心脏瓣膜支架的底部区域,在第五种可实现的方案中,传感器类型为电阻式传感器22,搭配一个定值电容23;因为电路中配置了电阻式传感器和定值电容,本方案的电路设置在两个相邻的网格内。导线缠绕两个网格同一侧的支撑杆,形成电感线圈;使用两个线圈连接电阻式传感器和定值电容,最终形成RLC串联电路。调整导线缠绕圈数,螺距等参数,或者调整定值电容23的电容值均可控制电路的共振频率,从而调节RLC串联电路的工作频率范围
本申请其他实施例中,图2所示主体区段的流入端104设置有平台结构105,图2中的平台结构105底部设置有用于检测心室总压的第三无源无线传感器13。结合图5所示,第三无源无线传感器13具有第二串联谐振电路,第二串联谐振电路包括第三电容式传感器130,以及在多个单元格的单一单元格内和/或单一单元格的支撑杆上绕制导线形成的电感,导线的两端与第三电容式传感器130的电极连接。
结合图2、图5和图6所示,底层网格下方添加了一个平台结构105;平台结构105伸向人工心脏瓣膜支架内部,将第三电容式传感器130用激光焊接或环氧树脂粘合剂等方式固定在平台结构105底部;然而第三电容式传感器130并不与人工心脏瓣膜支架形成回路,因此,从第三电容式传感器130引出两条导线;并使用导线在网格内部或网格支撑杆上绕制电感元件。
进一步地,本申请其他实施例中,在第六种可实现的方案中,图6中的A为导线在网格内部环绕形成电感,电感与平台结构105底部的第三电容式传感器130引出的导线107连接,形成RLC串联电路;通过调整导线缠绕圈数,螺距等参数,可调节RLC串联电路的工作频率范围。
进一步地,本申请其他实施例中,在第七种可实现的方案中,图6中的B为导线在环绕网格支撑杆形成电感,电感与平台结构105底部的第三电容式传感器130引出的导线连接,形成RLC串联电路;通过调整导线缠绕圈数,螺距等参数,可调节RLC串联电路的工作频率范围。
进一步地,本申请其他实施例中,在第八种可实现的方案中,图6中的C结合了图6中的A和图6中的B导线绕制方式形成电感,电感与电容式传感器引出的导线连接,形成RLC串联电路;通过调整导线缠绕圈数,螺距等参数,可调节RLC串联电路的工作频率范围。
需要说明的是,图5中第三无源无线传感器13为了便于描述,所以标注在平台结构105上,可以理解的,第三无源无线传感器13包括图5中平台结构105上的第三电容式传感器130、两根导线107、以及图6中多个单元格的单一单元格内和/或单一单元格的支撑杆上绕制导线形成的电感。
进一步地,针对搭载在上述人工心脏瓣膜支架上的电容式传感器和电阻式传感器的工作原理以及构造进行说明,
本申请中用到的电容式传感器,可以是平行板电容,电极附着在薄膜上,体内血压的变化使薄膜发生形变且改变平行板之间的距离,导致电容值改变从而影响RLC串联电路的共振频率;通过测量电路的共振频率,即可反推血压值。其中电容的计算公式为:
其中,C为电容值,P为血压值,ε为真空中介电常数,A为平行板的面积,d为平行板之间的距离,d随着血压变化而变化。
下面介绍可能使用的电容构造以及工作原理:
构造一:构造一的剖面图如图7中的A所示,中空的基底被两片薄膜夹在中间,活动薄膜表面有一层金属薄膜作为电极;活动薄膜受血压影响发生形变,改变金属薄膜之间的距离,从而改变电容值。基底的材料可选择二氧化硅如玻璃,使用离子反应刻蚀技术制造中空区域。活动薄膜选择硅片来制作,使用光刻蚀技术在硅片表面刻蚀出接线电极电路;然后使用金属溅射技术,使导电金属填满刻蚀电路并在表面形成一层金属薄膜,作为电极。在真空环境下,将两片带有电极的硅片和中空的基底进行高温键合,形成真空密封腔且金属薄膜朝内。键合后使用化学腐蚀技术对两侧带有电极的硅片进行腐蚀直到接线电极的位置,并得到硅薄膜。完成腐蚀后进行晶片切割和封装,并将接线电极与上述第二种可实现的方案至第四种可实现的方案,或第六种可实现的方案至第八种可实现的方案中的线圈进行焊接,形成回路。其中接线电极的电路可根据具体的接线方案进行设计,以方便与线圈的焊接。
构造二:构造二的剖面图如图7中的B所示,基底表面有一层金属薄膜电极,基底上方覆盖带有电极的活动薄膜,活动薄膜受血压影响发生形变,改变金属薄膜之间的距离,从而改变电容值。基底的材料可选择二氧化硅如玻璃,使用离子反应刻蚀技术,刻蚀出接线电极电路;然后使用金属溅射技术,在基底表面形成金属薄膜和接线电极。活动薄膜选择硅片来制作,使用光刻蚀技术在硅片上刻蚀出腔体和接线电极电路;然后使用金属溅射技术,形成接线电极和金属薄膜。在真空环境下,将硅片和基底进行高温键合,形成真空密封腔且金属薄膜朝内。键合后使用化学腐蚀技术对硅片进行腐蚀直到接线电极的位置,并得到硅薄膜。完成腐蚀后进行晶片切割和封装,并将接线电极与上述第二种可实现的方案至第四种可实现的方案,或第六种可实现的方案至第八种可实现的方案中的线圈进行焊接,形成回路。其中接线电极的电路可根据具体的接线方案进行设计,以方便与线圈的焊接。
构造三:构造三的剖面图如图7中的C所示,使用金属材料作为基底,基底上方覆盖一层活动薄膜,活动薄膜上又覆盖一层金属薄膜作为电极。基底的材料为可导电金属,而且是可应用于手术植入器材的金属材料,采用微放电加工技术或激光加工技术,在金属基底上刻出空腔。用聚酰亚胺作为活动薄膜,同时作为绝缘介质。使用电子束蒸发金属层,然后旋涂并固化在聚酰亚胺薄膜上,从而制作金属薄膜;或者直接使用金属溅射技术在聚酰亚胺形成金属薄膜。在真空环境下加热,并使聚酰亚胺薄膜键合到金属基底上,形成真空密封腔。构造三的电容用于第一种可实现的方案,通过将金属基底焊接在固定结构1011上,可直接与支架形成RLC回路。
本申请的第五种可实现的方案是一种使用电阻式传感器的方案,其工作原理是硅、锗等半导体具有压阻效应,在发生形变的情况下,其电阻会产生相应的变化,电阻随压力变化的表达式为:
其中,R为电阻值;ΔR为电阻的变化值;π
在第五种可实现的方案中,电阻式传感器因血压变化产生形变,从而改变RLC串联电路的电阻值以及RLC串联电路的带宽;测量带宽则可以反推电阻值和血压值。其中电阻式传感器的构造如图8所示,在基底上方有一片真空腔体和一块活动薄膜,活动薄膜由半导体制成,在血压下发生形变时其电阻值发生改变。选择硅片,通过掺入微量元素,如磷,硼等改善导电性能;使用化学腐蚀技术,在硅片上腐蚀出腔体并形成活动薄膜;选择玻璃为基底,在真空环境下将硅片与玻璃基底进行高温键合,形成真空密闭腔体。硅片掺入微量元素后具有导电性,导线与硅片连接即可形成回路。
本申请的第二种可实现的方案到第八种可实现的方案中,导线是RLC串联电路的主要电阻来源。已知电阻越小,RLC串联电路的带宽越小,更容易分辨电路的共振频率,提高测量精度。金,银的电导率高,本申请人考虑到导线强度问题,可能不适合制作导线,因此可以采用金属镀层工艺或金属喷涂工艺,在强度高的导线上覆盖一层金或银的薄膜,以此提高电导率。本申请的其中一个特点是可放置多个传感器,因此需要考虑第一种可实现的方案与其他方案共同应用在一个支架上的情况。为了防止其他方案的线圈或导线与支架接触且形成回路,可在以上导线或线圈表面添加绝缘涂料涂层,如聚四氟乙烯等材料,从而减小线圈或导线对支架的电感和电阻的影响,保证第一种可实现的方案正常工作。理想的情况下,导线在覆盖金属涂层以提高电导率后,再添加一层绝缘涂料;考虑到经济成本且电路带宽已经足够小的情况下,可只在导线表面添加绝缘涂料。
本申请中,RLC串联电路的两个特征参数被用于测量物理值,分别是共振频率和带宽。共振频率f
带宽Δf的表达式为:
如图9所示,支架植入后,可通过第一外部天线41与支架上的无源无线传感器进行交流,从而测量人体内部的生理参数。第一外部天线41为射频天线,实际上是电感线圈,以图9所示的线圈为为例,实际形状可根据实际场景的具体情况进行设计。电源42为第一外部天线41提供不同频率的电流或电压,使得射频天线附近产生交变电磁场;支架上搭载的电感在交变电磁场的作用下产生电流,并吸收交变电磁场的能量。图9展示了外部天线电路和内部传感器电路。其中,La是外部天线的电感,Ls是上述方案中的线圈电感或支架本身的电感,Lm是La和Ls耦合时产生的互感电感;Rs是上述方案中线圈的电阻、支架本身的电阻或电阻式传感器的电阻;Cs是上述方案中电容式传感器的电容或定值电容。Va是La两侧的电压,Vs是Ls两侧的电压,Ia是流经La的电流,Is是流经Ls的电流。根据互感耦合电路的特性可以得到:
V
V
其中,s=j·2π·f,j
联立公式(1)-(2),可得到Va与Ia之间的关系式:
因此,外部天线的电感线圈的输入阻抗Z等于:
其中,k为互感耦合参数,Q为质量因素,其表达式为:
输入阻抗Z是一个复数,Z的辐角反映了电流与电压之间的相位差,相位差随着频率变化而变化;对公式(5)进行求导分析可发现,相位差随着频率的变化有极小值且对应的频率是共振频率f
上述提到内部传感器电路在交变电磁场下吸收外部天线的能量从而产生电流;在撤走外部天线后,电流仍然存在且在电阻的作用下逐渐衰减。在电流消失前,传感器电路会产生交变电磁场,对该电磁场进行分析也能获得传感器电路的特征参数。如图11所示,在使用第三外部天线45对无源无线传感器进行激励后,断开电源并将第二外部天线44靠近传感器。第二外部天线44实际上也是电感线圈,在传感器产生的交变电磁场作用下,第二外部天线44从交变电场吸收能量并在内部产生电流。传感器电路在共振频率下吸收和释放的能量的功率都是最高的;测量第二外部天线44的电压和电流并换算为电功率,记录电功率随着频率的变化,最大电功率对应的频率就是共振频率。图12展示了第二外部天线44的功率变化曲线,频率等于共振频率f
RLC串联电路具有带通滤波的特性,吸收或释放一定频率范围内的能量,在该频率范围内外,其吸收或释放的能量很小,电流和电压的相位差也接近90度,图10和图12都反映了这种现象。因此,可以利用RLC串联电路这种带通特性,进行多个传感器的测量,如图13所示。确定传感器的压力测量范围后,通过调整电容值或电感值,使得传感器的共振频率在一定频率范围内变化,该频率范围称作工作范围。在对传感器进行信号分析时,只需要在对应的工作范围内读取共振频率或带宽,可保证多个传感器同时工作时不会互相影响。
参考图3中的电感绕制方案,本申请中的电感可归类为螺旋线圈电感(如图3中202-204,图3中306和图6中的B)或多匝环形线圈电感(如图3中201,图3中205和图6中的A),图6中的C则可以认为是两种电感的串联。如上文所说,通过调整电感值可调节电路的工作范围,从而实现多个传感器工作方案,其中电感的调节方式包括控制电感圈数,电线长度,线圈面积等参数。针对螺旋线圈电感,其电感值的计算公式如下:
其中,μ
针对多匝环形线圈电感,其电感值的计算公式如下:
d
ρ=(D
其中,d
在第一种实际应用场景中,使用上述的传感器搭载方案和测量方式,实现测量瓣膜跨壁压的功能,如图2所示。为了测量主动脉内部的压力,采用第一种可实现的方案在主动脉一侧放置一个传感器电路,传感器的构造参考图7中的C;为了测量心室的压力,采用第二种可实现的方案在支架底部网格内搭载一个RLC串联电路,其中传感器的构造参考图7中的A或图7中的B;在实际操作中,第二种可实现的方案可替换为第三种可实现的方案、第四种可实现的方案或第五种可实现的方案。利用裙边区段30包裹支架底部的网格以及RLC串联电路,使RLC串联电路固定在网格内,且避免电路与血液直接接触。
进行压力测量时,将外部天线靠近心脏区域,启动电源,电源提供的电流或电压频率覆盖两个传感器电路的工作范围,使外部天线内部产生交变电磁场并对传感器电路产生激励。借助信号分析系统,在两个传感器电路各自的工作范围内搜索对应的共振频率如图13所示,转换成压力数据,获得跨瓣压值。
在第二种实际应用场景中,使用上述的传感器搭载方案和测量方式,实现测量瓣膜跨壁压的功能,如图15所示,支架放置在心窦附近,两个传感器分别测量心室和主动脉的压力,心室一侧的传感器是电阻式传感器。为了测量主动脉内部的压力,采用第一种可实现的方案在主动脉一侧放置一个传感器电路,传感器的构造参考图7中的C;为了测量心室的压力,采用第五种可实现的方案在支架底部网格内搭载一个RLC串联电路,其中传感器的构造参考图8。利用裙边区段30包裹支架底部的网格以及RLC串联电路,使RLC串联电路固定在网格内,且避免电路与血液直接接触。
进行压力测量时,将外部天线靠近心脏区域,启动电源,电源提供的电流或电压频率覆盖两个传感器电路的工作范围,使外部天线内部产生交变电磁场并对传感器电路产生激励。借助信号分析系统,在电容式传感器电路的工作范围内搜索对应的共振频率,在电阻式传感器的工作范围内读取带宽,分别将共振频率和带宽转换成电容值和电阻值,进一步地获得主动脉压力和心室压力,两者作差计算跨瓣压。
在第三种实际应用场景中,使用上述的传感器搭载方案和测量方式,实现测量流速的功能。其中一个测量血液静压,采用第二种可实现的方案在网格内部放置一个传感器电路,传感器构造参考图7中的A或图7中的B;另一个用于测量血液总压,采用第六种可实现的方案,在底部平台放置一个电容式传感器,传感器构造参考图7中的A或图7中的B,并于网格内的线圈组成电路。其中,第二种可实现的方案可以用第三种可实现的方案,第四种可实现的方案或第五种可实现的方案代替;第六种可实现的方案可以用第七种可实现的方案或第八种可实现的方案代替。利用裙边区段30包裹支架底部的网格以及RLC串联电路,使RLC串联电路固定在网格内,且避免电路与血液直接接触。血液冲击平台底部的传感器,血液在传感器的表面停止,此时动压转换成静压并作用在传感器的活动薄膜上,因此平台底部测量的压力时血液的总压;而放置在网格内的传感器没有受血流正面冲击,因此测量的是静压。总压P
P
进行测量时,将外部天线靠近心脏区域,启动电源,电源提供的电流或电压频率覆盖两个传感器电路的工作范围,使外部天线内部产生交变电磁场并对传感器电路产生激励。借助信号分析系统,在两个传感器电路各自的工作范围内搜索对应的共振频率,参考图11所示,转换成压力数据并计算两侧的压力差,获得动压值。然后根据公式(8),计算血液速度v;这里ρ是血液的密度值,不同人的血液密度有差异,这里给出参考值为1060kg/m3。获得速度值后,可以借助医疗影像,如电子计算机断层扫描(Computed Tomography,CT)等,计算心室出口的面积,从而换算为流量数据。
在第四种实际应用场景中,在同一个支架内设置三个传感器电路,用于计算跨瓣压和流速,具体方案如图1所示,三个传感器一个放置在底部网格内,一个放置在底部平台下,一个在主动脉一侧。图1结合了第一种实际应用场景和第三种实际应用场景,使用第一种可实现的方案,第二种可实现的方案和第六种可实现的方案在支架上放置了三个传感器,分别用于测量主动脉静压,心室静压和心室总压。第二种可实现的方案可以用第三种可实现的方案至第五种可实现的方案代替,第六种可实现的方案可以用第七种可实现的方案、第八种可实现的方案代替。利用裙边区段30包裹支架底部的RLC串联电路,固定RLC串联电路,且避免电路与血液直接接触。参考第一种实际应用场景和第二种实际应用场景的操作方式,测量跨瓣压;参考第三种实际应用场景的方式,测量心室出口附近的流速。
本申请提供的人工心脏瓣膜支架,具有如下有益效果:人体的心动周期为0.8s左右,因此人体血压或流量的变化频率为1-2Hz;只要RLC串联电路的电流电压频率远高于血压的变化频率,可在血压发生明显变化前就测量出某一时刻的血压值。因此可以通过将RLC串联电路的工作频率范围设置为远高于2Hz,就能获得一个心动周期内每个时刻对应的压力值。因此本申请在无需压力导丝等介入类器材的情况下也实时能检测瓣膜附近的压力变化。本申请采用无源无线传感器的设计,电路设计简单,省略了电源电线等装置,减少了植入物的体积和数量,提高安全性和适用性。本申请设置了单个支架搭载多个传感器的方案,可测量人工心脏瓣膜使用过程中主要关注参数:跨瓣压和流量。本申请可对瓣膜跨壁压和瓣膜流量进行实时监测,获得参数可辅助医生进行监测病人状态,可提前发现问题及进行干预。
在本申请所提供的几个实施例中,应该理解到,所揭露的设备和方法,可以通过其它的方式实现。以上所描述的设备实施例仅仅是示意性的,例如,所述单元的划分,仅仅为一种逻辑功能划分,实际实现时可以有另外的划分方式,如:多个单元或组件可以结合,或可以集成到另一个系统,或一些特征可以忽略,或不执行。另外,所显示或讨论的各组成部分相互之间的耦合、或直接耦合、或通信连接可以是通过一些接口,设备或单元的间接耦合或通信连接,可以是电性的、机械的或其它形式的。
上述作为分离部件说明的单元可以是、或也可以不是物理上分开的,作为单元显示的部件可以是、或也可以不是物理单元,即可以位于一个地方,也可以分布到多个网络单元上;可以根据实际的需要选择其中的部分或全部单元来实现本实施例方案的目的。
另外,在本申请各实施例中的各功能单元可以全部集成在一个处理模块中,也可以是各单元分别单独作为一个单元,也可以两个或两个以上单元集成在一个单元中;上述集成的单元既可以采用硬件的形式实现,也可以采用硬件加软件功能单元的形式实现。本领域普通技术人员可以理解:实现上述方法实施例的全部或部分步骤可以通过程序指令相关的硬件来完成,前述的程序可以存储于一计算机可读取存储介质中,该程序在执行时,执行包括上述方法实施例的步骤;而前述的存储介质包括:移动存储设备、只读存储器(Read-Only Memory,ROM)、随机存取存储器(Random Access Memory,RAM)、磁碟或者光盘等各种可以存储程序代码的介质。
本申请所提供的几个方法实施例中所揭露的方法,在不冲突的情况下可以任意组合,得到新的方法实施例。
本申请所提供的几个产品实施例中所揭露的特征,在不冲突的情况下可以任意组合,得到新的产品实施例。
本申请所提供的几个方法或设备实施例中所揭露的特征,在不冲突的情况下可以任意组合,得到新的方法实施例或设备实施例。
以上所述,仅为本申请的具体实施方式,但本申请的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本申请揭露的技术范围内,可轻易想到变化或替换,都应涵盖在本申请的保护范围之内。因此,本申请的保护范围应以所述权利要求的保护范围为准。
