一种CD3抗原的制备方法及应用
文献发布时间:2023-06-19 11:26:00
技术领域
本发明属于生物技术领域,具体涉及一种CD3抗原的制备方法及应用。
背景技术
CD3蛋白是一种T细胞标志物,仅在T细胞中发现。在恶性淋巴瘤中,CD3是一种广泛的T细胞系限制性抗原,在80%~97%的T细胞淋巴瘤中能被检测到。CD3是恶性淋巴瘤和淋巴样白血病分类的重要标志物。
CD3在T淋巴细胞表面通过与T细胞受体(TCR)形成复合物来发挥信号传递作用,当抗原呈递细胞(APC)激活TCR时,TCR介导的信号通过CD3链CD3D,CD3E,CD3G和CD3Z跨细胞膜传输,而TCR-CD3复合体组装则是通过形成CD3D / CD3E和CD3G / CD3E两个异二聚体来启动的。除了信号转导在T细胞活化中的作用外,CD3E在正确的T细胞发育中也起着至关重要的作用。因此制备CD3不同亚基的两个异源二聚体对CD3与TCR的相互作用以及该信号传导在免疫应答中的分子机制研究非常重要,CD3不同亚基异源二聚体作为靶点蛋白成为研究热点,CD3的抗体靶向药物通常通过识别形成天然异源二聚体的CD3E,从而激活T细胞,使其行使肿瘤杀伤功能。然而,在体外重组表达制备 CD3E/CD3D,CD3E/CD3G异源二聚体蛋白的过程中,CD3E与CD3D或CD3G极易形成单体比例不均一的复合物,无法保证异源二聚体蛋白的结构和功能,并造成较大批间差异,是双抗药物开发的瓶颈。
现有技术有通过原核大肠杆菌表达系统表达单个亚基后进行等比例混合复性,得到二聚体,但是该方法相对哺乳表达系统制备的CD3抗原免疫活性低;目前通过真核哺乳细胞表达CD3不同亚基,多采用融合FC标签(野生型或者突变体)的方式帮助形成二聚体,但是由于FC标签本身能形成二聚体,融合野生型FC标签的方法容易引起同源二聚体的干扰、有异源二聚体比例低需多步骤纯化的缺点;融合突变体FC标签蛋白虽然能有效降低同源二聚体比例,但是也存在易于形成高聚体的问题,另外FC标签分子量较大,对目标蛋白构象、功能的影响尚无明确报道,且融合突变体FC标签对最终蛋白的ADCC效应是否有影响也尚未明确,同时在抗体药开发中也会因标签的相似性而造成检测的不便。
发明内容
为解决现有技术存在的缺陷,本发明提供一种CD3抗原的制备方法及应用。
为了解决上述技术问题,本发明提供了如下的技术方案:
本发明提供一种CD3抗原,所述抗原为由两个质粒共转形成的异二聚体,第一个质粒为CD3D胞外区通过Linker1融合Acidic Tail及C端6*His构成质粒A,第二个质粒为CD3E胞外区通过Linker2融合Base Tail构成质粒B;
其中,CD3D胞外区的氨基酸序列如SEQ ID NO:1所示;CD3E胞外区氨基酸序列如SEQ ID NO:2所示;Acidic Tail的氨基酸序列如SEQ ID NO:3所示;Base Tail的氨基酸序列如SEQ ID NO:4所示;Linker1的氨基酸序列如SEQ ID NO:5所示;Linker2的氨基酸序列如SEQ ID NO:6所示;6*His的氨基酸序列如SEQ ID NO:7所示。
作为本发明的一种优选技术方案,本发明还提供一种CD3抗原的制备方法,包括以下步骤:
S1、CD3抗原不同亚基表达载体的构建:
将CD3D胞外区通过Linker1融合Acidic Tail及C端6*His构成质粒A、CD3E胞外区通过Linker2融合Base Tail构成质粒B后,分别构建到哺乳细胞表达载体pcDNA3.1(+),酶切位点EcoRI、HindIII;
片段PCR扩增后,无缝克隆连接至载体,转化DH5α,测序正确后中抽质粒用于转染;
S2、CD3抗原异源二聚体的表达纯化:
S21、质粒A和质粒B 以1:1比例共转 Hek293细胞,转染5天后,离心收集细胞上清进行纯化;
S22、培养上清补加500mM NaCl后挂镍柱纯化获得CD3D&CD3E异源二聚体蛋白。
作为本发明的一种优选技术方案,所述步骤S22具体包括以下步骤:
第一步平衡 :用平衡缓冲液平衡柱子,直至 pH 达到 8.0,紫外检测读数稳定,检测调零后上样;
第二步上样 :样品应保持澄清,以一定流速上样;
第三步平衡 :上样结束,用平衡缓冲液平衡层析柱,直到紫外检测读数回到基线或相对稳定;
第四步预洗 :用预洗缓冲液预洗,收集洗脱组分;
第五步洗脱 :用洗脱液洗脱目标蛋白,收集洗脱组分;
第六步洗柱 :用洗柱缓冲液冲洗层析柱,收集洗脱组分,洗脱收集到的组分为CD3D异源二聚体蛋白和CD3E异源二聚体蛋白。
作为本发明的一种优选技术方案,平衡缓冲液为20mM PB和300mM NaC l混合液,pH7.4;预洗缓冲液为20mM PB、300mM NaCl和20mM 咪唑混合液,pH7.4;洗脱液为20mM PB、300mM NaCl和100-500mM 咪唑混合液,pH7.4。
作为本发明的一种优选技术方案,本发明还提供一种CD3D&CD3E异源二聚体蛋白,所述CD3D&CD3E异源二聚体蛋白采用CD3抗原的制备方法制备获得,所述CD3D&CD3E异源二聚体蛋白与CD3抗体UCHT1展示出较好的亲和力。
作为本发明的一种优选技术方案,本发明还提供一种CD3D&CD3E异源二聚体蛋白在其它异源二聚体蛋白构建表达制备方式中的应用,所述CD3D&CD3E异源二聚体蛋白采用CD3抗原的制备方法制备获得。
作为本发明的一种优选技术方案,本发明还提供一种CD3D&CD3E异源二聚体蛋白在抗体筛选及评价中的应用,所述CD3D&CD3E异源二聚体蛋白采用CD3抗原的制备方法制备获得。
本发明相较于现有技术,具有以下有益效果:本发明采用在CD3不同亚基上通过Linker分别融合表达一组小标签Acidic Tail和Base Tail的方法,可以提高异源二聚体比例,融合标签小,对蛋白影响小,制备便捷,一步提纯,二聚体比例HPLC达到95%以上,且与CD3抗原抗体UCHT1展示较好的亲和力。
附图说明
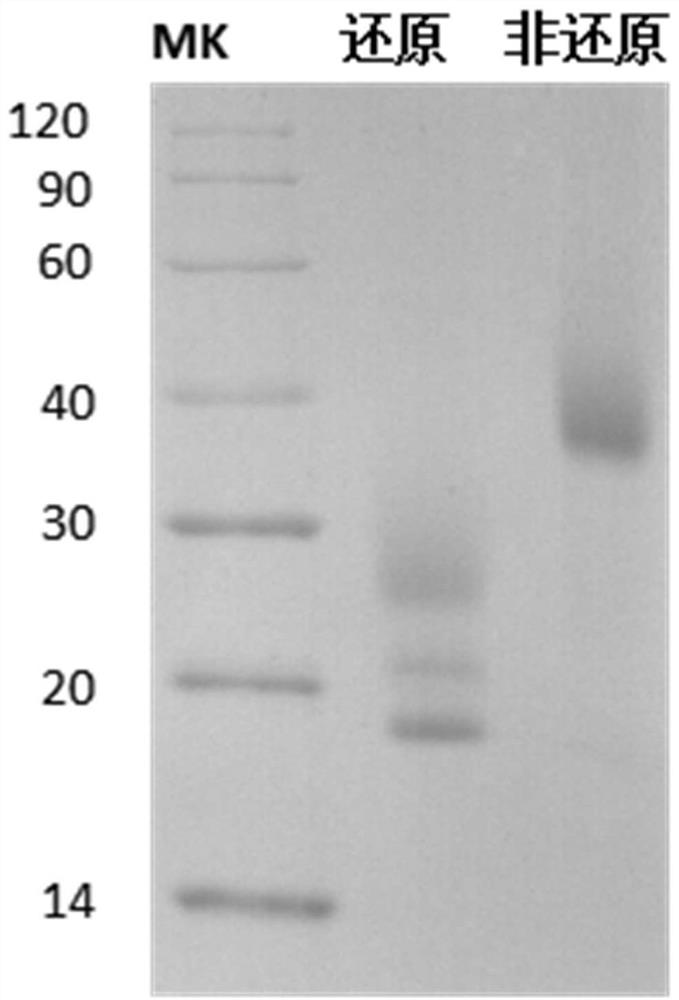
图1是本发明中CD3D&CD3E异源二聚体蛋白的SDS-PAGE电泳示意图。
图2是本发明中CD3D&CD3E异源二聚体蛋白的SEC-HPLC的示意图。
图3是本发明中CD3D&CD3E异源二聚体蛋白与CD3抗体UCHT1结合的Elisa曲线的示意图。
具体实施方式
以下结合附图对本发明的优选实施例进行说明,应当理解,此处所描述的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
本实施例提供一种CD3抗原,所述抗原为由两个质粒共转形成的异二聚体,第一个质粒为CD3D胞外区通过Linker1融合Acidic Tail及C端6*His构成质粒A,第二个质粒为CD3E胞外区通过Linker2融合Base Tail构成质粒B;
其中,CD3D胞外区的氨基酸序列如SEQ ID NO:1所示;CD3E胞外区氨基酸序列如SEQ ID NO:2所示;Acidic Tail的氨基酸序列如SEQ ID NO:3所示;Base Tail的氨基酸序列如SEQ ID NO:4所示;Linker1的氨基酸序列如SEQ ID NO:5所示;Linker2的氨基酸序列如SEQ ID NO:6所示;6*His的氨基酸序列如SEQ ID NO:7所示。
本发明还提供一种CD3抗原的制备方法,包括以下步骤:
S1、CD3抗原不同亚基表达载体的构建:
将CD3D胞外区(含自身信号肽)通过Linker1融合Acidic Tail及C端6*His构成质粒A、CD3E胞外区(含自身信号肽)通过Linker2融合Base Tail构成质粒B后,分别构建到哺乳细胞表达载体pcDNA3.1(+)(购自上海英骏生物科技有限公司),酶切位点EcoRI、HindIII;所有引物和扩增所需基因模板由苏州金唯智生物科技有限公司合成, 构建所用引物如表1所示。
具体地,针对质粒A: CD3D亚基的克隆构建,首先使用引物pcDNA3.1-CD3D-F和CD3D-R扩增出CD3D信号肽及其胞外区片段,然后分别利用引物CD3D-Linker1-F和CD3D-His-R、扩增出抗Linker1+Acidic Tail+C-6*His基因序列;
针对质粒B: CD3E亚基的克隆构建,首先使用引物pcDNA3.1-CD3E-F和CD3E-R扩增出信号肽及其胞外区片段,然后CD3E-Linker2-F和CD3E-Base tail-R扩增出Linker 2+Base Tail的基因序列;
扩增完毕后,利用NovoRec® PCR一步定向克隆试剂盒(吴江近岸蛋白质科技有限公司自产)分别拼接2个亚基各自胞外区、linker及相应的Tail基因序列并无缝克隆至经EcoRI和HindIII线性化处理的pcDNA3.1表达载体上,转化大肠杆菌DH5,利用菌落PCR进行阳性克隆鉴定,鉴定为阳性的重组子(重组质粒)进行测序鉴定。CD3D胞外区通过Linker1融合Acidic Tail及C端6*His构成质粒A、CD3E胞外区通过Linker2融合Base Tail构成质粒B,随后将测序正确的重组子(重组质粒)安排质粒中抽,用于Hek293细胞的转染。
表1. CD3抗原不同亚基基因克隆中使用的引物
经测序获知,CD3D亚基和CD3E亚基表达质粒基因序列正确,均与预期相符。
S2、CD3抗原异源二聚体的表达纯化:
S21、质粒A和质粒B 以1:1比例共转 Hek293细胞,转染5天后,离心收集细胞上清进行纯化;
S22、培养上清补加500mM NaCl后挂镍柱纯化获得CD3D&CD3E异源二聚体蛋白,具体包括以下步骤:
第一步平衡 :用平衡缓冲液平衡柱子,直至 pH 达到 8.0,紫外检测读数稳定,检测调零后上样;平衡缓冲液为20mM PB和300mM NaC l混合液,pH7.4;
第二步上样 :样品应保持澄清,以一定流速上样;
第三步平衡 :上样结束,用平衡缓冲液平衡层析柱,直到紫外检测读数回到基线或相对稳定;
第四步预洗 :用预洗缓冲液预洗,收集洗脱组分;预洗缓冲液为20mM PB和 300mMNaCl,20mM 咪唑混合液,pH7.4;
第五步洗脱 :用洗脱液洗脱目标蛋白,收集洗脱组分;洗脱液为20mM PB、 300mMNaCl和100mM 咪唑混合液,pH7.4;
第六步洗柱 :用洗柱缓冲液冲洗层析柱,收集洗脱组分,洗脱收集到的组分为CD3D&CD3E异源二聚体蛋白;洗柱缓冲液为20mM PB、300mM NaCl和500mM 咪唑混合液,pH7.4。
分步洗脱,分步收集各个洗脱组分。依据SDS-PAGE检测结果确定第六步洗脱收集到的组分为最终所需要的样品。
其中,洗脱组分SDS-PAGE如图1所示;最后得到所需的CD3D&CD3E异源二聚体蛋白纯度经SDS-PAGE检测大于95%,如图2所示,同时使用SEC-HPLC检测发现异源二聚体蛋白均一度较好,纯度也在95%以上,如图3所示。
S3、Elisa检测CD3抗原异源二聚体与UCHT1抗体结合活性:
ELISA操作步骤:
S31.重组抗原包被:S2纯化获得的CD3D&CD3E异源二聚体蛋白包被96孔板,抗原浓度为2μg/ml,包被体积为100μl/孔,包被条件为37℃ 1小时或4℃过夜,包被缓冲液 (PBS)的配方为:3.58g Na
S32.封闭:PBS洗板4次后,加入封闭液PBSA (PBS+2%BSA(V/W)),200μl/孔。37℃封闭1小时;
S33.加样:PBS洗板4次后,分别加入UCHT1抗体(采购自Merck)样品,100μl/孔,37℃孵育1小时,样品梯度配制方法:以20μg/mlUCHT1抗体作为起始浓度,进行3倍梯度稀释12个梯度,每个梯度设置2个复孔;
S34.显色:PBST(PBS+0.05%Tween-20(V/V))洗板4次后,用封闭液PBSA按1/5000稀释HRP标记的显色抗体(购自Abcam公司),按 100μl/孔加入,37℃孵育1小时。PBS洗板4次后,添加显色液TMB(购自KPL公司), 100μl/孔,室温避光显色5~10分钟;
5.终止反应与结果测定:添加终止液(1M HCl), 100μl/孔,在酶标仪上450nm波长下读取吸光值(OD
ELISA结果如图3所示: 图3说明制备的CD3D&CD3E异源二聚体蛋白与市售UCHT1抗体具有良好的体外结合活性,EC50为11.47ng/ml。
为了进一步地优化本发明的实施效果,在本发明的另一种实施方式中,本发明还提供一种CD3D&CD3E异源二聚体蛋白,所述CD3D&CD3E异源二聚体蛋白采用CD3抗原的制备方法制备获得,所述CD3D&CD3E异源二聚体蛋白与CD3抗体UCHT1展示出较好的亲和力。CD3D&CD3E异源二聚体蛋白与CD3抗体UCHT1结合的Elisa曲线的示意图如图3所示。
为了进一步地优化本发明的实施效果,在本发明的另一种实施方式中,本发明还提供一种CD3D&CD3E异源二聚体蛋白在其它异源二聚体蛋白构建表达制备方式中的应用,所述CD3D&CD3E异源二聚体蛋白采用CD3抗原的制备方法制备获得。
为了进一步地优化本发明的实施效果,在本发明的另一种实施方式中,本发明还提供一种CD3D&CD3E异源二聚体蛋白在抗体筛选及评价中的应用,所述CD3D&CD3E异源二聚体蛋白采用CD3抗原的制备方法制备获得。
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
序列表
<110> 吴江近岸蛋白质科技有限公司
<120> 一种CD3抗原的制备方法及应用
<160> 15
<170> SIPOSequenceListing 1.0
<210> 1
<211> 84
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 1
Phe Lys Ile Pro Ile Glu Glu Leu Glu Asp Arg Val Phe Val Asn Cys
1 5 10 15
Asn Thr Ser Ile Thr Trp Val Glu Gly Thr Val Gly Thr Leu Leu Ser
20 25 30
Asp Ile Thr Arg Leu Asp Leu Gly Lys Arg Ile Leu Asp Pro Arg Gly
35 40 45
Ile Tyr Arg Cys Asn Gly Thr Asp Ile Tyr Lys Asp Lys Glu Ser Thr
50 55 60
Val Gln Val His Tyr Arg Met Cys Gln Ser Cys Val Glu Leu Asp Pro
65 70 75 80
Ala Thr Val Ala
<210> 2
<211> 104
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 2
Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys Val
1 5 10 15
Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro Gly
20 25 30
Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp Glu
35 40 45
Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys Glu
50 55 60
Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg Gly
65 70 75 80
Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg Val
85 90 95
Cys Glu Asn Cys Met Glu Met Asp
100
<210> 3
<211> 40
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 3
His Pro Gly Gly Gly Ser Gly Gly Gly Ser Ala Gln Cys Glu Lys Glu
1 5 10 15
Leu Gln Ala Leu Glu Lys Glu Asn Ala Gln Leu Glu Trp Glu Leu Gln
20 25 30
Ala Leu Glu Lys Glu Leu Ala Gln
35 40
<210> 4
<211> 40
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 4
His Pro Gly Gly Gly Ser Gly Gly Gly Ser Ala Gln Cys Lys Lys Lys
1 5 10 15
Leu Gln Ala Leu Lys Lys Lys Asn Ala Gln Leu Lys Trp Lys Leu Gln
20 25 30
Ala Leu Lys Lys Lys Leu Ala Gln
35 40
<210> 5
<211> 10
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 5
His Pro Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10
<210> 6
<211> 10
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 6
His Pro Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10
<210> 7
<211> 6
<212> PRT
<213> 人工序列(Artificial Sequence)
<400> 7
His His His His His His
1 5
<210> 8
<211> 49
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
gctggctagc gtttaaactt aagcttgccg ccaccatgga acatagcac 49
<210> 9
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 9
agccacggtg gctggatcca gc 22
<210> 10
<211> 43
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 10
agctggatcc agccaccgtg gctcaccctg gaggcggaag cgg 43
<210> 11
<211> 47
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 11
tgtgctggat atctgcagaa ttcttaatgg tgatggtgat ggtgctg 47
<210> 12
<211> 49
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 12
gctggctagc gtttaaactt aagcttgccg ccaccatgca gtcgggcac 49
<210> 13
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 13
atccatctcc atgcagttct c 21
<210> 14
<211> 41
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 14
gagaactgca tggagatgga tcaccctgga ggcggaagcg g 41
<210> 15
<211> 49
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 15
tgtgctggat atctgcagaa ttcttactgg gccagtttct tcttcaggg 49
- 靶向CD30的嵌合抗原受体、嵌合抗原受体T细胞及其制备方法和应用
- 一种CD3抗原的制备方法及应用
