发酵乳杆菌以及其或其代谢产物用于制备增肌减脂的组合物之用途
文献发布时间:2023-06-19 19:30:30
技术领域
本发明关于一种发酵乳杆菌,特别是关于一种发酵乳杆菌TCI757(Lactobacillusfermentum TCI757),以及其或其代谢产物用于制备增肌减脂的组合物之用途。
背景技术
现在各类型的交通工具四通八达,生活形态又常处于缺乏运动、或饮食过度的状况,常造成现代人有体重过重的困扰。
虽然重视运动的意识已逐渐升高,然而在忙碌工作之余,运动时间有限之下,如何能提升肌肉量仍是许多人追求的目标。
发明内容
有鉴于此,如何协助现代人更轻松的提升肌肉量,是发明人重要的目标。是以本发明提供一种发酵乳杆菌TCI757,以及其或其代谢产物用于制备增肌减脂的组合物之用途。
在一些实施例中,一种发酵乳杆菌及其或其代谢产物用于制备增肌减脂之组合物的用途,其中发酵乳杆菌为Lactobacillus fermentum TCI757,保藏编号DSM 33914。
在一些实施例中,发酵乳杆菌可以抑制肌肉生长抑制剂。
在一些实施例中,发酵乳杆菌可以促进骨骼肌细胞增生。
在一些实施例中,发酵乳杆菌可以促进鸢尾素分泌量提升。
在一些实施例中,发酵乳杆菌可以提升脂联素分泌量。
在一些实施例中,发酵乳杆菌可以抑制脂肪堆积。
在一些实施例中,发酵乳杆菌可以减少体重。
在一些实施例中,发酵乳杆菌可以降低体脂肪重量。
在一些实施例中,发酵乳杆菌可以降低内脏脂肪面积。
在一些实施例中,发酵乳杆菌可以提升握力。
在一些实施例中,发酵乳杆菌的有效剂量系100mg/天,其中发酵乳杆菌含量为10
在一些实施例中,一种可增肌减脂的食品,其中包含至少100mg的发酵乳杆菌,发酵乳杆菌系为Lactobacillus fermentum TCI757,保藏编号DSM 33914。
综上所述,任一实施例的发酵乳杆菌TCI757及其或其代谢产物可以抑制肌肉生长抑制剂、促进骨骼肌细胞增生、促进鸢尾素分泌量提升、提升脂联素分泌量、抑制脂肪堆积、减少体重、降低体脂肪重量、降低内脏脂肪面积、提升握力,从而达到增肌减脂的用途。
附图说明
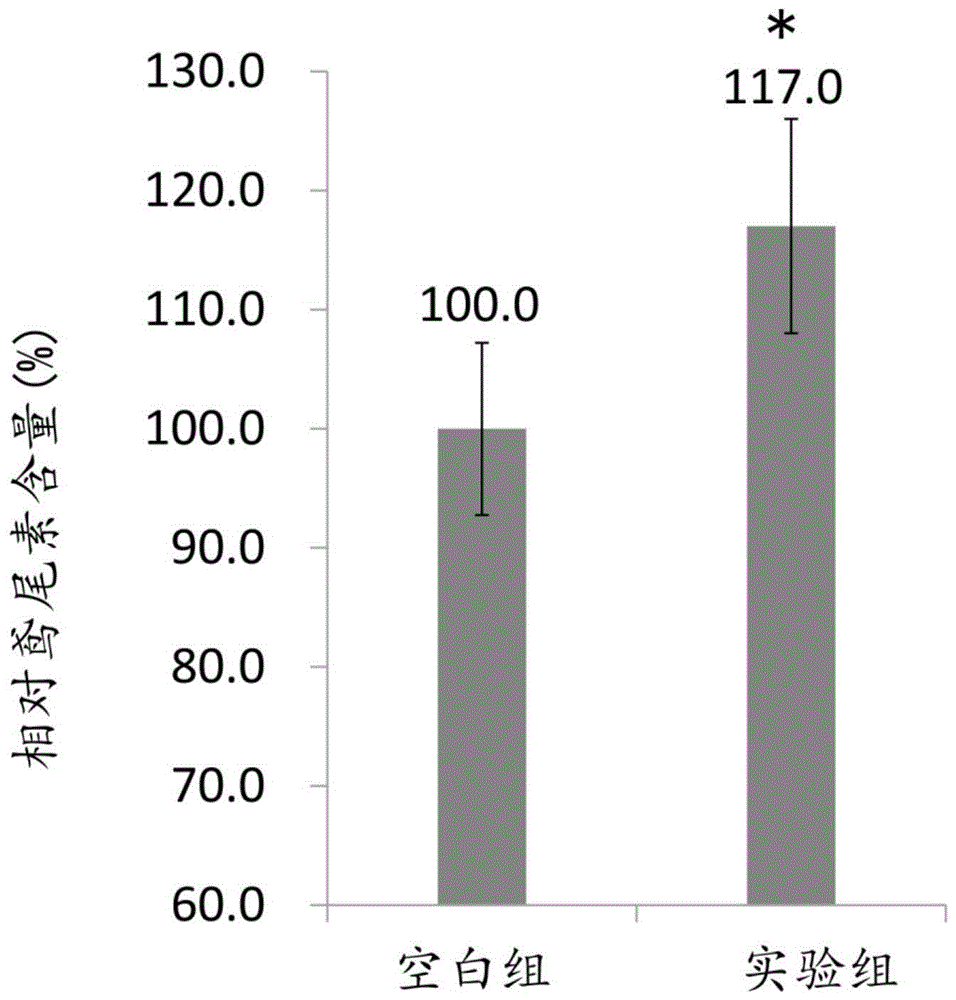
图1是发酵乳杆菌TCI757于促进鸢尾素分泌量测试的结果图。
图2是发酵乳杆菌TCI757于提升脂联素分泌量测试的结果图。
图3是发酵乳杆菌TCI757的抑制脂肪堆积测试的细胞状态图。
图4是发酵乳杆菌TCI757于抑制脂肪堆积测试的结果图。
图5是发酵乳杆菌TCI757的抑制肌肉生长抑制剂测试结果图。
图6是发酵乳杆菌TCI757的促进骨骼肌细胞增生测试的细胞状态图。
图7是发酵乳杆菌TCI757于促进骨骼肌细胞增生测试的结果图。
图8是发酵乳杆菌TCI757的人体实验体重变化结果图。
图9是发酵乳杆菌TCI757的人体实验体脂肪重量变化结果图。
图10是发酵乳杆菌TCI757的人体实验体脂率变化结果图。
图11是发酵乳杆菌TCI757的人体实验内脏脂肪面积重量变化结果图。
图12是发酵乳杆菌TCI757的人体实验体握力变化结果图。
生物材料的保藏
发酵乳杆菌TCI757保藏于德国微生物菌种保藏中心(德国);2021年6月24日;保藏编号为DSM 33914。
具体实施方式
发酵乳杆菌TCI757(Lactobacillus fermentum TCI757),是分离自印度尼西亚天贝的菌株。发酵乳杆菌TCI757以保藏编号BCRC 911064保藏于财团法人食品工业发展研究所,以及以保藏编号DSM 33914保藏于德国微生物菌种保藏中心,保藏日期为2021年6月24日。
发酵乳杆菌TCI757为一种乳杆菌属(Lactobacillus)的革兰氏阳性杆菌,属于兼性厌氧菌。
在一些实施例中,发酵乳杆菌TCI757或其代谢产物用于制备增肌减脂之组合物的用途,其中发酵乳杆菌TCI757是保藏于财团法人食品工业发展研究所其保藏编号为BCRC911064的发酵乳杆菌,以及保藏在德国微生物菌种保藏中心其保藏编号为DSM 33914的发酵乳杆菌。
在一些实施例中,发酵乳杆菌TCI757可以抑制肌肉生长抑制剂。
在一些实施例中,发酵乳杆菌TCI757可以促进骨骼肌细胞增生。
在一些实施例中,发酵乳杆菌TCI757可以促进鸢尾素分泌量提升。
在一些实施例中,发酵乳杆菌TCI757可以提升脂联素分泌量。
在一些实施例中,发酵乳杆菌TCI757可以抑制脂肪堆积。
在一些实施例中,发酵乳杆菌TCI757可以减少体重。
在一些实施例中,发酵乳杆菌TCI757可以降低体脂肪重量。
在一些实施例中,发酵乳杆菌TCI757可以降低内脏脂肪面积。
在一些实施例中,发酵乳杆菌TCI757可以提升握力。
在一些实施例中,发酵乳杆菌TCI757的有效剂量系100mg/天,其中发酵乳杆菌含量为10
在一些实施例中,前述之组合物包含特定含量的发酵乳杆菌TCI757或其代谢产物。
在一些实施例中,前述之组合物可为医药品。换言之,此医药品包含有效剂量的发酵乳杆菌TCI757或其代谢产物。
在一些实施例中,前述之医药品可利用熟习此技艺者所详知的技术而被制造成适合于经肠道地、非经肠道地(parenterally)、口服的、或局部地(topically)投药剂型。
在一些实施例中,经肠道或口服的投药剂型可为,但不限于,锭剂(tablet)、片剂(troche)、口含锭(lozenge)、丸剂(pill)、胶囊(capsule)、分散性粉末(dispersiblepowder)或细颗粒(granule)、溶液、悬浮液(suspension)、乳剂(emulsion)、糖浆(syrup)、酏剂(elixir)、浓浆(slurry)或类似之物。在一些实施例中,非经肠道地或局部地投药剂型可为,但不限于,注射品(injection)、无菌的粉末(sterile powder)、外部制剂(externalpreparation)或类似之物。在一些实施例中,注射品的投药方式可为皮下注射(subcutaneous injection)、表皮内注射(intraepidermal injection)、皮内注射(intradermal injection)或病灶内注射(intralesional injection)。
在一些实施例中,前述之医药品可包含被广泛地使用于药物制造技术之医药上可接受的载剂(pharmaceutically acceptable carrier)。在一些实施例中,医药上可接受的载剂可为下列载剂中一种或多种:溶剂(solvent)、缓冲液(buffer)、乳化剂(emulsifier)、悬浮剂(suspending agent)、分解剂(decomposer)、崩解剂(disintegrating agent)、分散剂(dispersing agent)、黏结剂(binding agent)、赋形剂(excipient)、安定剂(stabilizing agent)、螯合剂(chelating agent)、稀释剂(diluent)、胶凝剂(gellingagent)、防腐剂(preservative)、润湿剂(wetting agent)、润滑剂(lubricant)、吸收延迟剂(absorption delaying agent)、脂质体(liposome)以及类似之物。关于选用之载剂的种类与数量是落在熟习此项技术之人士的专业素养与例行技术范畴内。在一些实施例中,作为医药上可接受的载剂的溶剂可为水、生理盐水(normal saline)、磷酸盐缓冲液(phosphate buffered saline,PBS)、或含有醇的水性溶液(aqueous solutioncontaining alcohol)。
在一些实施例中,前述之组合物可包括食品产品,该食品产品包含特定含量的发酵乳杆菌TCI757或其代谢产物。
在一些实施例中,食品产品可为一般食品、保健食品或膳食补充品。换言之,此一般食品、保健食品(health foods)或膳食补充品包含有效剂量的发酵乳杆菌TCI757或其代谢产物。
在一些实施例中,前述之食品产品可利用熟习此技艺者所详知的技术而被制造成适合于口服的剂型。在一些实施例中,前述之一般食品可为食品产品本身或为另一食品产品的添加物(food additive)。在一些实施例中,一般食品可为但不限于:饮料(beverages)、发酵食品(fermented foods)、烘培产品(bakery products)或调味料。
例1:菌种鉴定
首先,将分离自天贝的分离菌株进行菌种鉴定。透过聚合酶连锁反应(PCR)得到此分离菌株的16S核醣体基因(16SrDNA)序列(即SEQ ID NO:1)。接着,将SEQ ID NO:1序列以美国国家生物技术信息中心(NCBI)网站与其他发酵乳杆菌(如表一所示)之16S核醣体基因(16SrDNA)进行序列比对后可知,此分离菌株的16SrDNA序列与其他发酵乳杆菌(Lactobacillus fermentum)的相似性为98.78%(如表一所示)。因此,将此分离菌株命名为发酵乳杆菌TCI757。
于此,上述天贝采购自印度尼西亚(Toko Indofamily Rui An公司,品名:KERIPIKTEMPE SAGU ORIGINAL),天贝(Tempeh)又称丹贝,是一种印度尼西亚的传统发酵食品,由黄豆制成。天贝是将生黄豆去皮、加热煮熟后,发酵而成。
表一
例2:发酵乳杆菌TCI757的保存及培育实验
首先,使用液态培养基(MRS)培养分离所得的发酵乳杆菌TCI757以得到菌液,然后将菌液与甘油以4:1的比例混合。之后,将菌液与甘油的混合液置于-80℃下进行保存。
接下来,将发酵乳杆菌TCI757以1%的植菌量(约1x10
将发酵乳杆菌TCI757菌液以5000rpm转速进行离心5分钟取得上清液,将上清液以0.2μm的滤膜进行过滤,所得滤液即为TCI757样品(即TCI757样品含有发酵乳杆菌TCI757之代谢产物)。
例3:促进鸢尾素分泌测试
鸢尾素(Irisin)是人体运动时肌肉分泌的一种运动激素,可使白色脂肪转化为棕色脂肪细胞,并促进骨骼肌增生。鸢尾素来自于FNDC5基因,在骨骼肌运动的情况下会促使FNDC5基因转译FNDC5蛋白水解而产生鸢尾素。
3-1.测试材料及设备说明:
细胞株:小鼠骨骼肌肉细胞(mouse skeletal muscle cells,以下称C2C12细胞;购自
前处理培养基:3.7克/升碳酸氢钠(sodium bicarbonate)、10体积%FBS(品牌:Gibco)及1体积%盘尼西林-链霉素的DMEM培养基(Dulbecco's Modified Eagle Medium)。
处理培养基:1体积%FBS及1体积%马血清(horse serum)的DMEM培养基。
纤连蛋白第三类含域蛋白5(FNDC5)之ELISA测试套组,ELISA Kit forFibronectin Type III Domain Containing Protein 5(FNDC5)(USCN;Cat.SEN576Mu)。
3-2.测试流程:
于此,以例2所培育的TCI757样品作为测试样品。检测小鼠肌肉纤维细胞C2C12经过测试样品处理后,能否提升细胞内鸢尾素(FNDC5/Irisin)含量。于此。实验进行三次重复。
首先,将小鼠骨骼肌肉细胞以每孔1×10
接下来,将细胞分为空白组及实验组,空白组未加入测试样品,实验组加入0.125%浓度的代测样品,培养48小时得到各组培养液。
后续,各组取出300μL/well的培养液,置于1.5mL微量离心管。再以10,000g于4℃将微量离心管进行离心10分钟,并收集上清液。
将上清液,使用ELISA测试套组检测细胞中的FNDC5/Irisin含量。
3-3.实验结果:
所得结果利用Excel软件进行student t-test以决定两个样本群体之间是否在统计上具有显著差异,如图1所示(图式中「*」代表p值小于0.05,「**」代表p值小于0.01,以及「***」代表p值小于0.001。当「*」越多时,代表统计上的差异越显著)。
请参阅图1。相较于空白组(即其相对鸢尾素含量视为100%),实验组的相对鸢尾素含量为117%。换言之,实验组的相对鸢尾素含量相对于空白组明显上升17%。由此可知,发酵乳杆菌TCI757对于能有效促进肌肉细胞分泌鸢尾素。进而促进白色脂肪转化为棕色脂肪,并且加速脂肪产热代谢。
例4:促进脂联素分泌测试
脂联素由脂肪细胞(adipocytes)所分泌一种功能性胜肽,其跟维持体内葡萄糖及脂质的代谢平衡有关,脂联素提升可以降低脂肪堆积,促进肌肉细胞燃烧脂肪转换成能量,更进一步也可预防冠状动脉疾病。
4-1.测试材料及设备说明:
细胞株:采用小鼠骨髓基质细胞(后续简称OP9细胞),OP9细胞购自美国典型培养物保存中心(American Type Culture Collection,
培养基:以Alpha-MEM细胞培养液(Minimum Essential Medium Alpha Medium,购自Gibco,美国,Cat.12000-022)为基底、添加20%之胎牛血清(Fetal Bovine Serum,购自Gibco,美国,Cat#10437-028),且加入0.1%之抗生素(Antibiotic-Antimycotic,购自Gibco,美国,Cat.15240-062)。
脂联素检测试剂套组(购自CUSABIO,型号CSB-E07272m)进行检测。
4-2.测试流程:
于此,以例2所培育的TCI757样品作为测试样品。检测分化后的脂肪细胞经过测试样品处理后,能否提升细胞内脂联素的含量。于此。实验进行三次重复。
取24孔培养盘,将每孔接种8×10
然后,将分化完成的脂肪细胞分为以下二组,系为空白组及实验组,空白组未加入测试样品,实验组加入0.25%浓度的代测样品,培养48小时得到各组培养液。
在37℃下培养24小时之后,将孔内培养液移至1.5mL微量离心管。于2℃至8℃以1000xg离心15分钟,将离心后的上清液移至新的1.5ml微量离心管,接着将上清液稀释2000倍,接着以脂联素检测试剂套组进行检测。
最终,以ELISA读取仪(BioTek)读取各组之OD548nm读值(O.D.值越大,表示脂联素的含量越高)。经过吸光值的比较换算并乘回稀释倍数,在空白组的脂联素含量为100%时,换算实验组的脂联素含量如图2。
4-3.实验结果:
所得结果利用Excel软件进行student t-test以决定两个样本群体之间是否在统计上具有显著差异,如图2所示(图式中「*」代表p值小于0.05,「**」代表p值小于0.01,以及「***」代表p值小于0.001。当「*」越多时,代表统计上的差异越显著)。
请参阅图2。相较于空白组(即其相对脂联素含量视为100%),实验组的相对脂联素含量为146.9%。换言之,实验组的相对脂联素含量相对于空白组明显上升46.9%。由此可知,发酵乳杆菌TCI757对于能有效促进脂肪细胞分泌脂联素。进而促进白色脂肪转化为棕色脂肪,并且加速脂肪产热代谢,本发明的发酵乳杆菌TCI757菌株具有效提升脂联素含量,具有减脂的潜力。
例5:脂质油滴堆积量测试
脂肪细胞内以油滴(Lipid droplet)的形式贮存脂肪。基此,本次试验分析染色后的油滴,以观察细胞内油滴的数量,藉以确认脂肪堆积的状态。后续,再将染剂溶出并分析以作为量化的数值指标。
5-1.测试材料及设备说明:
细株胞:采用小鼠骨髓基质细胞(后续简称OP9细胞),OP9细胞购自美国典型培养物保存中心(American Type Culture Collection,
前脂肪细胞增殖培养基(pre-adipocyte expansion medium):为添加有20vol%FBS(品牌:Gibco)及1vol%盘尼西林-链霉素之最低必需培养基α(Minimum EssentialMedium Alpha,MEMα,品牌:Gibco)。
所使用的分化培养基(differentiation medium):为添加有20vol%FBS(品牌:Gibco)及1vol%盘尼西林-链霉素之MEMα(品牌:Gibco)。
油-红O染色试剂的储备溶液:将油-红O染色试剂(品牌:Sigma)彻底溶解于100%异丙醇(isopropanol,供货商:ECHO)以配制3mg/mL之油-红O染色试剂的储备溶液。为获得可供使用的油-红O工作溶液(oil-red O working solution),于使用前实时将油-红O染色试剂的储备溶液以二次水(ddH
显微镜(品牌zeiss)、ELISA读取仪(厂牌:BioTek)
5-2.测试流程:
首先,以每孔8×10
实验组:依照每孔500μL培养基含有62.5μL的以例2所培育的TCI757样品作为测试样品(即,浓度为0.125%),并将测试样品添加至含分化后的培养基中,在37℃下培养7天。在7天的细胞处理期间每隔3天更换培养基。
空白组:不作任何处理,即不额外添加其他化合物至含分化后的脂肪细胞的分化培养基中,在37℃下培养7天。此7天的细胞处理期间每隔3天更换培养基。
接着,依据下列步骤进行红油O的染色。于7天细胞处理后,将培养基移除,以1mL之磷酸盐缓冲溶液(Phosphate buffered saline,PBS)清洗脂肪细胞两次,再加入1mL之10%甲醛并于室温下反应30分钟以固定脂肪细胞。接着移除甲醛后以1mL之PBS轻轻地清洗脂肪细胞两次,接着于每孔细胞内加入1mL之60%异丙醇,反应1分钟后,移除异丙醇并加入1mL之油红O作用溶液与脂肪细胞反应,于室温下反应1小时,接着移除与脂肪细胞作用的油红O作用溶液并迅速地以1mL之60%异丙醇进将脂肪细胞行脱色5秒钟,使用显微镜观察并拍摄细胞(放大倍率400X),结果示于图3。
后续,将染色后的各组再依下列步骤进行红油O的定量。加入100%异丙醇至各孔中,并置于振荡器(shaker)上反应10分钟以溶解油滴。然后,从各孔中取100μL前述之溶液至96孔培养盘并于510nm的波长下以ELISA读取仪读取各孔的吸光值(OD510nm)。
于量测后,藉由将所测得的吸光值代入下列公式I而计算出脂质油滴堆积量(%)。换言之,是将空白组的脂质油滴堆积量视为100%来计算各组别的脂质油滴堆积量(%),换算结果示于图4。
脂质油滴堆积量(%)=(OD
其中,OD
5-3.实验结果:
参阅图3。观察空白组的细胞可见细胞内红色(深色)的油滴数是明显多于实验组,细胞尺寸也更大。可知,发酵乳杆菌TCI757能有效地抑制脂肪细胞大小,进而达成减肥之功能。
参阅图4。以空白组的脂质油滴堆积量为100%的情况下,而实验组的脂质油滴堆积量只有74.8%。由此可知,发酵乳杆菌TCI757能有效地抑制脂肪累积,具有减少受体的脂肪形成的功能,进而达成减肥之功能。
例6:肌肉生长抑制素基因表现测试
肌肉生长抑制素(Myostatin,MSTN)抑制MSTN可活化卫星细胞而增加肌肉再生。
6-1.测试材料及设备说明:
细胞株:小鼠骨骼肌肉细胞(mouse skeletal muscle cells,以下称C2C12细胞;购自
培养基:以DMEM(Dulbecco’s modified Eagle’s medium,购自Gibco,产品编号12800017),添加10% FBS(Fetal Bovine Serum,购自Gibco,产品编号10437-028)以及1%抗生素(购自Gibco,产品编号15240-062)。
10X DPBS杜氏磷酸盐缓冲液(购自Gibco;Cat.14200-075)。
RIPA裂解与提取缓冲液(Thermo,产品编号#89900)。
6-2.测试流程:
首先,取6孔培养盘将每孔接种1×10
空白组:仅添加培养基,然后在37℃下培养24小时。
对照组:添加0.25%的MRSD,所述MRSD是指养菌时的空培液。
实验组:添加0.25%的依例2所制得的TCI757样品,然后在37℃下培养24小时。
将培养后的各组细胞以400xg进行5分钟离心后去除上清液之后,剩下的细胞以1XDPBS缓冲液清洗后再次以400xg进行5分钟离心,再去除上清液后,加入500μL的RIPA裂解与提取缓冲液以裂解细胞膜而分别形成细胞溶液。
接着,使用RNA萃取试剂套组(购自Geneaid公司,中国台湾,Lot No.FC24015-G)分别收集二组细胞溶液内之RNA。接着,每组取1000纳克(ng)所萃取出的RNA为模板,藉由
目标基因MSTN,所使用引子包括:引子名称MSTN-F,序列编号SEQID NO:2,序列:TTCCGGTTCCTTTTCCCTT,长度577bp。引子名称MSTN-R,序列编号SEQID NO:3,序列:TCTGCAGCTTGTGTTGCTCT,长度577bp。
参考图5。将空白组的MSTN基因的表现量视为1时,对照组的MSTN基因的表现量为0.68,而实验组相对于空白组的MSTN基因的表现量为0.19,也就是说,相较于空白组,实验组的MSTN基因的表现量显著地的减少达81%。即便是和一般常用的抑制剂MRSD相比,也具有更佳的效果。
需要特别说明的是,图5中显示的系以相对倍率呈现,即将空白组的定量结果视为1来将实验组的定量结果换算成相对于空白组的表现量。其中,使用Excel软件之STDEV公式计算标准偏差,并在Excel软件中以单尾学生t检验(Student t-test)分析是否具有统计上的显著差异。图式中,「*」代表相对于空白组p值小于0.05,「**」代表相对于空白组p值小于0.01,以及「***」代表相对于空白组p值小于0.001。
由此可知,当肌肉细胞存在有发酵乳杆菌TCI757的情况下,可以明显抑制肌肉生长抑制素相关基因的表现量。也就是说,发酵乳杆菌TCI757可以有效抑制肌肉生长抑制素,从而达到增生肌肉量,而预防肌少症。
例7:骨骼肌细胞增生测试
7-1.测试材料及设备说明:
细胞株:小鼠骨骼肌肉细胞(mouse skeletal muscle cells,以下称C2C12细胞;购自
培养基:以MEMAM细胞培养液(Minimum Essential Medium Alpha Medium,购自Gibco,美国)为基底、添加20%之胎牛血清(Fetal Bovine Serum,购自Gibco,美国,Cat#10437-028),且加入0.1%之青霉素/链霉素(Penicillin-streptomycin,购自Gibco,美国)。
细胞增生ELISA测试剂套组(购自Roche罗氏,型号11647229001),套组中包括细胞固定溶液(FixDenat)、抗BrdU-POD工作溶液(溴化脱氧尿苷BrdU,又称抗体偶联物antibodyconjugate)。
7-2.测试流程:
于此,以例2所培育的TCI757样品作为测试样品。检测分化后的骨骼肌细胞经过测试样品处理后,能否提升细胞数量。于此。实验进行三次重复。
取24孔培养盘,将每孔接种5000个C2C12细胞于96孔盘上,置于二氧化碳培养箱内在37℃下培养2小时。
然后,将C2C12细胞分为以下二组,系为空白组及实验组,实验组加入每孔100μL的代测样品及10μL的BrdU,而空白组仅加入10μL的BrdU而未加入测试样品,在培养24小时得到各组培养液。
各组培养液去除上清液后,加入200μL的细胞固定溶液,室温下处理30分钟。
去除细胞固定溶液后,使用1Xpbs洗涤一次。接着加入每孔的抗BrdU-POD工作溶液,室温下处理90分钟。
之后,去除抗BrdU-POD工作溶液后,使用200到300μL的洗涤液充份冲洗三次后,去除洗涤液再加入100μL的底物溶液(substrate solution),室温下处理15分钟。
接者,每孔加入25μL的1M的H
最终,于显微镜下拍摄照片,如图6所示,并于450nm的波长下以ELISA读取仪读取各孔的吸光值(OD450nm)。经过吸光值的比较换算并乘回稀释倍数,在空白组的细胞数量为100%时,换算实验组的细胞数量量如图7。
7-3.实验结果:
所得结果利用Excel软件进行student t-test以决定两个样本群体之间是否在统计上具有显著差异,如图7所示(图式中「*」代表p值小于0.05,「**」代表p值小于0.01,以及「***」代表p值小于0.001。当「*」越多时,代表统计上的差异越显著)。
请参阅图6。图中蓝色光点为细胞核,绿色光点为新增生的细胞核。相较于空白组,实验组中不论蓝色或绿色光点都明显较多,尤其是绿色光点增加数量更为显著。
请参阅图7。相较于空白组(即其相对细胞数量视为100%),实验组的相对骨骼肌数量为124.6%。换言之,实验组的相对骨骼肌数量相对于空白组明显上升接近25%。由此可知,发酵乳杆菌TCI757对于能有效促进骨骼肌细胞增生,具有增肌的潜力。
例8:人体测试
8-1.样品:采用例2所制备的发酵乳杆菌TCI757所制得的胶囊,内含100mg的菌粉。于此,菌粉系将例2所制备的发酵乳杆菌TCI757菌液加入2.2%(w/w)海藻糖、4.6%(w/w)乳糖及10%(w/w)脱脂奶粉,混合均匀,冷冻干燥后磨粉制成。
8-2.受试者:10位受试者。各受试者为20岁以上,欲减少体脂肪、提升肌肉量者,其中,10位受试者的平均体重为70.88公斤,平均体脂为28.35%。
8-3.测试项目:体重变化、体脂肪重量、体脂率、内脏脂肪面积及手掌握力。
8-4.测试方式:
令10位受试者每日摄取100mg的发酵乳杆菌TCI757所制得的胶囊,并每天持续摄入八周。于开始摄入前(即第0周,又称对照组)及饮用八周后(即第8周,又称为实验组)分别进行量测。
其中,以身体组成分析仪(型号:InBody 770)量测受试者的体重(kg)、体脂肪重量(kg)、体脂率(%)、内脏脂肪面积(cm
其中,利用握力器(型号CAMRY EH101 electronic hand dynamometer)量测受试者的握力(kg)。
8-5.测试结果:
请参阅图8。经过八周的每日摄取100mg的发酵乳杆菌TCI757后,10位受试者的平均体重从70.88kg(第0周)在维持日常饮食与运动量的情况下降至69.91kg(第8周)。使用本发明之发酵乳杆菌TCI757仅8周,其前后的平均体重差异达0.97kg。意即,每日摄取100mg的发酵乳杆菌TCI757可以有效降低体重。
请参阅图9。经过八周的每日摄取100mg的发酵乳杆菌TCI757后,10位受试者的平均体脂肪重量从20.07kg(第0周)在维持日常饮食与运动量的情况下降至19.37kg(第8周)。使用本发明之发酵乳杆菌TCI757仅8周,其前后的平均体脂肪重量差异达0.7kg。意即,每日摄取100mg的发酵乳杆菌TCI757可以有效降低体脂肪重量。
由上述二项数据可知,受试者的平均体重减少0.97kg,而平均体脂肪重量减少0.7kg,可见所减少的体重中,有72%以上是脂肪重量,而非肌肉重量,明显达成增肌减脂的效能。
请参阅图10。经过八周的每日摄取100mg的发酵乳杆菌TCI757后,10位受试者的平均体脂率从28.35%(第0周)在维持日常饮食与运动量的情况下降至27.74%(第8周)。使用本发明之发酵乳杆菌TCI757仅8周,其前后的平均体脂率减少0.61%。意即,每日摄取100mg的发酵乳杆菌TCI757可以有效降低体脂率。
请参阅图11。经过八周的每日摄取100mg的发酵乳杆菌TCI757后,10位受试者的平均内脏脂肪面积从83.13cm
参考图12。经过八周的每日摄取100mg的发酵乳杆菌TCI757后,10位受试者的平均手掌握力从37.8kg(第0周)在维持日常饮食与运动量的情况上升至38.8kg(第8周)。使用本发明之发酵乳杆菌TCI757仅8周,其前后的平均手掌握力增加1kg。意即,每日摄取100mg的发酵乳杆菌TCI757可以有效提升握力,达到改善肌肉力量。
由此可知,使用发酵乳杆菌TCI757及其或其代谢产物可以抑制肌肉生长抑制剂、促进骨骼肌细胞增生、促进鸢尾素分泌量提升、提升脂联素分泌量、抑制脂肪堆积、减少体重、降低体脂肪重量、降低内脏脂肪面积、提升握力,从而达到增肌减脂的功效。
虽然本发明的技术内容已经以较佳实施例揭露如上,然其并非用以限定本发明,任何熟习此技艺者,在不脱离本发明之精神所作些许之更动与润饰,皆应涵盖于本发明的范畴内,因此本发明之保护范围当视后附之申请专利范围所界定者为准。
