针对表皮生长因子受体的单克隆抗体治疗患有低氧血症型急性呼吸衰竭的患者的用途
文献发布时间:2024-04-18 19:59:31
技术领域
本发明涉及生物技术和医学领域并且具体涉及针对表皮生长因子受体的单克隆抗体(MAbs)治疗患有低氧血症型急性呼吸衰竭的患者的用途。
背景技术
低氧血症型急性呼吸衰竭是紧急入院的主要原因。死亡率接近20%。最常见的病因是肺炎、神经系统原因、非肺源性败血症和慢性阻塞性肺病。这种疾病的特征是静息时呼吸困难、动脉O2压力(PO2)小于60mmHg,和/或动脉CO2压力(PCO2)大于45mmHg(Joao D等(2019)J Crit Care 49:84-91;Piriano T等(2019)Respir Care.64(6):638-646)。
呼吸衰竭可能进展至急性呼吸窘迫综合征(ARDS),这是由肺病或并非肺病引起的威胁生命的疾患。(Butt Y和同事们(2016)Arch Pathol Lab Med.;140(4):345-50)。它是导致肺浸润、水肿和低氧的全身发炎性疾病的结果。这一过程在细胞层面上的特征是肺泡毛细血管膜的完整性损失、中性粒细胞过度浸润以及促炎细胞因子和趋化因子释放。(ShanX和同事们(2017)Oncotarget;8(16):26648-61)。在病理层面上,在急性期有肺泡内和间质水肿,在增殖期有II型肺泡细胞增殖,并且在更晚期有纤维化(Poletti V和同事们(2010)Pathologica.102(6):453-63)。
在临床上,ARDS表现为低氧血症,伴有胸部X光显示两侧不透明,这与顺应性下降相关联。在形态上,在ARDS的急性期观察到弥漫性肺泡损伤。ARDS所致的死亡率仍然很高,在35%至46%的范围内。(FergusonND和同事们(2012)Intensive Care Med.;38(10):1573-82;Huppert LA和同事们(2019)Semin Respir Crit Care Med.;40(1):31-9)。存活者可能有持续的病态,这与生活质量显著受损相关联(Butt Y和同事们(2016)Arch PatholLab Med.;140(4):345-50;Huppert LA和同事们(2019)SeminRespir Crit Care Med.;40(1):31-9;Fan E和同事们(2018)JAMA.;319(7):698-710)。
尽管一些通气策略已经改善了急性肺损伤的结果,但使用皮质类固醇或表面活性剂的大多数疗法已经显示出有争议的结果。(Fan E和同事们(2018)JAMA.;319(7):698-710)。
表皮生长因子受体(EGFR)是170kDa膜糖蛋白,它控制基础细胞过程,包括细胞迁移、细胞周期、细胞代谢和存活以及细胞增殖和分化。(ShanX和同事们(2017)Oncotarget;8(16):26648-61;Mendelsohn J,Baselga J.(2006)Semin Oncol.;33(4):369-85;Saba NF和同事们(2006)Oncology;20(2):153-61)。EGFR的生理作用是调控上皮组织发育和体内平衡。(Mendelsohn J,Baselga J.(2006)Semin Oncol.;33(4):369-85)。
EGFR及其配体在源于上皮的多种肿瘤中上调,包括非小细胞肺癌、神经胶质瘤、头颈部肿瘤、子宫颈肿瘤和食道肿瘤(Mendelsohn J,Baselga J.(2006)Semin Oncol.;33(4):369-85)。EGFR在肿瘤中的过度表达与转移增加、存活率降低以及不良预后相关。EGFR的细胞内结构域与特异性蛋白酪氨酸激酶活性相关联,并且EGFR由细胞的过度表现会改变细胞周期调控,阻断细胞凋亡,促进血管生成,增加运动性、细胞粘附性和转移性。(Mendelsohn J,Baselga J.(2006)Semin Oncol.;33(4):369-85;Saba NF和同事们(2006)Oncology;20(2):153-61)。以阻断经由EGFR的信号传导为目的已经开发了数种药物,诸如酪氨酸激酶抑制剂(TKI),包括吉非替尼(gefitinib)、埃罗替尼(erlotinib)和奥希替尼(osimertinib),以及抗EGFR MAb,诸如西妥昔单抗(cetuximab)、帕尼单抗(panitumumab)和尼妥珠单抗(nimotuzumab)。(Mendelsohn J,Baselga J.(2006)Semin Oncol.;33(4):369-85;Saba NF和同事们(2006)Oncology;20(2):153-61;Perez R和同事们(2011)Clinical Effects.Cancers(Basel);3(2):2014-31;Smith D和同事们(2009)BullCancer.;96增刊:S31-40)。
急性呼吸功能不全导致EGFR的正性调控和过度表达。本质上,EGFR激活导致更严重的肺部病变。肺纤维化中的主要节点是EGFR路径,它控制细胞增殖、粘液分泌、发炎反应和组织修复的许多级联。(Venkataraman T,Frieman MB.(2017)Antiviral Res.;143:142-50)。
尽管有这一证据,但在小鼠中,关于EGFR TKI对纤维化的作用有相互矛盾的报道。Suzuki和他的同事们报道了在吉非替尼治疗后纤维化增加。(Suzuki H和同事们(2003)Cancer Res.;63(16):5054-9),然而,Ishii和同事们观测到纤维化减少(Ishii Y,Fujimoto S,Fukuda T.(2006)Am J Respir Crit Care Med.;174(5):550-6)。这种矛盾的原因并不明朗,但小鼠品系和吉非替尼治疗持续时间的变化可以解释这些差异。(Suzuki H和同事们(2003)Cancer Res.;63(16):5054-9;Ishii Y,Fujimoto S,Fukuda T.(2006)AmJ Respir Crit Care Med.;174(5):550-6)。
在肺癌患者中,TKI可能诱导继发于间质性肺炎的急性低氧血症型呼吸衰竭。这种不良事件在1.1%至2.2%的低频率下发生,但可能是致命的,占所有EGFR-TKI治疗相关死亡的58%。(Ohmori T和同事们(2021)Int J Mol Sci.;22(2):792)。日本患者显示出显著更高的肺炎发病率,目前原因不明(Suh CH和同事们(2018)Lung Cancer;123:60-9)。
令人惊讶的是,当向罹患低氧血症型急性呼吸衰竭或ARDS的患者施用尼妥珠单抗时,本发明的发明者观测到炎症中、肺部病变中的通气参数改善以及存活率增加。
发明内容
在一个实施方案中,本发明涉及针对EGFR的MAb治疗导致传染源的低氧血症型急性呼吸衰竭并且特别是归类为ARDS的那些的疾病的用途。
在本发明的一个特定实施方案中,急性呼吸衰竭具有传染源并且可能由选自包含以下的组的微生物引起:冠状病毒、鼻病毒、巨细胞病毒、爱泼斯坦-巴尔病毒(EpsteinBarr)、流感病毒、呼吸道合胞病毒、酿脓链球菌(Streptococcus pyogenes)、肺炎链球菌(Streptococcus pneumoniae)、流感嗜血杆菌(Haemophilus influenza)、大肠杆菌(Escherichia coli)、铜绿假单胞菌(Pseudomonas aeruginosa)、奇异变形杆菌(Proteusmirabilis)、肠杆菌属某些种(Enterobacter spp)、克雷伯氏菌属某些种(Klebsiellaspp)、不动杆菌属某些种(Acinetobacter spp)、葡萄球菌属某些种(Staphylococcusspp)、沙雷氏菌属某种(Serratia sp)、新型隐球菌(Cryptococcus neoformans)、根霉属某种(Rhizopus sp)、曲霉属某些种(Aspergillus spp)、肺孢子虫属某些种(Pneumocystisspp)、毛霉属某种(Mucor sp)和根毛霉属某些种(Rhizomucor spp)。
本发明所预期的可以用于治疗低氧血症型急性呼吸衰竭或ARDS的抗EGFR MAb有尼妥珠单抗、西妥昔单抗和帕尼单抗。
在另一个实施方案中,本发明涉及一种治疗受试者的方法,所述方法包括静脉内或皮下施用1mg/Kg体重至6mg/Kg体重的剂量范围内的抗EGFR mAb至少两次并且最多五次,间隔72小时与168小时之间。
具体实施方式
药物组合物
本发明中所使用的针对EGFR的mAb作为药物组合物的一部分施用,所述药物组合物含有mAb作为活性成分和药理学上适当的赋形剂用于肠道外使用。具体地,这些MAb有尼妥珠单抗,其序列描述于美国专利5,891,996中;西妥昔单抗,描述于美国专利6,217,866B1中;以及帕尼单抗,其序列描述于US 5,558,864 B1中。
治疗应用和治疗方法
本发明描述了抗EGFR抗体治疗急性低氧血症型呼吸衰竭或ARDS的用途。具体地,针对急性呼吸衰竭或呼吸窘迫综合征由感染性因子,例如病毒、细菌或真菌引起的患者的情况来描述用途。具体地,抗EGFR可以用于治疗由诸如冠状病毒、鼻病毒、巨细胞病毒、爱泼斯坦-巴尔病毒、流感病毒和呼吸道合胞病毒等病毒诱发的急性呼吸衰竭或ARDS。在细菌感染的情况下,由链球菌(streptococci)、肺炎双球菌(pneumococci)或葡萄球菌(staphylococci)、流感嗜血杆菌、大肠杆菌、铜绿假单胞菌、奇异变形杆菌、肠杆菌属某些种、克雷伯氏菌属某些种、不动杆菌属某些种和沙雷氏菌属某些种(Serratia spp)引起的那些。当感染性因子是真菌时,这种真菌可能是新型隐球菌、根霉属某些种(Rhizopusspp)、曲霉属某些种、肺孢子虫属某些种、毛霉属某些种(Mucor spp)或根毛霉属某些种。
如本发明中所描述的抗EGFR抗体的使用改善了急性低氧血症型呼吸衰竭或急性呼吸窘迫综合征的症状和征象。
这些症状的减少使得患者有所改善并且由医疗团队更好地管理。所建议的治疗的特别优势是不会诱导患者的免疫缺陷,这与其它基于类固醇或其它免疫抑制剂的常规疗法不同。保留所治疗患者的免疫能力会减少在重症或危重症患者中极为常见的其它机会性感染出现的可能性。
接受抗EGFR抗体疗法的患者优选地获准进入加强或中级护理病房,不过他们也可以在常规病房中。他们至少显示出以下症状:静息时呼吸困难、动脉O2压力(PO2)小于60mmHg和/或动脉CO2压力(PCO2)大于45mmHg、在处于海平面上的室内空气中低氧饱和度(SO2)<94%或需要氧疗法来维持SO2>93%、动脉氧压/吸入氧分数(PaO2/FiO2)的比率<300mm Hg、呼吸速率>30次吸气/分钟或者在超过50%的双肺野中存在浸润物。考虑动脉血气和放射学发现的参数来建立确认性诊断,X光、肺超声波或计算机轴向断层摄影。
其它征象和症状包括呼吸困难、高呼吸速率、心动过速、紫绀、意识模糊、疲劳、低血压、干咳、发热38℃、头痛、神经系统表现。观测到不同实验室参数的变化,诸如:D-二聚体、铁蛋白、LDH、C反应蛋白、IL-6的值增加高于正常界限。
将在1mg/Kg体重与6mg/Kg体重之间的剂量范围内的抗EGFR MAb静脉内或皮下施加于患者,所述剂量分别对应于总共约50与600mg之间。优选地,在抗EGFR抗体尼妥珠单抗的情况下,将使用1.42mg/kg与2.85mg/kg之间的剂量。将向患者施用这些MAb至少两次并且最多有5次剂量。两次连续施用之间的时间将在72与168小时之间。在尼妥珠单抗的情况下,优选时程是每隔72小时两至三次剂量,使用200mg负荷剂量和100mg后续剂量。可以通过评估不同抗EGFR MAb识别EGFR的能力来调整有待用于这些抗EGFR MAb的剂量和时程。
本发明的另一个标的是抗EGFR抗体与抗病毒疗法或抗生素的连续或伴随组合。有待组合的可能抗生素尤其有头孢菌素家族的那些,诸如头孢曲松(ceftriaxone);大环内酯类,诸如阿奇霉素(azithromycin);糖肽类,诸如万古霉素(vancomycin);β-内酰胺类,诸如美罗培南(meropenem);以及噁唑烷酮类,诸如利奈唑胺(linezolid)。有待组合的可能抗病毒剂尤其有1型和2型干扰素;用于治疗HIV的抗逆转病毒剂,诸如瑞德西韦(remdesivir)。有待使用的抗生素或抗病毒方案将为常规用于每种药物的那些方案,而使用抗EGFR抗体的方案将响应于上文已描述的方案。
另外,本发明的标的是抗EGFR抗体与其它消炎疗法或抗凝剂疗法的连续或伴随组合,所述疗法诸如类固醇或其它免疫调节药物,以及抗凝剂疗法,诸如低分子量分级肝素或未分级肝素、肝素钠。
附图说明
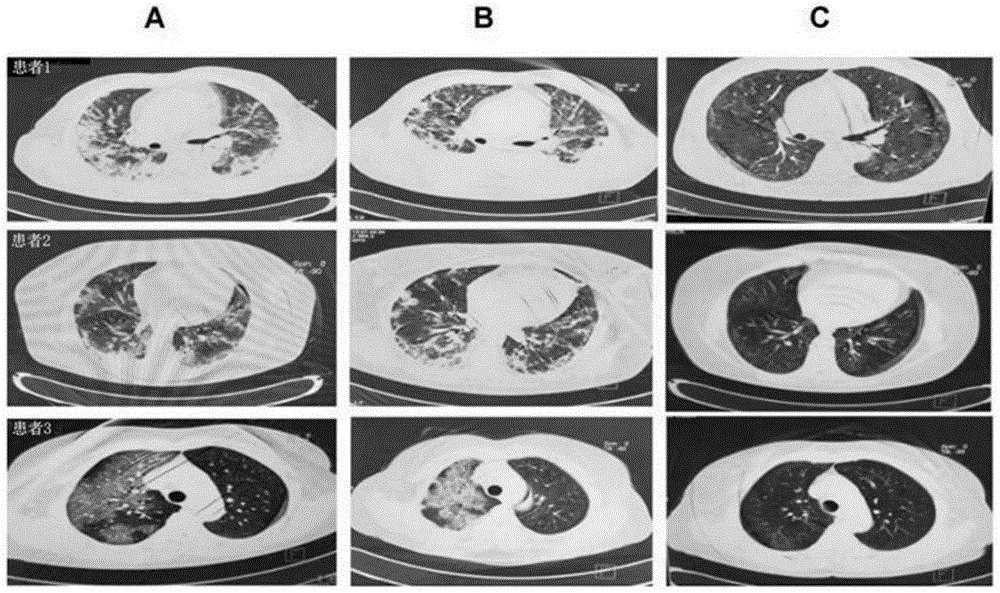
图1.用尼妥珠单抗治疗的3名患者的轴向胸部计算机断层扫描。连续图像A)入院时,B)出院时,以及C)随访(出院后30-60天)。
图2.在尼妥珠单抗施用前后PaO2/FiO2比率随时间而变的行为。
图3.在尼妥珠单抗施用前后乳酸脱氢酶(LDH)酶浓度的变化。
图4.在尼妥珠单抗治疗前后三名患者的放射学演化:A)患者JMTR,B)患者JHV,C)患者MESS。
图5.用尼妥珠单抗治疗的COVID-19患者的总体演化。
图6.用尼妥珠单抗治疗的患者的D-二聚体值。
实施例
实施例1.尼妥珠单抗的使用会降低患有低氧血症型急性呼吸衰竭的患者的SARS-CoV-2死亡率。
经诊断有SARS-CoV-2并且临床、放射学或实验室证据显示低氧血症型急性呼吸衰竭或呼吸窘迫综合征的十四名患者静脉内接受200-mg剂量的单克隆抗体尼妥珠单抗。在第一剂后72小时,所有患者都接受等效于100mg的第二剂。
为了评估对研究性产品使用的影响,选择一组对SARS-CoV-2呈阳性、归类为重度并且在古巴的20家医院中接受类固醇和抗凝剂的并行治疗的患者作为对照。
表1.用尼妥珠单抗治疗的重病患者的死亡率。
表1显示,与对照组相比,尼妥珠单抗的使用将死亡率降低16%。在国际上,在使用包括抗凝剂和类固醇的最佳支持疗法并且在一些患者中使用抗IL6受体抗体(托珠单抗(tocilizumab))之后,重度COVID-19患者的存活率在77%至81%的范围内(RC集团(2021)Lancet;397(10285):1637-45;Rosas IO和同事们(2021)N Engl J Med.;384(16):1503-16)。与古巴协议(Cuban protocol)中确立的疗法组合的尼妥珠单抗的恢复数据(92.85%)与古巴对照患者(77%)和跨国试验(77-81%)相比非常有利。
对三名用尼妥珠单抗治疗的患者进行轴向胸部计算机断层扫描。图1A和B显示了大面积的毛玻璃样不透明、渗出期的气腔实变以及组织期和纤维化期的肺体积减小。相比之下,图1C显示,3名患者显示出肺部炎性病变消退并且没有纤维化征象。
实施例2.尼妥珠单抗的使用会改善所治疗患者的通气参数。
在10名重病COVID-19患者中,计算动脉氧压(PaO2)与吸入氧分数(FiO2)之间的比率作为通气参数之一。图2显示了在尼妥珠单抗之前以及间隔72小时的2剂抗体之后这种比率随时间而变的行为。如图中所见,患者显示出肺通气随时间而变的改善。
实施例3:尼妥珠单抗的治疗会改善所治疗患者的炎症参数。
作为8名重度COVID-19患者的炎症的量度,在尼妥珠单抗治疗前后测量LDH和IL-6,后者通过ELISA(Quantikine)进行。在单克隆抗体施用前,所有患者都用类固醇治疗。
图3显示,在2剂MAb尼妥珠单抗后LDH减少。
表2显示了在尼妥珠单抗治疗前和治疗的不同时间IL-6的浓度。
表2.在尼妥珠单抗治疗前和治疗的不同时间IL-6值的变化。
在8名患者的5名中,第0天和第7天血清IL-6浓度的降低是显著的(p=0.048,弗里德曼检验(Friedman's test),第0天对比第7天,p=0.03,邓恩检验(Dunn's test))。在患者MVH中,在48小时IL-6增加(但保持低于平均值),然后减少,而在RGR患者中,IL-6浓度保持稳定。鉴于这种明显的增加趋势是疾病自然史的一部分,在这7名患者中,将演化归类为有利的。在MAST患者中,IL-6增加,这与迟缓的病程相关。
实施例4.尼妥珠单抗治疗会改善受多灶性间质性肺炎影响的区域。
在2剂尼妥珠单抗后具有不同时间的COVID-19演化的8名患者中,计算双肺野(右肺和左肺)的受影响区域的百分比。这些结果示于表3中。
表3.受影响的肺体积的百分比。
*结果示为双肺野的总和。
总之,在第一剂单克隆抗体后168小时,尼妥珠单抗的使用改善了62.5%的所治疗患者中的受影响区域。在1名患者中,双肺野的受影响区域没有变化,而在2名患者中,在演化第七天受影响区域仅增加10%。图4显示了在尼妥珠单抗治疗前后这些患者中的三名的放射学演化。
实施例4.由COVID-19引起的ARDS患者在尼妥珠单抗治疗后具有临床改善。
考虑到在这些评估的每个评估中常规测量的一些参数的改善,对这些患者的总体演化(临床、放射学和实验室)进行评估。图5显示,总之,在第一剂尼妥珠单抗后一周,75%的患者显示出临床改善的征象。
实施例5.尼妥珠单抗治疗会引起重度COVID-19患者中的D-二聚体减少。
对于用尼妥珠单抗和古巴协议中所包括的用于控制这种疾病的其余药物治疗的两名COVID-19患者,测量了他们的D-二聚体。图6显示,在尼妥珠单抗与古巴协议中针对COVID-19所提供的其余疗法组合后,两名患者的D-二聚体均显著减少。有必要澄清,甚至在抗凝剂(分级肝素)、类固醇和其它免疫调节剂治疗下,两名患者也达到高水平的D-二聚体。
权利要求书(按照条约第19条的修改)
1.单克隆抗体尼妥珠单抗治疗导致低氧血症型急性呼吸衰竭的疾病的用途。
2.根据权利要求1所述的用途,其中所述低氧血症型急性呼吸衰竭是急性呼吸窘迫综合征。
3.根据权利要求1-2中任一项所述的用途,其中所述疾病具有传染源。
4.根据权利要求3所述的用途,其中所述传染病由选自包含以下的组的微生物引起:
-冠状病毒、鼻病毒、巨细胞病毒、爱泼斯坦-巴尔病毒、流感病毒、呼吸道合胞病毒、酿脓链球菌、肺炎链球菌、流感嗜血杆菌、大肠杆菌、铜绿假单胞菌、奇异变形杆菌、肠杆菌属某些种、不动杆菌属某些种、葡萄球菌属某些种、克雷伯氏菌属、沙雷氏菌属某些种、新型隐球菌、根霉属某些种、曲霉属某些种、肺孢子虫属某些种、毛霉属某些种和根毛霉属某些种。
5.一种治疗有需要的受试者的低氧血症型急性呼吸衰竭的方法,所述方法包括通过静脉内或皮下途径施用1至6mg/Kg体重范围内的抗EGFR MAb。
6.根据权利要求5所述的方法,其中向所述受试者施用所述抗EGFR MAb至少两次至最多五次,其中两次连续施用之间的间隔时间在72小时与168小时之间。
- 一种物流模拟培养箱
- 一种物流专业中生鲜物流成本核算模拟用沙盘
