重大脑疾病闭环调控柔性脑机接口微器件及制备方法
文献发布时间:2024-04-18 19:58:53
技术领域
本发明属于脑机接口领域与微纳加工领域,尤其涉及重大脑疾病闭环调控柔性脑机接口微器件领域,具体涉及一种重大脑疾病闭环调控柔性脑机接口微器件及制备方法。
背景技术
在人脑的结构中约有1000亿个神经元、100万亿个连接,也正是由于结构的复杂性,人类对于大脑相关疾病的发病机制还缺乏足够的认知,绝大多数脑部疾病还缺乏有效的诊疗手段。仅我国确诊癫痫、帕金森病、阿尔兹海默症等重大脑疾病的患者人数就将近1.3亿。而近年来,由于全球老龄化趋势加剧以及有效的神经类药物紧缺,且使用药物或手术的方法治疗上述疾病存在治疗周期长,耐药性和损伤大的特点,因此使用脑机接口设备检测、缓解或治疗神经类疾病的神经调控技术,备受市场关注。
在神经信息检测方面,目前加工工艺成熟的硅基探针可以实现高质量神经记录。但由于其杨氏模量远高于脑组织,植入时造成的组织损伤与机械失配产生的脑异物反应、免疫排斥,使得这些设备的记录能力随着时间的推移而减弱,大多在几个月内失效。为减少植入物引起的免疫反应和机械损伤,实现脑机接口技术稳定、长期高保真记录的目标,使用较小杨氏模量和较高生物相容性的柔性材料所制成的微探针成为研究热点。
在神经电刺激调控方面,目前临床采用的脑电刺激疗法包括深部脑刺激、经颅电刺激等,该类电刺激一般使用毫米级硬基底电极作为工具,无法满足特定方向靶向脑区精准刺激。而柔性脑机接口设备多针对于脑电信息检测,现阶段仍缺乏用于脑疾病检测和调控一体的柔性脑机接口。
综上所述,为长期检测多脑区神经电生理活动变化,诊断、缓解或治疗各类重大脑疾病,亟需研制检测调控一体的长期稳定可植入式柔性脑机接口微器件。这有助于探索脑疾病产生机制,通过原位靶向电调控改善治疗疾病,对临床脑疾病诊断治疗具有重大意义。
发明内容
(一)要解决的技术问题
针对现有技术中的至少一种技术问题,本发明提供了一种重大脑疾病闭环调控柔性脑机接口微器件及制备方法。
(二)技术方案
为解决上述技术问题,本发明采用如下技术方案:
一种重大脑疾病闭环调控柔性脑机接口微器件,包括:
柔性基底层,所述柔性基底层为具备电绝缘性、生物相容性和保护防腐性能的材料;
电屏蔽层,所述电屏蔽层为具备化学稳定性和导电性能的材料,形成的扁平胶囊片结构及所述胶囊片结构上方的环状结构;
柔性中间层,所述柔性中间层与所述柔性基底层材料相同,附着于所述电屏蔽层和柔性基底层上方;
导电层,所述导电层与所述电屏蔽层材料相同,附着于所述柔性中间层上方,形成检测位点、调控位点、电屏蔽环、导线与焊盘;
柔性绝缘层,所述柔性绝缘层与所述柔性基底层材料相同,附着于所述导电层上方,并暴露出所述检测位点、电调控位点与焊盘;
生物材料保护层,所述保护层为具备生物相容性、亲水性的生物材料,内含抗炎药物及生长因子,包裹在所述柔性基底层和所述柔性绝缘层表面。
具体地,一种重大脑疾病闭环调控柔性脑机接口微器件,包括:
柔性基底层,所述柔性基底层为具备电绝缘性、生物相容性、低杨氏模量和保护防腐性能的材料;
电屏蔽层,所述电屏蔽层为具备化学稳定性、高延展性和优良导电性能的材料,形成扁平胶囊片结构及所述胶囊片结构上方的环状结构;
柔性中间层,所述柔性中间层与所述柔性基底层材料相同,附着于所述电屏蔽层和柔性基底层上方;
导电层,所述导电层与所述电屏蔽层材料相同,附着于所述柔性中间层上方,形成检测位点、调控位点、电屏蔽环、导线与焊盘;
柔性绝缘层,所述柔性绝缘层与所述柔性基底层材料相同,附着于所述导电金属层上方,并暴露出所述检测位点、电调控位点与焊盘;
生物材料保护层,所述保护层为具备生物相容性、亲水性的生物材料,内含抗炎药物及生长因子,包裹在所述柔性基底层和所述柔性绝缘层表面。
在一些实施例中,为实现长期植入检测调控脑疾病的目标,所述柔性基底层、柔性中间层与柔性绝缘层具备电绝缘性、生物相容性、保护防腐性以及与脑组织杨氏模量匹配的材料,包括但不限于聚氯代对二甲苯(Parylene-C)、环氧树脂(Epoxy)、聚酰亚胺(PI)、聚酰胺(PA)、液晶高分子聚合物(LCP)、全氟聚醚二甲基丙烯酸酯(PFPE-DMA)等。
在一些实施例中,可植入前端呈针尖轮廓,长度为4-10mm,宽度为0.5-1mm,非植入后端焊盘区域呈矩形;所述针尖型前端有梯形镂空设计,便于神经细胞包裹生长,其中梯形镂空区域上底长0.5mm,下底长1mm,高0.25mm;所述柔性基底层、柔性中间层和所述柔性绝缘层厚度为0.1-10μm。
在一些实施例中,所述电屏蔽层和导电层采用化学惰性、高延展性和高导电率材料,包括但不限于铂(Pt)、金(Au)、聚(3,4-亚乙基二氧噻吩)聚苯乙烯磺酸盐(PEDOT/PSS)、氮化钛(TiN)、碳纳米管(CNT)等。
在一些实施例中,所述检测位点直径为5-10μm,与神经细胞胞体宽度相吻合;所述检测位点间距为15μm以上,与神经细胞胞体高度相吻合。
在一些实施例中,所述检测位点包括但不限于60个,分布于海马CA区锥体细胞层及齿状回颗粒层(包括锥体上叶、锥体下叶及波峰)内,用于检测神经细胞电生理信息;所述电调控位点包括但不限于3个,呈胶囊形,分布于海马CA区及齿状回区,用于释放脉冲进行电刺激,调控神经放电。
在一些实施例中,形成特殊的电屏蔽结构:所述电屏蔽层中的扁平胶囊片结构处于所述调控位点正投影下方,面积略大于所述调控位点;所述电屏蔽环通过地线引入,呈环状围绕于所述调控位点周围,通过所述电屏蔽层中的环状结构与胶囊片结构相连接,将所述电调控位点释放的电场限制在所述电屏蔽环范围内部,实现特定方向电刺激精准调控。
在一些实施例中,所述电屏蔽环与电屏蔽层中的胶囊片结构、环状结构均连接同一地线,提高走线效率。
在一些实施例中,所述检测位点采用纳米颗粒修饰,包括但不限于铂纳米颗粒(PtNPs)、聚(3,4-亚乙基二氧噻吩)聚苯乙烯磺酸盐(PEDOT/PSS)、碳纳米管(CNT)。
在一些实施例中,所述柔性基底层和所述柔性绝缘层通过低功率等离子体(包括但不限于氧气、氩气、氦气等离子体)轰击活化,引入含氧官能团,改性为亲水表面。
在一些实施例中,表面涂覆乙二胺四乙酸二钠钙(Ca-EDTA)与海藻酸钠(SA)混合溶液,所述混合溶液通过D-葡萄糖酸内酯(GDL)的水解,形成离子交联结构的海藻酸钙水凝胶,粘附在所述柔性脑机接口微器件表面。
在一些实施例中,在所述离子交联结构中掺入抗炎药物和活性因子(包括但不限于地塞米松、神经粘附分子L1、神经生长因子NGF)以减少所述柔性脑机接口微器件植入大脑后产生的炎症反应。
作为本发明的另一方面,提供了一种如上所述的长期监测调控脑疾病的柔性脑机接口微器件的制备方法,包括以下步骤:
1)在真空腔体内将聚氯代对二甲苯裂解为单体,采用化学气相沉积法,在倾斜角度放置的硅片上沉积柔性基底层;
2)利用光刻、电子束蒸发、剥离工艺,在柔性基底上形成电屏蔽层的扁平胶囊片结构;
3)重复步骤2),在电屏蔽层胶囊片结构上方形成电屏蔽层环状结构;
4)重复步骤1),在柔性基底层和电屏蔽层上方沉积柔性中间层;
5)重复步骤2),在柔性中间层上方形成导电层;
6)重复步骤1),在导电层上方沉积柔性绝缘层;
7)在柔性绝缘层上方使用光刻胶或Al作为掩膜保护层,使用氧等离子体刻蚀工艺刻蚀柔性绝缘层,暴露出导电层的检测位点、电调控位点与焊盘;
8)重复步骤7),刻蚀柔性绝缘层、柔性中间层和柔性基底层,确定柔性探针的外形,去除掩膜保护层,并将柔性脑机接口微器件从硅片上释放;
9)利用等离子体刻蚀技术,将柔性基底层和柔性绝缘层表面由疏水改性为亲水;
10)在所述导电层的检测位点与调控位点上通过电化学方法修饰纳米粒子,得到电学性能优越的柔性脑机接口微器件。
本发明同时提供了一种如上所述的脑疾病长期闭环调控的柔性脑机接口器件的修饰方法,包括以下步骤:
1)制备预设浓度的海藻酸钠、乙二胺四乙酸二钠钙和抗炎药物、神经活性因子的混合溶液;
2)将获得的柔性脑机接口使用微推进器浸入所述混合溶液,并滴加预设浓度的D-葡萄糖酸内酯;
3)在所述混合溶液中重复微推进器推拉过程后静置,在所述柔性传感器表面形成包裹药物的水凝胶保护层,得到可实现长期稳定植入的柔性脑机接口器件。
(三)有益效果
与现有技术相比,本发明的有益效果在于:
1)本公开提供的重大脑疾病闭环调控柔性脑机接口微器件,整体为杨氏模量与脑组织相近的柔性材料,可植入前端为针形轮廓,且带有梯形镂空设计使得检测位点更靠近电极边缘,在减少植入损伤的同时促进神经细胞包裹生长,获得更好的检测效果。
2)本公开提供的重大脑疾病闭环调控柔性脑机接口微器件,神经信息检测位点及电调控刺激位点分布于海马CA区及齿状回内,可实现高时空分辨率、跨脑区同步检测调控,用于探究癫痫等脑疾病的发病机制和通过电调控实现疾病治疗。
3)本公开提供的重大脑疾病闭环调控柔性脑机接口微器件,含有电屏蔽结构,三面围绕于调控位点,可将调控位点释放的电场限制在屏蔽结构一侧,实现特定方向的电刺激精准调控,有利于原位靶向治疗。
4)本公开提供的重大脑疾病闭环调控柔性脑机接口微器件,在柔性绝缘层和柔性基底层外形成内含抗炎药物、高生物相容性的水凝胶层,抑制蛋白质附着的同时,减少探针植入后脑内产生的免疫排斥反应,有效降低胶质瘢痕的出现,能够实现脑机接口长期稳定植入。
附图说明
为了更清楚地说明本申请实施例或现有技术中的技术方案和优点,下面将对实施例或现有技术描述中所需要使用的附图作简单的介绍。
图1为本发明实施例提供的重大脑疾病闭环调控柔性脑机接口微器件结构层次示意图;
图2为本发明实施例提供的重大脑疾病闭环调控柔性脑机接口微器件平面示意图;
图3为本发明实施例提供的重大脑疾病闭环调控柔性脑机接口微器件制备流程图;
图4为本发明实施例提供的重大脑疾病闭环调控柔性脑机接口微器件修饰生物材料保护层的示意图。
上述附图中,附图标记含义如下:
1-柔性基底层与柔性中间层;2-导电层;3-柔性绝缘层;4-可植入前端;5-非植入后端;6-梯形镂空区域;7-检测位点;8-调控位点;9-电屏蔽结构;10-焊盘;11-导线。
具体实施方式
为长期检测多脑区神经电生理活动变化,诊断、缓解或治疗包括癫痫在内的各类重大脑疾病,本发明提供了一种重大脑疾病闭环调控柔性脑机接口微器件及制备方法。
下面将结合本申请实施例中的附图,对本申请实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本申请一部分实施例,而不是全部的实施例。基于本申请中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本申请保护的范围。
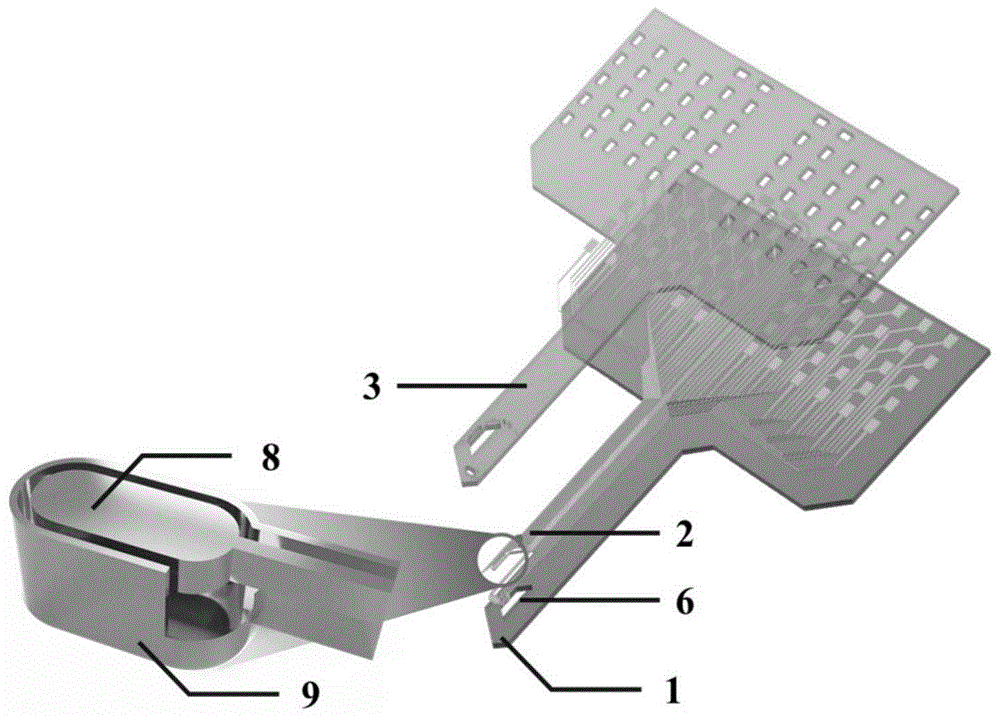
图1为本发明实施例提供的重大脑疾病闭环调控柔性脑机接口微器件结构层次示意图。如图1所示,本公开的柔性脑机接口微器件包含:柔性基底层与柔性中间层1(由于柔性基底层和柔性中间层二者相连,这里使用图例1表示二者)、导电层2、柔性绝缘层3、电屏蔽结构9。其中柔性基底层与柔性中间层1、和柔性绝缘层3为具备电绝缘性、生物相容性、低杨氏模量和保护防腐性能的材料,本实施例中选择聚氯代对二甲苯作为柔性材料;导电层2处于柔性基底层与柔性中间层1和柔性绝缘层3中间,电屏蔽结构9处于导电层2下方,围绕调控位点8分布;导电层2和电屏蔽结构9为具备化学稳定性、高延展性和高导电率的材料,本实施例中选择Cr/Au作为金属材料。调控位点8为电调控位点。
图2为本发明实施例提供的重大脑疾病闭环调控柔性脑机接口微器件平面示意图,包括可植入前端4和非植入后端5。整个传感器内部分布有检测位点7、电调控位点8、电屏蔽环9、焊盘10以及导线11,所述导线11分别将检测位点、电调控位点和电屏蔽环与所述焊盘相连接。
具体的,柔性电极的可植入前端4呈针尖轮廓,长度为4-10mm,宽度为0.5-1mm,优选的,长6mm、宽0.7mm;非植入后端5焊盘区域呈矩形,长8.3mm,宽4.9mm;焊盘10尺寸在200×300μm以内,呈矩阵式排布;针尖形可植入前端4有梯形镂空区域6,其上底长0.5mm,下底长1mm,高0.25mm,该设计便于神经细胞包裹生长,使得原本处于电极中央的检测刺激位点7成为靠近电极边缘的位点,可获得更好的检测与刺激效果。
仅作为示例,本柔性脑机接口器件的通道数量为64通道,包括60位检测位点,3位电调控位点以及1位地线,在实际应用中可根据需要扩展通道数量。
在本实施例中,检测位点分布于海马CA区锥体细胞层及齿状回颗粒层(包括锥体上叶、锥体下叶及波峰)内,用于检测神经细胞电生理信息。检测位点为直径5-20μm的圆形,与神经细胞胞体宽度相吻合;检测位点彼此间距为15-35μm,与神经细胞胞体高度相吻合。该设计在提高柔性传感器空间分辨率的同时,避免多位点同时捕捉单一神经元放电,使得检测效率大大提高。
在本实施例中,电调控位点包括但不限于3个,呈胶囊形,面积为6000μm
需要说明的是,电屏蔽环并不限于椭圆环状结构,可根据所刺激脑区形状进行合理改变;同时,在本实施例中,不同的电屏蔽结构均与同一地线相连,减少通道占用。
图3为本发明实施例的重大脑疾病闭环调控柔性脑机接口微器件制备流程图。如图3所示,柔性脑机接口器件的制备方法,包括如下步骤:
1)将洁净的硅片倾斜角度沉积聚氯代对二甲苯(Parylene-C)获得孤立的纤维状结构,形成如图3(a)所示的柔性基底层,该结构具有更好的细胞粘附性。柔性基底层厚度为0.1-20μm,优选的,采用6μm基底层。
2)在柔性基底层表面旋涂光刻胶,通过光刻显影得到图形化的光刻胶掩膜,然后通过低功率短时间的氧气或氩气、氦气等离子体轰击柔性基底层表面,使之获得更高的表面能,利于粘附屏蔽层。
3)在活化的柔性基底表面采用电子束蒸发技术沉积10nm-1μm金属作为屏蔽层,可为Cr/Pt、Cr/Au、TiN等。当然,在其他实施例中,屏蔽层的选材及其厚度可根据实际情况调整。
4)通过lift-off工艺剥离金属层,清洗残留光刻胶,得到如图3(b)所示的屏蔽层扁平胶囊片结构,优选的,采用20nm Cr/200nmAu作为屏蔽层胶囊片状结构。
5)通过甩胶光刻显影、电子束蒸发、剥离工艺,在胶囊片结构上方形成如图3(c)所示的屏蔽层环状结构,优选的,采用20nm Cr/200nmAu作为屏蔽层环状结构。
6)重复步骤1),在柔性基底层和屏蔽层上方沉积柔性中间层,用以分隔屏蔽层和导电层,柔性中间层厚度大于屏蔽层总厚度,优选的,为0.5μm。
7)在柔性中间层表面旋涂1-2μm光刻胶,通过光刻显影得到图形化的光刻胶掩膜,而后通过低功率反应离子刻蚀技术,采用40-60W氧等离子体刻蚀,暴露出屏蔽层环状结构,如图3(d)所示。
8)通过甩胶光刻显影、电子束蒸发、剥离工艺,在屏蔽层和柔性中间层上方形成如图3(e)所示的柔性脑机接口器件的检测位点、调控位点、电屏蔽环、导线与焊盘。
9)如图3(f)所示,重复步骤1)的过程,在柔性中间层和导电金属层上方沉积柔性绝缘层,优选的,沉积2μm绝缘层。
10)在柔性绝缘层表面旋涂7-9μm光刻胶,通过光刻显影得到图形化的光刻胶掩膜,而后通过高功率感应耦合等离子体刻蚀技术,优选的,采用600-700W氧等离子体刻蚀,暴露出导电层的检测位点、调控位点与焊盘,获得如图3(h)所示结构。
11)清洁干燥表面后,旋涂11-13μm光刻胶,通过光刻显影得到柔性微电极阵列形状的光刻胶掩膜,通过高功率感应耦合等离子体刻蚀技术,优选的,采用600-700W氧气等离子体深刻蚀,暴露出传感器轮廓直至将多余柔性基底层刻蚀完全。随后通过丙酮、乙醇、去离子水浸泡清洗,释放柔性脑机接口器件,如图3(i)所示。
12)利用低功率反应离子刻蚀技术,优选的,采用40-50W氧气等离子体刻蚀,将所得柔性传感器的基底层与绝缘层表面由疏水改性为亲水。
13)将柔性传感器的焊盘连接在FPC软板上,接入电化学工作站,通过恒电流或恒电位法电镀铂黑、PEDOT/PSS等纳米粒子,降低金属位点阻抗与相位延迟,同时提高电荷存储容量,提升传感器的电学性能。
图4为本发明实施例提供的重大脑疾病闭环调控柔性脑机接口微器件修饰生物材料保护层的示意图。如图4所示,柔性脑机接口器件保护层的修饰方法,包括如下步骤:
1)称取适量海藻酸钠(SA)粉末溶于去离子水中,放置过夜使其完全溶解,获得0.6wt%粘稠的SA溶液。
2)将乙二胺四乙酸二钠(EDTA-2Na·2H
3)室温下,将SA溶液和Ca-EDTA溶液按照质量比5:1混合均匀后加入适量地塞米松制备成地塞米松浓度为0.1mg/ml溶液,其中地塞米松药物可减轻设备植入大脑后产生的炎症反应。需要说明的是,加入的药物不仅限于地塞米松,还包括L1细胞粘附分子(L1CAM)、神经生长因子NGF等,可根据实际情况进行调整。
4)室温下,将获得的柔性脑机接口使用微推进器浸入所述混合溶液,并滴加适量现配的1M D-葡萄糖酸内酯(GDL)溶液,使得Ca-EDTA和GDL的摩尔比为1:2,通过GDL的水解,Ca
5)在所述混合溶液中重复微推进器推拉过程,速度为1μm/s~100μm/s,优选的,采用20μm/s的速度使柔性传感器在凝胶中浸渍并提出。随后静置,在所述柔性传感器表面形成20-50μm包裹药物的水凝胶保护层,得到可实现长期稳定植入的柔性传感器。需要说明的是,推拉速度不限于此,可根据实际情况进行调整,改变推拉次数与速度可改变外层生物材料保护层的厚度。
下面描述本发明提供的柔性脑机接口微器件如何进行重大脑疾病调控与检测。以大小鼠为实验对象,将本发明提供的柔性脑机接口微器件植入至鼠海马区进行长期在体记录与刺激调控。
使用异氟烷气体将鼠麻醉后通过脑立体定位仪固定,使用脱毛膏去除头部毛发后剪开头皮,清除多余的脂肪与结缔组织后使用颅骨钻在海马区上方开窗。随后将柔性脑机接口传感器涂覆聚乙二醇(PEG)固化后植入鼠大脑,在传感器周围滴加生理盐水以溶解PEG。待PEG溶解完全后使用牙科水泥封住裸露的颅骨,手术3天后可通过柔性脑机接口的检测位点进行鼠的脑电信号检测。
这里针对癫痫重大脑疾病进行试验说明,在脑机接口传感器植入小鼠脑内后,腹腔注射1mg/kg东莨菪碱,30min后腹腔注射300mg/kg匹罗卡品进行慢性癫痫小鼠造模,出现Racine3~5级癫痫症状且持续发作1h的小鼠视为造模成功。针对癫痫小鼠,可通过柔性脑机接口传感器的检测位点进行海马区脑电信息检测,同时可以通过分布在海马CA区及齿状回的电调控位点进行脉冲电刺激,以此抑制鼠脑内异常放电,改善癫痫症状。
至此,已经结合附图对本公开实施例进行了详细描述。需要说明的是,在附图或说明书正文中,未绘示或描述的实现方式,均为所属技术领域中普通技术人员所知的形式,并未进行详细说明。此外,上述对各元件和方法的定义并不仅限于实施例中提到的各种具体结构、形状或方式,本领域普通技术人员可对其进行简单地更改或替换。
根据上述描述,本领域技术人员应当对本公开重大脑疾病闭环调控柔性脑机接口微器件的制备方法有了清楚的认识。
综上所述,本公开提供一种重大脑疾病闭环调控柔性脑机接口微器件及制备方法,可实现高时空分辨率、跨脑区同步检测调控,有效降低脑异物反应、免疫排斥反应及胶质瘢痕的出现,能够实现脑机接口长期稳定植入,这有助于探索脑疾病产生机制,通过原位靶向电调控改善治疗疾病,对临床脑疾病诊断治疗具有重大意义。
另外需要说明的是,实施例中提到的方向用语,例如“上”、“下”、“前”、“后”、“左”、“右”等,仅是参考附图的方向,并非用来限制本公开的保护范围。贯穿附图,相同的元素由相同或相近的附图标记来表示。在可能导致对本公开的理解造成混淆时,将省略常规结构或构造。
并且图中各部件的形状和尺寸不反映真实大小和比例,而仅示意本公开实施例的内容。另外,在权利要求中,不应将位于括号之间的任何参考符号构造成对权利要求的限制。
除非有所知名为相反之意,本说明书及所附权利要求中的数值参数是近似值,能够根据通过本公开的内容所得的所需特性改变。具体而言,所有使用于说明书及权利要求中表示组成的含量、反应条件等等的数字,应理解为在所有情况中是受到“约”的用语所修饰。一般情况下,其表达的含义是指包含由特定数量在一些实施例中±10%的变化、在一些实施例中±5%的变化、在一些实施例中±1%的变化、在一些实施例中±0.5%的变化。
再者,单词“包含”不排除存在未列在权利要求中的元件或步骤。位于元件之前的单词“一”或“一个”不排除存在多个这样的元件。
此外,除非特别描述或必须依序发生的步骤,上述步骤的顺序并无限制于以上所列,且可根据所需设计而变化或重新安排。并且上述实施例可基于设计及可靠度的考虑,彼此混合搭配使用或与其他实施例混合搭配使用,即不同实施例中的技术特征可以自由组合形成更多的实施例。
类似地,应当理解,为了精简本公开并帮助理解各个公开方面中的一个或多个,在上面对本公开的示例性实施例的描述中,本公开的各个特征有时被一起分组到单个实施例、图、或者对其的描述中。然而,并不应将该公开的方法解释成反映如下意图:即所要求保护的本公开要求比在每个权利要求中所明确记载的特征更多的特征。更确切地说,如下面的权利要求书所反映的那样,公开方面在于少于前面公开的单个实施例的所有特征。因此,遵循具体实施方式的权利要求书由此明确地并入该具体实施方式,其中每个权利要求本身都作为本公开的单独实施例。
以上所述的具体实施例,对本公开的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本公开的具体实施例而已,并不用于限制本公开,凡在本公开的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本公开的保护范围之内。
