用于预测,诊断和预后包括癌症在内的各种疾病的代谢组学签名
文献发布时间:2023-06-19 10:58:46
相关申请数据
本申请要求若干临时专利申请的优先权,包括2018年6月14日提交的序列号为62/685,275的专利,2018年8月3日提交的序列号为62/714,650的专利,2019年4月6日提交的序列号为62/830,389的专利,2019年4月25日提交的序列号为62/838,683的专利,其主题在此通过引用全文并入。
背景技术
1.技术领域
本发明涉及用于评估各种疾病的新的生物标志物,尤其涉及通过质谱法对带注释的代谢物进行绝对定量以鉴定某些可用于筛选,诊断,预测,预后和治疗各种疾病的生物标志物及其衍生物(即签名),所述疾病包括但不限于乳腺癌,卵巢癌,结肠直肠癌,胰腺癌和急性移植物抗宿主病,仅举几例。
2.
MYC是编码转录因子的调节基因和原癌基因家族的成员。这样,MYC导致许多基因的表达增加,其中一些基因参与代谢重编程和细胞增殖,从而导致癌症的形成。实际上,人们普遍认为,为了满足癌症的生化要求,肿瘤代谢沉迷于局部MYC原癌基因激活。然而,发明人进行的研究表明,原位肿瘤基因激活应被视为先前存在的系统性先天性病况的有限复制,该病况已可在处于癌症发展的高风险的无癌参与者中检测到。
后者是对表现出表型轻度缺陷的患者的可变胰岛素抵抗水平升高的影响,该缺陷称为脂肪酸氧化缺陷(FAOD),其由于β-氧化损伤而表现出能量产生缺陷,随后由于糖原异生途径不足而表现出低血糖。
实际上,在这些患者中,高胰岛素水平系统性激活MYC原癌基因,从而诱导谷氨酰胺分解,糖酵解,Δ9-硬脂酰-CoA去饱和酶(SCD)活性并抑制肝糖异生。当添加到非常长链酰基肉碱,乳酸盐,延胡索酸盐和琥珀酸盐的显著血液水平时,最终的表型情况高度暗示了过氧化物酶体和/或线粒体的β-氧化功能障碍。
例如,在发明人进行的研究中,这种MYC诱导的“环境”的表型定量能够在AUC=0.994(95%Cl:0.978-1),灵敏性=98.72%,特异性=98.26%,PPV=98.09%,NPV=98.83%,平均准确度=0.982(100倍交叉验证)和预测准确度统计数据p<9.2e-06(1000次置换)的情况下准确地区分乳腺癌患者与对照,不受疾病阶段,组织学,内在亚型分类,BMI,绝经状态,年龄和患者的大陆地理位置(南美或欧洲大陆)的影响。
作为与干性(stemness)和癌症直接相关的原理证明,研究中确定的表型代谢偏差与人类胚胎代谢高度相关,并显示出化学疗法反应和生存结果的提高的预测能力。这些发现的验证过程,除了在独立分组中得到证实外,在其它腺源性恶性肿瘤中也在很大程度上存在。
这项研究为癌症的假说提供了生化支持,即癌症是先前存在的MYC诱导的系统性病况的身体副现象(epiphenomenon)。除了认可局部恶性脂质生成,谷氨酰胺分解和糖酵解是癌症的主要驱动因素外,该研究还是第一个为癌症的假说提供经过充分验证的生化支持的研究之一,该假说即癌症是系统性,先前存在的,干性样MYC-相关病况的身体副现象,根据研究结果,其与特定的先天性代谢错误非常相似。
这样,发明人依赖于靶向定量代谢组学,即通过液相色谱法随后通过串联质谱法(LC-MS/MS)进行的低分子量化合物的绝对定量测量,该低分子量化合物涵盖了属于途径的整个范围的关键生化活性代谢物,所述途径涉及(i)结构和非结构脂质,(ii)氨基酸,(iii)生物胺和(iv)中间代谢的组分的生物合成,信号传导和分解代谢。
由于对构成特定分析物的离子进行直接分析,而没有如所述的直接抗体测定检测的交叉反应的风险,被认为是定量的金标准的临床质谱的最新普及可归因于高特异性,准确性和可靠性。
分析大批带注释的代谢物的能力提取了反映出明显生物事件的真正功能终点的生化信息,而基因组学,转录组学和蛋白质组学技术虽然价值很高,但仅表明表型反应的潜在原因,因此除非添加了功能验证,不一定能预测表型水平的药物作用,毒理学反应或疾病状态。代谢组学通过描述功能信息弥合了这种信息鸿沟,因为生物体液和组织中的代谢物差异提供了与各种表型反应的最紧密联系。
不用说,一旦适当的技术可以经济高效地挖掘和整合该信息,则生化表型的此类变化将直接引起制药,生物技术和保健行业的关注。通常,表型不一定是通过基因型预测的。基因型和表型之间的差距被许多生化反应所跨越,每个生化反应都对包括药物,营养和环境因素在内的各种影响有独立的依赖性。
在从基因到表型的生物分子链中,代谢物是与表型联系最紧密的可定量分子。发明人进行的研究表明,许多表型和基因型状态,例如对药物的毒性反应或疾病流行,是通过生物体液和组织中功能相关代谢物浓度的差异来预测的。
因此,鉴于上述情况,开发使用靶向代谢组学或通过质谱对带注释的代谢物进行绝对定量以鉴定某些生物标志物及其衍生物,例如比率等(如,“签名”)的系统和方法将是有利的,所述生物标志物及其衍生物可用于筛选,诊断,预测,预后和治疗各种疾病。
发明内容
本发明提供了使用新的生物标志物评估个体疾病的系统和方法。本发明的优选实施方案包括通过质谱法对带注释的代谢物进行绝对定量以鉴定某些生物标志物及其衍生物(即“签名”),然后可以将其用于筛选,诊断,预测,预后和治疗各种疾病。
在本发明的一个实施方案中,进行血浆和/或组织样品的靶向代谢组学分析。血液代谢物的绝对定量(μmol/L)是通过电喷雾电离(ESI)串联质谱(MS/MS)对某些(例如最多186种)带注释的代谢物进行靶向定量分析来实现的。
在本发明的一个实施方案中,靶向分析方案用以使用多重反应监测,中性损失和前体离子扫描来定量筛选完全注释的代谢物。对代谢物浓度进行定量,得到至少一个文件包括(i)样品鉴定,(ii)代谢物名称(例如,最多186个)和(iii)浓度(例如,μmol/L的血浆)。
对于代谢组学数据分析,然后将对数转化应用于所有定量代谢物以标准化浓度分布,并提供给软件以与以前已知的“签名”进行比较(例如,定位,绘图等)。在一个实施方案中,签名识别可以涉及将数据上传到MetaboAnalyst3.0(基于网络的分析管线)和ROCCET(Receiver Operating Characteristic Curve Explorer&Tester)中,以生成通过SVM(支持向量机),PLS_DA(偏最小二乘判别分析),和随机森林以及逻辑回归模型获得的单变量和多元ROC(接收机工作特性)曲线。
在本发明的某些实施方案中,存在多达186种为了比较而定量的注释代谢物,包括40种酰基肉碱类(AC),21种氨基酸(AA),19种生物胺(BA),己糖(Hex)总和,76种磷脂酰胆碱(PC),14种溶血磷脂酰胆碱(LPC)和15种鞘磷脂(SM)。关于甘油部分中酯(a)和醚(e)键的存在,甘油磷脂得以进一步区分,其中两个字母表示两个甘油位置结合至脂肪酸残基(aa=二酰基,ae=酰基-烷基),而单个字母表示存在单个脂肪酸残基(a=酰基或e=烷基)。还可以分析样品的能量代谢代谢物,包括乳酸盐,丙酮酸盐/草酰乙酸盐,α-酮戊二酸盐,延胡索酸盐和琥珀酸盐。
除了单独的代谢物定量外,还基于以前的观察结果将与特定功能相关的代谢物组按比率进行组装/组合,所述观察结果即代谢物浓度之间的比例可以增强关联信号,并同时提供有关可能的代谢途径的新信息。如下所述,这些比率(至少在某些实施方案中)是疾病“签名”的极其重要的方面,并且可以本身指示特定疾病的存在或可能性,患者的预后以及可用的治疗方法。
在其它实施方案中,还发现其它分组也很重要,包括氨基酸(AA)组,其是通过根据它们的功能总结属于某些家族或化学结构的AA的水平而计算的,如以下的总和:1)必需氨基酸(必需AA);2)非必需氨基酸(非必需AA);3)生糖(Ala+Gly+Ser)氨基酸(Gluc AA);4)支链(Leu+Ile+Val)氨基酸(BCAA);5)芳香族(His+Tyr+Trp+Phe)氨基酸(Arom AA);6)谷氨酰胺分解衍生物(Ala+Asp+Glu);和7)总氨基酸的总和。
对于评估线粒体功能很重要的酰基肉碱(AC)组,也可以通过总结总的酰基肉碱(AC),C2+C3,C16+C18,C16+C18:1和C16-OH+C18:1-OH来计算。对于评估脂质代谢重要的脂质组也可以通过总结以下来分析:1)总溶血磷脂酰胆碱(总LPC);2)总酰基-酰基;和3)总的酰基-烷基磷脂酰胆碱(分别为总PC aa和总PC ae);4)总鞘磷脂(总SM);和5)总(LPC+PC aa+PC ae+SM)脂质(结构脂质)的总和。
饱和,单不饱和及多不饱和结构脂质的总和中的比例也可以组装为代理来估计对醚脂质的延伸酶和去饱和酶活性:1)去饱和酶9[((PC ae C36:1+PC ae C38:1+PC ae C42:1)/(PC ae C42:0)],去饱和酶6[(PC ae C44:6+PC ae C44:5+PC ae C42:5+PC ae C40:6+PC ae C40:5+PC AE C38:6+PC ae C38:5+PC ae C36:5)/(PC ae C36:1+PC ae C38:1+PCae C42:1)]。
肝代谢和功能的临床指标还可以通过采用Fischer商的经典(亮氨酸+异亮氨酸+缬氨酸/(酪氨酸+苯丙氨酸)或变体(Val/Phe,Xleu/Phe)获得。异戊酸血症,酪氨酸血症,尿素循环不足和β氧化异常的临床指标也可以通过分别采用戊酰基肉碱比丁酰基肉碱(C5/C4),酪氨酸比丝氨酸(Tyr/Ser),甘氨酸比丙氨酸和谷氨酰胺(Gly/Ala,Gly/Gln)和乳酸比丙酮酸(Lac/Pyr)的比率计算得出。也可以通过组装比率(C16+C18:1/C2),(C14:1/C4),(C14:1-OH/C9),(C14/C9),(C14:1/C9)和非常长链脂肪酸(ELOVL2)(PC aa C40:3/PC aaC42:5)的伸长,来实现与诊断非常长链酰基CoA脱氢酶(VLCAD)和2型肉碱-棕榈酰转移酶(CPT-2)缺陷有关的酶功能的代理。可以对单独(Met-SO)或与未修饰的甲硫氨酸(Met-SO/Met)以及精氨酸残基的对称(SDMA),不对称(ADMA)和总二甲基化(总DMA)组合的甲硫氨酸亚砜的水平进行定量,以分别获取ROS介导的蛋白质修饰以及系统性精氨酸甲基化状态的途径。
知道肝脏对糖异生的抑制作用是真正的胰岛素-MYC依赖的生化反应,在胰岛素施用后葡萄糖与生糖氨基酸(葡萄糖/Ser,葡萄糖/Gly和葡萄糖/Ala)的比率从正常值到更低值的转变可以用作胰岛素-MYC相关活性的量度。
然后可以如下将相同的程序应用于其它MYC反应酶:精氨酸甲基转移酶(ADMA,ADMA/Arg,SDMA,SDMA/Arg和总DMA,总DMA/Arg),鸟氨酸脱羧酶(Glu,Glu/Orn,Pro,Pro/Orn,Orn,Orn/Arg,腐胺,腐胺/Orn,亚精胺,亚精胺/腐胺,精胺和精胺/亚精胺),丙氨酸氨基转移酶(Ala),(Ala/Glu),天冬氨酸转氨酶(Asp)和(Asp/Glu),谷氨酰胺酶(Glu),(Gln/Glu),[(Glu+Asp+Ala)/Gln],[(Gln/Glu)/Asp],(Glu/葡萄糖)/(Ala/Glu)和[(Glu/Gln)/葡萄糖]/(Ala/Glu)。
后两个比率与“谷氨酸牵引效应”有关,所述“谷氨酸牵引效应”定义为通过胰岛素-MYC依赖性谷氨酸脱氢酶(GDH)刺激谷氨酰胺分解(伴净酮酸的量增加至回补(anaplerosis))导致的由低血糖症诱导的脱氨而非转氨产生的谷氨酸的上调。
也可以考虑(Ser/C2,Ser/Gln,Ser/Thr)和(PC aa C42:0/PC ae C32:3,PC aaC32:2/PC ae C34:2)的比率作为糖酵解相关磷酸甘油酸酯脱氢酶(PHGDH)和葡萄糖激酶调节剂(GCKR)活性的代理。后者抑制肝脏和胰腺中的葡萄糖激酶活性,并且前者是催化丝氨酸生物合成的限速步骤。
平行地,并假设谷氨酰胺相较于谷氨酸(Gln/Glu)和相较于天冬氨酸[(Gln/Glu)/Asp]的比值作为谷氨酰胺分解活性的代理,可以将比率[(Ser/C2)/(Gln/Glu)],[(Ser/C2)/(Gln/Glu)/Asp],[(PC aa C32:2/PC ae C34:2)/(Gln/Glu)]和[(PC aa C32:2/PC aeC34:2)/(Gln/Glu)/Asp]组装为理论方程式以获取糖酵解和谷氨酰胺分解之间的平衡。
应当理解,关于前述代谢物及其组(例如,总和,比率等),某些对于分析特定疾病可能至关重要,而其它可能不太重要。因此,以下提供对于个体签名至关重要(即最重要)的代谢物和/或其组。为了简洁起见,在下面各个适当的部分将介绍各个疾病的个体签名的关键方面。
通过考虑以下优选实施方案的详细描述,本领域技术人员将对使用新的生物标志物评估个别疾病的系统和方法有更全面的了解,及其附加优点和目的的实现。将参考附图,首先将对附图进行简要描述。
图1示出了根据本发明的一个实施方案的关于如何识别一种疾病的代谢签名并随后用于对该疾病评估患者血样的方法;
图2-6提供了认为是在本发明的某些实施方案中使用的代谢物(或其组)的分析物的列表,包括其缩写;
图7A和图7B提供了已鉴定为可用于评估不同类型疾病的比率的列表;
图8提供了已鉴定为可用于评估至少卵巢癌的参数的列表;
图9提供了已鉴定为可用于评估至少卵巢癌的比率的列表;
图10提供了发明人在进行统计单变量分析期间使用的似然比及其解释;
图11提供了发明人在根据Sokoll和Chan鉴定理想的肿瘤标志物时所使用的特征和与其相关的评论;
图12A和B分别提供了卵巢癌的多变量ROC曲线分析以及其性能特征;
图13提供了卵巢癌患者与健康受试者以及其它恶性和非恶性病况相比的Ortho-PLSDA评分图;
图14A-D示出了可用于确定卵巢癌患者的生存率(预后)的某些比率;
图15提供了在本发明的一个实施方案中用于评估(例如诊断,预后等)患者中卵巢癌的代谢物及其数学推导物(例如比率等);
图16A和B分别提供了结肠癌的多变量ROC曲线分析以及其性能特征;
图17提供了结肠癌患者与健康受试者以及其它恶性和非恶性病况相比的Ortho-PLSDA评分图;
图18A-C示出了可用于确定结肠癌患者的生存率(预后)的某些比率;
图19提供了在本发明的一个实施方案中用于评估(例如诊断,预后等)患者中结肠癌的代谢物及其数学推导物(例如比率等);
图20A和B分别提供了胰腺癌的多变量ROC曲线分析以及其性能特征;
图21提供了胰腺癌患者与健康受试者以及其它恶性和非恶性病况相比的Ortho-PLSDA评分图;
图22A和B示出了可用于确定胰腺癌患者的生存率(预后)的某些比率;和
图23提供了在本发明的一个实施方案中用于评估(例如诊断,预后等)患者中胰腺癌的代谢物及其数学推导物(例如比率等)。
本发明的优选实施方案涉及使用靶向代谢组学或通过质谱法对带注释的代谢物进行绝对定量,以鉴定从未描述过的适于评估各种疾病的生物标志物和/或其衍生物(例如比率等)(即“签名”),所述疾病包括但不限于乳腺癌、卵巢癌、结肠直肠癌、胰腺癌和急性移植物抗宿主病。
应当理解,当第一疾病(例如,乳腺癌)可具有第一签名时,第二疾病(例如,卵巢癌)可具有不同的第二签名,但是用于鉴定每个签名的方法非常相似,并且在某些情况下是相同的。因此,尽管在下面的不同部分讨论了不同的疾病,但是为了简洁起见,除非另有说明,否则关于如何鉴定签名并将签名随后用于评估特定疾病的细节同样适用于其它签名和其它疾病。例如,除非另外说明,否则在乳腺癌部分中提供的关于通过质谱法对带注释的代谢物进行绝对定量的细节同样适用于卵巢癌部分,其它方面也是如此。
还应当理解,疾病可具有多于一种签名或其部分。例如,第一签名可用于诊断,第二签名(或第一签名的部分)可用于预后等。还应当理解,尽管疾病可具有多于一种签名,但是可能存在几种签名共有的各个方面(例如,单个代谢物或其衍生物),并且因此可以以其自身提供有关诊断、预后、治疗等方面的信息。关于签名的详细信息将在下面的相应部分中讨论。
还应当理解,本发明不限于任何特定的疾病,并且本领域技术人员将理解,本文公开的方法可以用于鉴定其它疾病的签名并评估其它疾病,包括本文未特别提及的那些疾病。本发明也不限于使用质谱法或任何特定类型的质谱法(例如电喷雾电离(ESI)串联质谱法(MS/MS)等),并且包括用于定量代谢物的其它方法,例如色谱法或光谱法。话虽如此,但发明人发现使用质谱法,特别是ESI MS/MS,以及本文所述的数据分析(例如,对数转化、ROC曲线等)是有益的。同样地,本文详细描述的方法是优选实施方案,并且应照此对待。
在讨论包括单个签名、用于鉴别该签名以及评估各种疾病的方法的本发明之前,将首先提供本文使用的术语或短语的某些定义。
通过使用生物标志物(或其特定组)和根据本发明的方法,有可能以改进的准确性和可靠性来评估疾病(例如,卵巢癌、结肠直肠癌等)。本发明中出人意料地实现了通过测量受试者的样品(例如血液样品)中某些代谢物的量和/或比率来提供生物标志物或生物标志物组,使得可能以改进的方式在疾病的早期筛选和诊断疾病(例如卵巢癌等)。
通常,生物标志物是有价值的工具,因为它有可能将两种或更多种生物学状态区分开来,从而作为正常生物学过程、致病过程或对药物干预的反应的指标。
代谢物是低分子量化合物(<1kDa),小于大多数蛋白质、DNA和其它大分子。蛋白质活性的微小变化导致生化反应及其代谢物(=代谢性生物标志物,取决于机体的新陈代谢)的重大变化,其浓度、通量和转运机制对疾病和药物干预敏感。
这使得能够获得生理和病理生理物质的单个概况,从而反映遗传和环境因素两者,例如营养、身体活动、肠道微生物和药物。因此,代谢性生物标志物比例如蛋白质或激素(其为生物标志物但不是代谢性生物标志物)提供了更全面的信息。
鉴于此,本文所用的术语“代谢性生物标志物”或简称“生物标志物”定义为适合作为疾病(例如癌症)及其亚型(例如肿瘤亚型)的存在和状态的指标的化合物,其为哺乳动物体内代谢过程中存在的代谢物或代谢化合物。
术语“生物标志物”和“代谢性生物标志物”在本发明的上下文中通常被同义地使用,并且通常是指代谢物的量或两种或更多种代谢物的比率。因此,术语代谢性生物标志物或生物标志物还意图包括两种或更多种代谢物之间的比率(或其它数学关系)。
术语“量”通常是指样品(例如血液样品)中代谢物的浓度,通常以微mol/L给出,但是也可以以本领域通常使用的其它单位度量,例如g/L、mg/dl等。术语“总和”通常是指在各个实施方案中指定的所有代谢物的摩尔量的总和。
术语“比率”通常是指各个实施方案中指定的代谢物的量的比率。根据本发明测量的代谢性生物标志物(组)可以包括氨基酸和生物胺、酰基肉碱、己糖、鞘脂和甘油磷脂的代谢物(即分析物)类别,如图2-6所示。
图2中的生物胺被理解为通过天然氨基酸的酶促脱羧作用衍生的一组天然存在的生物活性化合物。生物物质是由生命过程提供的物质,并且生物胺含有胺基。
出人意料地发现,测量包含这些类别的代谢物的一组生物标志物,即测量某些指示性代谢物的量和/或比率,可以以改进的方式在早期筛选和诊断各种疾病(例如卵巢癌等),并且可以评估肿瘤活动的生化反应,从而可以预测治疗响应并对疾病表现进行亚分类。
尽管可以使用修饰的“签名”,但是如果省略了相应生物标志物组合所指定的一种代谢物或一类代谢物,或者如果其数量减少,则疾病的评估变得不太灵敏且不太可靠。
这尤其适用于根本无法使用已知生物标志物根据已知方法可靠地检测出疾病的早期阶段。实际上,同时测量各组生物标志物中包含的代谢物可以更准确且更可靠地评估疾病,通常(A)灵敏度大于80%,优选大于90%,且更优选大于98%,(B)特异性大于80%,优选大于85%,且更优选大于90%,(C)阳性预测值(PPV)大于40%,优选大于50%,且更优选大于60%,和(D)阴性预测值(NPV)大于80%,优选大于90%,且更优选大于98%。显然,需要可达到或实现100%(或接近100%)灵敏性、特异性、PPV和/或NPV的生物标志物(或其组)。
术语“灵敏性”、“特异性”、“阳性预测值”和“阴性预测值”的含义在本领域通常是已知的,并且在本发明的上下文中根据由美国爱荷华大学建立的“预测值理论”而定义。在该理论中,程序的诊断价值由其灵敏性、特异性、预测值和效率来定义。公式的说明总结如下。
测试的灵敏性是所有具有阳性测试的疾病患者的百分比。(TP/(TP+FN))x100=灵敏性(%),其中TP=测试阳性;FN=假阴性。
测试的特异性是所有具有阴性测试的无疾病患者的百分比。(TN/(FP+TN)x100=特异性(%),其中TN=测试阴性;FP=假阳性。
测试的预测值是值(阳性或阴性)为真实值的次数的度量(%),即,所有为真阳性的阳性测试的百分比为阳性预测值((TP/(TP+FP)x100=阳性结果的预测值(%);((TN/(FN+TN))x100=阴性结果的预测值(%))。
似然比:可以通过在统计单变量分析期间确定本文使用的阳性和阴性似然比(LR),进一步评估生物标志物的性能(参见图10)。
多变量数据分析:通过逻辑回归分析,将训练案例用于标志物发现并确定可能与疾病(例如卵巢癌、结肠直肠癌等)相关的任何临床变量。代谢物浓度的定量和质量控制评估通过
然后将数据上传到基于网络的分析管线MetaboAnalyst 2.0(www.metaboanalyst.ca),并使用MetaboAnalyst的标准化方案(Xia et al,2012)进行标准化,以进行单变量和多变量分析、高维特征选择、聚类和监督分类、功能富集以及代谢途径分析。
数据还导入可获自http://www.roccet.ca/ROCCET/的ROCCET(ROC CurveExplorer&Tester),用于生成通过支持向量机(SVM)、偏最小二乘判别分析(PLS-DA)和随机森林获得的单变量和多变量接收机工作特性(ROC)曲线。
使用平衡子采样通过蒙特卡洛交叉验证(MCCV)生成曲线,其中三分之二(2/3)的样本用于评估特征重要性。然后使用重要特征构建分类模型,并在剩下的1/3样本中对其进行验证。重复相同的步骤多次,以计算每个模型的性能和置信区间。
上调和下调:上调是指代谢物浓度的增加,例如由于例如酶活性的改变,导致该生化反应发生的速率增加。对于下调,正好相反。
T检验:t检验是一种统计假设检验,使用的是集成于MarkerView软件中的检验,适用于表格中的每个变量,并根据标准差和样品数量确定每组的均值是否存在显著差异,例如以找出两个不同组的均值(平均值)之间是否存在真正的差异。
P值:p值是当假定原假设(无变化或无影响的假设)为真时,获得与实际观察到的结果至少一样极端的结果的概率。p值始终为正,并且值越小,改变发生的可能性就越低。p值等于或小于0.05拒绝5%水平的原假设,这意味着只有5%的时间,变化是偶然事件。这是本文提供的表中设置的水平。
Log倍数变化:Log倍数变化定义为每种条件下平均对数转化浓度之间的差异。这是描述一组中的值比另一组中的值更高或更低的方法。例如,0.3的log倍数变化“相当于”与对照(较健康的组)相比,exp(.3)=1.34的倍数变化增加。此外,-0.3的log倍数变化“相当于”与对照相比,exp(-.3)=0.74=(1/1.34)的倍数变化增加,或与疾病相比1.34的倍数变化降低。根据Sokoll和Chan,理想的肿瘤标志物参见图11。
现在将讨论用于特定疾病的签名,包括其鉴定及其在评估(例如,筛选、诊断、预后、治疗等)特定疾病中的用途。
首先进行研究以鉴定可用于评估乳腺癌的签名。总计使用了1113个基线样品,其中935个来自血液,170个来自组织样品。在相同的集中式独立按服务收费公司(Biocrates,Austria),通过相同的标准化靶向定量质谱技术对样品进行分析。
癌症组(n=447)由以下构成:i)乳腺癌志愿者(n=217),包括pT1pN0(n=68),pT1N1(n=77),pT2N1(n=8),T2N0M0(n=1)和T3N2M0(n=63)]。内在亚型为:i-luminal A(n=33),B(n=98),B-HER2(n=23),三阴性(n=37),HER-2(n=14)和RE-/PR-(n=4)。欧洲患者(n=154)除了由ii)肺癌(n=23),iii)头颈癌(n=56),iv)肝癌(n=30),v)血液恶性肿瘤(n=65),以及vi)结肠癌患者(n=85)以及相应的正常组织(n=85)和肿瘤组织(n=85)外,还包括回顾性臂(n=62)和前瞻性臂(n=92)。结肠癌患者为T1N0M0(n=9),T2N0M0(n=15),T3N0M0(n=20),T3N0M1(n=1),T3N1M0(n=10),T3N1M1(n=6),T3N2M0(n=6),T3N2M1(n=7),T4N0M0(n=2),T4N1M0(n=1),T4N1M1(n=3),T4N2M0(n=2),T4N2M1(n=3)。
其余666个样品作为对照组包括在内,其中:169个对照(79名女性和90名男性)来自基于圣保罗(
患有局部区域晚期肿瘤T3N2M0的乳腺癌患者(n=63)计划接受新辅助化疗方案,该方案包括在巴雷图斯癌症医院进行4个周期的阿霉素(60mg/m2)和环磷酰胺(600mg/m2),然后进行4个周期的紫杉醇(175mg/m2)。
在完成“局部晚期乳腺癌(LABC)的新辅助化疗”项目(临床试验NCT00820690)的过程中,该部分研究设计为将III期疾病患者的肿瘤响应的预测签名的鉴定作为终点。患者在开始化疗前2周内进行了基线评估,通过全血细胞计数、肝肾功能以及每个周期的临床评估(每3周和治疗结束后一个月)记录血液学和非血液学毒性。
使用临床和放射学测量来计算基线肿瘤尺寸,并将其与由专门病理学家直接记录在手术产品上的最终肿瘤直径进行比较。完全病理反应(pCR)被定义为没有组织病理学证据表明乳房或结节中有任何残留的浸润性和/或非浸润性疾病(ypTO/ypNO)。
采用相同的程序评估本文鉴定的针对不同良性状况的代谢签名,以测试它们对乳腺癌的特异性和独特性。为此,将乳腺癌女性与以下无癌群体进行比较:A)处于低风险乳腺癌进展的女性(n=31),B)基于群体的对照(79名女性和90名男性),C)自身免疫性疾病(n=27),D)高风险的乳腺癌进展(n=36),E)多囊卵巢综合征(n=49),F)任何治疗之前被HIV感染的个体(n=18),G)骨髓异源干细胞移植后的移植当天患者的化学诱导的免疫抑制(n=26)。
为了测试在III期乳腺癌女性中检测到的代谢偏差是否可以在无病生存期中发挥任何作用,最初的研究结果遭到了早期阶段的研究“乳腺癌转移的风险预测研究”(意大利和奥地利)的挑战。该研究设计为将鉴定5年生存结果的代谢签名作为终点,并包括在包括pT1pN0(n=68),pT1N1(n=77),pT2N1(n=8),T2N0M0(n=1)的女性前瞻性臂(n=92)和回顾性臂(n=62)期间分为luminal(75.3%,116/154)和非luminal(24.6%,38/154)的总共154例。
进行乳腺癌代谢组学与基于群体的对照的比较,以进一步探讨以下假设:初始结果可能与先天性代谢错误有关。因此,将基于圣保罗群体的健康调查项目(ISA 2008)中的169名年龄相匹配的男性和女性与可用的处于基线的血液样品进行比较,该项目设计为前瞻性地分析巴西圣保罗州圣保罗市公共卫生服务的使用情况。
为了确定乳腺癌签名和处于乳腺癌进展风险升高的女性之间是否存在任何新陈代谢相似之处,我们的研究结果受到了一组表现出1.2至2.0范围相对风险的41名女性以及一组表现出HOMA-IR>2.5(n=8)和<2.5(n=10)的PCOS女性的挑战。
参加者填写了健康史调查表,包括种族、初潮年龄、首次活产的年龄、活组织检查次数、非典型增生的存在以及乳腺癌和卵巢癌家族史的信息。使用乳腺癌风险评估工具(BCRAT),使用美国国家癌症研究所网站上的源代码3.0版来评估乳腺癌的5年绝对风险和相对风险(RR)。
为了探讨乳腺癌后能量代谢不足的可能性,将Lac/Pyr摩尔比应用于154名截止值>25的欧洲乳腺癌患者,以表明患者患有原发性(或继发性)呼吸链功能障碍。为此,除了对在所有参与者中定量的186种代谢物进行定量外,还通过使用其它测量所采用的相同的质谱方法对154名欧洲乳腺癌参与者血液中的以下代谢物进行了定量(mmol/L):乳酸盐、丙酮酸盐-草酰乙酸盐、琥珀酸盐、延胡索酸盐和α酮戊二酸盐。
为了了解我们的结果可以如何接近于代谢干性,将我们的研究结果与辅助生殖程序中使用的人类胚胎培养基进行了比较。按照巴西圣保罗联邦大学生殖科卵细胞质内单精子注射(ICSI)程序所采用的常规方案(Borges et al 2015)进行培养。在胚胎子宫移植后,将剩余的无胚胎培养基立即冷冻并保持在-80℃,直到通过相同的靶向定量MS/MS方法进行分析。根据样品在第3天的扩增程度和孵化状态将其分组。因此,将包括不良发育(n=100)和良好发育(n=100)的胚胎的培养基的两个合并的组组合,并进行质谱分析。
为了进一步证实该理论并验证与胰岛素依赖性MYC激活相关的酶活性的代理的比率,将从圣保罗联邦大学生物医学实验中心(Centro de Desenvolvimento de ModelosExperimentais para Medicina e Biologia,CEDEME)获得的小鼠维持在12小时的明暗循环下,并可以随意获得自来水和饲料(chow diet)。饮食热量限制根据美国国立衰老研究所(National Institute on Aging)的方案进行。简而言之,将12周龄的小鼠分为两组:随意组,其在整个实验过程中可以自由获取NIH31饮食(Flarlan-Teklab);或饮食限制组,其被喂养NIH31/NIA强化饮食(Harlan-Teklab),以一周的热量摄入减少10%开始,随后一周增加到25%的限制,直到方案结束增加到40%的限制。每周评估食物摄入和体重。动物使用方案已由圣保罗联邦大学的IACUC批准(CEP-0218/11、CEP-0237/12和CEUA4603261015),并且符合NIH准则。
在BIOCRATES Life Sciences AG,Innsbruck,Austria的定量代谢组学平台上基于集中化独立按服务收费,对于任何表型信息为盲的,通过电喷雾电离(ESI)串联质谱(MS/MS)对302个血浆样品中的186种带注释的代谢物进行靶向定量分析,以实现血液代谢物的绝对定量(μmol/L)。
实验性的代谢组学测量技术(包括靶向分析方案)用于使用多重反应监测、中性损失扫描和前体离子扫描来定量筛选完全带注释的代谢物。代谢物浓度的定量和质量控制评估通过MetlQ软件包(BIOCRATES Life Sciences AG,Innsbruck,Austria)按照21CFR Part11进行,这意味着证明了在给定的误差范围内的可重复性。然后生成xls文件,其中包含样品鉴定和186种代谢物名称和浓度,单位为μmol/L的血浆。
对于代谢组学数据分析,将对数转化应用于所有定量的代谢物以使浓度分布标准化,并将其上传到基于网络的分析管线MetaboAnalyst 3.0(www.metaboanalyst.ca)和可从http://www.roccet.ca/ROCCET获得的Receiver Operating Characteristic CurveExplorer&Tester(ROCCET)(Xia et al 2013),用于生成通过支持向量机(SVM)、偏最小二乘判别分析(PLS-DA)、随机森林以及逻辑回归模型获得单变量和多变量接收机工作特性(ROC)曲线,以计算特定代谢物的优势比。
ROC曲线通过蒙特卡洛交叉验证(MCCV)使用平衡子采样生成,其中三分之二(2/3)的样本用于评估特征重要性。然后将重要特征用于构建分类模型,该模型在第一次分析中剩余的1/3样本中得到了验证。重复相同的程序10-100次,以计算每个模型的性能和置信区间。
为了进一步验证每个模型的统计意义,ROC计算包括针对所需模型特异性的bootstrap 95%置信区间,以及1000次置换和错误发现率(FDR)计算后的准确性。
使用p180试剂盒(BIOCRATES Life Sciences AG,Innsbruck,Austria)总计定量了186种带注释的代谢物,其中包括40种酰基肉碱(AC)、21种氨基酸(AA)、19种生物胺(BA)、己糖(Hex)总和、76种磷脂酰胆碱(PC)、14种溶血磷脂酰胆碱(LPC)和15种鞘磷脂(SM)。关于甘油部分中酯(a)和醚(e)键的存在,进一步区分了甘油磷脂,其中两个字母表示两个甘油位置与脂肪酸残基结合(aa=二酰基,ae=酰基-烷基),而单个字母表示存在单个脂肪酸残基(a=酰基或e=烷基)。在同一家公司(Biocrates)中,还对欧洲参与者的样品进行了以下能量代谢代谢物的分析:乳酸盐、丙酮酸盐/草酰乙酸盐、α-酮戊二酸盐、延胡索酸盐和琥珀酸盐。
除了单个定量分析外,还分析了与特定功能相关的代谢物组。通过根据功能将属于某些族或化学结构的氨基酸的水平求和来计算氨基酸组,例如以下各项的总和:1)必需氨基酸(必需AA),2)非必需氨基酸(非必需AA),3)生糖(Ala+Gly+Ser)氨基酸(Gluc AA),4)带支链(Leu+Ile+Val)氨基酸(BCAA),5)芳香族(His+Tyr+Trp+Phe)氨基酸(Arom AA),6)谷氨酰胺分解衍生物(Ala+Asp+Glu)和7)总氨基酸总和。
还通过将总AC、C2+C3、C16+C18、C16+C18:1和C16-OH+C18:1-OH求和来计算对于评估线粒体功能重要的酰基肉碱(AC)组。还通过将以下各项求和来分析对于评估脂质代谢重要的脂质组:1)总溶血磷脂酰胆碱(总LPC),2)总酰基-酰基和3)总酰基烷基磷脂酰胆碱(分别为总PC aa和总PC ae),4)总鞘磷脂(总SM)和5)总(LPC+PC aa+PC ae+SM)脂质(结构性脂质)的总和。
还将饱和结构脂质、单不饱和结构脂质和多不饱和结构脂质的总和的比例组装为代理,以便定量针对醚脂质的延伸酶和去饱和酶活性:1)去饱和酶9[(PC ae C36:1+PC aeC38:1+PC ae C42:1)/(PC ae C42:0)],去饱和酶6[(PC ae C44:6+PC ae C44:5+PC aeC42:5+PC ae C40:6+PC ae C40:5+PC ae C38:6+PC ae C38:5+PC ae C36:5)/(PC aeC36:1+PC ae C38:1+PC ae C42:1)]。
通过应用Fischer商的经典(亮氨酸+异亮氨酸+缬氨酸/(酪氨酸+苯丙氨酸)或变体(Val/Phe,Xleu/Phe)来获得肝脏代谢和功能的临床指标。通过分别采用戊酰基肉碱与丁酰基肉碱(C5/C4)、酪氨酸与丝氨酸(Tyr/Ser)、甘氨酸与丙氨酸和谷氨酰胺(Gly/Ala,Gly/Gln)以及乳酸与丙酮酸(Lac/Pyr)的比率来计算异戊酸血症、酪氨酸血症、尿素循环不足和β氧化异常的临床指标。
通过将比率(C16+C18:1/C2)、(C14:1/C4)、(C14:1-OH/C9)、(C14/C9)、(C14:1/C9)与非常长链脂肪酸(ELOVL2)的延伸率(PC aa C40:3/PC aa C42:5)组合,实现了与诊断非常长链酰基CoA脱氢酶(VLCAD)和2型肉碱-棕榈酰转移酶(CPT-2)缺陷相关的酶功能的指示。对单独的甲硫氨酸亚砜(Met-SO)水平或与未修饰的甲硫氨酸组合的甲硫氨酸亚砜水平(Met-SO/Met)以及精氨酸残基的对称二甲基化水平(SDMA)、不对称二甲基化水平(ADMA)和总二甲基化水平(总DMA)进行定量,以分别获取ROS介导的蛋白质修饰以及系统性精氨酸甲基化状态。
为了获得血液中的MYC活性,在施用胰岛素之前和之后的低血糖小鼠的血液中以及在表现出正常(<2.5)和升高(>2.5)HOMA(IR)值的无癌女性中对由MYC响应酶活性产生的代谢物和比率进行特异性定量。知道肝脏对糖异生的抑制作用是真正的胰岛素-MYC依赖性生化反应,在施用胰岛素后以及在HOMA(IR)值升高的女性中,葡萄糖与生糖氨基酸的比率(葡萄糖/Ser,葡萄糖/Gly和葡萄糖/Ala)从正常值到更低值的转变用作胰岛素MYC相关活性的量度。
然后将相同的程序应用于如下其它MYC响应酶:精氨酸甲基转移酶(ADMA、ADMA/Arg、SDMA、SDMA/Arg和总DMA、总DMA/Arg),鸟氨酸脱羧酶(Glu、Glu/Orn、Pro、Pro/Orn、Orn、Orn/Arg、腐胺,腐胺/Orn、亚精胺、亚精胺/腐胺、精胺和精胺/亚精胺),丙氨酸氨基转移酶(Ala),(Ala/Glu),天冬氨酸氨基转氨酶(Asp)和(Asp/Glu),谷氨酰胺酶(Glu),(Gln/Glu),[(Glu+Asp+Ala)/Gln],[(Gln/Glu)/Asp],(Glu/葡萄糖)/(Ala/Glu)和[(Glu/Gln)/葡萄糖]/(Ala/Glu)。
后两个比率是基于与“谷氨酸牵引效应”相关的体外实验专门组合的,“谷氨酸牵引效应”被定义为低血糖引起的通过胰岛素-MYC依赖性谷氨酸脱氢酶(GDH)刺激谷氨酰胺分解导致谷氨酸的脱氨而非转氨产生的上调,从而导致净酮酸的量增加至回补(anaplerosis)。由于较低的微环境pH值也被报告为有利于“谷氨酸牵引效应”,因此我们还通过Pearson r相关性分析计算了乳酸和谷氨酸增加之间的相关程度。
还包括了丝氨酸与C2的比率(Ser/C2)和(PC aa C42:0/PC ae C32:3)的比率以指示糖酵解相关磷酸甘油酸脱氢酶(PHGDH)和葡萄糖激酶调节剂(GCKR)活性。后者抑制肝脏和胰腺中的葡萄糖激酶活性,前者催化丝氨酸生物合成的限速步骤。并列地,假设谷氨酰胺与谷氨酸的比值(Gln/Glu)以及与天冬氨酸的比值[(Gln/Glu)/Asp]作为谷氨酰胺分解活性的指标,发明人组合了比率[(Ser/C2)/(Gln/Glu)]、[(Ser/C2)/(Gln/Glu)/Asp]、[(PCaa C32:2/PC ae C34:2)/(Gln/Glu)]和[(PC aa C32:2/PC ae C34:2)/(Gln/Glu)/Asp]作为理论方程式来获得糖酵解和谷氨酰胺分解之间的平衡。
鉴于前述内容,随后进行了研究以鉴定可用于评估其它疾病例如卵巢癌、结肠直肠癌、胰腺癌和急性移植物抗宿主病的签名(即其它签名)。
在某些实施方案中,所讨论的疾病是癌症(例如,卵巢癌等),并且可以处于特定阶段(例如,I期、II期、III期或IV期)。癌症医学阶段的定义由美国国立卫生研究院美国国家癌症研究所的美国癌症联合委员会(American Joint Committee on Cancer,AJCC)定义。分期系统提供了根据预后对患者进行分组的策略。治疗决策部分根据分期类别制定,但主要根据肿瘤大小、淋巴结和远端转移状态制定。
不管所讨论的疾病为何,生物样品获自哺乳动物,优选获自小鼠、大鼠、豚鼠、狗、小型猪或人,最优选获自人,还优选获自女性。生物样品优选是血液,然而,允许根据本发明进行测量的技术人员已知的任何其它生物样品也是合适的。血液样品通常是全血、血清或血浆,其中血浆是优选的。也可以接受用纸过滤器收集的干燥样品。因此,根据本发明的方法通常是体外方法。
为了测量生物样品中的代谢物浓度,采用了定量分析方法,例如色谱法,光谱法或质谱法,其中色谱法可包括GC、LC、HPLC和UPLC,光谱法可包括UV/Vis、IR和NMR,质谱分析仪/光谱仪可包括ESI-QqQ、ESI-QqTOF、MAL-DI-QqQ、MAL-DI-QqTOF和MAL-DI-TOF-TOF。更优选地,质谱分析仪/光谱仪包括四极质谱分析仪、离子阱质谱分析仪、TOF(飞行时间)质谱分析仪、轨道阱质谱分析仪、磁区质谱分析仪、静电区质谱分析仪、离子回旋共振(ICR)以及质谱分析仪的组合,包括单四极杆(Q)和三重四极杆(QqQ)、QqTOF、TOF-TOF、Q-轨道阱。发明人发现,使用FIA-和FIPLC-串联质谱法是优选的并且具有一定的益处。
本文使用的缩写如下:GC=气相色谱法,CE=毛细管电泳,LC=液相色谱法,HPLC=高压液相色谱法,UHPLC=超高压液相色谱法,UV-Vis=紫外-可见,IR=红外,NIR=近红外,NMR=核磁共振,ESI=电喷雾电离,MALDI=基质辅助激光解吸/电离,TOF=飞行时间,APCI=大气压化学电离,QqQ=三重四极杆配置,也称为Q1q2Q3(Q1和Q3四极杆是质量过滤器,q2是无质量解析的四极杆)。
为了测量代谢物的量,使用靶向代谢组学来定量生物样品中的代谢物,包括氨基酸、生物胺、酰基肉碱、己糖、鞘脂和甘油磷脂的分析物类别。在存在同位素标记的内标物的情况下进行定量,并通过上述方法来确定。在图2-6中示出了适合作为根据本发明指定的代谢物的分析物(包括其缩写(BC代码))的列表。
为了达到使用代谢组学检测疾病的最高能力,本发明不仅通过将患病的患者(即患有特定疾病如卵巢癌的患者)与健康对照进行比较,还与患有其它恶性和良性病况的更多参与者进行比较,从而鉴定其区别性的生化特征和比率。在相同的集中式独立公司(Biocrates,Austria),使用相同的按服务收费的标准化靶向定量质谱技术对样品进行了前瞻性收集和分析。
包括了一组未曾接受过治疗的具有处于不同阶段(即I期、II期和III期)的某些癌症的女性血浆样品,癌症患者(n=473)由以下构成:i)来自巴西和欧洲的乳腺癌志愿者(n=213),以及ii)肺癌患者(n=23),iii)头颈癌患者(n=56),iv)肝癌患者(n=30),v)血液恶性肿瘤患者(n=65)和vi)结肠癌患者(n=85)以及各自的正常组织(n=85)和肿瘤组织(n=85)。
其余752个样品作为对照组,其中:169名对照(79名女性和90名男性)来自基于圣保罗群体的健康调查项目(ISA 2008),由于该群体的特征,允许我们按照国际糖尿病联盟流行病学和预防特别小组联合临时声明;国家心肺血液研究所;美国心脏协会;世界心脏联合会;国际动脉粥样硬化学会;和国际肥胖症研究协会的建议,根据代谢综合征在6个进展阶段分布的频率对其进行分析。
对照组还包括33名处于乳腺癌进展风险升高的女性,23名经组织学证实为非浸润性原位癌的参与者,31名处于乳腺癌进展低风险的女性,49名多囊卵巢综合征,18例治疗前被HIV感染的个体,34名具有类风湿性关节炎的女性,58例自身免疫性溶血性病症,30名具有肝硬化的参与者,8名甲状腺功能亢进,8名甲状腺功能减退。
在两个独立的按服务收费的基础上使用Biocrates Life Sciences AG,Innsbruck,Austria和Quest Diagnostics Nichols Institute San Juan Capistrano,CA,USA的定量代谢组学平台,采用患有各种癌症的女性血浆样品以及多个对照进行的独立验证集中进行了靶向(ESI-MS/MS)定量代谢组学/脂质组学分析。
简而言之,使用靶向分析方案通过多重反应监测、中性损失扫描和前体离子扫描对已知的小分子代谢物进行定量筛选。通过参考合适的内标物实现对生物样品的代谢物的定量,并且该方法已证明符合21C.F.R.,Part 11,这意味着证明了在给定的误差范围内的可重复性。所有分析的代谢物的浓度均以μM示出。
总计检测了186种不同的代谢物,其中包括40种酰基肉碱,19种蛋白氨基酸、鸟氨酸和瓜氨酸,19种生物胺,己糖总和,76种磷脂酰胆碱,14种溶血磷脂酰胆碱和15种鞘磷脂。参见图2-6。
根据甘油部分中酯(a)键和醚(e)键的存在进一步区分甘油磷脂,其中两个字母(aa=二酰基,ae=酰基-烷基,ee=二烷基)表示两个甘油位置与脂肪酸残基结合,而单个字母(a=酰基或e=烷基)表示存在单个脂肪酸残基。
脂质侧链组成缩写为Cx:y,其中x表示侧链中的碳数,y表示双键数,例如“PC aeC38:1”表示缩醛磷脂/纤溶酶原(plasmenogen)磷脂酰胆碱,其中两个脂肪酸侧链中具有38个碳原子数并且其中一个具有单个双键。
训练病例用于标志物发现,并通过逻辑回归分析来确定可能与特定疾病相关的任何临床变量。代谢物浓度的定量和质量控制评估通过
然后将数据上传到基于网络的分析管线MetaboAnalyst 2.0(www.metaboanalyst.ca),并使用MetaboAnalyst的标准化方案(Xia et al 2012)进行标准化,以进行单变量和多变量分析(参见上述关于标准化的讨论)、高维特征选择、聚类和监督分类、功能富集以及代谢途径分析。
数据还导入可获自http://www.roccet.ca/ROCCET/的ROCCET(ROC CurveExplorer&Tester),用于生成通过支持向量机(SVM)获得的单变量和多变量接收机工作特性(ROC)曲线、偏最小二乘判别分析(PLS-DA)和随机森林。
使用平衡子采样通过蒙特卡洛交叉验证(MCCV)生成曲线,其中三分之二(2/3)的样本用于评估特征重要性。然后使用重要特征构建分类模型,并在剩下的1/3样本中对其进行验证。重复相同的步骤多次,以计算每个模型的性能和置信区间。
乳腺癌在世界范围内仍然是发病率和死亡率的主要原因。通过应用乳房摄影术(mammography)和磁共振成像的早期诊断改善了较小体积疾病的检测,为内科医生在癌症最可治愈的较早期阶段提供了干预的机会。
广泛应用于预后确定的分子技术的出现已经发展成为诊断工具,其利用循环肿瘤细胞和无细胞DNA进行较早期检测,预后和在适用的情况下响应预测。许多临床试验现在正在探索这些方法的临床效用。
研究表明,人类癌症在代谢应激的环境中发展。剥夺足够氧、营养物、激素和生长因子的迅速增殖肿瘤细胞上调解决这些缺陷的途径,以克服缺氧(HIF)、血管功能不全(VEGF)、生长因子剥夺(EGFR,FIR2)和激素支持物(ER,PR,AR)的损失,都增强存活和增殖。
现在已知许多原癌基因调节代谢途径,所述代谢途径对于在氧和营养物源高度有限的不适宜的肿瘤微环境中的细胞存活是关键的。实际上,RAS、PI3K、TP53和MYC等现在被认为是重要的代谢调节剂,其功能对于肿瘤细胞的存活是基本的。
基于癌细胞在其对营养物的使用、生物分子的合成和能量的产生上不同于其正常对应物的日益增长的认识,我们将定量质谱法应用于乳腺癌患者的血液和组织,并将结果与在正常对照中观察到的结果进行比较。为了探索共性,发明人将这些研究扩展到包括腺和非腺祖系的其它癌症,以及包括多囊卵巢综合征和晚期代谢综合征在内的与代谢应激相关的非恶性疾病状态。
发现导致代谢应激的胰岛素/葡萄糖介导的鼠模型,并且最终导致在植入前人胚胎的分泌物组(secretome)的探索以检查观察到的信号的“干性”。
为了评估乳腺癌和独特组织学和位置的肿瘤之间的可能的差异和相似性,将鉴定的血液签名与来自未治疗的肺癌患者的血液样品(n=23),来自前列腺癌患者(n=10),头颈癌(n=57),肝癌(n=30)和结肠癌患者(n=85)的血浆进行比较,后者具有相应的正常组织(n=85)和肿瘤组织(n=85)以及血液学恶性(n=36)。来自患有结肠癌的患者的正常组织(N=85)和肿瘤组织(N=85)也用于在组织水平上验证血液中鉴定并由乳腺癌和结肠癌共有的代谢集体性(communality)。
重要的是,除了与不同恶性进行比较外,还将每种个别类型的癌症与含有12种不同良性代谢状况的上述666个对照组进行比较。在多变量ROC曲线分析之后,图7A和图7B中所示的比率作为描述对每个个别肿瘤的最高特异性的代谢情况的表示。
寻找代谢中间体(其血液浓度(μM/L)可用作乳腺癌生物标志物)导致一个探索性数据集的组装,该数据集将来自低乳腺癌风险的女性(n=31)的血浆样品与来自患有未治疗的III期(T3N2M0)侵入性疾病的患者(n=59)的血浆样品进行比较。结合无监督聚类分析(在线方法)的靶向性定量MS/MS分析(1)鉴定出病例和对照之间的清楚的代谢差异(图1a)。然后进行验证(统计能力(power)=0.8),其将169个基于群体的对照样品与154个病例中从独立且较早报道的分组“乳腺癌转移研究的风险预测”的结果(意大利和奥地利)进行比较。
结果表明,乳腺癌女性表现出血液中定量的5种主要类别的代谢物中的至少一种上调或下调的代谢物。统计分析描述了最初在探索阶段中鉴定的这些代谢物中的9种的个别验证,包括谷氨酰胺(Gln)、天冬氨酸(Asp)、谷氨酸(Glu)、溶血磷脂酰胆碱酰基C26:1(lysoPC a C26::1)、鞘磷脂C18:0(SM C18:0)、3-羟基十四烯酰基肉碱(C14:1-OH)、磷脂酰胆碱酰基-烷基C38:3(PC ae C38:3),甲硫氨酸亚砜(Met-SO)和牛磺酸。
在探测和验证集两者的观察结果中发现癌症患者的谷氨酰胺浓度降低到正常群体中观察到的水平的近1/8(约800μM/L)(p=7.8e-53,FDR=2.7e-52),而天冬氨酸(P=1.7e-67,FDR=8.3e-67)(图1e)和谷氨酸(P=6.4e-96,FDR=6.2e-95)的血液浓度分别比0-5μM/L和40μM/L的正常范围高出近10倍。
因为与谷氨酸和天冬氨酸的并行增加相关的谷氨酰胺消耗被认为是MYC驱动的“谷氨酰胺分解”的标志,所以这些发现导致检查其它MYC相关现象以询问观察结果。
肝谷氨酰胺(Gln)代谢调节循环中的氨基酸水平,并且谷氨酸(GLU)通过其在许多反式脱氨反应中的作用对该过程是关键的。
由于MYC激活与包括谷氨酰胺、谷氨酸及其比率等的特定代谢物的血液水平的可测量变化有关,使用靶向定量MS/MS来评价(μM/L)这些中间体作为MYC激活的替代标志物。然后,发明人组装直接在血液中测量的代谢物比率,以充当MYC-协调的代谢功能的“代替”。
与他们的假设一致,Gln/Glu比率是谷氨酰胺代谢的阴性替代,i)区分乳腺癌病例与对照;ii)与乳腺癌风险升高反相关(相关性=-0.54,p=3.67e-6FDR=3.06e-5);iii)与病理I期患者的5年死亡的风险相关,和iv)与新辅助化疗(NAC)后实现病理完全缓解(pCR)的失败反相关(相关性=-0.81,P=1.15e-81,FDR=2.13e-80)。
并行分析发现,Gln/Glu比率与i)晚期代谢综合征和ii)欧洲分组的回顾性和前瞻性臂中增加的死亡机会反相关(相关性=-0.68,p=2.30e-38,FDR=1.59e-37)。
理论上,由Gln/Glu比率反映的谷氨酰胺消耗的变化可以提供乳腺癌引发和糖尿病之间的代谢联系,反映从葡萄糖到谷氨酰胺的系统性代谢重编程作为生物合成反应和细胞能量的优选前体来源。
发明人发现在几乎100%的乳腺癌患者中,Gln/Glu比率的相同的变化,而与固有亚型无关。这些乳腺癌患者揭示出先前体外描述的系统性MYC相关的生化转变,与谷氨酰胺利用优于葡萄糖来合成结构磷脂相关,如分别由比率(结构脂质/Gln)和(结构脂质/己糖)测量。乳腺癌患者的MYC签名及其与糖尿病的相似性提出了是否可以通过测量其它生化中间体来鉴定代谢重编程的问题。
为了检查乳腺癌与其它疾病状态,将结果与从其它癌症(30个肝;23个肺;85个结肠;58个头颈和65个血液学)获得的结果和从患有包括代谢综合征晚期(n=70),HCV诱导的肝硬化(n=30);甲状腺功能亢进(n=8);甲状腺功能减退症(n=8);HIV感染(n=18);多囊卵巢综合征(n=49);自身免疫疾病(n=86)在内的各种代谢病症的个体和那些患乳腺癌风险升高的女性(n=33)获得的结果进行比较。
发明人测量了以前在大代谢组学(metabolomics)和全基因组关联研究中描述的具有生化活性的代谢物,以检查与以下相关的已建立的单一代谢物和代谢物比率:i)肝功能(Val/Phe,Xle/Phe),ii)脂质去饱和酶活性(PC aa C36:6)和iii)丝氨酸棕榈酰基转移酶(SPTLC3)活性(PC aa C28:1和C10:2)。这些测量用于开发查询数据集的算法。
发现使用方程式{[PC aa 36:6/[(Val/Phe)/牛磺酸]/C10:2}和脂质PC aa C28:1得到的结果(作为多变量接收机算子曲线(ROC)分析)在探索集[AUC=0.987(95%Cl:0.964-1),灵敏性=96.72%,特异性=96.78%,阳性预测值=98.33%,阴性预测值=93.94%,平均准确度(100倍交叉验证)=0.95和预测准确度统计学(1000次置换)=p<2.04e-05]和验证集[AUC=0.995(95%Cl:0.991-0.998),灵敏性=98.09%,特异性=96.18%,阳性预测值=82.35%,阴性预测值=99.64%,平均准确度(100倍交叉验证)=0.96和预测准确度统计学(1000次置换)=p<1.28e-06]两者中将乳腺癌与对照分开,与阶段(I至III)和固有亚型无关。
为了证实这些关联,进行了Pearson r相关性(www.metaboanalyst.ca),其将所述比率与我们154名欧洲乳腺癌患者的血液中测定的肿瘤代谢物(oncometabolites)延胡索酸盐,琥珀酸盐,乳酸盐,谷氨酰胺和己糖的水平进行比较。发现与乳酸盐(p=1.42e-08,FDR=3.24e-07),乳酸盐/丙酮酸盐(p=7.96e-06,FDR=7.47e-05),延胡索酸盐/己糖(p=0.0004,FDR=0.002),琥珀酸盐/己糖(p=0.0001,FDR=0.0007)和谷氨酰胺分解相关的比率(Ala+Asp+Glu/Gln)(p=0.0004,FDR=0.002)的最高的正相关性。当(Lac/Pyr)值应用于逻辑回归方程式logit(P)=log[P/(1-P)]=-12.24+1.80Lac/Pyr,其中P是Pr(y=1|x)时,当分析原发性肿瘤不大于2.0cm的患者(n=103)时,该比率的升高与5年死亡的风险增加相关(几率=6.08[Pr(>|z|)=0.001])。
对己糖/乳酸盐(p=5.88e-08,FDR=1.11e-06);己糖(p=0.002,FDR=0.007);和肝糖异生比率(己糖/PHGDH Act)(p=0.002,FDR=0.007);和(己糖/Ala+Gly+Ser)(p=0.0014,FDR=0.005);[己糖/(C14:1/C4)](p=0.003,FDR=0.009);[己糖/(C18:1/C8)](p=9.94e-05,FDR=0.0006);(己糖/CPTII)(p=0.0007,FDR=0.003);[己糖/(C16/C3)](p=0.001,FDR=0.004);(己糖/AcylC-DC)(p=0.002,FDR=0.007)观察到最高负相关性。
当检查具有不同肿瘤(肺,结肠,肝,白血病,淋巴瘤和头颈鳞状细胞癌)的患者的代谢概况时,结果再次表明谷氨酰胺消耗增加,特别是在患有腺祖系肿瘤的患者中。
将这些研究扩展到包括患有多囊卵巢综合征(PCOS),肝硬化,乳腺癌的高风险和5期代谢综合征的患者揭示了这些无癌参与者表现出与在腺癌患者中发现者非常相似的谷氨酰胺分解概况。
我们在体外证明“谷氨酸牵引效应”之后组装比率(Glu/己糖),其中恶性细胞培养物中葡萄糖饥饿通过MYC协调反应导致谷氨酸升高。
此种效应在患有腺癌、有较高风险形成乳腺癌的患者和患有PCOS的个体的血液中清楚地鉴定。值得注意的是,由基于群体的正常对照或患有非腺肿瘤(白血病,淋巴瘤,多发性骨髓瘤和鳞状细胞癌)的患者组成的对照组都没有揭示出该比率的显著变化,特别是揭示出与对照相似水平的鳞状细胞癌。
已经在由葡萄糖剥夺诱导的代谢应激条件下描述了“谷氨酸牵引效应”的增加。一致地,发明人发现患者血液己糖浓度与其乳腺癌方程式{[PC aa 36:6/[(Val/Phe)/牛磺酸]/C10:2}的值之间存在显著的(P=0.003,FDR=0.009)反相关性。
与在以“谷氨酸牵引效应”测量的相对低血糖的条件下促进腺癌的前提一致,他们的结果提示,血糖水平的分离测定可以相对于其它代谢中间体不像测量己糖水平那样提供信息,所述代谢中间体包括:i)线粒体肉碱棕榈酰基转移酶II(CPT-2)缺陷比率(C16/C3),ii)过氧化物酶体损伤生物标志物lysoPC a C26:0,lysoPC a C26:1和lysoPC a C28:1,或iii)其与谷氨酰胺分解[Phe/(Gln/Glu)/Asp]的关系。重要的是,CPT-2和过氧化物酶体缺陷两者(公知的先天代谢错误)都与患病患者的低血糖有关。
如果由于先天样的代谢错误而在乳腺癌中出现相对低血糖状态,那么与慢性低血糖相关的超高胰岛素血症将构成一种强有力的代谢应激者,即使在没有癌症的情况下,该代谢应激者也能够系统地上调糖酵解和谷氨酰胺分解。
为了检验低血糖的前提,发明人开发了一种实验鼠模型,其中在血糖正常和低血糖条件下对小鼠施用胰岛素。在此鼠模型中,仅接受胰岛素的低血糖小鼠重演癌症患者中已经观察到的MYC依赖性转变,其特征在于以下各项的胰岛素/MYC依赖性反应:i)谷氨酰胺分解(Gln/Glu),(Ala/Glu)和[(Gln/Glu)/Asp]以及糖酵解(Ser/C2)和(Ser/C2)/[(Gln/Glu)/Asp]两者的组合,ii)谷氨酸牵引效应(Glu/己糖),iii)精氨酸甲基转移酶活性[总DMA/[(Gln/Glu)/Asp]和[Tau/[(Gln/Glu)/Asp],iv)肝功能[BCAA/(Phe+Tyr)],鸟氨酸脱羧酶活性(亚精胺),v)肝脏糖异生[己糖/(Ala+Gly+Ser)]和vi)过氧化物酶体损伤(lysoPCa C26:0)。
为了证实在人中的这些发现,我们检查了己糖血液浓度是否与过氧化物酶体功能障碍相关,如含有非常长链脂肪酸(VLCFA)的特异性脂质升高所代表的。进行“Pearson r”相关性以比较癌症低风险的女性(n=31)与相对风险升高(评分1.7-1.9)的女性(n=14),患有非侵入性(原位)癌的女性(n=23),患有多囊卵巢综合征的女性(n=49),以及患有侵入性乳腺癌腔(n=118)和非腔(n=36)两者的那些女性。
来自己糖与lysoPC a C26:1(相关性=-0.73,p=3.41e-49,FDR=2.89e-48)和己糖与lysoPC a C28:1(相关性=-0.60,p=9.88e-30和FDR=6.29e-29)的比率的结果表明从高危女性和原位癌开始,至PCOS和最终在侵入性疾病患者血浆中达到最低点的进行性负相关性,而与内在亚型无关。
结果提示,乳腺癌可以先于葡萄糖-胰岛素稳态的系统性亚临床紊乱,其特征在于温和的,可能无症状的,IEM-样的生化变化。过程包括超高胰岛素血症的可变时期,随后糖酵解、谷氨酰胺分解、结构性脂质生成(lipidogenesis)的系统性MYC激活以及低血糖的进一步恶化,MYC作为肝脏糖异生抑制剂的已知作用的结果。
在正常条件下,低血糖导致从储存池中募集脂肪酸。然而,患有利用脂肪酸作为能量来源的原发性不能的个体,如脂肪酸氧化缺陷(FAOD)所见,容易积累毒性肿瘤代谢物以及肉碱和脂肪酸衍生物,伴有ROS产生增加和进一步线粒体混乱。
在此上下文中,取而代之,特征为过度糖酵解,谷氨酰胺分解和恶性脂质生成的癌症的代谢依赖性(以前认为是局部肿瘤DNA异常的结果)可以代表早于并很可能促进肿瘤发生的系统性生化异常。
此外,这些代谢紊乱预计在治疗干预后仍然存在,这与乳腺癌复发率在最初治疗后长达24年保持不变的最近观察结果一致。
为了支持我们的假设并与IEM的定义一致,发明人检测到非常长链酰基肉碱如C14:1-OH(p=0.0,FDR=0.0),C16(p=0.0,FDR=0.0),C18(p=0.0,FDR=0.0)和C18:1(p=1.73e-322,FDR=1.16-321)和含有VLCFA的脂质(lysoPC a C28:0)(p=1.14-e95,FDR=1.65e-95)在乳腺癌和结肠癌患者血液中的积累。引人注目的是,这些相同概况不仅在结肠癌组织中被鉴定,而且在手术时从这些相同结肠癌患者中取出的相邻正常结肠粘膜中也被鉴定。
他们在乳腺癌中描述的代谢变化与氧化磷酸化中的IEM样变化一起发生,如通过Ox/Phos缺陷的乳酸盐/丙酮酸盐比率特征的数值增加检测的。在该研究中,76%(70/92)的欧洲乳腺癌患者的乳酸盐/丙酮酸盐比率高于25.8的正常值。
最近的报道已经鉴定患有能量代谢病症的患者中癌症(包括乳房)的频率高四倍,并且IEM与升高的己糖/胰岛素病症和性腺和甲状腺功能障碍有关,它们本身与高乳酸盐/丙酮酸比率有关。
由于原发性脂肪酸氧化缺陷(FAOD)与毒性脂肪酸和肉碱衍生物中间体的系统性线粒体积累有关,因此氧化磷酸化缺陷可能发生。
为了确定如在当前研究中定量的过量谷氨酰胺分解和糖酵解是否反映系统性而非局部事件,假设所鉴定的致癌紊乱应当存在于携带恶性的患者的正常组织而非血液中。
如果正确,那么在这些正常组织活组织检查中鉴定的生化概况应当对直接从肿瘤活组织检查材料产生的数据提供关于反应和存活的相似预后信息。
MYC-激活的最有力的代谢方程式之一将广泛使用的MYC-驱动的SFA/MUFA的去饱和标志物比率与MYC谷氨酰胺分解相关的比率(Asp/Gln)联系起来的方程式。本发明人在213例乳腺癌和200例对照中的先前经验揭示,由该方程式[(SFA/MUFA)/(Asp/Gln)]强调的代谢偏差是最稳健的乳腺癌判别式之一(AUC=1.0,p=1.32e-127)。
组装ANOVA和无监督聚类比较,以将来自对照(n=200),乳腺癌(n=213)和结肠癌(n=85)的血液代谢表型与来自正常结肠上皮(n=85)和来自相同85名CRC患者的手术切除的结肠癌两者的签名进行比较。
这些结果证明了在乳腺癌和结肠癌患者的血液中由此方程式揭示的实际上相同的生化表型,它们与在正常和结肠癌组织中检测到的表型偏差在数量上不能区分。当与对照组(n=200)比较时,来自癌症患者的血液或组织(正常粘膜和肿瘤两者)的结果是一致的,使得代表实际上不能区分的生物样品。
令人感兴趣的是,在正常结肠粘膜中发现的生化紊乱以比率{(Ser/C2)/[(Gln/Glu)/Asp]}反映,与5年复发的风险显著相关(p=1.63e-33,FDR=2.21e-33),该风险与用这些患者的结肠肿瘤获得的结果不能区别。此比率不仅清楚地区分乳腺癌与对照以及低和高癌症风险的女性,而且也区分i)具有较短(2.1年)与较长(5.1年)无复发存活的女性,和ii)获得完全病理反应(pCR)的女性与NAC后具有残留疾病的患者(p=3.73e-108,FDR=2.31e-107)(即预后)。
在本研究中的另外的观察发现,肝功能障碍与IEM和癌症两者共享许多特征,表明肝功能障碍在癌症发生中起作用。
Fischer商[(Ile+Leu+Val)/(Tyr+Phe)和ALT活性(Ala/Glu)的较低数值在患有PCOS的无癌女性,癌症发展风险升高的女性和已建立的腺恶性(肝脏,乳房,结肠,肺)的女性中发现。这些重复出现的生化偏差包括转氨基和糖异生脆弱以及不能适当代谢支链(BCAA)和芳族氨基酸。
在反映血液中,主要在较后期疾病中BCAA积累的任何代谢综合征参与者中,未检测到由较低的Fischer比率证明的代谢转变,其中发现Fischer比率较高。在腺癌患者中,较低的Fischer比率数值似乎反映了肝功能的恶化,导致BCAA的同时减少和芳族氨基酸的积累。实际上,发现乳腺癌患者的苯丙氨酸水平在55%(85/154)的欧洲乳腺癌患者中比正常期望值(40-74μM/L)高,平均为89.3μM/L(75-128μM/L)。尤其当与低风险女性70.3μM/L(46.5-97.9μM/L)和平均68μM/L(47-95μM/L)的晚期代谢综合征相比时,对乳腺癌发展的相对风险评分为1.8的女性也揭示82.8μM/L(64.6-98.8μM/L)的升高水平。甲状腺功能障碍患者也表现出较高水平的苯丙氨酸94.6μM/L(49.5-142μM/L)。如所预期的,患有肝硬化的无癌参与者表现出最高水平,平均为114.3μM/L(84.4至163μM/L)。
为了证实这些发现与肝功能有关,发明人包括HCV诱导的肝硬化的无癌患者(n=30)和甲状腺功能减退(n=8)的患者和甲状腺功能亢进(n=8)的患者,因为甲状腺功能障碍通常与肝功能障碍和包括乳房在内的癌症的风险增加有关,因此甲状腺功能亢进(n=8)。他们还分析了HIV患者,这是由于他们的癌症风险增加和HIV感染对肝功能的直接影响。
结果揭示肝硬化、甲状腺功能障碍和HIV感染的无癌患者和:1)乳腺癌发展的相对风险升高的研究参与者,2)患有PCOS的患者和3)患有已知腺恶性(乳房,结肠,肺和肝)的患者的血液代谢概况之间的一致性。
发明人根据以下项划分他们的无癌组:i)增加癌症的风险,ii)升高gamma-谷氨酰转移酶(GGT)的水平,和iii)游离甲状腺素(游离T4)的累积值。结果揭示,当应用于高危女性时Gln/Glu比率的相同模式在无癌症的女性中通过游离-T4和GGT值的渐进变化而得到重演。与甲状腺功能障碍相似,已经发现血液GGT的升高显著增加了包括乳房恶性在内的整个癌症风险。为了探索这些条件之间的生化重叠,发明人进行了正交偏最小二乘方判别分析(Ortho-PLSDA),其揭示了甲状腺功能亢进/甲状腺功能减退和肝硬化患者之间的高度生化相似性,所述患者一起似乎将一侧的乳腺癌与相对侧的血液恶性相互联系起来。
以前已经发现IEM不仅干扰肝功能,而且影响适当的内分泌生理,导致糖尿病,性腺和甲状腺功能障碍的风险增加。
鉴定肝功能障碍的研究结果与在脂肪酸氧化缺陷(FAOD)环境中产生乳腺癌的前提一致。在这些类型的IEM中最常见的实验室发现中,与低血糖并行的是肝功能障碍,因为肝脏的生化如此依赖于肝细胞线粒体的正常功能。
因此,这些发现类似于那些与β-氧化的线粒体和/或过氧化物酶体病症有关的发现,这两种病症都已知与由非常长链脂肪酸(VLCFA)和肉碱衍生物(脂肪酸的低效氧化的结果)组成的脂质在血液和组织中的积累有关。
与此概念一致,当对照(n=92)与乳腺癌患者(n=63)比较时,非靶向质谱法脂质组(lipidomic)数据显示在癌症患者样品中含有非常长链脂肪酸(VLCFA>C40)的磷脂种类的总体积累。
值得注意的是lysoPC a C26:0(通常用于诊断β-氧化的过氧化物酶体病症的生物标志物)的血液升高。随后,通过特异性靶向MS/MS(p=9.07e-71,FDR=2.81e-70)获得此发现的验证。通过定量功能富集分析(www.metaboanalyst.ca)获得了过氧化物酶体作为与这些代谢发现相关的推定亚细胞位置的进一步提示,该分析揭示了使用代谢物L-乙酰肉碱,琥珀酸,甘氨酸,草酰乙酸,丙酮酸,肌氨酸,D-精氨酸和牛磺酸的过氧化物酶体定位的显著(p=1e-121)250倍富集。
另外的发现是乳腺癌患者血液中牛磺酸的显著升高及其与癌症风险,反应和存活的相关性,以及其与肿瘤代谢物延胡索酸盐(p=3.05e-06)和琥珀酸盐(p=1.87e-05)的血液水平的相关性。
已知延胡索酸盐和琥珀酸盐都增加HIF-1基因(低氧诱导因子-1)产物的半衰期,该产物促进血管生成和肿瘤存活(33-36)。
这些肿瘤代谢物还增强导致全基因组表观遗传重编程(39)的组蛋白和DNA甲基化(37,38)。还发现牛磺酸水平与以二甲基化精氨酸残基总量(总DMA)测量的精氨酸甲基转移酶活性的上调相关(p=0.001,FDR=0.006)。
总DMA水平也与乳腺癌发生的进展阶段逐渐、正地和统计学(p=5.57e-12,FDR=1.56e-11)相关。
精氨酸甲基转移酶活性直接与MYC活性相关,并且据报道与细胞干性状态有关。
这导致乳腺癌的发现是否反映细胞生化干性的状态的问题,因为已经提示有人胚胎发生与癌症之间的相当多的平行。
为了评估此假设,发明人将乳腺癌代谢物组学签名与体外受精的、发育中的人胚胎的分泌物组中鉴定的那些签名进行比较,所述人胚胎处于最终的植入准备下。
结果证明了成功发育的胚胎的代谢概况与乳腺癌高危女性、胰岛素抗性女性和新辅助化疗后最短无复发存活的女性中鉴定的生化表型之间具有强的相似性。
本发明包括癌发生的新概念,其将对癌症的基因组基础的现有理解并入到根本不同的范例中。发现提示人基因组的癌症“应征者(conscript)”满足其在系统性代谢应激条件下的需要。
可以看到健康和癌症反映由线粒体和过氧化物酶体功能障碍的不同水平引起的潜在的IEM样表型状态。这些在正常寿命过程内的功能障碍可以导致或可以不导致那些识别为癌症的“代谢不全”的状况。随着年龄的增长,毒性代谢物、肿瘤代谢物、DNA和组蛋白甲基化的积累随恶性产生使它们从状态相对代偿倾斜为去代偿(de-compensation)之一。
本文描述了基于IEM,肝和甲状腺功能障碍以及腺祖系癌症所共有的表型特征的血液生物标志物组。
使用所鉴定的签名,发明人探索了与其它代谢应激状态的相关性,包括糖尿病和多囊卵巢综合征,并显示他们可以通过将低血糖小鼠暴露于外源胰岛素而在鼠模型中重演恶性表型。
这些表型签名共享人细胞代谢性干性的特征,并且提示在胰岛素/葡萄糖不平衡期间在系统上共享或重新激活发起成功胚胎发生(干性范例)的相同代谢级联。
在大多数群体中,所述代谢应激将被糖异生和脂肪酸氧化的上调所抵消。然而,表现出IEM样表型的人可能无法安排这些关键反应,导致对MYC相关代谢重编程的异常依赖性。
这将反映由应激物释放的恶性转化的根本“趋势”,所述应激物在乳腺癌中由恶化风险因子,例如未经产,肥胖和生活方式“揭示”,但是仅在那些携带先天引发特征的有素因的女性中表现。
发现在结肠癌患者的血液和肿瘤组织中鉴定的代谢表型与在那些相同患者的正常结肠粘膜中发现的签名相同,这支持癌症作为系统性代谢功能不全状态的局部表现出现的假设。
因此,根据遗传的、轻度到中度但不严重得足以在大部分生命期间引起疾病的代谢缺陷(暗示IEM),代谢应激的不同水平将在个体间不同。
这些签名以95%的准确度鉴定临床乳腺癌,而与阶段、组织学、固有亚型、BMI、绝经状态或年龄无关,并且还显示预测对新辅助化疗的肿瘤反应和总存活。
这些发现的临床意义有几个,并且包括开发用于早期检测乳腺癌的新的诊断测试及其用于预后和预测反应的应用。发现也可应用于腺组织学的其它癌症。更重要的是,这些结果反映了表型签名的应用,其当我们努力更全面理解人类疾病时能够与基因组学、转录物组学和蛋白质组学的进步充分吻合。
总之,本发明包括支持如下假设的表型证据:腺祖系癌症,特别是乳腺癌代表与MYC诱导的系统性病况相关的先前存在的代谢紊乱的最终结果:癌症为代谢副现象。
今天认为卵巢癌是一类恶性,其在大多数时间在其周围组织,特别是输卵管的非常外端的伞毛中起源。美国癌症协会估计,在美国,对于2018年,有约22,240例新病例,其中超过50%(14,070)的女性将死于该疾病。因此,卵巢癌比女性生殖系统的任何其它癌症造成更多的死亡。这种癌症主要在63岁以上的女性中形成,并且它在白人中比非洲裔美国女性中更常见。
卵巢癌难以检测,特别是在早期。这部分是由于卵巢——子宫任一侧的两个小杏仁形器官——在腹腔内较深的事实。
诊断患有卵巢癌的女性的少于一半存活超过5年,并且尽管患有局部卵巢癌的患者的5年存活超过90%,但所有女性中只有15%诊断患有局部疾病。
目前,没有组织推荐筛选卵巢癌的平均风险女性。然而,卵巢癌的筛选和诊断方法包括盆腔检查,作为肿瘤标志物的癌抗原125(CA125),经阴道超声(TVU),以及潜在地多标志物组和蛋白质组模式的生物信息学分析。
然而,当单独使用或组合使用时,用于筛选的这些测试的性能较差。盆腔检查检测无症状卵巢癌的灵敏性和特异性较差,并且不支持体检作为筛选法。CA125具有有限的灵敏性和特异性,当独立或组合使用时TVU也是如此。
在2011年,前列腺肺结肠直肠和卵巢(PLCO)倡导推断,对于卵巢癌的筛选,有足够的证据表明,用CA125和TVU进行每年筛选不降低卵巢癌的死亡率,并且有足够的证据表明,卵巢癌的筛选可导致重要的危害,主要是在没有卵巢癌的女性中的外科干预。
因此,在本领域中迫切需要新的且高度灵敏的筛选程序,优选不太苛求,不需要几个专门的装置和人员或资源。
鉴于本领域中存在的上述问题,本发明的基本目的是提供用于评估卵巢癌的新的生物标志物,其允许在疾病发展的早期阶段以高精确性和可靠性筛选卵巢癌。
最佳地,标志物应当容易地在生物样品如血液中检测到,并且其水平应当始终与卵巢癌的阶段相关。此外,本发明的一个目的是提供一种用于评估生物样品中卵巢癌的方法,其允许快速、方便和高通量的性能。
为了解决本发明的基本目的,发明人基于他们对代谢物组学的研究,因为它可以给出卵巢癌发展过程中发生的生化变化的认识,并提供几种新的且潜在更好的生物标志物。
本发明是一种早期诊断工具,当干预提供了最高的治愈可能性时,其鉴定最早期阶段的卵巢癌患者。本发明提供预后信息,并且充当临床反应和存活的预测性测试。
发明人发现,当使用一组与癌症并行改变的代谢物而不是使用本领域中进行的筛选技术,如超声时,给出了涉及卵巢癌的所有代谢物组学途径和机制的更全面的图像。
因此,本发明提供了适于评估卵巢癌的从未描述过的生物标志物(即新的生物标志物集),包括疾病的早期和更晚期阶段,并且还提供了在基线上清楚地区分初始治疗后复发风险升高的患者的生物标志物集。
此外,本发明还提供了一种评估哺乳动物受试者的卵巢癌的方法,该方法是在考虑到不仅与几种其它恶性,而且还与几种代谢良性状况的全面和广泛比较的情况下实现和发展的,因此,可被认为是理想的肿瘤标志物的最近阶段。
特别地,将靶向性定量质谱法(MS/MS)应用于卵巢癌患者的血液导致产生代谢签名,其为患有卵巢癌的女性和处于该疾病风险的那些女性提供临床上经验证的诊断和预后信息。
靶向性定量MS/MS提供了对于精确确定临床上相关代谢签名必需的代谢物的注释血液浓度。个别的代谢物浓度和定性非靶向性测量不提供精确鉴定癌症相关的代谢紊乱所需要的必需严格性。
在第一个实施方案中,本发明的生物标志物和生物标志物组用于筛选潜在患有卵巢癌的受试者,例如人类患者,以及诊断这些受试者中的卵巢癌。
令人惊讶地发现,在本发明中,本文所述的生物标志物和生物标志物组特别可用于大量受试者,诸如人患者的快速、简单且高通量的筛选,并可用于以改善的结果准确性诊断来自这些受试者的血液样品的卵巢癌。
尽管使用上述指定的生物标志物组合得到的筛选和/或诊断的准确性和可靠性(如通过特异性,灵敏性,PPV和NPV中的一种或多种参数确定)与现有技术如超声相比已经大大改善,但是可以通过使用一种或多种,优选两种或多种,进一步优选三种或多种另外的代谢物来进一步改善准确性和可靠性。
因此,在优选的实施方案中,生物标志物组还包括一个或多个另外的氨基酸,例如包括在图2中的那些。另外的氨基酸优选选自生成葡萄糖/生酮氨基酸,例如甘氨酸,半胱氨酸,丙氨酸,精氨酸,脯氨酸,天冬氨酸,天冬酰胺,甲硫氨酸,异亮氨酸,亮氨酸,赖氨酸,苏氨酸,苯丙氨酸,酪氨酸和色氨酸,最优选天冬酰胺和天冬氨酸。
此外,脂质优选选自鞘脂和甘油脂,例如甘油磷脂,例如图4-6中所包括的一种或多种脂质。
进一步优选地,脂质源自花生四烯酸,优选含有36个或更多个碳原子的花生四烯酸衍生的脂质,最优选选自花生四烯酸多不饱和磷脂酰胆碱酰基-烷基或酰基-酰基,花生四烯酸单不饱和磷脂酰胆碱酰基-烷基或酰基-酰基和花生四烯酸饱和磷脂酰胆碱酰基-烷基或酰基-酰基。
在另一个优选的实施方案中,代谢物的组合还包括图4-6中所述的一种或多种脂质和图3中所述的一种或多种酰基肉碱以及肉碱(C0)。
由于本实施方案的方法可以从血液样品中进行,因此与现有技术的筛选技术如超声相比,该方法大大提高了受试者的顺应性。特别地,该方法大大提高了筛选结果的可靠性和灵敏性,特别是减少了假阳性和假阴性结果的数量,并且耗时较少,因此可以针对大量患者进行。
这可以在例如图12A和B中看到,显示为评估卵巢癌而开发的签名(即,本发明的一个实施方案)具有98.46%的灵敏性,96.62%的特异性和99.90%的阴性预测值。特别地,图12A示出了卵巢癌患者(n-64)与健康参与者以及其它恶性和非恶性病况(n=1001)相比的多变量ROC曲线分析。图12B描述了卵巢癌患者的鉴定的代谢物和比率的性能。近100%的阴性预测值(99.90%)使得本测试高度指示为有力的筛选工具。
图13示出卵巢癌患者(n=64)与健康参与者以及其它恶性和非恶性病况(n=1001)相比的Ortho-PLSDA评分图。通过处理(例如,分离,定量,标准化等)每个样品(例如血液样品),然后基于至少一个卵巢癌签名(如发明人所鉴定)绘制初始结果(例如,使用Ortho-PLSDA评分图),每个患者清楚落入(a)对照组或(b)卵巢癌组。
此外,签名的部分提供了关于每个患者预后的细节。这可以在例如图14A-D中看到,其中各种方程式(在每个图表的顶部鉴定)为每个患者提供存活率(预后)信息。因此,本发明人不仅鉴定可用于诊断卵巢癌的签名,而且还鉴定用于预后卵巢癌的签名。应当理解,虽然图13和14A-D中提供的图显示了(a)卵巢癌的诊断和(b)存活率,但是本发明不限于此,并且卵巢签名(或其部分)可用于提供卵巢癌的其它评估,包括筛选,诊断,预后,治疗,如以下结果部分中更详细讨论的。
在图15中提供了用于评估卵巢癌的优选签名(或其部分),包括核心卵巢癌方程式,代谢物增强剂,比率增强剂和具有增强剂的核心方程式。如图15中可以看到,核心卵巢癌方程式为(C5:1/C5:1-DC),或甲基巴豆酰肉碱与戊烯二酰肉碱的比率(见图3)。发明人已经发现,在定量,标准化等之后个体代谢物的此比率对于评估卵巢癌患者是关键的。其它关键部分包括[Orn/(AspdC18:1)](其中“d”除以,即Asp/C18:1)),[(Orn/Arg)Trp],[C12-DC/(C5:1/C5:1-DC)]和[(C18:1/Asp)/(C5:1/C5:1-DC)],其不仅可用于卵巢癌的诊断,而且可用于卵巢癌的预后。
虽然不是对本发明的限制,但是血浆和组织样品的靶向代谢物组学分析可以使用Biocrates Absolute-IDQ P180(BIOCRATES,Life Science AG,Innsbruck,Austria)进行。此种验证的靶向测定允许以高通量的方式同时检测和定量血浆和组织样品中的代谢物。
如乳腺癌患者和方法部分所讨论的,血液代谢物的绝对定量(μmol/L)可以通过在多个生物样品中通过电喷雾电离(ESI)串联质谱法(MS/MS)对186个注释的代谢物进行靶向定量概况分析来实现。在该部分中所述的过程同样适用于本文,其中靶向概况分析方案用于定量筛选完全注释的代谢物,生成xls文件,其包括样品鉴定和186个代谢物名称和浓度,单位为μmol/L血浆,并且对所有定量的代谢物应用对数转化以使浓度分布标准化并进行处理。然后生成ROC曲线,并使用显著特征来建立分类模型。
使用p180试剂盒(BIOCRATES Life Sciences AG,Innsbruck,Austria)定量总共186种注释的代谢物,包括在乳腺癌-患者和方法部分中描述的。同样,将与特定功能相关的代谢物组作为比率组装,并观察其它数学关系(如上所讨论)(例如,氨基酸水平的总和,总酰基肉碱的总和,饱和,单不饱和及多不饱和结构脂质总和之间的比率等)。参见上文在乳腺癌患者和方法学部分中的讨论。
对于卵巢癌,将样品注射到与AB-Sciex 5600Triple TOF质谱仪偶联的ShimadzuProminence LC系统,采集扫描速率为100谱/秒,稳定质量精确性约2ppm。以甲醇/水(90/10)与5.0mM甲酸铵使用等度洗脱进行流动注射分析(FIA)。流速和注射体积分别为0.025mL/min和50μL。
没有进行离子源或去聚类(declustering)电位(50V和-40V)的优化。施加以下电离参数:CUR=20psi,GS1=20psi,GS2=15psi,温度=250℃,IS=5000V(-4000V)。范围为m/z 100至1200,积累时间0.25s的MS扫描和m/z 100至1200和积累时间0.03s的产物离子扫描分别是测量和从属扫描期间采用的参数。
图8提供了使用靶向定量MS/MS限定卵巢癌存在的具体参数。图9提供了使用靶向定量MS/MS限定卵巢癌存在的特定代谢比率。
当检查具有不同肿瘤(肺,结肠,肝,白血病,淋巴瘤和头颈鳞状细胞癌)的患者的代谢概况时,结果证明谷氨酰胺消耗增加,特别是在患有腺祖祖系肿瘤的患者中。将这些研究扩展到包括患有多囊卵巢综合征(PCOS),肝硬化,乳腺癌的高风险和5期代谢综合征的患者,揭示了这些无癌参与者表现出与在腺癌患者中的发现情况非常相似的谷氨酰胺分解概况。
在体外证明了“谷氨酸牵引效应”之后,组装比率(Glu/己糖),其中恶性细胞培养物中葡萄糖饥饿通过MYC协调反应导致谷氨酸升高。在患有腺癌的患者,乳腺癌风险较高的患者和患有PCOS的个体的血液中清楚地鉴定出此种效应。值得注意的是,由基于群体的正常对照或患有非腺肿瘤(白血病,淋巴瘤,多发性骨髓瘤和鳞状细胞癌)的患者组成的对照组都没有揭示该比率的显著变化,特别是揭示出与对照组相似水平的鳞状细胞癌。“谷氨酸牵引效应”的增加已经在由葡萄糖饥饿诱导的代谢应激条件下描述。
一致地,发明人发现患者血液己糖浓度与我们的乳腺癌方程式{[PC aa 36:6/[(Val/Phe)/牛磺酸]/C10:2}的值之间的显著的(P=0.003,FDR=0.009)反相关性。与在以“谷氨酸牵引效应”测量的相对低血糖的条件下促进腺癌的前提一致,他们的结果提示,血糖水平的分离测定相对于其它代谢中间体可能不像测量己糖水平那样提供信息,所述代谢中间体包括:i)线粒体肉碱棕榈酰基转移酶II(CPT-2)缺陷比率(C16/C3),ii)过氧化物酶体损伤生物标志物lysoPC a C26:0,lysoPC a C26:1和lysoPC a C28:1,或iii)其与谷氨酰胺分解的关系[Phe/(Gln/Glu)/Asp]。
重要的是,CPT-2和过氧化物酶体缺陷两者(公知的先天代谢错误)都与患病患者的低血糖有关。如果由于先天样的代谢错误而在卵巢癌中出现相对低血糖状态,那么与慢性低血糖相关的超高胰岛素血症将构成一种强有力的代谢应激者,即使在没有癌症的情况下,该代谢应激者也能够系统地上调糖酵解和谷氨酰胺分解。
总之,致癌是一种复杂的多基因过程,它利用了许多改变的细胞功能,最终导致几十年来不可逆的恶性转化状态。作为静态测量的分子签名不能捕获生物过程的动态特性,因为它们不能涵盖这些事件的复杂性、冗余性和混杂性。
恶性转化需要细胞成功经过代谢,结构和免疫规避策略。该方法使用多维发明将恶性转化定义为代谢签名。
本发明使用靶向性定量MS/MS来定义卵巢癌患者中生物能学、生物合成和免疫表型之间的独特且以前未知的关系。该签名定义卵巢癌表型,并应用于诊断卵巢癌患者和有形成卵巢癌风险的患者并为其提供预后信息。
本发明扩展到其它恶性,因为在卵巢癌和其它肿瘤类型之间存在共同性,并且适用于尿液和唾液,因为这些体液代表了用于评估血液中定义的代谢签名的其它材料来源。
结肠直肠癌是美国男性和女性两者中诊断的第三常见的恶性,并且根据美国癌症协会估计预计来年总共有101,523例CRC新病例,即97,220例结肠癌和43,030例直肠癌。
总体上,形成结肠直肠癌的终身风险是:在美国,约22分之一(4.49%)的男性和约24分之一(4.15%)的女性是癌症相关死亡的第三主要原因。
目前有3种体外诊断(IVD)试验通常用于CRC筛选,粪便免疫化学测试(FIT),基于粪便的DNA测试和基于血液的DNA测试(SEPT9测定)。代替旧的粪便潜血测试(FOBT)的FIT测试以低成本表现出令人满意的灵敏性(79%)和特异性(94%),因此成为目前CRC的主要筛选测试。
由于多种方法的组合,粪便DNA测试的灵敏性似乎非常高,尽管其高成本是阻碍测试广泛使用的障碍。CRC筛选中SEP9测试的灵敏性和特异性都低于FIT和粪便DNA测试的,但是如果其准确性可以得到改善,则其显示出高的顺应性,具有有希望的未来。
具有多个标志物的组合测试应当是CRC筛选的未来方向,然而,在它们能够用于针对无症状平均风险群体的大规模CRC筛选之前,需要克服一些障碍,例如技术集成,测试/解释优化和高成本等。
CEA和碳水化合物抗原199(CA199)是两种最常见的基于血清的糖蛋白CRC标志物,但是它们不适于CRC筛选,这是由于它们的低灵敏性和缺乏CRC特异性,特别是对于早期CRC。
例如,CEA测试在三个研究中对于CRC检测表现出40.9%-51.8%的灵敏性和85.2%-95%的特异性。因此,它更适合用于监测CRC复发或患者对手术或全身治疗的反应,而不是筛选。CRC筛选中血清糖蛋白标志物的主要缺点是任何单一标志物的灵敏性和特异性高得不足以使其成为可靠的指标。
鉴于本领域中存在的上述问题,本发明的基本目的是提供新的用于评估结肠直肠癌的生物标志物,其允许在疾病进展的早期阶段中以高精确性和可靠性筛选结肠直肠癌。
优选地,标志物应当容易地在生物样品如血液中检测到,并且其水平应当始终与结肠直肠癌的阶段相关。此外,本发明的一个目的是提供一种用于评估生物样品中结肠直肠癌的方法,其允许快速、方便和高通量的性能。
为了解决本发明的基本目的,发明人基于他们对代谢物组学的研究,因为它可以给出结肠直肠癌形成过程中发生的生化变化的认识,并提供几种新的和潜在更好的生物标志物。
发明人发现,当使用与癌症并行改变的代谢物组而不是使用本领域中进行的筛选技术,诸如超声时,给出了涉及结肠直肠癌的所有代谢物组学途径和机制的更全面的图像。
因此,在本发明的一个实施方案中,提供了适用于评估结肠直肠癌,包括疾病的早期和更晚期的从未描述的生物标志物(即新的生物标志物组)。还包括生物标志物组,其在基线上清楚地区分初期治疗后具有升高的复发风险的患者。
此外,本发明还提供了一种评估哺乳动物受试者中的结肠直肠癌的方法,该方法是在考虑到不仅与几种其它恶性,而且还与几种代谢良性病况的全面和广泛比较的情况下实现和发展的,因此,可被认为是理想的肿瘤标志物的最近阶段。
在第一个实施方案中,本发明的生物标志物和生物标志物组用于筛选潜在患有结肠直肠癌的受试者,例如人类患者,以及诊断这些受试者中的结肠直肠癌。
令人惊讶地发现,在本发明中,本文所述的生物标志物和生物标志物组特别可用于大量受试者,诸如人患者的快速、简单且高通量的筛选,并可用于以改善的结果准确性诊断来自这些受试者的血液样品的结肠直肠癌。
尽管使用上述指定的生物标志物组合得到的筛选和/或诊断的准确性和可靠性(如通过特异性,灵敏性,PPV和NPV中的一种或多种参数确定)与现有技术如超声相比已经大大改善,但是可以通过使用一种或多种,优选两种或多种,进一步优选三种或多种另外的代谢物来进一步改善准确性和可靠性。
因此,在优选的实施方案中,生物标志物组还包括一个或多个另外的氨基酸,例如包括在图2中的那些。另外的氨基酸优选选自生成葡萄糖/生酮氨基酸,例如甘氨酸,半胱氨酸,丙氨酸,精氨酸,脯氨酸,天冬氨酸,天冬酰胺,甲硫氨酸,异亮氨酸,亮氨酸,赖氨酸,苏氨酸,苯丙氨酸,酪氨酸和色氨酸,最优选天冬酰胺和天冬氨酸。
此外,脂质优选选自鞘脂和甘油脂,例如甘油磷脂,例如图4-6中所包括的一种或多种脂质。
进一步优选地,脂质源自花生四烯酸,优选含有36个或更多个碳原子的花生四烯酸衍生的脂质,最优选选自花生四烯酸多不饱和磷脂酰胆碱酰基-烷基或酰基-酰基,花生四烯酸单不饱和磷脂酰胆碱酰基-烷基或酰基-酰基和花生四烯酸饱和磷脂酰胆碱酰基-烷基或酰基-酰基。
在另一个优选的实施方案中,代谢物的组合还包括图4-6中所述的一种或多种脂质和图3中所述的一种或多种酰基肉碱以及肉碱(C0)。
由于本实施方案的方法可以从血液样品中进行,因此与现有技术的筛选技术如超声相比,该方法大大提高了受试者的顺应性。特别地,该方法大大提高了筛选结果的可靠性和灵敏性,特别是减少了假阳性和假阴性结果的数量,并且耗时较少,因此可以针对大量患者进行。
这可以在例如图16A和B中看到,显示为评估结肠癌而开发的签名(即,本发明的一个实施方案)具有98.84%的灵敏性,98.40%的特异性和99.88%的阴性预测值。特别地,图16A示出了结肠癌患者(n-85)与健康参与者以及其它恶性和非恶性病况(n=800)相比的多变量ROC曲线分析。图16B描述了结肠癌患者的鉴定的代谢物和比率的性能。近100%的阴性预测值(99.88%)使得本测试高度指示为有力的筛选工具。
图17示出了结肠癌患者(n=85)与健康参与者以及其它恶性和非恶性病况(n=800)相比的Ortho-PLSDA评分图。通过处理(例如,分离,定量,标准化等)每个样品(例如血液样品),然后基于至少一个结肠癌签名(如发明人所鉴定)绘制初始结果(例如,使用Ortho-PLSDA评分图),每个患者清楚落入(a)对照组或(b)结肠癌组。
此外,签名的部分提供了关于每个患者预后的细节。这可以在例如图18A-C中看到,其中各种方程式(在每个图表的顶部鉴定)为每个患者提供存活率(预后)信息。因此,本发明人不仅鉴定可用于诊断结肠癌的签名,而且还鉴定用于预后结肠癌的签名。应当理解,虽然图17和18A-C中提供的图显示了(a)结肠癌的诊断和(b)存活率,但是本发明不限于此,并且结肠签名(或其部分)可用于提供结肠癌的其它评估,包括筛选,诊断,预后,治疗结肠癌,如以下结果部分中更详细讨论的。
在图19中提供了用于评估结肠癌的优选签名(或其部分),包括核心卵巢癌方程式,代谢物增强剂,和具有增强剂的核心方程式。如图19中可以看到,核心卵巢癌方程式为(C16:1/PC aa C34:2),或十六烯酰基肉碱与磷脂酰胆碱与二酰基残基总和的比率(见图3和5)。发明人已经发现,在定量,标准化等之后个体代谢物的此比率对于评估结肠癌患者是关键的。其它关键部分包括{SM C20:2/[(C16:1/PC aa C34:2)/C5:1-DC]},{SM OH C16:1/[(C16:1/PC aa C34:2)/C5:1-DC]},和{SM OH C14:1/[(C16:1/PC aa C34:2)/C5:1-DC]},其不仅可用于结肠癌的诊断,而且可用于结肠癌的预后。
当胰腺(胃后面的腺器官)中的细胞开始失控增殖并形成团块时发生胰腺癌。这些癌性细胞可侵入身体的其它部分。通常在疾病的早期阶段中没有症状,并且足够特异以提示胰腺癌的症状典型地直到疾病达到晚期才形成。在诊断时,胰腺癌常常传播到身体的其它部位。
在2015年,所有类型的胰腺癌导致全球411,600人死亡。胰腺癌在英国是第五常见的癌症死亡原因,在美国是第三常见的癌症死亡原因。该疾病最常在发展中世界形成,其中在2012年起源约70%的新病例。胰腺腺癌通常具有非常差的预后:诊断后,25%的人存活一年,并且5%的人存活五年。对于早期诊断的癌症,5年存活率提高到约20%。
胰腺癌通常通过医学成像技术的组合来诊断,所述医学成像技术例如超声或计算机断层摄影术,血液测试和组织样品的检查(活组织检查)。疾病分为早期(I期)到晚期(IV期)的阶段。尚未发现筛选一般群体是有效的。
鉴于本领域中存在的上述问题,本发明的基本目的是提供用于评估胰腺癌的新的生物标志物,其允许在疾病发展的早期阶段以高精确性和可靠性筛选胰腺癌。
最佳地,标志物应当容易地在生物样品如血液中检测到,并且其水平应当始终与胰腺癌的阶段相关。此外,本发明的一个目的是提供一种用于评估生物样品中胰腺癌的方法,其允许快速、方便和高通量的性能。
为了解决本发明的基本目的,发明人基于他们对代谢物组学的研究,因为它可以给出胰腺癌发展过程中发生的生化变化的认识,并提供几种新的且潜在更好的生物标志物。
发明人发现,当使用一组与癌症并行改变的代谢物而不是使用本领域中进行的筛选技术,如超声或计算机断层摄影术时,给出了涉及胰腺癌的所有代谢物组学途径和机制的更全面的图像。
因此,在本发明的一个实施方案中,提供了适于评估胰腺癌的从未描述过的生物标志物(即新的生物标志物组),包括疾病的早期和更晚期阶段。还包括在基线上清楚地区分初始治疗后复发风险升高的患者的生物标志物组。
此外,本发明还提供了一种评估哺乳动物受试者的胰腺癌的方法,该方法是在考虑到不仅与几种其它恶性,而且还与几种代谢良性病况的全面和广泛比较的情况下实现和发展的,因此,可被认为是理想的肿瘤标志物的最近阶段。
在第一个实施方案中,本发明的生物标志物和生物标志物组用于筛选潜在患有胰腺癌的受试者,例如人类患者,以及诊断这些受试者中的胰腺癌。
令人惊讶地发现,在本发明中,本文所述的生物标志物和生物标志物组特别可用于大量受试者,诸如人患者的快速、简单且高通量的筛选,并可用于以改善的结果准确性诊断来自这些受试者的血液样品的卵巢癌。
尽管使用上述指定的生物标志物组合得到的筛选和/或诊断的准确性和可靠性(如通过特异性,灵敏性,PPV和NPV中的一种或多种参数确定)与现有技术如超声相比已经大大改善,但是可以通过使用一种或多种,优选两种或多种,进一步优选三种或多种另外的代谢物来进一步改善准确性和可靠性。
因此,在优选的实施方案中,生物标志物组还包括一个或多个另外的氨基酸,例如包括在图2中的那些。另外的氨基酸优选选自生成葡萄糖/生酮氨基酸,例如甘氨酸,半胱氨酸,丙氨酸,精氨酸,脯氨酸,天冬氨酸,天冬酰胺,甲硫氨酸,异亮氨酸,亮氨酸,赖氨酸,苏氨酸,苯丙氨酸,酪氨酸和色氨酸,最优选天冬酰胺和天冬氨酸。
此外,脂质优选选自鞘脂和甘油脂,例如甘油磷脂,例如图4-6中所包括的一种或多种脂质。
进一步优选地,脂质源自花生四烯酸,优选含有36个或更多个碳原子的花生四烯酸衍生的脂质,最优选选自花生四烯酸多不饱和磷脂酰胆碱酰基-烷基或酰基-酰基,花生四烯酸单不饱和磷脂酰胆碱酰基-烷基或酰基-酰基和花生四烯酸饱和磷脂酰胆碱酰基-烷基或酰基-酰基。
在另一个优选的实施方案中,代谢物的组合还包括图4-6中所述的一种或多种脂质和图3中所述的一种或多种酰基肉碱以及肉碱(C0)。
由于本实施方案的方法可以从血液样品中进行,因此与现有技术的筛选技术相比,该方法大大提高了受试者的顺应性。特别地,该方法大大提高了筛选结果的可靠性和灵敏性,特别是减少了假阳性和假阴性结果的数量,并且耗时较少,因此可以针对大量患者进行。
这可以在例如图20A和B中看到,显示为评估胰腺癌而开发的签名(即,本发明的一个实施方案)具有100%的灵敏性,97.93%的特异性和100%的阴性预测值。特别地,图20A示出了胰腺癌患者(n-10)与健康参与者以及其它恶性和非恶性病况(n=709)相比的多变量ROC曲线分析。图20B描述了胰腺癌患者的鉴定的代谢物和比率的性能。100%的阴性预测值使得本测试高度指示为有力的筛选工具。
图21示出胰腺癌患者(n=10)与健康参与者以及其它恶性和非恶性病况(n=709)相比的Ortho-PLSDA评分图。通过处理(例如,分离,定量,标准化等)每个样品(例如血液样品),然后基于至少一个胰腺癌签名(如发明人所鉴定)绘制初始结果(例如,使用Ortho-PLSDA评分图),每个患者清楚落入(a)对照组或(b)胰腺癌组。
此外,签名的部分提供了关于每个患者预后的细节。这可以在例如图22A和B中看到,其中各种方程式(在每个图表的顶部鉴定)为每个患者提供存活率(预后)信息。例如,图22A区分短存活期(如6个月)和长存活期(如15个月)。图22B也区分短期和长期存活期,但进一步验证了这些发现能够证明代谢方程式在存活预测中是完全有功能的,即使是在不同来源的恶性中,如多发性骨髓瘤(M.M.)、白血病、淋巴瘤和脊髓发育不良(ISS 1,2,3=国际标度系统,Hem=血液恶性,Panc=胰腺癌)。因此,发明者不仅鉴定出可以用来诊断胰腺癌的签名,而且还可以预后胰腺癌的签名。
应当理解,虽然图21和22A-B中提供的图显示了(a)胰腺癌的诊断和(B)存活率,但是本发明并不限于此,并且胰腺签名(或其部分)可用于提供胰腺癌的其它评估,包括筛查、诊断、预后、治疗胰腺癌,如在下文的结果部分中更详细讨论。
在图23中提供了用于评估胰腺癌的优选签名(或其部分),包括核心胰腺癌方程式,代谢物增强剂,和具有增强剂的核心方程式。如图23中可以看到,两个核心胰腺癌方程式为(C3:1/C12-DC),或丙烯酰肉碱与癸基二酰肉碱的比率和(2)(C6:1/C12-DC),或十六烯酰基肉碱与癸基二酰肉碱的比率。参见图3。发明人已经发现在定量,标准化等之后个体代谢物的此比率对于评估胰腺癌患者是关键的。其它关键部分包括(C:12-DC/lysoPC a C17:0)和(C12-DC/lysoPC a C17:0),其不仅可用于胰腺癌的诊断,而且可用于胰腺癌的预后。
急性移植物抗宿主病(AGVHD)和同种异体造血干细胞移植(AHSCT)风险签名
同种异体造血干细胞移植(AHSCT)举例说明了对多种血液学恶性的有效治疗策略的使用,使得该技术的无瑕性(flawlessness)现在延长其实施。然而,该技术不是没有任何问题。
实际上,免疫仲裁(arbitrated)的困难,例如急性(AGVHD)和慢性移植物抗宿主病(CGVHD),通常在超过50%的经受AHSCT的患者中观察到,仍然是存活中非常重要的限制因素。
因此,AHSCT的适应症应当更加个体化,并且基于用常规化疗预期的长期无疾病存活与移植后复发的风险和治疗相关的死亡率/发病率的风险。
然而,基于移植前预后因素的一些策略与长期存活相关;可用的临床和/或生化工具无一能够准确地预测AGVHD的发生。
考虑到本领域中存在的上述问题,本发明的基本目的是提供新的生物标志物,用于在启动同种异体造血干细胞移植(AHSCT)程序之前评估形成AGVHD风险增加的患者。
最佳地,标志物应当容易地在生物样品如血液中检测到,并且其水平应当始终与血液学癌症的阶段相关。此外,本发明的一个目的是提供一种用于评估生物样品中血液学癌症的方法,其允许快速、方便和高通量的性能。
为了解决本发明的基本目的,发明人基于他们对代谢物组学的研究,因为它可以给出血液学癌症发展过程中发生的生化变化的认识,并提供几种新的且潜在更好的生物标志物。
发明人发现,当使用一组与癌症行为并行改变的代谢物时,给出了涉及血液学恶性的所有代谢物组学途径和机制的更全面的图像。
因此,在本发明的一个实施方案中,提供了适于在基线评估同种异体造血干细胞移植(AHSCT)移植物后形成AGVHD的风险的新的生物标志物(即新的生物标志物组)。
此外,本发明还提供了一种基于本文所述的生物标志物和生物标志物组来评估哺乳动物受试者的血液学癌症的方法。
令人惊讶地发现,在本发明中,本文所述的生物标志物和生物标志物组特别可用于大量受试者,诸如人患者的快速、简单且高通量的筛选,并可用于以改善的结果准确性诊断来自这些受试者的血液样品的血液学癌症。
尽管使用上述指定的生物标志物组合得到的筛选和/或诊断的准确性和可靠性(如通过特异性,灵敏性,PPV和NPV中的一种或多种参数确定)与现有技术如超声相比已经大大改善,但是可以通过使用一种或多种,优选两种或多种,进一步优选三种或多种另外的代谢物来进一步改善准确性和可靠性。
因此,在优选的实施方案中,生物标志物组还包括一个或多个另外的氨基酸,例如包括在图2中的那些。另外的氨基酸优选选自生成葡萄糖/生酮氨基酸,例如甘氨酸,半胱氨酸,丙氨酸,精氨酸,脯氨酸,天冬氨酸,天冬酰胺,甲硫氨酸,异亮氨酸,亮氨酸,赖氨酸,苏氨酸,苯丙氨酸,酪氨酸和色氨酸,最优选天冬酰胺和天冬氨酸。
此外,脂质优选选自鞘脂和甘油脂,例如甘油磷脂,例如图4-6中所包括的一种或多种脂质。
进一步优选地,脂质源自花生四烯酸,优选含有36个或更多个碳原子的花生四烯酸衍生的脂质,最优选选自花生四烯酸多不饱和磷脂酰胆碱酰基-烷基或酰基-酰基,花生四烯酸单不饱和磷脂酰胆碱酰基-烷基或酰基-酰基和花生四烯酸饱和磷脂酰胆碱酰基-烷基或酰基-酰基。
在另一个优选的实施方案中,代谢物的组合还包括图4-6中所述的一种或多种脂质和图3中所述的一种或多种酰基肉碱以及肉碱(C0)。
由于本实施方案的方法可以从血液样品中进行,因此与现有技术的筛选技术如超声相比,该方法大大提高了受试者的顺应性。特别地,该方法大大提高了筛选结果的可靠性和灵敏性,特别是减少了假阳性和假阴性结果的数量,并且耗时较少,因此可以针对大量患者进行。
确定和提供结果
本发明可涉及访问医生,临床医师,技师,护士等的患者,其中收集血液或不同的样品。然后将样品提供给实验室进行分析,如上所讨论(例如质谱法,对数转化,比较等)。在另一个实施方案中,使用试剂盒获得样品,其中试剂盒通过医疗设施,药店,因特网等可供给患者。在本实施方案中,试剂盒可以包括一个或多个孔和一个或多个浸渍有至少一种内部标准品的插入物。该试剂盒可用于从患者收集样品,然后将样品提供给实验室进行分析。
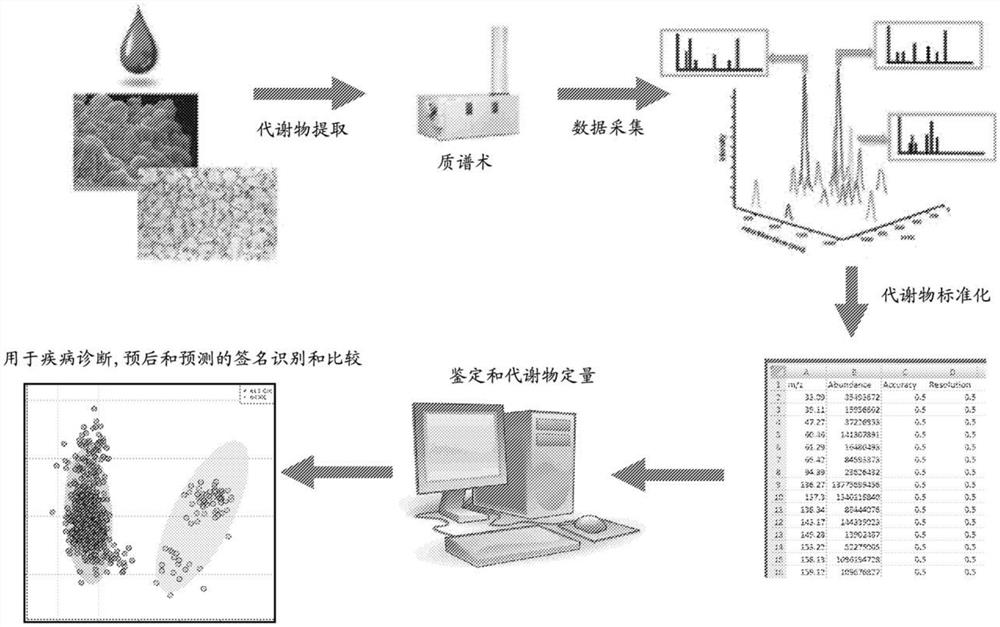
例如,如图1所示,外周血可以收集到EDTA-抗凝剂管中。通过离心分离血浆。然后可以将血浆样品提交到p180 AbsolutelDQ试剂盒中进行提取和处理。在一个实施方案中,然后将制备的样品进行液相色谱(LC),接着通过串联质谱法(MS/MS)进行流动注射分析(FIA)(即,代谢物提取)。然后使用计算机软件处理所提取的数据。例如,所获得的数据然后可以进行标准化(例如,通过对数转化),并存储在数据库中,该数据库至少包括(i)患者识别,(ii)代谢物名称,和(iii)定量。如果该数据是关于已知个体(具有已知状况的个体),则可以分析它以确定可用于评估特定疾病的签名。然而,如果数据关于病况未知的患者,则可以将其与已知的签名(例如,存储在存储器中)进行比较,以筛选,诊断,预测和治疗患者。
应当理解,本发明不限于使定量代谢物标准化。换言之,本文讨论的和/或本领域技术人员通常已知的其它过程可以在标准化之前或之后进行。还应理解,尽管某些过程可以手动进行,但是大多数(如果不是所有)应当优选地使用软件进行,其中将初始结果(质谱法后,标准化后数据)存储在存储器中,呈现在显示器(例如计算机监视器等)上和/或打印。然后可以将初始结果与不同疾病的已知“签名”进行比较,其中相似性和差异用于筛选,诊断,预测,治疗等特定疾病。应当理解,可以根据患者的性别,年龄等来针对特定疾病或多种疾病评估样品。因此,可以使用软件来评估特定疾病或评估多种疾病中的至少一种疾病。
还应当理解,“比较”步骤可通过(i)软件,(ii)人或(iii)两者来进行。例如,相对于现有技术,计算机程序可用于将样品结果与已知签名进行比较,并使用其差异和/或相似性来评估至少一种疾病,并为其提供诊断,预后和/或治疗。或者,在第二实施方案中,技术人员可以用来将样品结果与已知签名(或其方面)进行比较并基于感知的相似性和/或差异做出诊断,预后和/或治疗决定。最后,关于后者,可以使用计算机程序来绘制(例如,在计算机显示器上)样品结果与已知的签名(例如,健康患者的签名,不健康患者的签名,预期寿命等)。然后,技术人员可以查看它,并基于所绘制的信息中的相似性和/或差异做出至少一个诊断,预后,治疗建议等。
最重要的是,允许评估疾病的是已知签名之间的差异和/或相似性,该评估是自动的(例如,由计算机执行),手动进行的(例如,由人进行),或者两者的组合。
然后将结果(例如,评估)直接(例如,通过电子邮件,电子通信等)或通过患者的医生提供给患者,并且可以包括筛选信息,诊断信息,预后信息和治疗信息。
特别地,本发明可用于区分癌性样品与正常样品。如果它是癌性的,则本发明可进一步用于区分乳房与卵巢,卵巢与肺,肺与结肠等。一旦鉴定出癌症(例如卵巢,乳房等),本发明可用于按程度,即癌症的相对恶性定义癌症。这可以使用术语(例如,非侵入性(例如,原位),侵入性,转移性,和致死性),至少一个量表(例如,1-10,1-100,A-F等)完成,其中量表的一端是低等级(例如,非侵入性),另一端是高等级(致死性),或其它可视形式(例如,彩色编码,2D或3D模型等)。
本发明也可用于提供预后。例如,在卵巢癌中,一旦鉴定出卵巢签名,本发明可用于提供签名(或多个签名)内的分级,将患者细分类为可能存活(例如,大于3年,5年,10年等),可能复发(例如,在3年,5年,10年等内),或可能死亡(例如,在3年,5年,10年等内)的患者。同样,可以使用术语(例如,低风险,中等风险,高风险等),至少一个量表或其它可视形式来提供预后。
本发明不仅可用于确定预期寿命和缓解率,它还可用于确定治疗或治疗的存活力(另一种形式的预后)。这可以是对疗法(例如激素,放射,化学治疗等)响应的可能性,这同样可以使用术语,至少一个量表或其它可视形式来提供。
因此,举例而言,本发明可用于确定(i)患者患有癌症的高可能性(诊断),(ii)癌症是卵巢癌的高可能性(诊断),(iii)可能的耐药性(预后),(iv)复发的高风险(预后),和(v)在3-5年内死亡的高风险(预后)。显然这是示例性的,并且可以使用本发明来鉴定(预测)其它疾病(例如,乳房,结肠,卵巢等),亚分类(例如,无痛,侵入性,非常侵入性等),预后(例如,在3年,5年,10年等内复发)和治疗(例如,对激素疗法,化疗,放射疗法等的抗性)。
本发明还可用于疾病的筛选。医学筛选是测试或询问的系统应用,以鉴定具有足够的特定病症风险的个体,从而受益于进一步的调查或直接的预防作用(这些个体没有因为该病症的症状而寻求医学关注)。本发明使用代谢签名来筛选被认为处于风险中的群体中的疾病。对于卵巢癌,这可以是具有家族史的40多岁(40s)或50多岁(50s)的女性,或其它风险因素。
应当理解,虽然已经关于本发明能从血液样品(或类似物)中识别何物提供了几个实施方案,但是本发明不限于此,并且其它类型的诊断和预后(包括治疗)在本发明的精神和范围之内。例如,乳腺癌可以被鉴定为导管、管状、髓质、粘液、乳头状、筛状、小叶等。它也可以通过其预后(例如三阴性等)来鉴定。本领域的技术人员将理解,可以为其它癌症提供类似的分类,其中此类分类对于本领域的技术人员是公知的。对于诊断和预后两者,所有这些分类都在本发明的精神和范围之内。
如图1所示,一旦接收和处理了样品(例如,使用技术,如用于首先鉴定签名的技术,例如质谱法处理(以定量代谢物),对数转化(或其它数学操作以使数据标准化)等),然后可以将初始结果(例如代谢物和/或其组)与签名(或其部分)比较,所述签名已经(由发明人)鉴定为可用于评估至少一种疾病。签名可以存储在存储器中,并且初始数据(即处理过的样品)可以与至少一个签名进行手动(例如,通过观察样品,或其初始结果,针对已知签名),自动(例如,使用计算机程序来识别样品或其初始结果与已知签名之间的差异和/或相似性)比较,或以这两种方式(例如,程序确定至少一个诊断/预后,并且技术人员审查数据以验证数据)进行比较。基于结果(即,比较结果),鉴定至少一个诊断和/或预后并将其提供给患者,所述诊断和/或预后可以包括或者可以不包括治疗。
结论
因此,描述了使用新的生物标志物来评估不同疾病的系统和方法的几个实施方案,对于本领域的技术人员来说应当明显的是,已经实现了系统和方法的某些优点。还应当理解,在本发明的范围和精神内可以对其进行各种修改、改编和替代实施方案。本发明仅由所附权利要求书限定。
- 用于预测,诊断和预后包括癌症在内的各种疾病的代谢组学签名
- 用于预测对抗血管生成药的应答和癌症预后的分子诊断测试
