SPNS2中和抗体
文献发布时间:2023-06-19 09:52:39
技术领域
本发明涉及SPNS2中和抗体。具体而言,涉及与脊椎动物的SPNS2特异性结合的SPNS2中和抗体。
背景技术
鞘氨醇-1-磷酸(S1P)是磷脂之一,作为S1P前体的鞘氨醇是从作为细胞膜构成要素的神经酰胺切出而生成的。鞘氨醇通过鞘氨醇磷酸化酶(SphK1、SphK2)进行磷酸化,在细胞内产生S1P(非专利文献1)。S1P经由5种受体(S1PR1、S1PR2、S1PR3、S1PR4、S1PR5)将各种信号传导至细胞内。根据使用S1PR1缺损小鼠的分析,S1PR1与以血管形成、淋巴细胞的迁移、心肌细胞的收缩为代表的多种生理作用有关(非专利文献2、3、4、5)。根据使用S1PR2缺损小鼠的分析,S1PR2与以神经的兴奋、内耳的结构维持、血管形成为代表的多种生理作用有关(非专利文献6、7、8)。根据使用S1PR3缺损小鼠的分析,S1PR3与心律(心拍リズム)、心肌细胞的存活、血管舒张相关(非专利文献9、10、11)。根据使用S1PR4缺损小鼠的分析,S1PR4与巨核细胞的分化、T细胞的分化、活化相关(非专利文献12、13、14)。根据使用S1PR5缺损小鼠的分析,S1PR5与少突胶质细胞的存活、NK细胞的迁移有关(非专利文献15、16)。
血液中(血中)和淋巴液中的S1P浓度为100nM~300nM,而在淋巴组织或其他组织内保持为10nM以下的低值(非专利文献17、18)。在淋巴细胞中表达的S1PR1,若存在高浓度的S1P则受体内化,与细胞外S1P不反应(非专利文献19)。在血液中和淋巴液中,淋巴细胞暴露于高浓度的S1P中,引起S1PR1的内化,其结果,淋巴细胞向淋巴组织内迁移。在淋巴组织内,由于细胞外S1P浓度保持较低水平,因此随着时间的经过,S1PR1的表达恢复。其结果,淋巴细胞开始向淋巴液中迁移(非专利文献17、18)。主要由红细胞、血小板、血管内皮、淋巴管内皮细胞产生S1P(非专利文献20)。ATP依赖性转运蛋白参与从红细胞、血小板向细胞外转运S1P。另一方面,SLC(Solute Carriers)样转运蛋白SPNS2参与从血管内皮、淋巴管内皮细胞向细胞外转运S1P(非专利文献21-27、专利文献1)。
SPNS2是与SLC家族的S1P的转运相关的转运蛋白。SPNS2存在于细胞膜表面,具有多次贯穿细胞膜的区域(跨膜区)。然而,SPNS2的跨膜结构域的数目在报道中有为11次(EMBL登录号:Q8IVW8)或12次(非专利文献28)的情况,关于SPNS2的氨基酸序列中的与相当于跨膜区的部位对应的部分氨基酸序列的位置或氨基酸残基数等,也根据要分析的软件而成为不同的结果。
SPNS2主要在血管内皮、淋巴管内皮细胞中表达,将S1P从细胞内向细胞外转运。根据使用SPNS2缺损小鼠的分析,可见血液中淋巴细胞的减少,在由OVA致敏而诱导过敏性气道(呼吸道)过敏反应的病态模型中,可见肺泡灌洗液中的炎性细胞因子的减少,在乙酰甲胆碱(methacholine)负荷气道阻力试验中,观察到气道阻力值的改善。在噁唑酮诱导性特应性皮炎模型中,皮肤的肥厚得到抑制。在DSS诱导性肠炎模型中,在SPNS2缺损小鼠中,体重减轻得到抑制,病态评分也降低。在通过直肠给予噁唑酮而引起的肠炎模型中观察到同样的结果。在实验性自身免疫性脑脊髓炎模型中,SPNS2缺损小鼠的病态评分降低,小脑中的炎症影像减少。在胶原蛋白诱导性关节炎模型中,SPNS2缺损小鼠的关节肿胀减轻,病态评分也减轻(非专利文献29)。在静脉内给予以恶性黒色肿瘤细胞为代表的各种肿瘤细胞而诱导的实验性肺转移模型中,在SPNS2缺损小鼠中,转移到肺的肿瘤数目显著降低(非专利文献30)。调节S1P受体信号的药剂芬戈莫德(fingolimod),具有S1P受体的激动剂活性,引起S1P受体的内化。通过给予芬戈莫德,S1PR1丧失功能,血液中淋巴细胞降低,从而发挥免疫抑制作用,被用作多发性硬化治疗药(非专利文献18)。根据非临床研究,期待对类风湿性关节炎(非专利文献31、32)、自身免疫性肠炎(非专利文献33)、哮喘(非专利文献34)、系统性红斑狼疮(非专利文献35,36、37)、抑制器官移植时的排斥反应(非专利文献38)等各种免疫疾病有效。在S1PR1选择性激动剂Ponesimod的第2期试验(临床试验)中改善了牛皮癣病态(非专利文献39)。
芬戈莫德是除外S1PR2的S1P受体活化药,被用作多发性硬化治疗药(非专利文献40)。已知芬戈莫德引起作为临床上的副作用的缓慢性心律失常(非专利文献41,42)。S1P受体在心肌细胞中表达,经由该S1P受体,芬戈莫德活化异三聚体G蛋白。经活化的G
恶性肿瘤(癌症)是日本人的主要死亡原因,在许多癌症种类中,仍然不存在根治疗法。如果是癌症的初期则也有可能通过切除而根治,但癌症由于远处转移而扩散到全身的情况下,预后变得非常差,治疗法的选择项也受到限制。
在癌症治疗中,使用对肿瘤细胞具有细胞障碍或增殖抑制作用的药剂、或抑制特定信号的分子靶向药(非专利文献46)。除了对肿瘤细胞直接作用以外,还使用通过活化自身免疫来排除肿瘤细胞的治疗法。CD8阳性T细胞、NK细胞具有去除肿瘤细胞的功能(非专利文献47)。由于具有抗新颖抗原的嵌合T细胞受体的嵌合抗原受体T细胞对癌症的治疗有效,因此得知抗新颖抗原的CD8阳性T细胞在癌症防御中承担重要的作用(非专利文献48)。已知NK细胞也承担守护自身不受肿瘤细胞侵害的重要作用。由于肿瘤细胞的异常增殖速度等所致的压力,压力依赖性分子在膜表面表达。该压力依赖性配体识别NK细胞的受体,承担将异常细胞从生物体内去除的作用。若在去除了NK细胞的小鼠中移植肿瘤细胞,则由于对肿瘤细胞的抵抗性显著减少,因此NK细胞也被识别为是具有抗肿瘤效果的重要细胞(非专利文献49)。近年来,在恶性黑色素瘤治疗中,可使用免疫疗法派姆单抗(Pembrolizumab)、纳武单抗(Nivolumab),虽然增加了新的选择项,但每种治疗法的奏功率均为50%左右,有必要建立新的治疗法(非专利文献50、51)。根据使用SPNS2缺损小鼠的分析,报道了SPNS2缺损小鼠显著地减少了从静脉内移入的恶性黑色素瘤在肺或肝脏中的定居(定着)。在该报道中,通过增加效应T细胞相对于调节性T细胞的比率,显示出T细胞的抗肿瘤效果更容易发挥。根据利用抗体去除CD8阳性T细胞、NK细胞的实验,报道了SPNS2缺损小鼠的肿瘤转移抑制效果是通过T细胞、NK细胞发挥的。根据该报道显示出,SPNS2抑制剂不仅是自身免疫疾病还可用作癌症的治疗药,而且还期待增强现有癌症免疫疗法的作用的效果(非专利文献30)。
根据现有信息,可期待SPNS2抑制剂成为对自身免疫疾病、癌症治疗有效的治疗药,到目前为止没有SPNS2抑制剂的报道。现有SLC转运蛋白的抑制剂主要是低分子化合物,但低分子化合物抑制剂的靶向选择性低,还会导致副作用的出现。与低分子化合物抑制剂相比,抗体药物的靶向特异性高,因脱靶而引起的副作用小(非专利文献52),但目前为止尚未报道存在抑制SLC转运蛋白的配体转运功能的抗体。另外,为了将抑制SPNS2功能的抗体(SPNS2中和抗体)应用于药物,该抗体必需识别SPNS2结构中暴露至细胞外的区域(细胞外环),且该细胞外环必需是发挥SPNS2功能的重要部分。然而,在以往的技术中,与SPNS2的结构有关的信息缺乏,并未特定出相当于细胞外环的部位,而且,没有关于对SPNS2功能而言为重要的细胞外环的部分的信息,因此难以获取可应用于医药的SPNS2中和抗体。
另一方面,作为抗S1P抗体的Sonepcizumab在肾癌的治疗用途中进行了临床试验,但目前尚未报道有充分的效果。另外,认为为了中和存在于血液或淋巴液中的S1P,需要大量的抗体,但是认为抑制将S1P向细胞外转运的SPNS2的功能,能够以更少的抗体有效地抑制S1P的作用。
现有技术文献
专利文献
专利文献1:日本专利第5885154号公报;
非专利文献
非专利文献1:Spiegel, S. and Milstien, S., Sphingosine-1-phosphate: anenigmatic signalling lipid. Nat Rev Mol Cell Biol. 2003; 4(5): 397-407页;
非专利文献2:Liu, Y., 等人, Edg-1, the G protein-coupled receptor forsphingosine-1-phosphate, is essential for vascular maturation. J Clin Invest.2000; 106(8): 951-61页;
非专利文献3:Allende, ML., 等人, Expression of the sphingosine 1-phosphatereceptor, S1P1, on T-cells controls thymic emigration. J Biol Chem. 2004 Apr9; 279(15): 15396-401页;
非专利文献4:Means, CK., 等人, S1P1 receptor localization confersselectivity for Gi-mediated cAMP and contractile responses. J Biol Chem. 2008May 2; 283(18): 11954-63页;
非专利文献5:O'Sullivan, C. and Dev, K. K. The structure and function ofthe S1P1 receptor. Trends Pharmacol Sci. 2013; 34(7): 401-12页;
非专利文献6:MacLennan, A. J., 等人, An essentialrole for the H218/AGR16/Edg-5/LP(B2) sphingosine 1-phosphate receptor in neuronal excitability. Eur JNeurosci. 2001; 14(2): 203-9页;
非专利文献7:MacLennan, A. J., 等人, The S1P2 sphingosine 1-phosphatereceptor is essential for auditory and vestibular function. Hear Res. 2006;220(1-2): 38-48页;
非专利文献8:Kono, M., 等人, The sphingosine-1-phosphatereceptors S1P1,S1P2, and S1P3 function coordinatelyduring embryonic angiogenesis. J BiolChem. 2004; 279(28): 29367-73页;
非专利文献9:Nofer, J. R., 等人, HDLinduces NO-dependent vasorelaxationvia the lysophospholipid receptor S1P3. J Clin Invest. 2004; 113(4): 569-81页;
非专利文献10:Sanna, M. G., 等人, Bitopic Sphingosine 1-Phosphate Receptor3 (S1P3) Antagonist Rescue from Complete Heart Block: Pharmacological andGeneticEvidence for Direct S1P3 Regulation of Mouse Cardiac Conduction. MolPharmacol. 2016; 89(1): 176-86页;
非专利文献11:Means, C. K., 等人, Sphingosine1-phosphate S1P2 and S1P3receptor-mediated Akt activation protects against in vivo myocardialischemia-reperfusion injury. Am J Physiol Heart Circ Physiol. 2007; 292(6):H2944-51页;
非专利文献12:Golfier, S., 等人, Shaping of terminal megakaryocytedifferentiation and proplateletdevelopment by sphingosine-1-phosphatereceptorS1P4. FASEB J. 2010; 24(12): 4701-10页;
非专利文献13:Wang, W., 等人, Type 4 sphingosine 1-phosphate G protein-coupled receptor (S1P4) transduces S1P effects on T cell proliferation andcytokine secretion without signalingmigration. FASEB J. 2005; 19(12): 1731-3页;
非专利文献14:Schulze, T., 等人, Sphingosine-1-phospate receptor 4 (S1P4)deficiency profoundly affects dendritic cell function and TH17-celldifferentiation in a murine model. FASEB J. 2011; 25(11): 4024-36页;
非专利文献15:Jaillard, C., 等人, Edg8/S1P5: an oligodendroglial receptorwith dual function on process retraction and cell survival. J Neurosci. 2005;25(6): 1459-69页;
非专利文献16:Jenne, C. N., 等人, T-bet-dependent S1P5 expression in NKcells promotes egress from lymph nodes and bone marrow. J Exp Med. 2009; 206(11): 2469-81页;
非专利文献17:Lo, C. G., 等人, Cyclical modulation of sphingosine-1-phosphatereceptor 1 surface expression during lymphocyte recirculationandrelationship to lymphoidorgan transit. J Exp Med. 2005; 201(2): 291-301页;
非专利文献18:Chiba K,. A new therapeutic approach for autoimmune diseasesby the sphingosine 1-phosphate receptor modulator, fingolimod (FTY720) NihonRinsho Meneki Gakkai Kaishi. 2009 Apr; 32(2): 92-101页;
非专利文献19:Matloubian, M., 等人, Lymphocyte egress from thymus andperipheral lymphoid organs is dependent on S1P receptor 1. Nature. 2004; 427(6972): 355-60页;
非专利文献20:Schwab, S. R.. and Cyster, J. G., Finding a way out:lymphocyte egress from lymphoid organs. Nat Immunol. 2007; 8(12): 1295-301页;
非专利文献21:Nagahashi, M., 等人, Sphingosine-1-phosphatetransporters astargetsfor cancer therapy. Biomed Res Int. 2014; 2014: 651727页;
非专利文献22:Osborne, N., 等人, The spinster homolog, two of hearts, isrequired for sphingosine 1-phosphate signaling in zebrafish. Curr Biol. 2008Dec 9; 18(23): 1882-8页;
非专利文献23:Kawahara, A., 等人, The sphingolipidtransporter spns2functions in migration of zebrafish myocardial precursors. Science. 2009; 323(5913): 524-7页;
非专利文献24:Fukuhara, S., 等人, The sphingosine-1-phosphatetransporterSpns2 expressed on endothelial cells regulates lymphocyte trafficking inmice. J Clin Invest. 2012; 122(4): 1416-26页;
非专利文献25:Nijnik, A., 等人, The role of sphingosine-1-phosphatetransporterSpns2 in immune systemfunction. J Immunol. 2012; 189(1): 102-11页;
非专利文献26:Hisano, Y., 等人, Mouse SPNS2 functions as a sphingosine-1-phosphate transporterin vascular endothelial cells. PLoS One. 2012; 7(6):e38941页;
非专利文献27:Nagahashi, M., 等人, Spns2, a transporter ofphosphorylatedsphingoid bases, regulates their blood and lymph levels, andthe lymphatic network. FASEB J. 2013; 27(3): 1001-11页;
非专利文献28:Perland, E., 等人, Characteristics of 29 novel atypicalsolute carriers of major facilitator superfamily type: evolutionaryconservation, predicted structure and neuronal co-expression. Open Biol. 2017Sep; 7(9). pii: 170142;
非专利文献29:Donoviel, M. S., 等人, Spinster 2, a sphingosine-1-phosphatetransporter, plays a critical role in inflammatory and autoimmune diseases.FASEB J. 2015; 29(12): 5018-28页;
非专利文献30:van der Weyden, L., 等人, Genome-wide in vivo screenidentifies novel host regulators of metastatic colonization. Nature. 2017;541(7636): 233-236页;
非专利文献31:Matsuura, M., 等人, Effect of FTY720, a novelimmunosuppressant, on adjuvant-inducedarthritis in rats. Inflamm Res. 2000;49(8): 404-10页;
非专利文献32:Wang, F., 等人, Reduction of CD4 positive T cells andimprovement of pathologicalchanges of collagen-induced arthritis by FTY720.Eur J Pharmacol. 2007; 573(1-3): 230-40页;
非专利文献33:Deguchi, Y., 等人, The S1P receptor modulator FTY720prevents the development of experimentalcolitis in mice. Oncol Rep. 2006; 16(4): 699-703页;
非专利文献34:Idzko, M., 等人, Local application of FTY720 to the lungabrogates experimental asthma by altering dendritic cell function. J ClinInvest. 2006; 116(11): 2935-44页;
非专利文献35:Ando, S., 等人, FTY720 exerts a survival advantage throughthe prevention of end-stageglomerular inflammation in lupus-prone BXSB mice.Biochem Biophys Res Commun. 2010; 394(3): 804-10页;
非专利文献36:Okazaki, H., 等人, Effects of FTY720 in MRL-lpr/lpr mice:therapeutic potential in systemic lupus erythematosus. J Rheumatol. 2002; 29(4): 707-16页;
非专利文献37:Sui, M., 等人, The sphingosine-1-phosphate receptor agonistFTY720 prevents the development of anti-glomerular basement membraneglomerulonephritis. Mol Biol Rep. 2012; 39(1): 389-97页;
非专利文献38:Habicht, A., 等人, Novel insights into the mechanism ofaction of FTY720 in a transgenic model of allograft rejection: implicationsfor therapy of chronic rejection. J Immunol. 2006; 176(1): 36-42页;
非专利文献39:D'Ambrosio, D., 等人, Ponesimod, a selective S1P1 receptormodulator: a potential treatment for multiple sclerosis and other immune-mediated diseases. Ther Adv Chronic Dis. 2016; 7(1): 18-33页;
非专利文献40:Brinkmann, V., 等人, The immune modulator FTY720 targetssphingosine 1-phosphate receptors. J Biol Chem. 2002; 277(24): 21453-7页;
非专利文献41:Kappos, L., 等人, A placebo-controlledtrial of oralfingolimod in relapsing multiple sclerosis. N Engl J Med. 2010; 362(5): 387-401页;
非专利文献42:Cohen, J. A., 等人, Oralfingolimod or intramuscularinterferon for relapsingmultiple sclerosis. N Engl J Med. 2010; 362(5): 402-15页;
非专利文献43:Koyrakh, L., 等人, The heart rate decrease caused by acuteFTY720 administration is mediated by the G protein-gated potassium channel I.Am J Transplant. 2005; 5(3): 529-36页;
非专利文献44:Hoch, M., 等人, Effectof ponesimod, a selectiveS1P1 receptormodulator, on the QT interval in healthy individuals. Basic Clin PharmacolToxicol. 2015; 116(5): 429-37页;
非专利文献45:Legangneux, E., 等人, Cardiac Effects of Siponimod (BAF312)Re-initiation After Variable Periods of Drug Discontinuation in HealthySubjects. Clin Ther. 2016; 38(3): 631-45页e1;
非专利文献46:一般社団法人日本皮膚悪性腫瘍学会、悪性黒色腫(メラノーマ)薬物療法の手引(一般社团法人日本皮肤恶性肿瘤学会、恶性黑色素瘤(melanoma)药物疗法的指南) version 1. 2016、Skin Cancer Vol. 32 No.1 2017;
非专利文献47:Smyth, M. J., 等人, NKG2D function protects the host fromtumor initiation. J Exp Med. 2005; 202(5): 583-8页;
非专利文献48:Xia, A. L., 等人, Chimeric-antigenreceptor T (CAR-T) celltherapy for solid tumors: challenges and opportunities. Oncotarget. 2017; 8(52): 90521-90531页;
非专利文献49:Kim, S.,等人, In vivonatural killer cell activities revealedby natural killer cell-deficient mice. Proc Natl Acad Sci U S A. 2000; 97(6):2731-6页;
非专利文献50:Robert, C.,等人, Nivolumab in previously untreated melanomawithout BRAF mutation. N Engl J Med. 2015; 372(4): 320-30页;
非专利文献51:Schachter, J., 等人, Pembrolizumabversus ipilimumab foradvanced melanoma: final overall survival results of a multicentre,randomised, open-label phase 3 study (KEYNOTE-006). Lancet. 2017; 390(10105):1853-1862页;
非专利文献52:Mocsai, A., 等人, What is the future of targeted therapy inrheumatology: biologics or small molecules
发明内容
发明所要解决的课题
本发明的目的在于,提供与脊椎动物的SPNS2特异性结合且抑制S1P的转运的SPNS2中和抗体或其片段、或它们的衍生物。另外,本发明的目的在于,提供抑制SPNS2介导的淋巴细胞的迁移,治疗自身免疫疾病或癌症的抗体。
用于解决课题的手段
即,本发明例如涉及以下内容。
[1] SPNS2中和抗体或其片段、或它们的衍生物,其与脊椎动物的SPNS2特异性结合,且具有抑制鞘氨醇-1-磷酸(S1P)的转运的活性。
[2] [1]所述的SPNS2中和抗体或其片段、或它们的衍生物,其特征在于,在使用了SPNS2表达细胞的Cell-based ELISA中,具有1×10
[3] [1]或[2]所述的SPNS2中和抗体或其片段、或它们的衍生物,其特征在于,以1×10
[4] [1]~[3]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其与SPNS2的细胞外环1(SEQ ID NO: 3)、细胞外环3(SEQ ID NO: 4)或细胞外环5(SEQ ID NO:5)结合,且抑制S1P的转运。
[5] [4]所述的SPNS2中和抗体或其片段、或它们的衍生物,其与SPNS2的细胞外环1(SEQ ID NO: 3)或5(SEQ ID NO: 5)结合,且抑制S1P的转运。
[6] [4]或[5]所述的SPNS2中和抗体或其片段、或它们的衍生物,其特征在于,与包含SPNS2的细胞外环1(SEQ ID NO: 3)的至少部分序列的表位或其附近结合。
[7] [4]或[5]所述的SPNS2中和抗体或其片段、或它们的衍生物,其特征在于,与包含SPNS2的细胞外环3(SEQ ID NO: 4)的至少部分序列的表位或其附近结合。
[8] [4]或[5]所述的SPNS2中和抗体或其片段、或它们的衍生物,其特征在于,与包含SPNS2的细胞外环5(SEQ ID NO: 5)的至少部分序列的表位或其附近结合。
[9] [1]~[8]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2为人SPNS2。
[10] [1]~[9]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其具有通过对脊椎动物进行给予而诱导该脊椎动物的血液中淋巴细胞减少的活性。
[11] [1]~[10]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其是以每周1次以下的频率对脊椎动物进行给予。
[12] [1]~[11]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列或在SEQ ID NO: 98的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 108或SEQ ID NO: 111的氨基酸序列或在SEQ ID NO: 108或SEQ ID NO: 111的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 120或SEQ ID NO: 123的氨基酸序列或在SEQ ID NO: 120或SEQ IDNO: 123的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列或在SEQ ID NO: 101的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 113的氨基酸序列或在SEQ ID NO: 113的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列或在SEQ ID NO: 124的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 103或SEQ ID NO: 105的氨基酸序列或在SEQID NO: 103或SEQ ID NO: 105的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列或在SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列或在SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 100或SEQ ID NO: 106的氨基酸序列或在SEQID NO: 100或SEQ ID NO: 106的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO: 117的任一氨基酸序列或在SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO: 117的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(5) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列或在SEQ ID NO: 99的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 109的氨基酸序列或在SEQ ID NO: 109的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列或在SEQ ID NO: 121的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列或在SEQ ID NO: 102的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 114的氨基酸序列或在SEQ ID NO: 114的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列或在SEQ ID NO: 125的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;或
(7) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列或在SEQ ID NO: 104的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 116的氨基酸序列或在SEQ ID NO: 116的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
[13] [1]~[12]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的与SEQ ID NO: 98具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 108或SEQ ID NO: 111具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 120或SEQ ID NO: 123具有83%以上相似性的氨基酸序列;
(2) 包含作为CDR-H1序列的与SEQ ID NO: 101具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 113具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 124具有88%以上相似性的氨基酸序列;
(3) 包含作为CDR-H1序列的与SEQ ID NO: 103或SEQ ID NO: 105具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 115或SEQ ID NO: 118具有89%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 126或SEQ ID NO: 127具有85%以上相似性的氨基酸序列;
(4) 包含作为CDR-H1序列的与SEQ ID NO: 100或SEQ ID NO: 106具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO:117的任一者具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 122具有83%以上相似性的氨基酸序列;
(5) 包含作为CDR-H1序列的与SEQ ID NO: 99具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 109具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 121具有80%以上相似性的氨基酸序列;
(6) 包含作为CDR-H1序列的与SEQ ID NO: 102具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 114具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 125具有83%以上相似性的氨基酸序列;或
(7) 包含作为CDR-H1序列的与SEQ ID NO: 104具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 116具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 122具有83%以上相似性的氨基酸序列。
[14] [1]~[13]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列或SEQ ID NO: 108的第1位的氨基酸残基由Thr取代为Ser而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列或SEQ ID NO: 123的第4位的氨基酸残基由Ser取代为Thr而得的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 113的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列或SEQ ID NO: 105的第1位的氨基酸残基由Asp取代为Glu而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115的氨基酸序列或SEQ ID NO: 115的第9位的氨基酸残基由Tyr取代为Ser和/或第17位的氨基酸残基由Val取代为Ile的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列或SEQ ID NO: 126的第9位的氨基酸残基由Ser取代为Gly的氨基酸序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列或SEQ ID NO: 100的第1位的氨基酸残基由Arg取代为Ala而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110的氨基酸序列或SEQ ID NO: 110的第8位的氨基酸残基由Thr取代为Ser和/或第17位的氨基酸残基由Asn取代为Lys的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;
(5) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 109的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 114的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列;或
(7) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 116的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列。
[15] [1]~[14]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 120的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 109的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 110的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 111的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;
(5) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 112的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;
(7) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 113的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列;
(8) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 114的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列;
(9) 包含作为CDR-H1序列的SEQ ID NO: 103的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 115的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列;
(10) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQID NO: 116的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;
(11) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQID NO: 115的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列;
(12) 包含作为CDR-H1序列的SEQ ID NO: 106的氨基酸序列;作为CDR-H2序列的SEQID NO: 117的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;或
(13) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQID NO: 118的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 127的氨基酸序列。
[16] [1]~[11]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-L1序列的SEQ ID NO: 129或SEQ ID NO: 132的氨基酸序列或在SEQID NO: 129或SEQ ID NO: 132的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列或在SEQ ID NO: 140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L3序列的SEQ ID NO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一氨基酸序列或在SEQ IDNO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(2) 包含作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列或在SEQ ID NO: 134的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列或在SEQ ID NO: 142的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列或在SEQ ID NO: 153的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(3) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列或在SEQ ID NO: 136的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列或在SEQ ID NO:144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 155或SEQ ID NO: 158的氨基酸序列或在SEQ ID NO: 155或SEQ ID NO: 158的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(4) 包含作为CDR-L1序列的SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一氨基酸序列或在SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 141的氨基酸序列或在SEQ ID NO: 141的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列或在SEQ ID NO: 151的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(5) 包含作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列或在SEQ ID NO: 130的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列或在SEQ ID NO: 140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列或在SEQ ID NO: 150的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(6) 包含作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列或在SEQ ID NO: 135的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列或在SEQ ID NO: 143的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列或在SEQ ID NO: 154的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;或
(7) 包含作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列或在SEQ ID NO: 137的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列或在SEQ ID NO: 145的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列或在SEQ ID NO: 156的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
[17] [1]~[11]或[16]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-L1序列的与SEQ ID NO: 129或SEQ ID NO: 132具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一者具有88%以上相似性的氨基酸序列;
(2) 包含作为CDR-L1序列的与SEQ ID NO: 134具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 142具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 153具有88%以上相似性的氨基酸序列;
(3) 包含作为CDR-L1序列的与SEQ ID NO: 136具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一者具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 155或SEQ ID NO: 158具有88%以上相似性的氨基酸序列;
(4) 包含作为CDR-L1序列的与SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一者具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 141具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 151具有88%以上相似性的氨基酸序列;
(5) 包含作为CDR-L1序列的与SEQ ID NO: 130具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 150具有88%以上相似性的氨基酸序列;
(6) 包含作为CDR-L1序列的与SEQ ID NO: 135具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 143具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 154具有88%以上相似性的氨基酸序列;或
(7) 包含作为CDR-L1序列的与SEQ ID NO: 137具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 145具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 156具有88%以上相似性的氨基酸序列。
[18] [1]~[11]、[16]或[17]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列或SEQ ID NO: 129的第1位的氨基酸残基由Thr取代为Lys和/或第4位的氨基酸残基由Ile取代为Thr而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO:149的氨基酸序列或SEQ ID NO: 149的第5位的氨基酸残基由Ser取代为Asn和/或第7位的氨基酸残基由Ile取代为Met而得的氨基酸序列;
(2) 包含作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列;
(3) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 146的氨基酸序列或SEQ ID NO: 146的第6位的氨基酸残基由Ile取代为Met和/或第7位的氨基酸残基由Ser取代为Ala而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列或SEQ ID NO: 158的第3位的氨基酸残基由Thr取代为Ser和/或第5位的氨基酸残基由Ser取代为Asn而得的序列;
(4) 包含作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列或含有选自SEQ ID NO:133的第2位的氨基酸残基由Ala取代为Pro/第5位的氨基酸残基由Asn取代为Ser/第8位的氨基酸由Ser取代为Asn的任意1或2个以上的取代的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(5) 包含作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列;
(6) 包含作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列;或
(7) 包含作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列。
[19] [1]~[11]、[16]~[18]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列;
(2) 包含作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列;
(3) 包含作为CDR-L1序列的SEQ ID NO: 131的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(4) 包含作为CDR-L1序列的SEQ ID NO: 132的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 152的氨基酸序列;
(5) 包含作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(6) 包含作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列;
(7) 包含作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列;
(8) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 144的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 155的氨基酸序列;
(9) 包含作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列;
(10) 包含作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 157的氨基酸序列;
(11) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQID NO: 146的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列;
(12) 包含作为CDR-L1序列的SEQ ID NO: 138的氨基酸序列;作为CDR-L2序列的SEQID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;或
(13) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQID NO: 147的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列。
[20] [1]~[19]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列或在SEQ ID NO: 98的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 108或SEQ ID NO: 111的氨基酸序列或在SEQ ID NO: 108或SEQ ID NO: 111的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 120或SEQ ID NO: 123的氨基酸序列或在SEQ ID NO: 120或SEQ IDNO: 123的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129或SEQ ID NO: 132的氨基酸序列或在SEQ ID NO: 129或SEQID NO: 132的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列或在SEQ ID NO: 140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO:149、SEQ ID NO: 152或SEQ ID NO: 157的任一氨基酸序列或在SEQ ID NO: 149、SEQ IDNO: 152或SEQ ID NO: 157的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列或在SEQ ID NO: 101的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 113的氨基酸序列或在SEQ ID NO: 113的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列或在SEQ ID NO: 124的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列或在SEQ ID NO: 134的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQID NO: 142的氨基酸序列或在SEQ ID NO: 142的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列或在SEQ ID NO: 153的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 103或SEQ ID NO: 105的氨基酸序列或在SEQID NO: 103或SEQ ID NO: 105的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列或在SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列或在SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列或在SEQ IDNO: 136的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列或在SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 155或SEQID NO: 158的氨基酸序列或在SEQ ID NO: 155或SEQ ID NO: 158的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 100或SEQ ID NO: 106的氨基酸序列或在SEQID NO: 100或SEQ ID NO: 106的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO: 117的任一氨基酸序列或在SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO: 117的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一氨基酸序列或在SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO:138的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列或在SEQ ID NO: 141的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO:151的氨基酸序列或在SEQ ID NO: 151的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(5) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列或在SEQ ID NO: 99的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 109的氨基酸序列或在SEQ ID NO: 109的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列或在SEQ ID NO: 121的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列或在SEQ ID NO: 130的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQID NO: 140的氨基酸序列或在SEQ ID NO: 140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列或在SEQ ID NO: 150的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列或在SEQ ID NO: 102的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 114的氨基酸序列或在SEQ ID NO: 114的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列或在SEQ ID NO: 125的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列或在SEQ ID NO: 135的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQID NO: 143的氨基酸序列或在SEQ ID NO: 143的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列或在SEQ ID NO: 154的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;或
(7) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列或在SEQ ID NO: 104的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 116的氨基酸序列或在SEQ ID NO: 116的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列或在SEQ ID NO: 137的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQID NO: 145的氨基酸序列或在SEQ ID NO: 145的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列或在SEQ ID NO: 156的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
[21] [1]~[20]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的与SEQ ID NO: 98具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 108或SEQ ID NO: 111具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 120或SEQ ID NO: 123具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO: 129或SEQ ID NO: 132具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一者具有88%以上相似性的氨基酸序列;
(2) 包含作为CDR-H1序列的与SEQ ID NO: 101具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 113具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 124具有88%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO:134具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 142具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 153具有88%以上相似性的氨基酸序列;
(3) 包含作为CDR-H1序列的与SEQ ID NO: 103或SEQ ID NO: 105具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 115或SEQ ID NO: 118具有89%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 126或SEQ ID NO: 127具有85%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO: 136具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一者具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 155或SEQ ID NO:158具有88%以上相似性的氨基酸序列;
(4) 包含作为CDR-H1序列的与SEQ ID NO: 100或SEQ ID NO: 106具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO:117的任一者具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 122具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一者具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQID NO: 141具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 151具有88%以上相似性的氨基酸序列;
(5) 包含作为CDR-H1序列的与SEQ ID NO: 99具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 109具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 121具有80%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO:130具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 150具有88%以上相似性的氨基酸序列;
(6) 包含作为CDR-H1序列的与SEQ ID NO: 102具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 114具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 125具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO:135具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 143具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 154具有88%以上相似性的氨基酸序列;或
(7) 包含作为CDR-H1序列的与SEQ ID NO: 104具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 116具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 122具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO:137具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 145具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 156具有88%以上相似性的氨基酸序列。
[22] [1]~[21]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列或SEQ ID NO: 108的第1位的氨基酸残基由Thr取代为Ser而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列或SEQ ID NO: 123的第4位的氨基酸残基由Ser取代为Thr而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列或SEQ ID NO: 129的第1位的氨基酸残基由Thr取代为Lys和/或第4位的氨基酸残基由Ile取代为Thr而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列或SEQ ID NO: 149的第5位的氨基酸残基由Ser取代为Asn和/或第7位的氨基酸残基由Ile取代为Met而得的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 113的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列或SEQ ID NO: 105的第1位的氨基酸残基由Asp取代为Glu而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115的氨基酸序列或SEQ ID NO: 115的第9位的氨基酸残基由Tyr取代为Ser和/或第17位的氨基酸残基由Val取代为Ile的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列或SEQ ID NO: 126的第9位的氨基酸残基由Ser取代为Gly的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 146的氨基酸序列或SEQ IDNO: 146的第6位的氨基酸残基由Ile取代为Met和/或第7位的氨基酸残基由Ser取代为Ala而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列或SEQ ID NO: 158的第3位的氨基酸残基由Thr取代为Ser和/或第5位的氨基酸残基由Ser取代为Asn而得的序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列或SEQ ID NO: 100的第1位的氨基酸残基由Arg取代为Ala而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110的氨基酸序列或SEQ ID NO: 110的第8位的氨基酸残基由Thr取代为Ser和/或第17位的氨基酸残基由Asn取代为Lys的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列或以选自SEQ ID NO: 133的第2位的氨基酸残基由Ala取代为Pro/第5位的氨基酸残基由Asn取代为Ser/第8位的氨基酸由Ser取代为Asn的1处或2处以上氨基酸残基被取代而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO:141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(5) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 109的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 114的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列;或
(7) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 116的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列。
[23] [1]~[22]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 120的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 109的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 110的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 131的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 111的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 132的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 152的氨基酸序列;
(5) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 112的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(7) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 113的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列;
(8) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 114的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列;
(9) 包含作为CDR-H1序列的SEQ ID NO: 103的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 115的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 144的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 155的氨基酸序列;
(10) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQID NO: 116的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列;
(11) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 157的氨基酸序列;
(12) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQID NO: 115的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 146的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列;
(13) 包含作为CDR-H1序列的SEQ ID NO: 106的氨基酸序列;作为CDR-H2序列的SEQID NO: 117的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 138的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;或
(14) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQID NO: 118的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 127的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 147的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列。
[24] [1]~[23]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其进一步包含免疫球蛋白的框架序列。
[25] [24]所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,免疫球蛋白的框架序列为人或包括猴、小鼠、或大鼠的非人动物的免疫球蛋白的各类的框架序列。
[26] [1]~[15]、[20]~[25]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为重链可变区的与选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO:50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQID NO: 62的序列具有90%以上相似性的氨基酸序列。
[27] [1]~[15]、[20]~[26]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为重链可变区的选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ IDNO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQ IDNO: 62的任一氨基酸序列,或在选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO:50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQID NO: 62的任一氨基酸序列中1处或多处的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
[28] [1]~[15]、[20]~[27]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:作为重链可变区,
(1) 包含SEQ ID NO: 42的氨基酸序列或含有选自SEQ ID NO: 42的第1位(Kabat编号:H1)的氨基酸残基由Glu取代为Ala、第6位(Kabat编号:H6)的氨基酸残基由Gly取代为Glu、第23位(Kabat编号:H23)的氨基酸残基由Glu取代为Ala、第43位(Kabat编号:H43)的氨基酸残基由Lys取代为Arg、第50位(Kabat编号:H50)的氨基酸残基由Thr取代为Ser、第75位(Kabat编号:H74)的氨基酸残基由Ala取代为Thr、第76位(Kabat编号:H75)的氨基酸残基由Arg取代为Lys、第78位(Kabat编号:H77)的氨基酸残基由Thr取代为Ile、第80位(Kabat编号:H79)的氨基酸残基由Ser取代为Tyr、第97位(Kabat编号:H93)的氨基酸残基由Ala取代为Thr、和第102位(Kabat编号:H98)的氨基酸残基由Ser取代为Thr的1或2个以上的取代的氨基酸序列;
(2) 包含SEQ ID NO: 46的氨基酸序列或SEQ ID NO: 46的第82位(Kabat编号:H81)的氨基酸残基由Gln取代为Lys而得的氨基酸序列;
(3) 包含SEQ ID NO: 58的氨基酸序列或含有选自SEQ ID NO: 58的第13位(Kabat编号:H13)的氨基酸残基由Gln取代为Arg、第23位(Kabat编号:H23)的氨基酸残基由Ala取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Asp取代为Glu、第49位(Kabat编号:H49)的氨基酸残基由Ala取代为Gly、第58位(Kabat编号:H55)的氨基酸残基由Tyr取代为Ser、第66位(Kabat编号:H63)的氨基酸残基由Val取代为Ile、第79位(Kabat编号:H76)的氨基酸残基由Arg取代为Ser、第86位(Kabat编号:H82A)的氨基酸残基由Phe取代为Tyr或Asn、第100位(Kabat编号:H94)的氨基酸残基由Ser取代为Arg、第109位(Kabat编号:H100C)的氨基酸残基由Ser取代为Gly、和第117位(Kabat编号:H105)的氨基酸残基由His取代为Gln的1或2个以上的取代的氨基酸序列;
(4) 包含SEQ ID NO: 44的氨基酸序列或含有选自SEQ ID NO: 44的第3位(Kabat编号:H3)的氨基酸残基由Gln取代为His、第10位(Kabat编号:H10)的氨基酸残基由Glu取代为Ala或Gly、第16位(Kabat编号:H16)的氨基酸残基由Thr取代为Ala、第19位(Kabat编号:H19)的氨基酸残基由Lys取代为Arg、第24位(Kabat编号:H24)的氨基酸残基由Val取代为Ile、第30位(Kabat编号:H30)的氨基酸残基由Thr取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Arg取代为Ala、第57位(Kabat编号:H56)的氨基酸残基由Thr取代为Ser、第66位(Kabat编号:H65)的氨基酸残基由Lys取代为Asn、第67位(Kabat编号:H66)的氨基酸残基由Lys取代为Arg、第74位(Kabat编号:H73)的氨基酸残基由Ala取代为Val、第77位(Kabat编号:H76)的氨基酸残基由Asn取代为Asp或Ser、第80位(Kabat编号:H79)的氨基酸残基由Tyr取代为Ser、第83位(Kabat编号:H82)的氨基酸残基由Phe取代为Leu、第85位(Kabat编号:H82B)的氨基酸残基由Gly取代为Ser、第89位(Kabat编号:H85)的氨基酸残基由Glu取代为Asp、和第91位(Kabat编号:H87)的氨基酸残基由Thr取代为Ser的1或2个以上的取代的氨基酸序列;或
(5) 包含选自SEQ ID NO: 36、SEQ ID NO: 48、或SEQ ID NO: 52的氨基酸序列。
[29] [1]~[15]、[20]~[28]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为重链可变区的选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ IDNO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQ IDNO: 62的氨基酸序列。
[30] [1]~[11]、[16]~[25]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为轻链可变区的与选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO:82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的序列具有90%以上相似性的氨基酸序列。
[31] [1]~[11]、[16]~[25]或[30]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为轻链可变区的选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ IDNO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQID NO: 94的任一氨基酸序列,或在选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ IDNO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的任一氨基酸序列中1处或多处的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
[32] [1]~[11]、[16]~[25]、[30]和[31]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:作为轻链可变区,
(1) 包含SEQ ID NO: 88的氨基酸序列或含有选自SEQ ID NO: 88的第23位(Kabat编号:L24)的氨基酸残基由Thr取代为Lys、第26位(Kabat编号:L27)的氨基酸残基由Ile取代为Thr、第38位(Kabat编号:L37)的氨基酸残基由Lys取代为Gln、第48位(Kabat编号:L47)的氨基酸残基由Met取代为Leu、第80位(Kabat编号:L77)的氨基酸残基由Asn取代为Ser、第86位(Kabat编号:L83)的氨基酸残基由Glu取代为Gly、第96位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第98位(Kabat编号:L95)的氨基酸残基由Met取代为Ile、第102位(Kabat编号:L99)的氨基酸残基由Gly取代为Ala、和第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr或Gln的1或2个以上的取代的氨基酸序列;
(2) 包含SEQ ID NO: 78的氨基酸序列或SEQ ID NO: 78的第48位(Kabat编号:L47)的氨基酸残基由Leu取代为Met和/或第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr而得的氨基酸序列;
(3) 包含SEQ ID NO: 90的氨基酸序列或含有选自SEQ ID NO: 90的第9位(Kabat编号:L9)的氨基酸残基由Ala取代为Pro、第39位(Kabat编号:L39)的氨基酸残基由Lys取代为Arg、第42位(Kabat编号:L42)的氨基酸残基由Gly取代为Glu、第55位(Kabat编号:L55)的氨基酸残基由Ile取代为Met、第56位(Kabat编号:L56)的氨基酸残基由Ser取代为Ala、第72位(Kabat编号:L72)的氨基酸残基由Thr取代为Ile、第74位(Kabat编号:L74)的氨基酸残基由Arg取代为Ser、第91位(Kabat编号:L91)的氨基酸残基由Thr取代为Ser、第93位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第100位(Kabat编号:L100)的氨基酸残基由Ser取代为Pro、第103位(Kabat编号:L103)的氨基酸残基由Arg取代为Lys、和第106位(Kabat编号:L106)的氨基酸残基由Ile取代为Val的1或2个以上的取代的氨基酸序列;
(4) 包含SEQ ID NO: 76的氨基酸序列或含有选自SEQ ID NO: 76的第13位(Kabat编号:L13)的氨基酸残基由Thr取代为Ala、第22位(Kabat编号:L22)的氨基酸残基由Arg取代为Ser、第25位(Kabat编号:L25)的氨基酸残基由Ala取代为Pro、第28位(Kabat编号:L28)的氨基酸残基由Asn取代为Ser、第31位(Kabat编号:L31)的氨基酸残基由Ser取代为Asn、第69位(Kabat编号:L69)的氨基酸残基由Thr取代为Ser、第79位(Kabat编号:L79)的氨基酸残基由Gln取代为Arg、和第80位(Kabat编号:L80)的氨基酸残基由Pro取代为Ala的1或2个以上的取代或缺损的氨基酸序列;或
(5) 包含选自SEQ ID NO: 68、SEQ ID NO: 80、或SEQ ID NO: 84的氨基酸序列。
[33] [1]~[11]、[16]~[25]、[30]~[32]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为轻链可变区的选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ IDNO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQID NO: 94的氨基酸序列。
[34] [1]~[33]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为重链可变区的与选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO:50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQID NO: 62的序列具有90%以上相似性的氨基酸序列,
包含作为轻链可变区的与选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO:82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的序列具有90%以上相似性的氨基酸序列。
[35] [1]~[34]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为重链可变区的选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ IDNO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQ IDNO: 62的任一氨基酸序列,或在选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO:50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQID NO: 62的任一氨基酸序列中1处或多处的氨基酸残基被取代、缺失或添加而得的氨基酸序列,
包含作为轻链可变区的选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ IDNO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQID NO: 94的任一氨基酸序列,或在选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ IDNO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的任一氨基酸序列中1处或多处的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
[36] [1]~[35]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为重链可变区的SEQ ID NO: 42的氨基酸序列或含有选自SEQ ID NO: 42的第1位(Kabat编号:H1)的氨基酸残基由Glu取代为Ala、第6位(Kabat编号:H6)的氨基酸残基由Gly取代为Glu、第23位(Kabat编号:H23)的氨基酸残基由Glu取代为Ala、第43位(Kabat编号:H43)的氨基酸残基由Lys取代为Arg、第50位(Kabat编号:H50)的氨基酸残基由Thr取代为Ser、第75位(Kabat编号:H74)的氨基酸残基由Ala取代为Thr、第76位(Kabat编号:H75)的氨基酸残基由Arg取代为Lys、第78位(Kabat编号:H77)的氨基酸残基由Thr取代为Ile、第80位(Kabat编号:H79)的氨基酸残基由Ser取代为Tyr、第97位(Kabat编号:H93)的氨基酸残基由Ala取代为Thr、和第102位(Kabat编号:H98)的氨基酸残基由Ser取代为Thr的1或2个以上的取代的氨基酸序列,
包含作为轻链可变区的SEQ ID NO: 88的氨基酸序列或含有选自SEQ ID NO: 88的第23位(Kabat编号:L24)的氨基酸残基由Thr取代为Lys、第26位(Kabat编号:L27)的氨基酸残基由Ile取代为Thr、第38位(Kabat编号:L37)的氨基酸残基由Lys取代为Gln、第48位(Kabat编号:L47)的氨基酸残基由Met取代为Leu、第80位(Kabat编号:L77)的氨基酸残基由Asn取代为Ser、第86位(Kabat编号:L83)的氨基酸残基由Glu取代为Gly、第96位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第98位(Kabat编号:L95)的氨基酸残基由Met取代为Ile、第102位(Kabat编号:L99)的氨基酸残基由Gly取代为Ala、和第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr或Gln的1或2个以上的取代的氨基酸序列;
(2) 包含作为重链可变区的SEQ ID NO: 46的氨基酸序列或SEQ ID NO: 46的第82位(Kabat编号:H81)的氨基酸残基由Gln取代为Lys而得的氨基酸序列,
包含作为轻链可变区的SEQ ID NO: 78的氨基酸序列或SEQ ID NO: 78的第48位(Kabat编号:L47)的氨基酸残基由Leu取代为Met和/或第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr而得的氨基酸序列;
(3) 包含作为重链可变区的SEQ ID NO: 58的氨基酸序列或含有选自SEQ ID NO: 58的第13位(Kabat编号:H13)的氨基酸残基由Gln取代为Arg、第23位(Kabat编号:H23)的氨基酸残基由Ala取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Asp取代为Glu、第49位(Kabat编号:H49)的氨基酸残基由Ala取代为Gly、第58位(Kabat编号:H55)的氨基酸残基由Tyr取代为Ser、第66位(Kabat编号:H63)的氨基酸残基由Val取代为Ile、第79位(Kabat编号:H76)的氨基酸残基由Arg取代为Ser、第86位(Kabat编号:H82A)的氨基酸残基由Phe取代为Tyr或Asn、第100位(Kabat编号:H94)的氨基酸残基由Ser取代为Arg、第109位(Kabat编号:H100C)的氨基酸残基由Ser取代为Gly、和第117位(Kabat编号:H105)的氨基酸残基由His取代为Gln的1或2个以上的取代的氨基酸序列,
包含作为轻链可变区的SEQ ID NO: 90的氨基酸序列或含有选自SEQ ID NO: 90的第9位(Kabat编号:L9)的氨基酸残基由Ala取代为Pro、第39位(Kabat编号:L39)的氨基酸残基由Lys取代为Arg、第42位(Kabat编号:L42)的氨基酸残基由Gly取代为Glu、第55位(Kabat编号:L55)的氨基酸残基由Ile取代为Met、第56位(Kabat编号:L56)的氨基酸残基由Ser取代为Ala、第72位(Kabat编号:L72)的氨基酸残基由Thr取代为Ile、第74位(Kabat编号:L74)的氨基酸残基由Arg取代为Ser、第91位(Kabat编号:L91)的氨基酸残基由Thr取代为Ser、第93位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第100位(Kabat编号:L100)的氨基酸残基由Ser取代为Pro、第103位(Kabat编号:L103)的氨基酸残基由Arg取代为Lys、和第106位(Kabat编号:L106)的氨基酸残基由Ile取代为Val的1或2个以上的取代的氨基酸序列;
(4) 包含作为重链可变区的SEQ ID NO: 44的氨基酸序列或含有选自SEQ ID NO: 44的第3位(Kabat编号:H3)的氨基酸残基由Gln取代为His、第10位(Kabat编号:H10)的氨基酸残基由Glu取代为Ala或Gly、第16位(Kabat编号:H16)的氨基酸残基由Thr取代为Ala、第19位(Kabat编号:H19)的氨基酸残基由Lys取代为Arg、第24位(Kabat编号:H24)的氨基酸残基由Val取代为Ile、第30位(Kabat编号:H30)的氨基酸残基由Thr取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Arg取代为Ala、第57位(Kabat编号:H56)的氨基酸残基由Thr取代为Ser、第66位(Kabat编号:H65)的氨基酸残基由Lys取代为Asn、第67位(Kabat编号:H66)的氨基酸残基由Lys取代为Arg、第74位(Kabat编号:H73)的氨基酸残基由Ala取代为Val、第77位(Kabat编号:H76)的氨基酸残基由Asn取代为Asp或Ser、第80位(Kabat编号:H79)的氨基酸残基由Tyr取代为Ser、第83位(Kabat编号:H82)的氨基酸残基由Phe取代为Leu、第85位(Kabat编号:H82B)的氨基酸残基由Gly取代为Ser、第89位(Kabat编号:H85)的氨基酸残基由Glu取代为Asp、和第91位(Kabat编号:H87)的氨基酸残基由Thr取代为Ser的1或2个以上的取代的氨基酸序列,
包含作为轻链可变区的SEQ ID NO: 76的氨基酸序列或含有选自SEQ ID NO: 76的第13位(Kabat编号:L13)的氨基酸残基由Thr取代为Ala、第22位(Kabat编号:L22)的氨基酸残基由Arg取代为Ser、第25位(Kabat编号:L25)的氨基酸残基由Ala取代为Pro、第28位(Kabat编号:L28)的氨基酸残基由Asn取代为Ser、第31位(Kabat编号:L31)的氨基酸残基由Ser取代为Asn、第69位(Kabat编号:L69)的氨基酸残基由Thr取代为Ser、第79位(Kabat编号:L79)的氨基酸残基由Gln取代为Arg、和第80位(Kabat编号:L80)的氨基酸残基由Pro取代为Ala的1或2个以上的取代或缺损的氨基酸序列;或
(5) 包含作为重链可变区的选自SEQ ID NO: 36、SEQ ID NO: 48、或SEQ ID NO: 52的氨基酸序列,
包含作为轻链可变区的选自SEQ ID NO: 68、SEQ ID NO: 80、和SEQ ID NO: 84的氨基酸序列。
[37] [1]~[36]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
包含作为重链可变区的选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ IDNO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQ IDNO: 62的氨基酸序列,
包含作为轻链可变区的选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ IDNO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQID NO: 94的氨基酸序列。
[38] [1]~[37]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为重链可变区的SEQ ID NO: 34的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 66的氨基酸序列;
(2) 包含作为重链可变区的SEQ ID NO: 36的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 68的氨基酸序列;
(3) 包含作为重链可变区的SEQ ID NO: 38的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 70的氨基酸序列;
(4) 包含作为重链可变区的SEQ ID NO: 40的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 72的氨基酸序列;
(5) 包含作为重链可变区的SEQ ID NO: 42的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 74的氨基酸序列;
(6) 包含作为重链可变区的SEQ ID NO: 44的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 76的氨基酸序列;
(7) 包含作为重链可变区的SEQ ID NO: 46的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 78的氨基酸序列;
(8) 包含作为重链可变区的SEQ ID NO: 48的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 80的氨基酸序列;
(9) 包含作为重链可变区的SEQ ID NO: 50的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 82的氨基酸序列;
(10) 包含作为重链可变区的SEQ ID NO: 52的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 84的氨基酸序列;
(11) 包含作为重链可变区的SEQ ID NO: 54的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 86的氨基酸序列;
(12) 包含作为重链可变区的SEQ ID NO: 56的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 88的氨基酸序列;
(13) 包含作为重链可变区的SEQ ID NO: 58的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 90的氨基酸序列;
(14) 包含作为重链可变区的SEQ ID NO: 60的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 92的氨基酸序列;或
(15) 包含作为重链可变区的SEQ ID NO: 62的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 94的氨基酸序列,
在SPNS2中和抗体或其片段或它们的衍生物的任一者与SPNS2的结合上呈竞争性结合。
[39] [1]~[38]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,上述SPNS2中和抗体或其片段、或它们的衍生物为:
(1) 包含作为重链可变区的SEQ ID NO: 34的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 66的氨基酸序列;
(2) 包含作为重链可变区的SEQ ID NO: 36的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 68的氨基酸序列;
(3) 包含作为重链可变区的SEQ ID NO: 38的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 70的氨基酸序列;
(4) 包含作为重链可变区的SEQ ID NO: 40的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 72的氨基酸序列;
(5) 包含作为重链可变区的SEQ ID NO: 42的氨基酸序列,且作为轻链可变区的SEQID NO: 74的氨基酸序列;
(6) 包含作为重链可变区的SEQ ID NO: 44的氨基酸序列;包含作为轻链可变区的SEQID NO: 76的氨基酸序列;
(7) 包含作为重链可变区的SEQ ID NO: 46的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 78的氨基酸序列;
(8) 包含作为重链可变区的SEQ ID NO: 48的氨基酸序列,且作为轻链可变区的SEQID NO: 80的氨基酸序列;
(9) 包含作为重链可变区的SEQ ID NO: 50的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 82的氨基酸序列;
(10) 包含作为重链可变区的SEQ ID NO: 52的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 84的氨基酸序列;
(11) 包含作为重链可变区的SEQ ID NO: 54的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 86的氨基酸序列;
(12) 包含作为重链可变区的SEQ ID NO: 56的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 88的氨基酸序列;
(13) 包含作为重链可变区的SEQ ID NO: 58的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 90的氨基酸序列;
(14) 包含作为重链可变区的SEQ ID NO: 60的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 92的氨基酸序列;或
(15) 包含作为重链可变区的SEQ ID NO: 62的氨基酸序列,且包含作为轻链可变区的SEQ ID NO: 94的氨基酸序列。
[40] [1]~[39]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其进一步包含作为恒定区的人或包括小鼠、大鼠、或猴的非人动物的免疫球蛋白的各类的恒定区。
[41] 核酸分子,其由编码[1]~[40]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物的多核苷酸序列构成。
[42] 克隆载体或表达载体,其至少包含一个[41]所述的核酸分子。
[43] 重组细胞,其是在宿主细胞中导入有[42]所述的载体而得的。
[44] [1]~[40]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物的制造方法,所述方法包括:培养[43]所述的重组细胞,纯化该SPNS2中和抗体或其片段、或它们的衍生物的步骤。
[45] 药物组合物,其包含[1]~[40]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物、[41]所述的核酸分子、[42]所述的载体、或[43]所述的重组细胞。
[46] [45]所述的药物组合物,其中,上述药物组合物用于脊椎动物的癌症或自身免疫疾病的治疗、抑制或预防。
[47] [45]或[46]所述的药物组合物,其进一步包含药学上可接受的稀释剂或药物载体和/或其他的添加剂。
[48] [45]~[47]中任一项所述的药物组合物,其进一步包含除了[1]~[40]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物、[41]所述的核酸分子、[42]所述的载体、或[43]所述的重组细胞以外的活性成分。
[49] [48]所述的药物组合物,其中,活性成分选自下述的一种以上的成分:氮卓斯汀(Azelastine)、苯咪唑嗪(Oxatomide)、美喹他嗪(Mequitazine)、非索非那定(Fexofenadine)、依匹斯汀(Epinastine)、依巴斯汀(Ebastine)、西替利嗪(Cetirizine)、左西替利嗪(Levocetirizine)、贝他斯汀(Bepotastine)、依美斯汀(Emedastine)、奥洛他定(Olopatadine)、氯雷他定(Loratadine)、左卡巴斯汀(Levocabastine)、奥扎格雷(Ozagrel)、塞曲司特(Seratrodast)、雷马曲班(Ramatroban)、普鲁司特(Pranlukast)、孟鲁司特(Montelukast)、扎鲁司特(Zafirlukast)、甲磺司特(Suplatast)、苯海拉明(Diphenhydramine)、茶苯海明(Dimenhydrinate)、双苯比拉林(Diphenylpyraline)、氯马斯汀(Clemastine)、氯苯那敏(Chlorpheniramine)、曲普利啶(Triprolidine)、异丙嗪(Promethazine)、阿利马嗪(Alimemazine)、羟嗪(Hydroxyzine)、高氯环嗪(Homochlorcyclizine)、赛庚啶(Cyproheptadine)、美沙拉嗪(Mesalazine)、干扰素
[50] [48]所述的药物组合物,其中,活性成分包含选自下述的一种以上的成分:皮质类固醇、止吐药、盐酸昂丹司琼(Ondansetron Hydrochloride)、盐酸格拉司琼(Granisetron Hydrochloride)、甲氧氯普胺(Metoclopramide)、多潘立酮(Domperidone)、氟哌啶醇(Haloperidol)、赛克利嗪(Cyclizine)、劳拉西泮(Lorazepam)、丙氯拉嗪(Prochlorperazine)、地塞米松(Dexamethasone)、左美丙嗪(Levomepromazine)、托烷司琼(Tropisetron)、癌症疫苗、GM-CSF抑制剂、GM-CSF DNA疫苗、基于细胞的疫苗、树突状细胞疫苗、重组病毒疫苗、热休克蛋白(HSP)疫苗、同种肿瘤疫苗、自体肿瘤疫苗、镇痛药、布洛芬(Ibuprofen)、萘普生(Naproxen)、三水杨酸胆碱镁、盐酸羟考酮(OxycodoneHydrochloride)、抗血管生成药、抗血栓药、抗PD-1抗体、纳武单抗(Nivolumab)、派姆单抗(Pembrolizumab)、抗PD-L1抗体、阿特珠单抗(Atezolizumab)、抗CTLA4抗体、伊匹单抗(Ipilimumab)、抗CD20抗体、利妥昔单抗(Rituximab)、抗HER2抗体、曲妥珠单抗(Trastuzumab)、抗CCR4抗体、莫格利珠单抗(Mogamulizumab)、抗VEGF抗体、贝伐珠单抗(Bevacizumab)、抗VEGF受体抗体、可溶性VEGF受体片段、抗TWEAK抗体、抗TWEAK受体抗体、可溶性TWEAK受体片段、AMG 706、AMG 386、抗增殖药、法尼基蛋白转移酶抑制剂、
[51] [1]~[40]中任一项所述的SPNS2中和抗体或其片段、或它们的衍生物,其中,SPNS2中和抗体或其片段、或它们的衍生物为Fab、scFv、双抗体(Diabody)或双特异性抗体、或它们的衍生物。
发明效果
本发明的SPNS2中和抗体或其片段、或它们的衍生物与脊椎动物的SPNS2特异性结合,具有自身免疫疾病的改善效果或抗癌作用等。
附图说明
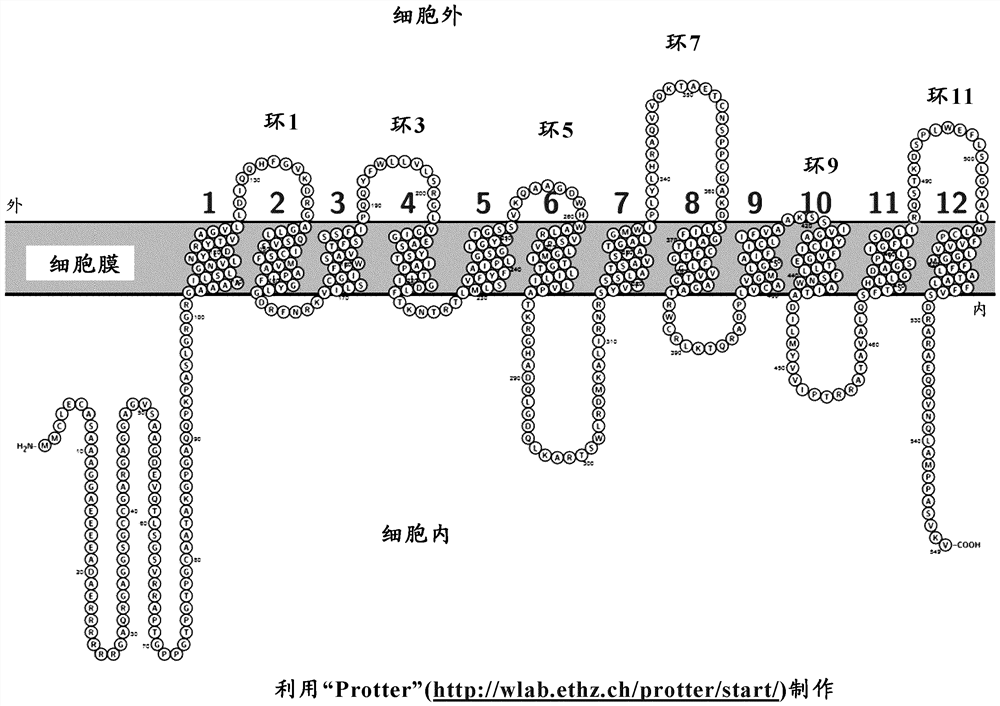
[图1]是人SPNS2的结构的模式图。
[图2-1]是显示在豚鼠、小鼠、大鼠、猴和人中比较SPNS2的氨基酸序列的结果的图。
[图2-2]是显示在豚鼠、小鼠、大鼠、猴和人中比较SPNS2的氨基酸序列的结果的图。
[图3]是显示确认人SPNS2、SphK1双重稳定表达细胞系的S1P产生功能的结果的图表。
[图4]是显示在N末端、C末端添加有FLAG的SPNS2表达细胞的免疫染色结果的图像。
[图5]是显示SPNS2中和抗体所致的抑制由人SPNS2表达细胞产生S1P的活性的FLIPR测定结果的图表。
[图6]是显示SPNS2中和抗体所致的抑制由小鼠SPNS2表达细胞产生S1P的活性的FLIPR测定结果的图表。
[图7]是显示SPNS2中和抗体所致的抑制由人SPNS2表达细胞产生S1P的活性的LC-MS/MS测定结果的图表。
[图8]是显示SPNS2中和抗体所致的抑制由小鼠SPNS2表达细胞产生S1P的活性的LC-MS/MS测定结果的图表。
[图9-1]是显示针对15个克隆的SPNS2中和抗体、分析在重链可变区的氨基酸序列之间的相似性的结果的图。
[图9-2]是显示针对15个克隆的SPNS2中和抗体、分析在轻链可变区的氨基酸序列之间的相似性的结果的图。
[图10-1]是显示SPNS2中和抗体的重链可变区的氨基酸序列的系统树(Phylogenetic Tree)分析的结果的图。
[图10-2]是显示SPNS2中和抗体的轻链可变区的氨基酸序列的系统树(Phylogenetic Tree)分析的结果的图。
[图11-1-1]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的重链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-1-2]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的轻链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-2-1]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的重链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-2-2]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的轻链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-3-1]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的重链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-3-2]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的轻链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-4-1]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的重链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-4-2]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的轻链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-5-1]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的重链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
[图11-5-2]是针对15个克隆的SPNS2中和抗体、比较经分类的组间的抗体中的轻链可变区的氨基酸序列、并显示与Kabat编号(Kabat No.)的对比的图。
具体实施方式
以下,根据具体的实施方式来说明本发明,但本发明不受这些实施方式的任何限定。需要说明的是,本说明书中引用的包含专利公报、专利申请公开公报、和非专利公报的所有文献,出于所有目的,其整体通过援引而并入本说明书中。
[S1P]
S1P是指鞘氨醇-1-磷酸。S1P为与后述的S1P受体结合而具有将细胞骨架变化或抗细胞凋亡或增殖的信号传送到细胞内的激动剂活性的生物体内的配体。已知S1P受体有S1PR1、S1PR2、S1PR3、S1PR4和S1PR5的5种亚型(Subtype)。在本说明书中,主要涉及与S1PR1介导的S1P的淋巴细胞迁移相关的作用,但在进行S1P介导的作用或疾病等的研究的情况下,有时记载包括所有S1P受体的作用。
已知S1P是磷脂之一,且在许多物种中作为生理活性脂质发挥功能。主要由红细胞、血小板、血管内皮、淋巴管内皮细胞产生S1P。ATP依赖性转运蛋白参与了从红细胞、血小板向细胞外转运S1P。另一方面,SLC样转运蛋白的SPNS2参与了从血管内皮、淋巴管内皮细胞向细胞外转运S1P。
S1P是通过从作为细胞膜构成要素的神经酰胺切出作为S1P的前体的鞘氨醇,且将鞘氨醇利用鞘氨醇磷酸化酶(SphK1、SphK2)进行磷酸化而产生的。
[SPNS2]
SPNS2(Spinster homolog 2)是位于细胞膜的膜转运体(转运蛋白)蛋白,是指与SEQID NO: 1具有85%以上相似性的蛋白中具有S1P转运蛋白活性的蛋白。已知在许多脊椎动物的物种中保有SPNS2蛋白,作为其例子,可举出:人(SEQ ID NO: 1)、猴(SEQ ID NO: 31)、小鼠(SEQ ID NO: 19)、大鼠(SEQ ID NO: 33)、和豚鼠(SEQ ID NO: 32)等。另外,人或其他物种中的SPNS2的氨基酸序列可参照NCBI或EMBL等数据库,例如SEQ ID NO: 1所示的人SPNS2蛋白的氨基酸序列可参照NCBI的登录号NP_001118230或EMBL的登录号:Q8IVW8等。在本说明书中,在记载为“SPNS2”的情况下,只要没有特别说明,则是指SPNS2蛋白。SPNS2是具备多个跨膜结构域的蛋白,由类似的转运蛋白的蛋白结构或最近的跨膜区的预测程序中的分析结果,认为是11次或12次跨膜型蛋白。构成SPNS2的结构的各氨基酸区域所具备的功能至今尚未明确,但通过使其在培养细胞中过剩表达,培养上清中的S1P増加,因此将其鉴定为从细胞内向细胞外转运S1P的转运蛋白。
根据氨基酸序列的特征,认为SPNS2是具备Major Facilitator Superfamily结构域的转运蛋白,且是11次或12次跨膜型蛋白,其采取部分的多肽链在细胞外和细胞内以线缝合的方式暴露的形式。将暴露在该细胞外或细胞内的多肽链的部分称为环(loop)。SPNS2的N末端和C末端的多肽链存在于细胞内,这通过本说明书的实施例4来确认。根据该结果,认为SPNS2蛋白的跨膜结构域有偶数个,暗示为12次跨膜型蛋白。若为12次跨膜型蛋白,则其结构,是通过自N末端侧起,为N末端细胞内区-跨膜区1-细胞外环1(loop1)-跨膜区2-细胞内环2(loop2)-跨膜区3-细胞外环3(loop3)-跨膜区4-细胞内环4(loop4)-跨膜区5-细胞外环5(loop5)-跨膜区6-细胞内环6(loop6)-跨膜区7-细胞外环7(loop7)-跨膜区8-细胞内环8(loop8)-跨膜区9-细胞外环9(loop9)-跨膜区10-细胞内环10(loop10)-跨膜区11-细胞外环11(loop11)-跨膜区12-C末端细胞内区的部分(结构域)所构成(图1)。
关于各细胞的跨膜区、细胞内环序列、细胞外环序列是相当于SPNS2的结构的何种氨基酸序列部分,在现有技术中并未特定。因此,在本发明中,除了实施例4中的跨膜区的预测之外,也在实施例10中进行了本发明的抗SPNS2抗体与在细胞外环序列插入有FLAG序列的SPNS2的结合部位的分析和实施例11的将细胞外环序列中的各氨基酸取代成丙氨酸(Ala)或苯丙氨酸(Phe)的抗SPNS2抗体的表位确定的研究,来分析细胞外环序列的结构。其结果,在本发明中阐明了:作为人SPNS2的细胞外环1序列,是相当于包含自SEQ ID NO: 1的至少N末端起第127位的亮氨酸(Leu或L)~第139位的甘氨酸(Gly或G)的氨基酸序列,作为细胞外环3序列,是相当于包含自SEQ ID NO: 1的N末端起第190位的谷氨酰胺(Gln或Q)~第200位的精氨酸(Arg或R)的氨基酸序列,作为细胞外环5序列,是相当于包含自SEQ IDNO: 1的N末端起第252位的缬氨酸(Val或V)~第260位的组氨酸(His或H)的氨基酸序列。另外,在非人物种中,也如图2所示,SPNS2的氨基酸序列在种间的保存性高,特别是在细胞外环1、细胞外环3和细胞外环5中,在人、猴、小鼠、大鼠、豚鼠的SPNS2之间具有同一序列。
已知SPNS2主要在血管内皮、淋巴管内皮表达,与S1P的细胞外转运介导的淋巴细胞的移动相关。S1P转运功能能够以使SPNS2过剩表达的培养细胞的培养上清中S1P量为指标来评价。该SPNS2表达细胞可用于抗体的结合性分析或S1P转运功能的研究。
[SPNS2中和抗体]
抗体是指包含通过二硫键相互结合的至少2个重(H)链和2个轻(L)链的糖蛋白。各自的重链包含重链可变区(简称为VH)和重链恒定区,重链恒定区包含3个结构域CH1、CH2和CH3。各自的轻链包含轻链可变区(简称为VL)和轻链恒定区。轻链恒定区包含1个结构域CL。轻链的恒定区存在有被称为
本发明中的抗体可为抗体的片段和/或衍生物。作为抗体的片段,可举出:F(ab’)2、Fab、Fv等。作为抗体的衍生物,可举出:在恒定区部分人工导入有氨基酸突变而得的抗体、将恒定区的结构域的构成进行修饰而得的抗体、每1分子具备2个以上Fc的形态的抗体、仅由重链或仅由轻链构成的抗体、糖链修饰抗体、双特异性抗体、抗体或抗体的片段化合物或与除了抗体以外的蛋白结合而得的抗体共轭物、抗体酶、纳米抗体、串联scFv、双特异性串联scFv、双抗体(Diabody)、VHH等。需要说明的是,在本发明中,在简称为“抗体”的情况下,只要没有另外说明,则也包含抗体的片段和/或衍生物。
另外,经典而言,单克隆抗体是指从来源于单一抗体产生细胞的克隆得到的抗体分子,但是指包含由特定的氨基酸序列构成的VH与VL的组合的单一种类的抗体分子。单克隆抗体也可得到具有编码其抗体的蛋白的氨基酸的基因序列的核酸分子,也可使用这样的核酸分子来基因工程学地制作抗体。另外,H链、L链、使用它们的可变区或CDR序列等的基因信息来进行用以提高抗体的结合性或特异性的修饰等、或通过自小鼠等动物的抗体修饰成人型抗体来制作适合用于治疗剂的结构的抗体,这对于该领域中的本领域技术人员而言是周知的技术。另外,通过使用导入有人抗体基因的转基因动物作为使抗原致敏的动物,也可获取人的单克隆抗体。除此之外,作为不需要对动物致敏的方法,本领域技术人员也可适当进行如下技术:使用表达人抗体的抗原结合区或其一部分的噬菌体文库(人抗体噬菌体展示),获取与所对应的抗原特异性结合的抗体或由特定的氨基酸序列构成的噬菌体克隆,并根据该信息制作人抗体(例如,参照Taketo Tanaka等、Keio J. Med.、60卷、37-46页的评论等)。另外,在设计给予非人动物的抗体的情况下,与人源化的技术同样地,本领域技术人员可适当使用CDR或可变区的氨基酸序列信息进行设计。
抗体的特异性是指抗体对某抗原引起高的抗原抗体反应。关于抗原抗体反应的测定,只要是本领域技术人员,则可适当选择并进行固相或液相的体系中的结合测定。作为这样的方法,可举出:酶联免疫吸附法(enzyme-linked immunosorbent assay:ELISA)、酶免疫测定法(enzyme immunoassay:EIA)、表面等离子体共振法(surface plasmonresonance:SPR)、荧光共振能量转移法(fluorescence resonance energy transfer:FRET)、发光共振能量转移法(luminescence resonance energy transfer:LRET)等,但不限于这些。另外,在测定这样的抗原抗体结合时,也可将抗体和/或抗原用酶、荧光物质、发光物质、放射性同位素等进行标识,使用适合于该标识的物质的物理和/或化学特性的测定方法,来检测抗原抗体反应。
本发明的SPNS2中和抗体具有SPNS2的S1P转运抑制作用。本发明中的、与SPNS2的特异性结构域强力地结合的SPNS2中和抗体,在体外具有SPNS2的S1P转运抑制作用。具体而言,如实施例12、13所记载,可通过在SPNS2表达细胞中添加SPNS2中和抗体,测定培养上清中的S1P浓度,来测定SPNS2中和抗体的S1P转运抑制活性。
S1P受体激动剂的芬戈莫德引起缓慢性心律失常,但本发明的SPNS2中和抗体,由于推定不具有S1PR1激动剂活性,因此预期不会引起缓慢性心律失常。
根据使用SPNS2缺损小鼠的分析,报道了从静脉内移入的恶性黑色素瘤在肺或肝脏中的定居显著地减少。根据该报道显示出,SPNS2中和抗体不仅是自身免疫疾病还可用作癌症的治疗药,而且还期待增强现有癌症免疫疗法的作用的效果。
综上所述,本发明的SPNS2中和抗体具有成为S1P受体信号所关联的各种疾病的治疗药、抑制药或预防药的可能性,可克服作为S1P受体激动剂的问题的缓慢性心律失常,并延长血液中半衰期。SPNS2是12次跨膜型的蛋白,是自N末端侧起,作为细胞外环1序列(SEQID NO: 3)、细胞外环3序列(SEQ ID NO: 4)、细胞外环5序列(SEQ ID NO: 5)、细胞外环7序列(SEQ ID NO: 6)、细胞外环9序列(SEQ ID NO: 7)和细胞外环11序列(SEQ ID NO: 8)来进行分析。构建了在细胞外环1、3、5、7、9和11插入有FLAG序列的6种突变体基因(SEQ IDNO: 161、163、165、167、169、171)。通过将插入有该突变体基因的表达质粒导入到细胞中,如实施例10所记载,来制作一过性地表达细胞外环1突变体(SEQ ID NO: 160)、细胞外环3突变体(SEQ ID NO: 162)细胞外环5突变体(SEQ ID NO: 164)、细胞外环7突变体(SEQ IDNO: 166)、细胞外环9突变体(SEQ ID NO: 168)和细胞外环11突变体(SEQ ID NO: 170)的细胞,并通过流式细胞术(Flow cytometry)法确认了抗体的反应性。需要说明的是,针对各细胞外环突变体的表达细胞,在使用识别FLAG序列的抗体通过流式细胞术进行分析时,细胞外环3突变体和细胞外环9突变体未被染色。显示出其他的突变体暴露于细胞外。其结果,由于显示出表7所示的结合反应性,因此确定了各自的抗SPNS2抗体的结合部位(实施例10)。
由于SPNS2中和抗体是与细胞外环1和5结合的抗体,因此为了更加限定结合部位,针对在细胞外环1、5和FLAG序列插入突变体中未见到表达的细胞外环3,制作了取代了氨基酸的突变体。使用细胞外环1的丙氨酸突变体(SEQ ID NO: 1的序列的第127位亮氨酸取代体L127A(SEQ ID NO: 172)、第128位天冬氨酸取代体D128A(SEQ ID NO: 173)、第129位异亮氨酸取代体I129A(SEQ ID NO: 174)、第130位谷氨酰胺取代体Q130A(SEQ ID NO: 175)、第131位谷氨酰胺取代体Q131A(SEQ ID NO: 176)、第132位组氨酸取代体H132A(SEQ IDNO: 177)、第133位苯丙氨酸取代体F133A(SEQ ID NO: 178)、第134位甘氨酸取代体G134A(SEQ ID NO: 179)、第135位缬氨酸取代体V135A(SEQ ID NO: 180)、第136位赖氨酸取代体K136A(SEQ ID NO: 181)、第137位天冬氨酸取代体D137A(SEQ ID NO: 182)、第138位精氨酸取代体R138A(SEQ ID NO: 183)、第139位甘氨酸取代体G139A(SEQ ID NO: 184))、细胞外环3的丙氨酸突变体(SEQ ID NO: 1的序列的第189位脯氨酸取代体P189A(SEQ ID NO:185)、第190位谷氨酰胺取代体Q190A(SEQ ID NO: 186)、第191位谷氨酰胺取代体Q191A(SEQ ID NO: 187)、第192位酪氨酸取代体Y192A(SEQ ID NO: 188)、第193位苯丙氨酸取代体F193A(SEQ ID NO: 189)、第194位色氨酸取代体W194A(SEQ ID NO: 190)、第195位亮氨酸取代体L195A(SEQ ID NO: 191)、第196位亮氨酸取代体L196A(SEQ ID NO: 192)、第197位缬氨酸取代体V197A(SEQ ID NO: 193)、第198位亮氨酸取代体L198A(SEQ ID NO: 194)、第199位丝氨酸取代体S199A(SEQ ID NO: 195)、第200位精氨酸取代体R200A(SEQ ID NO:196)、第201位甘氨酸取代体G201A(SEQ ID NO: 197)、第202位亮氨酸取代体L202A(SEQ IDNO: 198))、细胞外环5的丙氨酸或苯丙氨酸突变体(SEQ ID NO: 1的序列的第252位缬氨酸取代体V252A(SEQ ID NO: 199)、第253位赖氨酸取代体K253A(SEQ ID NO: 200)、第254位谷氨酰胺取代体Q254A(SEQ ID NO: 201)、第255位丙氨酸取代体A255F(SEQ ID NO: 206)、第256位丙氨酸取代体A256F(SEQ ID NO: 207)、第257位甘氨酸取代体G257A(SEQ ID NO:202)、第258位天冬氨酸取代体D258A(SEQ ID NO: 203)、第259位色氨酸取代体W259A(SEQID NO: 204)、第260位组氨酸取代体H260A(SEQ ID NO: 205)),如实施例11所记载地制作表达细胞,确定了对SPNS2中和抗体的抗原抗体反应重要的氨基酸。根据该结果,在细胞外环1中,在SEQ ID NO: 1的序列的第127位的亮氨酸~第139位的甘氨酸的各自的取代体中,观察到结合能力的降低。在细胞外环3中,在SEQ ID NO: 1的序列的第190位的谷氨酰胺~第200位的精氨酸的各自的取代体中,观察到结合能力的降低。在细胞外环5中,在SEQ IDNO: 1的序列的第252位的缬氨酸~第260位的组氨酸的各自的取代体中,观察到结合能力的降低。
在实施例5和6中所制作的抗体中,与SPNS2显示结合性、且具有细胞的S1P产生抑制活性的抗体15个克隆,显示出与细胞外环1、细胞外环3和细胞外环5的任一者结合。因此,细胞外环1、细胞外环3和细胞外环5中的至少一部分序列显示出暴露至细胞外,特别是,显示出:细胞外环1是至少包含从SEQ ID NO: 3的末端起第1位的Leu(SEQ ID NO: 1的第127位的Leu)~第13位的Gly(SEQ ID NO: 1的第139位的Gly)的序列,细胞外环3是至少包含从SEQ ID NO: 4的N末端起第2位的Gln(SEQ ID NO: 1的第190位的Gln)~第12位的Arg(SEQID NO: 1的第200位的Arg)的序列,细胞外环5是至少包含从SEQ ID NO: 5的N末端起第1位的Val(SEQ ID NO: 1的第252位的Val)~第9位的His(SEQ ID NO: 1的第260位的His)的序列。另外,认为抑制SPNS2的S1P转运的抗体通过与细胞外环1、细胞外环3或细胞外环5结合,而抑制S1P转运所需的结构变化。
因此,本发明的SPNS2中和抗体是以SPNS2的细胞外环中的氨基酸序列为表位的抗体。特别是,本发明的SPNS2中和抗体优选与SPNS2的细胞外环1、细胞外环3或细胞外环5结合的抗体。另外,本发明的SPNS2中和抗体优选为与从SEQ ID NO: 3的N末端起第1位~第13位的氨基酸序列或其部分序列、从SEQ ID NO: 4的N末端起第2位~第12位的氨基酸序列或其部分序列、或者从SEQ ID NO: 5的N末端起第1位~第9位的氨基酸序列或其部分序列结合的抗体。
本发明的SPNS2中和抗体只要是与脊椎动物的SPNS2特异性结合、且具有抑制SPNS2的S1P转运功能的抗体即可,对序列没有特别限定。
作为本发明的SPNS2中和抗体的方案,优选具有特定的氨基酸序列作为各CDR序列。具体而言,如下所述。需要说明的是,在本发明中,氨基酸序列的“同一性”(identity)是指一致的氨基酸残基的比例,相似性(similarity)是指一致或类似的氨基酸残基的比例。相似性和同一性例如可通过BLAST法(NCBI的PDLAST的默认条件)进行确定。另外,例如在表述为“80%以上相似性”时,明显可知包括“80%以上同一性”的情况(而且,也包括“100%相似性”和“100%同一性”)。
在此,“类似的氨基酸残基”是指具有具备同样的化学特质(例如,电荷或疏水性)的侧链的氨基酸残基。作为类似的氨基酸残基,例如可举出以下的组合。
1) 具有脂肪族侧链的氨基酸残基:甘氨酸(Gly或G)、丙氨酸(Ala或A)、缬氨酸(Val或V)、亮氨酸(Leu或L)、和异亮氨酸(Ile或I)残基。
2) 具有脂肪族羟基侧链的氨基酸残基:丝氨酸(Ser或S)和苏氨酸(Thr或T)残基。
3) 具有含酰胺侧链的氨基酸残基:天冬酰胺(Asn或N)和谷氨酰胺(Gln或Q)残基。
4) 具有芳香族侧链的氨基酸残基:苯丙氨酸(Phe或F)、酪氨酸(Tyr或Y)、和色氨酸(Trp或W)残基。
5) 具有碱性侧链的氨基酸残基:赖氨酸(Lys或K)、精氨酸(Arg或R)、和组氨酸(His或H)残基。
6) 具有酸性侧链的氨基酸残基:天冬氨酸(Asp或D)和谷氨酸(Glu或E)残基。
7) 具有含硫侧链的氨基酸残基:半胱氨酸(Cys或C)和蛋氨酸(Met或M)残基。
作为本发明中的SPNS2中和抗体的一个方案,是包含具有以下的(1)~(3)的任一特征的重链可变区的抗体。
(1) 包含作为CDR-H1序列的与选自SEQ ID NO: 98、SEQ ID NO: 99、SEQ ID NO:100、SEQ ID NO: 101、SEQ ID NO: 102、SEQ ID NO: 103、SEQ ID NO: 104、SEQ ID NO:105或SEQ ID NO: 106的氨基酸序列具有80%以上相似性的氨基酸序列。
(2) 包含作为CDR-H2序列的与选自SEQ ID NO: 108、SEQ ID NO: 109、SEQ IDNO: 110、SEQ ID NO: 111、SEQ ID NO: 112、SEQ ID NO: 113、SEQ ID NO: 114、SEQ IDNO: 115、SEQ ID NO: 116、SEQ ID NO: 117或SEQ ID NO: 118的氨基酸序列具有88%以上相似性的氨基酸序列。
(3) 包含作为CDR-H3序列的与选自SEQ ID NO: 120、SEQ ID NO: 121、SEQ IDNO: 122、SEQ ID NO: 123、SEQ ID NO: 124、SEQ ID NO: 125、SEQ ID NO: 126或SEQ IDNO: 127的氨基酸序列具有80%以上相似性的氨基酸序列。
上述方案中的SPNS2中和抗体优选重链可变区的CDR1、2和3具有以下的(1)~(7)的任一特征。
(1) 包含作为CDR-H1序列的与SEQ ID NO: 98具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 108或SEQ ID NO: 111具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 120或SEQ ID NO: 123具有83%以上相似性的氨基酸序列。
(2) 包含作为CDR-H1序列的与SEQ ID NO: 101具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 113具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 124具有88%以上相似性的氨基酸序列。
(3) 包含作为CDR-H1序列的与SEQ ID NO: 103或SEQ ID NO: 105具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 115或SEQ ID NO: 118具有89%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 126或SEQ ID NO: 127具有85%以上相似性的氨基酸序列。
(4) 包含作为CDR-H1序列的与SEQ ID NO: 100或SEQ ID NO: 106具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 110、SEQ ID NO: 112或SEQ IDNO: 117的任一者具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO:122具有83%以上相似性的氨基酸序列。
(5) 包含作为CDR-H1序列的与SEQ ID NO: 104具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 116具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 122具有83%以上相似性的氨基酸序列。
(6) 包含作为CDR-H1序列的与SEQ ID NO: 99具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 109具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 121具有80%以上相似性的氨基酸序列。
(7) 包含作为CDR-H1序列的与SEQ ID NO: 102具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 114具有88%以上相似性的氨基酸序列;和作为CDR-H3序列的与SEQ ID NO: 125具有83%以上相似性的氨基酸序列。
作为本发明中的SPNS2中和抗体的另外一个方案,是包含具有以下的(1)~(7)的任一特征的重链可变区的抗体。
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列或在SEQ ID NO: 98的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 108或SEQ ID NO: 111的氨基酸序列或在SEQ ID NO: 108或SEQ ID NO:111的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 120或SEQ ID NO: 123的氨基酸序列或在SEQ ID NO: 120或SEQ IDNO: 123的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列或在SEQ ID NO: 101的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 113的氨基酸序列或在SEQ ID NO: 113的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列或在SEQ ID NO: 124的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(3) 包含作为CDR-H1序列的SEQ ID NO: 103或SEQ ID NO: 105的氨基酸序列或在SEQ ID NO: 103或SEQ ID NO: 105的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列或在SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列或在SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(4) 包含作为CDR-H1序列的SEQ ID NO: 100或SEQ ID NO: 106的氨基酸序列或在SEQ ID NO: 100或SEQ ID NO: 106的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110、SEQ ID NO: 112或SEQ IDNO: 117的任一氨基酸序列或在SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO: 117的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(5) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列或在SEQ ID NO: 99的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 109的氨基酸序列或在SEQ ID NO: 109的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列或在SEQ ID NO: 121的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(6) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列或在SEQ ID NO: 102的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 114的氨基酸序列或在SEQ ID NO: 114的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列或在SEQ ID NO: 125的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(7) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列或在SEQ ID NO: 104的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 116的氨基酸序列或在SEQ ID NO: 116的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
另外,上述方案中的SPNS2中和抗体更优选重链可变区的CDR1、2和3具有以下的(1)~(7)的任一特征:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列或SEQ ID NO: 108的第1位的氨基酸残基由Thr取代为Ser而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列或SEQ ID NO: 123的第4位的氨基酸残基由Ser取代为Thr而得的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 113的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列或SEQ ID NO: 105的第1位的氨基酸残基由Asp取代为Glu而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115的氨基酸序列或SEQ ID NO: 115的第9位的氨基酸残基由Tyr取代为Ser和/或第17位的氨基酸残基由Val取代为Ile的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列或SEQ ID NO: 126的第9位的氨基酸残基由Ser取代为Gly的氨基酸序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列或SEQ ID NO: 100的第1位的氨基酸残基由Arg取代为Ala而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110的氨基酸序列或SEQ ID NO: 110的第8位的氨基酸残基由Tyr取代为Ser和/或第17位的氨基酸残基由Asn取代为Lys的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;
(5) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 116的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 109的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列;或
(7) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 114的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列。
上述方案中的SPNS2中和抗体进一步优选重链可变区的CDR1、2和3具有以下的(1)~(13)的任一特征。
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQID NO: 108的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 120的氨基酸序列。
(2) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQID NO: 109的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列。
(3) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列。
(4) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQID NO: 111的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列。
(5) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQID NO: 108的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列。
(6) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 112的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列。
(7) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 113的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列。
(8) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 114的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列。
(9) 包含作为CDR-H1序列的SEQ ID NO: 103的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列。
(10) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 116的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列。
(11) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列。
(12) 包含作为CDR-H1序列的SEQ ID NO: 106的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 117的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列。
(13) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 118的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 127的氨基酸序列。
作为本发明中的SPNS2中和抗体的一个方案,是包含具有以下的(1)~(3)的任一特征的轻链可变区的抗体。
(1) 包含作为CDR-L1序列的与选自SEQ ID NO: 129、SEQ ID NO: 130、SEQ IDNO: 131、SEQ ID NO: 132、SEQ ID NO: 133、SEQ ID NO: 134、SEQ ID NO: 135、SEQ IDNO: 136、SEQ ID NO: 137或SEQ ID NO: 138的氨基酸序列具有81%以上相似性的氨基酸序列。
(2) 包含作为CDR-L2序列的与选自SEQ ID NO: 140、SEQ ID NO: 141、SEQ IDNO: 142、SEQ ID NO: 143、SEQ ID NO: 144、SEQ ID NO: 145、SEQ ID NO: 146、或SEQ IDNO: 147的氨基酸序列具有85%以上相似性的氨基酸序列。
(3) 包含作为CDR-L3序列的与选自SEQ ID NO: 149、SEQ ID NO: 150、SEQ IDNO: 151、SEQ ID NO: 152、SEQ ID NO: 153、SEQ ID NO: 154、SEQ ID NO: 155、SEQ IDNO: 156、SEQ ID NO: 157或SEQ ID NO: 158的氨基酸序列具有88%以上相似性的氨基酸序列。
上述方案中的抗SPNS2抗体优选轻链可变区的CDR1、2和3具有以下的(1)~(7)的任一特征。
(1) 包含作为CDR-L1序列的与SEQ ID NO: 129或SEQ ID NO: 132具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一者具有88%以上相似性的氨基酸序列。
(2) 包含作为CDR-L1序列的与SEQ ID NO: 134具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 142具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 153具有88%以上相似性的氨基酸序列。
(3) 包含作为CDR-L1序列的与SEQ ID NO: 136具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一者具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 155或SEQ ID NO:158具有88%以上相似性的氨基酸序列。
(4) 包含作为CDR-L1序列的与SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO:138的任一者具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 141具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 151具有88%以上相似性的氨基酸序列。
(5) 包含作为CDR-L1序列的与SEQ ID NO: 137具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 145具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 156具有88%以上相似性的氨基酸序列。
(6) 包含作为CDR-L1序列的与SEQ ID NO: 130具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 150具有88%以上相似性的氨基酸序列。
(7) 包含作为CDR-L1序列的与SEQ ID NO: 135具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 143具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 154具有88%以上相似性的氨基酸序列。
作为本发明中的SPNS2中和抗体的另外一个方案,是包含具有以下的(1)~(7)的任一特征的轻链可变区的抗体。
(1) 包含作为CDR-L1序列的SEQ ID NO: 129或SEQ ID NO: 132的氨基酸序列或在SEQ ID NO: 129或SEQ ID NO: 132的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列或在SEQ ID NO:140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L3序列的SEQ ID NO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一氨基酸序列或在SEQID NO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(2) 包含作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列或在SEQ ID NO: 134的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列或在SEQ ID NO: 142的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列或在SEQ ID NO: 153的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(3) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列或在SEQ ID NO: 136的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列或在SEQ IDNO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 155或SEQ ID NO:158的氨基酸序列或在SEQ ID NO: 155或SEQ ID NO: 158的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(4) 包含作为CDR-L1序列的SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一氨基酸序列或在SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQID NO: 141的氨基酸序列或在SEQ ID NO: 141的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列或在SEQ ID NO: 151的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(5) 包含作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列或在SEQ ID NO: 130的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列或在SEQ ID NO: 140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列或在SEQ ID NO: 150的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(6) 包含作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列或在SEQ ID NO: 135的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列或在SEQ ID NO: 143的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列或在SEQ ID NO: 154的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(7) 包含作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列或在SEQ ID NO: 137的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列或在SEQ ID NO: 145的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列或在SEQ ID NO: 156的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
上述方案中的SPNS2中和抗体更优选轻链可变区的CDR1、2和3具有以下的(1)~(7)的任一特征:
(1) 包含作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列或SEQ ID NO: 129的第1位的氨基酸残基由Thr取代为Lys和/或第4位的氨基酸残基由Ile取代为Thr而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO:149的氨基酸序列或SEQ ID NO: 149的第5位的氨基酸残基由Ser取代为Asn和/或第7位的氨基酸残基由Ile取代为Met而得的氨基酸序列;
(2) 包含作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列;
(3) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 146的氨基酸序列或SEQ ID NO: 146的第6位的氨基酸残基由Ile取代为Met和/或第7位的氨基酸残基由Ser取代为Ala而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列或SEQ ID NO: 158的第3位的氨基酸残基由Thr取代为Ser和/或第5位的氨基酸残基由Ser取代为Asn而得的序列;
(4) 包含作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列或含有选自SEQ ID NO:133的第2位的氨基酸残基由Ala取代为Pro/第5位的氨基酸残基由Asn取代为Ser/第8位的氨基酸由Ser取代为Asn的任意1或2个以上的取代的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(5) 包含作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列;
(6) 包含作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列;或
(7) 包含作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列。
另外,上述方案中的抗SPNS2抗体进一步优选轻链可变区的CDR1、2和3具有以下的(1)~(13)的任一特征。
上述抗SPNS2抗体或其片段、或它们的衍生物为:
(1) 包含作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ IDNO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列。
(2) 包含作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列。
(3) 包含作为CDR-L1序列的SEQ ID NO: 131的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列。
(4) 包含作为CDR-L1序列的SEQ ID NO: 132的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 152的氨基酸序列。
(5) 包含作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列。
(6) 包含作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列。
(7) 包含作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列。
(8) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 144的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 155的氨基酸序列。
(9) 包含作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列。
(10) 包含作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 157的氨基酸序列。
(11) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 146的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列。
(12) 包含作为CDR-L1序列的SEQ ID NO: 138的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列。
(13) 包含作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 147的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列。
作为本发明中的SPNS2中和抗体的一个方案,是包含具有以下的(1)~(3)的任一特征的重链可变区和具有(4)~(6)的任一特征的轻链可变区的抗体。
(1) 重链可变区为:包含作为CDR-H1序列的与选自SEQ ID NO: 98、SEQ ID NO:99、SEQ ID NO: 100、SEQ ID NO: 101、SEQ ID NO: 102、SEQ ID NO: 103、SEQ ID NO:104、SEQ ID NO: 105或SEQ ID NO: 106的氨基酸序列具有80%以上相似性的氨基酸序列。
(2) 重链可变区为:包含作为CDR-H2序列的与选自SEQ ID NO: 108、SEQ ID NO:109、SEQ ID NO: 110、SEQ ID NO: 111、SEQ ID NO: 112、SEQ ID NO: 113、SEQ ID NO:114、SEQ ID NO: 115、SEQ ID NO: 116、SEQ ID NO: 117或SEQ ID NO: 118的氨基酸具有88%以上相似性的氨基酸序列。
(3) 重链可变区为:包含作为CDR-H3序列的与选自SEQ ID NO: 120、SEQ ID NO:121、SEQ ID NO: 122、SEQ ID NO: 123、SEQ ID NO: 124、SEQ ID NO: 125、SEQ ID NO:126或SEQ ID NO: 127的氨基酸序列具有80%以上相似性的氨基酸序列。
(4) 轻链可变区为:包含作为CDR-L1序列的与选自SEQ ID NO: 129、SEQ ID NO:130、SEQ ID NO: 131、SEQ ID NO: 132、SEQ ID NO: 133、SEQ ID NO: 134、SEQ ID NO:135、SEQ ID NO: 136、SEQ ID NO: 137或SEQ ID NO: 138的氨基酸序列具有81%以上相似性的氨基酸序列。
(5) 轻链可变区为:包含作为CDR-L2序列的与选自SEQ ID NO: 140、SEQ ID NO:141、SEQ ID NO: 142、SEQ ID NO: 143、SEQ ID NO: 144、SEQ ID NO: 145、SEQ ID NO:146或SEQ ID NO: 147的氨基酸序列具有85%以上相似性的氨基酸序列。
(6) 轻链可变区为:包含作为CDR-L3序列的与选自SEQ ID NO: 149、SEQ ID NO:150、SEQ ID NO: 151、SEQ ID NO: 152、SEQ ID NO: 153、SEQ ID NO: 154、SEQ ID NO:155、SEQ ID NO: 156、SEQ ID NO: 157或SEQ ID NO: 158的氨基酸序列具有88%以上相似性的氨基酸序列。
上述方案中的抗SPNS2抗体优选重链可变区的CDR1、2和3、以及轻链可变区的CDR1、2和3具有以下的(1)~(7)的任一特征。
(1) 包含作为CDR-H1序列的与SEQ ID NO: 98具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 108或SEQ ID NO: 111具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 120或SEQ ID NO: 123具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO: 129或SEQ ID NO: 132具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 149、SEQ ID NO: 152或SEQ ID NO: 157的任一者具有88%以上相似性的氨基酸序列。
(2) 包含作为CDR-H1序列的与SEQ ID NO: 101具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 113具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 124具有88%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ IDNO: 134具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 142具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 153具有88%以上相似性的氨基酸序列。
(3) 包含作为CDR-H1序列的与SEQ ID NO: 103或SEQ ID NO: 105具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 115或SEQ ID NO: 118具有89%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 126或SEQ ID NO: 127具有85%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO: 136具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一者具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 155或SEQ IDNO: 158具有88%以上相似性的氨基酸序列。
(4) 包含作为CDR-H1序列的与SEQ ID NO: 100或SEQ ID NO: 106具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 110、SEQ ID NO: 112或SEQ IDNO: 117的任一者具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO:122具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ ID NO: 131、SEQ ID NO:133或SEQ ID NO: 138的任一者具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 141具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO:151具有88%以上相似性的氨基酸序列。
(5) 包含作为CDR-H1序列的与SEQ ID NO: 104具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 116具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 122具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ IDNO: 137具有81%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 145具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 156具有88%以上相似性的氨基酸序列。
(6) 包含作为CDR-H1序列的与SEQ ID NO: 99具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 109具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 121具有80%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ IDNO: 130具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 140具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 150具有88%以上相似性的氨基酸序列。
(7) 包含作为CDR-H1序列的与SEQ ID NO: 102具有80%以上相似性的氨基酸序列;作为CDR-H2序列的与SEQ ID NO: 114具有88%以上相似性的氨基酸序列;作为CDR-H3序列的与SEQ ID NO: 125具有83%以上相似性的氨基酸序列;作为CDR-L1序列的与SEQ IDNO: 135具有84%以上相似性的氨基酸序列;作为CDR-L2序列的与SEQ ID NO: 143具有85%以上相似性的氨基酸序列;和作为CDR-L3序列的与SEQ ID NO: 154具有88%以上相似性的氨基酸序列。
作为本发明中的SPNS2中和抗体的另外一个方案,是重链可变区的CDR1、2和3、以及轻链可变区的CDR1、2和3具有以下的(1)~(7)的任一特征的抗体。
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列或在SEQ ID NO: 98的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 108或SEQ ID NO: 111的氨基酸序列或在SEQ ID NO: 108或SEQ ID NO:111的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 120或SEQ ID NO: 123的氨基酸序列或在SEQ ID NO: 120或SEQ IDNO: 123的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129或SEQ ID NO: 132的氨基酸序列或在SEQ ID NO: 129或SEQID NO: 132的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列或在SEQ ID NO: 140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L3序列的SEQ ID NO:149、SEQ ID NO: 152或SEQ ID NO: 157的任一氨基酸序列或在SEQ ID NO: 149、SEQ IDNO: 152或SEQ ID NO: 157的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列或在SEQ ID NO: 101的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 113的氨基酸序列或在SEQ ID NO: 113的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列或在SEQ ID NO: 124的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列或在SEQ ID NO: 134的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列或在SEQ ID NO: 142的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列或在SEQ ID NO: 153的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(3) 包含作为CDR-H1序列的SEQ ID NO: 103或SEQ ID NO: 105的氨基酸序列或在SEQ ID NO: 103或SEQ ID NO: 105的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列或在SEQ ID NO: 115或SEQ ID NO: 118的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列或在SEQ ID NO: 126或SEQ ID NO: 127的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列或在SEQ ID NO: 136的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列或在SEQ ID NO: 144、SEQ ID NO: 146或SEQ ID NO: 147的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO:155或SEQ ID NO: 158的氨基酸序列或在SEQ ID NO: 155或SEQ ID NO: 158的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(4) 包含作为CDR-H1序列的SEQ ID NO: 100或SEQ ID NO: 106的氨基酸序列或在SEQ ID NO: 100或SEQ ID NO: 106的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 110、SEQ ID NO: 112或SEQ IDNO: 117的任一氨基酸序列或在SEQ ID NO: 110、SEQ ID NO: 112或SEQ ID NO: 117的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 131、SEQID NO: 133或SEQ ID NO: 138的任一氨基酸序列或在SEQ ID NO: 131、SEQ ID NO: 133或SEQ ID NO: 138的任一氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列或在SEQ ID NO: 141的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQID NO: 151的氨基酸序列或在SEQ ID NO: 151的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(5) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列或在SEQ ID NO: 99的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 109的氨基酸序列或在SEQ ID NO: 109的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列或在SEQ ID NO: 121的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列或在SEQ ID NO: 130的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列或在SEQ ID NO: 140的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列或在SEQ ID NO: 150的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(6) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列或在SEQ ID NO: 102的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 114的氨基酸序列或在SEQ ID NO: 114的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列或在SEQ ID NO: 125的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列或在SEQ ID NO: 135的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列或在SEQ ID NO: 143的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列或在SEQ ID NO: 154的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
(7) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列或在SEQ ID NO: 104的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 116的氨基酸序列或在SEQ ID NO: 116的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列或在SEQ ID NO: 122的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列或在SEQ ID NO: 137的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列或在SEQ ID NO: 145的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列或在SEQ ID NO: 156的氨基酸序列中1或2个的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
上述方案中的SPNS2中和抗体更优选重链可变区的CDR1、2和3、以及轻链可变区的CDR1、2和3具有以下的(1)~(7)的任一特征。
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQID NO: 108的氨基酸序列或SEQ ID NO: 108的第1位的氨基酸残基由Thr取代为Ser而得的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列或SEQ ID NO: 123的第4位的氨基酸残基由Ser取代为Thr而得的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列或SEQ ID NO: 129的第1位的氨基酸残基由Thr取代为Lys和/或第4位的氨基酸残基由Ile取代为Thr而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列或SEQ ID NO: 149的第5位的氨基酸残基由Ser取代为Asn和/或第7位的氨基酸残基由Ile取代为Met而得的氨基酸序列。
(2) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 113的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列。
(3) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列或SEQ ID NO: 105的第1位的氨基酸残基由Asp取代为Glu而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO:115的氨基酸序列或SEQ ID NO: 115的第9位的氨基酸残基由Tyr取代为Ser和/或第17位的氨基酸残基由Val取代为Ile的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列或SEQ ID NO: 126的第9位的氨基酸残基由Ser取代为Gly的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 146的氨基酸序列或SEQ ID NO: 146的第6位的氨基酸残基由Ile取代为Met和/或第7位的氨基酸残基由Ser取代为Ala而得的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列或SEQ IDNO: 158的第3位的氨基酸残基由Thr取代为Ser和/或第5位的氨基酸残基由Ser取代为Asn而得的序列。
(4) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列或SEQ ID NO: 100的第1位的氨基酸残基由Arg取代为Ala而得的氨基酸序列;作为CDR-H2序列的SEQ ID NO:110的氨基酸序列或SEQ ID NO: 110的第8位的氨基酸残基由Thr取代为Ser和/或第17位的氨基酸残基由Asn取代为Lys的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列或选自在SEQ ID NO: 133的第2位的氨基酸残基由Ala取代为Pro/第5位的氨基酸残基由Asn取代为Ser/第8位的氨基酸残基由Ser取代为Asn的任意1处或2处以上氨基酸残基被取代而得的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列。
(5) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 116的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列。
(6) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQID NO: 109的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列。
(7) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ ID NO: 114的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列。
另外,上述方案中的抗SPNS2中和抗体进一步优选重链可变区的CDR1、2和3、以及轻链可变区的CDR1、2和3具有以下的(1)~(14)的任一特征:
(1) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 120的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列;
(2) 包含作为CDR-H1序列的SEQ ID NO: 99的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 109的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 121的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 130的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 150的氨基酸序列;
(3) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 110的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 131的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(4) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 111的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 132的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 152的氨基酸序列;或
(5) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 149的氨基酸序列;
(6) 包含作为CDR-H1序列的SEQ ID NO: 100的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 112的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 133的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(7) 包含作为CDR-H1序列的SEQ ID NO: 101的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 113的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 124的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 134的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 142的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 153的氨基酸序列;
(8) 包含作为CDR-H1序列的SEQ ID NO: 102的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 114的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 125的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 135的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 143的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 154的氨基酸序列;
(9) 包含作为CDR-H1序列的SEQ ID NO: 103的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 115的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 144的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 155的氨基酸序列;
(10) 包含作为CDR-H1序列的SEQ ID NO: 104的氨基酸序列;作为CDR-H2序列的SEQID NO: 116的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 137的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 145的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 156的氨基酸序列;
(11) 包含作为CDR-H1序列的SEQ ID NO: 98的氨基酸序列;作为CDR-H2序列的SEQ IDNO: 108的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 123的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 129的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 140的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 157的氨基酸序列;
(12) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQID NO: 115的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 126的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 146的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列;
(13) 包含作为CDR-H1序列的SEQ ID NO: 106的氨基酸序列;作为CDR-H2序列的SEQID NO: 117的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 122的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 138的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 141的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 151的氨基酸序列;
(14) 包含作为CDR-H1序列的SEQ ID NO: 105的氨基酸序列;作为CDR-H2序列的SEQID NO: 118的氨基酸序列;作为CDR-H3序列的SEQ ID NO: 127的氨基酸序列;作为CDR-L1序列的SEQ ID NO: 136的氨基酸序列;作为CDR-L2序列的SEQ ID NO: 147的氨基酸序列;和作为CDR-L3序列的SEQ ID NO: 158的氨基酸序列。
另外,作为本发明中的SPNS2中和抗体的一个方案,是包含下述氨基酸序列作为重链可变区的抗体:与选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ IDNO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQ ID NO: 62的序列具有80%以上、优选90%以上、进一步优选95%以上相似性的氨基酸序列。
作为本发明中的SPNS2中和抗体的另外一个方案,是包含下述氨基酸序列作为重链可变区的抗体:选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ IDNO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60或SEQ ID NO: 62的任一氨基酸序列;或在选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO:40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60或SEQ ID NO:6的任一氨基酸序列中1或2个以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列,优选所述序列的第1位~第17位的部位中的1或2个以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
上述方案中的SPNS2中和抗体优选作为重链可变区具有以下的(1)~(5)的任一特征。
(1) 包含SEQ ID NO: 42的氨基酸序列或含有选自SEQ ID NO: 42的第1位(Kabat编号:H1)的氨基酸残基取代为Glu以外的氨基酸残基、第6位(Kabat编号:H6)的氨基酸残基取代为Gly以外的氨基酸残基、第23位(Kabat编号:H23)的氨基酸残基取代为Glu以外的氨基酸残基、第43位(Kabat编号:H43)的氨基酸残基取代为Lys以外的氨基酸残基、第50位(Kabat编号:H50)的氨基酸残基取代为Thr以外的氨基酸残基、第75位(Kabat编号:H74)的氨基酸残基取代为Ala以外的氨基酸残基、第76位(Kabat编号:H75)的氨基酸残基取代为Arg以外的氨基酸残基、第78位(Kabat编号:H77)的氨基酸残基取代为Thr以外的氨基酸残基、第80位(Kabat编号:H79)的氨基酸残基取代为Ser以外的氨基酸残基、第97位(Kabat编号:H93)的氨基酸残基取代为Ala以外的氨基酸残基、和第102位(Kabat编号:H98)的氨基酸残基取代为Ser以外的氨基酸残基的1或2个以上的取代的SEQ ID NO: 42的氨基酸序列。
(2) 包含SEQ ID NO: 46的氨基酸序列或SEQ ID NO: 46的第82位(Kabat编号:H81)的氨基酸残基取代为Gln以外的氨基酸残基而得的氨基酸序列。
(3) 包含SEQ ID NO: 58的氨基酸序列或含有选自SEQ ID NO: 58的第13位(Kabat编号:H13)的氨基酸残基取代为Gln以外的氨基酸残基、第23位(Kabat编号:H23)的氨基酸残基取代为Ala以外的氨基酸残基、第31位(Kabat编号:H31)的氨基酸残基取代为Asp以外的氨基酸残基、第49位(Kabat编号:H49)的氨基酸残基取代为Ala以外的氨基酸残基、第58位(Kabat编号:H55)的氨基酸残基取代为Tyr以外的氨基酸残基、第66位(Kabat编号:H63)的氨基酸残基取代为Val以外的氨基酸残基、第79位(Kabat编号:H76)的氨基酸残基取代为Arg以外的氨基酸残基、第86位(Kabat编号:H82A)的氨基酸残基取代为Phe以外的氨基酸残基、第100位(Kabat编号:H94)的氨基酸残基取代为Ser以外的氨基酸残基、第109位(Kabat编号:H100C)的氨基酸残基取代为Ser以外的氨基酸残基、和第117位(Kabat编号:H105)的氨基酸残基取代为His以外的氨基酸残基的1或2个以上的取代的氨基酸序列。
(4) 包含SEQ ID NO: 44的氨基酸序列或含有选自SEQ ID NO: 44的第3位(Kabat编号:H3)的氨基酸残基取代为Gln以外的氨基酸残基、第10位(Kabat编号:H10)的氨基酸残基取代为Glu以外的氨基酸残基、第16位(Kabat编号:H16)的氨基酸残基取代为Thr以外的氨基酸残基、第19位(Kabat编号:H19)的氨基酸残基取代为Lys以外的氨基酸残基、第24位(Kabat编号:H24)的氨基酸残基取代为Val以外的氨基酸残基、第30位(Kabat编号:H30)的氨基酸残基取代为Thr以外的氨基酸残基、第31位(Kabat编号:H31)的氨基酸残基取代为Arg以外的氨基酸残基、第57位(Kabat编号:H56)的氨基酸残基取代为Thr以外的氨基酸残基、第66位(Kabat编号:H65)的氨基酸残基取代为Lys以外的氨基酸残基、第67位(Kabat编号:H66)的氨基酸残基取代为Lys以外的氨基酸残基、第74位(Kabat编号:H73)的氨基酸残基取代为Ala以外的氨基酸残基、第77位(Kabat编号:H76)的氨基酸残基取代为Asn以外的氨基酸残基、第80位(Kabat编号:H79)的氨基酸残基取代为Tyr以外的氨基酸残基、第83位(Kabat编号:H82)的氨基酸残基取代为Phe以外的氨基酸残基、第85位(Kabat编号:H82B)的氨基酸残基取代为Gly以外的氨基酸残基、第89位(Kabat编号:H85)的氨基酸残基取代为Glu以外的氨基酸残基、和第91位(Kabat编号:H87)的氨基酸残基取代为Thr以外的氨基酸残基的1或2个以上的取代的氨基酸序列。
(5) 包含选自SEQ ID NO: 52、SEQ ID NO: 36、或SEQ ID NO: 48的氨基酸序列。
上述方案中的SPNS2中和抗体更优选作为重链可变区具有以下的(1)~(5)的任一特征。
(1) 包含SEQ ID NO: 42的氨基酸序列或含有选自SEQ ID NO: 42的第1位(Kabat编号:H1)的氨基酸残基由Glu取代为Ala、第6位(Kabat编号:H6)的氨基酸残基由Gly取代为Glu、第23位(Kabat编号:H23)的氨基酸残基由Glu取代为Ala、第43位(Kabat编号:H43)的氨基酸残基由Lys取代为Arg、第50位(Kabat编号:H50)的氨基酸残基由Thr取代为Ser、第75位(Kabat编号:H74)的氨基酸残基由Ala取代为Thr、第76位(Kabat编号:H75)的氨基酸残基由Arg取代为Lys、第78位(Kabat编号:H77)的氨基酸残基由Thr取代为Ile、第80位(Kabat编号:H79)的氨基酸残基由Ser取代为Tyr、第97位(Kabat编号:H93)的氨基酸残基由Ala取代为Thr、和第102位(Kabat编号:H98)的氨基酸残基由Ser取代为Thr的1或2个以上的取代的氨基酸序列。
(2) 包含SEQ ID NO: 46的氨基酸序列或SEQ ID NO: 46的第82位(Kabat编号:H81)的氨基酸残基由Gln取代为Lys而得的氨基酸序列。
(3) 包含SEQ ID NO: 58的氨基酸序列或SEQ ID NO: 58的第13位(Kabat编号:H13)的氨基酸残基由Gln取代为Arg、第23位(Kabat编号:H23)的氨基酸残基由Ala取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Asp取代为Glu、第49位(Kabat编号:H49)的氨基酸残基由Ala取代为Gly、第58位(Kabat编号:H55)的氨基酸残基由Tyr取代为Ser、第66位(Kabat编号:H63)的氨基酸残基由Val取代为Ile、第79位(Kabat编号:H76)的氨基酸残基由Arg取代为Ser、第86位(Kabat编号:H82A)的氨基酸残基由Phe取代为Tyr或Asn、第100位(Kabat编号:H94)的氨基酸残基由Ser取代为Arg、第109位(Kabat编号:H100C)的氨基酸残基由Ser取代为Gly、和第117位(Kabat编号:H105)的氨基酸残基由His取代为Gln的1或2个以上的取代的氨基酸序列。
(4) 包含SEQ ID NO: 44的氨基酸序列或含有选自SEQ ID NO: 44的第3位(Kabat编号:H3)的氨基酸残基由Gln取代为His、第10位(Kabat编号:H10)的氨基酸残基由Glu取代为Ala或Gly、第16位(Kabat编号:H16)的氨基酸残基由Thr取代为Ala、第19位(Kabat编号:H19)的氨基酸残基由Lys取代为Arg、第24位(Kabat编号:H24)的氨基酸残基由Val取代为Ile、第30位(Kabat编号:H30)的氨基酸残基由Thr取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Arg取代为Ala、第57位(Kabat编号:H56)的氨基酸残基由Thr取代为Ser、第66位(Kabat编号:H65)的氨基酸残基由Lys取代为Asn、第67位(Kabat编号:H66)的氨基酸残基由Lys取代为Arg、第74位(Kabat编号:H73)的氨基酸残基由Ala取代为Val、第77位(Kabat编号:H76)的氨基酸残基由Asn取代为Asp或Ser、第80位(Kabat编号:H79)的氨基酸残基由Tyr取代为Ser、第83位(Kabat编号:H82)的氨基酸残基由Phe取代为Leu、第85位(Kabat编号:H82B)的氨基酸残基由Gly取代为Ser、第89位(Kabat编号:H85)的氨基酸残基由Glu取代为Asp、和第91位(Kabat编号:H87)的氨基酸残基由Thr取代为Ser的1或2个以上的取代的氨基酸序列。
(5) 包含选自SEQ ID NO: 52、SEQ ID NO: 36、或SEQ ID NO: 48的氨基酸序列。
另外,上述方案中的SPNS2中和抗体进一步优选包含作为重链可变区的选自SEQID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO: 40、SEQ ID NO: 42、SEQ ID NO:44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60或SEQ ID NO: 62的氨基酸序列。
作为本发明中的SPNS2中和抗体的一个方案,是包含下述氨基酸序列作为轻链可变区的抗体:与选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO:84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、或SEQ ID NO: 94的序列具有80%以上、优选90%以上、更优选95%以上相似性的氨基酸序列。
作为本发明中的SPNS2中和抗体的另外一个方案,是包含下述氨基酸序列作为轻链可变区的抗体:选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ IDNO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO:94的任一氨基酸序列;或在选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ IDNO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQID NO: 94的任一氨基酸序列中1或2以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列,优选所述序列的第1位~第12位的部位中的1或2以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
上述方案中的SPNS2中和抗体优选作为轻链可变区具有以下的(1)~(5)的任一特征。
(1) 包含SEQ ID NO: 88的氨基酸序列或含有选自SEQ ID NO: 88的第23位(Kabat编号:L24)的氨基酸残基取代为Thr以外的氨基酸残基、第26位(Kabat编号:L27)的氨基酸残基取代为Ile以外的氨基酸残基、第38位(Kabat编号:L37)的氨基酸残基取代为Lys以外的氨基酸残基、第48位(Kabat编号:L47)的氨基酸残基取代为Met以外的氨基酸残基、第80位(Kabat编号:L77)的氨基酸残基取代为Asn以外的氨基酸残基、第86位(Kabat编号:L83)的氨基酸残基取代为Glu以外的氨基酸残基、第96位(Kabat编号:L93)的氨基酸残基取代为Ser以外的氨基酸残基、第98位(Kabat编号:L95)的氨基酸残基取代为Met以外的氨基酸残基、第102位(Kabat编号:L99)的氨基酸残基取代为Gly以外的氨基酸残基、和第106位(Kabat编号:L103)的氨基酸残基取代为Lys以外的氨基酸残基的1或2个以上的取代的氨基酸序列。
(2) 包含SEQ ID NO: 78的氨基酸序列或SEQ ID NO: 78的第48位(Kabat编号:L47)的氨基酸残基取代为Leu以外的氨基酸残基和/或第106位(Kabat编号:L103)的氨基酸残基取代为Lys以外的氨基酸残基而得的氨基酸序列。
(3) 包含SEQ ID NO: 90的氨基酸序列或含有选自SEQ ID NO: 90的第9位(Kabat编号:L9)的氨基酸残基取代为Ala以外的氨基酸残基、第39位(Kabat编号:L39)的氨基酸残基取代为Lys以外的氨基酸残基、第42位(Kabat编号:L42)的氨基酸残基取代为Gly以外的氨基酸残基、第55位(Kabat编号:L55)的氨基酸残基取代为Ile以外的氨基酸残基、第56位(Kabat编号:L56)的氨基酸残基取代为Ser以外的氨基酸残基、第72位(Kabat编号:L72)的氨基酸残基取代为Thr以外的氨基酸残基、第74位(Kabat编号:L74)的氨基酸残基取代为Arg以外的氨基酸残基、第91位(Kabat编号:L91)的氨基酸残基取代为Thr以外的氨基酸残基、第93位(Kabat编号:L93)的氨基酸残基取代为Ser以外的氨基酸残基、第100位(Kabat编号:L100)的氨基酸残基取代为Ser以外的氨基酸残基、第103位(Kabat编号:L103)的氨基酸残基取代为Arg以外的氨基酸残基、和第106位(Kabat编号:L106)的氨基酸残基取代为Ile以外的氨基酸残基的1或2个以上的取代的氨基酸序列。
(4) 包含SEQ ID NO: 76的氨基酸序列或含有选自SEQ ID NO: 76的第13位(Kabat编号:L13)的氨基酸残基取代为Thr以外的氨基酸残基、第22位(Kabat编号:L22)的氨基酸残基取代为Arg以外的氨基酸残基、第25位(Kabat编号:L25)的氨基酸残基取代为Ala以外的氨基酸残基、第28位(Kabat编号:L28)的氨基酸残基取代为Asn以外的氨基酸残基、第31位(Kabat编号:L31)的氨基酸残基取代为Ser以外的氨基酸残基、第69位(Kabat编号:L69)的氨基酸残基取代为Thr以外的氨基酸残基、第79位(Kabat编号:L79)的氨基酸残基取代为Gln以外的氨基酸残基、和第80位(Kabat编号:L80)的氨基酸残基取代为Pro以外的氨基酸残基的1或2个以上的取代或缺损的氨基酸序列。
(5) 包含选自SEQ ID NO: 84、SEQ ID NO: 68、和SEQ ID NO: 80的氨基酸序列。
上述方案中的SPNS2中和抗体更优选作为轻链可变区具有以下的(1)~(5)的任一特征。
(1) 包含SEQ ID NO: 88的氨基酸序列或含有选自SEQ ID NO: 88的第23位(Kabat编号:L24)的氨基酸残基由Thr取代为Lys、第26位(Kabat编号:L27)的氨基酸残基由Ile取代为Thr、第38位(Kabat编号:L37)的氨基酸残基由Lys取代为Gln、第48位(Kabat编号:L47)的氨基酸残基由Met取代为Leu、第80位(Kabat编号:L77)的氨基酸残基由Asn取代为Ser、第86位(Kabat编号:L83)的氨基酸残基由Glu取代为Gly、第96位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第98位(Kabat编号:L95)的氨基酸残基由Met取代为Ile、第102位(Kabat编号:L99)的氨基酸残基由Gly取代为Ala、和第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr或Gln的1或2个以上的取代的氨基酸序列。
(2) 包含SEQ ID NO: 78的氨基酸序列或SEQ ID NO: 78的第48位(Kabat编号:L47)的氨基酸残基由Leu取代为Met和/或第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr而得的氨基酸序列。
(3) 包含SEQ ID NO: 90的氨基酸序列或含有选自SEQ ID NO: 90的第9位(Kabat编号:L9)的氨基酸残基由Ala取代为Pro、第39位(Kabat编号:L39)的氨基酸残基由Lys取代为Arg、第42位(Kabat编号:L42)的氨基酸残基由Gly取代为Glu、第55位(Kabat编号:L55)的氨基酸残基由Ile取代为Met、第56位(Kabat编号:L56)的氨基酸残基由Ser取代为Ala、第72位(Kabat编号:L72)的氨基酸残基由Thr取代为Ile、第74位(Kabat编号:L74)的氨基酸残基由Arg取代为Ser、第91位(Kabat编号:L91)的氨基酸残基由Thr取代为Ser、第93位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第100位(Kabat编号:L100)的氨基酸残基由Ser取代为Pro、第103位(Kabat编号:L103)的氨基酸残基由Arg取代为Lys、和第106位(Kabat编号:L106)的氨基酸残基由Ile取代为Val的1或2个以上的取代的氨基酸序列。
(4) 包含SEQ ID NO: 76的氨基酸序列或含有选自SEQ ID NO: 76的第13位(Kabat编号:L13)的氨基酸残基由Thr取代为Ala、第22位(Kabat编号:L22)的氨基酸残基由Arg取代为Ser、第25位(Kabat编号:L25)的氨基酸残基由Ala取代为Pro、第28位(Kabat编号:L28)的氨基酸残基由Asn取代为Ser、第31位(Kabat编号:L31)的氨基酸残基由Ser取代为Asn、第69位(Kabat编号:L69)的氨基酸残基由Thr取代为Ser、第79位(Kabat编号:L79)的氨基酸残基由Gln取代为Arg、和第80位(Kabat编号:L80)的氨基酸残基由Pro取代为Ala的1或2个以上的取代或缺损的氨基酸序列。
(5) 包含选自SEQ ID NO: 84、SEQ ID NO: 68、或SEQ ID NO: 80的氨基酸序列。
上述方案中的SPNS2中和抗体进一步优选包含作为轻链可变区的选自SEQ ID NO:66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO:88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的氨基酸序列。
作为本发明中的SPNS2中和抗体的一个方案,其是下述的抗体:包含作为重链可变区的与选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO: 40、SEQ ID NO:42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60、和SEQ ID NO: 62的序列具有80%以上、优选90%以上、进一步优选95%以上相似性的氨基酸序列;且包含作为轻链可变区的与选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO:74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的序列具有80%以上、优选90%以上、更优选95%以上相似性的氨基酸序列。
作为本发明中的SPNS2中和抗体的另外一个方案,其是下述的抗体:
包含作为重链可变区的选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ IDNO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60、和SEQID NO: 62的任一氨基酸序列;或在选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ IDNO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60和SEQ ID NO: 62的任一氨基酸序列中1或2个以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列,优选所述序列的第1位~第17位的部位中的1或2个以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列;
包含作为轻链可变区的选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ IDNO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQID NO: 94的任一氨基酸序列;或在选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ IDNO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的任一氨基酸序列中1或2个以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列,优选所述序列的第1位~第12位的部位中的1或2个以上的氨基酸残基被取代、缺失或添加而得的氨基酸序列。
上述方案中的SPNS2中和抗体优选作为重链可变区和轻链可变区具有以下的(1)~(5)的任一特征。
(1) 包含作为重链可变区的SEQ ID NO: 42的氨基酸序列或含有选自SEQ ID NO:42的第1位(Kabat编号:H1)的氨基酸残基取代为Glu以外的氨基酸残基、第6位(Kabat编号:H6)的氨基酸残基取代为Gly以外的氨基酸残基、第23位(Kabat编号:H23)的氨基酸残基取代为Glu以外的氨基酸残基、第43位(Kabat编号:H43)的氨基酸残基取代为Lys以外的氨基酸残基、第50位(Kabat编号:H50)的氨基酸残基取代为Thr以外的氨基酸残基、第75位(Kabat编号:H74)的氨基酸残基取代为Ala以外的氨基酸残基、第76位(Kabat编号:H75)的氨基酸残基取代为Arg以外的氨基酸残基、第78位(Kabat编号:H77)的氨基酸残基取代为Thr以外的氨基酸残基、第80位(Kabat编号:H79)的氨基酸残基取代为Ser以外的氨基酸残基、第97位(Kabat编号:H93)的氨基酸残基取代为Ala以外的氨基酸残基、和第102位(Kabat编号:H98)的氨基酸残基取代为Ser以外的氨基酸残基的1或2个以上的取代的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 88的氨基酸序列或含有选自SEQ ID NO: 88的第23位(Kabat编号:L24)的氨基酸残基取代为Thr以外的氨基酸残基、第26位(Kabat编号:L27)的氨基酸残基取代为Ile以外的氨基酸残基、第38位(Kabat编号:L37)的氨基酸残基取代为Lys以外的氨基酸残基、第48位(Kabat编号:L47)的氨基酸残基取代为Met以外的氨基酸残基、第80位(Kabat编号:L77)的氨基酸残基由Asn取代为Ser、第86位(Kabat编号:L83)的氨基酸残基取代为Glu以外的氨基酸残基、第96位(Kabat编号:L93)的氨基酸残基取代为Ser以外的氨基酸残基、第98位(Kabat编号:L95)的氨基酸残基取代为Met以外的氨基酸残基、第102位(Kabat编号:L99)的氨基酸残基取代为Gly以外的氨基酸残基、和第106位(Kabat编号:L103)的氨基酸残基取代为Lys以外的氨基酸残基的1或2个以上的取代的氨基酸序列。
(2) 包含作为重链可变区的SEQ ID NO: 46的氨基酸序列或SEQ ID NO: 46的第82位(Kabat编号:H81)的氨基酸残基取代为Gln以外的氨基酸残基而得的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 78的氨基酸序列或SEQ ID NO: 78的第48位(Kabat编号:L47)的氨基酸残基取代为Leu以外的氨基酸残基和/或第106位(Kabat编号:L103)的氨基酸残基取代为Lys以外的氨基酸残基而得的氨基酸序列。
(3) 包含作为重链可变区的SEQ ID NO: 58的氨基酸序列或含有选自SEQ ID NO:58的第13位(Kabat编号:H13)的氨基酸残基取代为Gln以外的氨基酸残基、第23位(Kabat编号:H23)的氨基酸残基取代为Ala以外的氨基酸残基、第31位(Kabat编号:H31)的氨基酸残基取代为Asp以外的氨基酸残基、第49位(Kabat编号:H49)的氨基酸残基取代为Ala以外的氨基酸残基、第58位(Kabat编号:H55)的氨基酸残基取代为Tyr以外的氨基酸残基、第66位(Kabat编号:H63)的氨基酸残基取代为Val以外的氨基酸残基、第79位(Kabat编号:H76)的氨基酸残基取代为Arg以外的氨基酸残基、第86位(Kabat编号:H82A)的氨基酸残基取代为Phe以外的氨基酸残基、第100位(Kabat编号:H94)的氨基酸残基取代为Ser以外的氨基酸残基、第109位(Kabat编号:H100C)的氨基酸残基取代为Ser以外的氨基酸残基、和第117位(Kabat编号:H105)的氨基酸残基取代为His以外的氨基酸残基的1或2个以上的取代的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 90的氨基酸序列或含有选自SEQ ID NO: 90的第9位(Kabat编号:L9)的氨基酸残基取代为Ala以外的氨基酸残基、第39位(Kabat编号:L39)的氨基酸残基取代为Lys以外的氨基酸残基、第42位(Kabat编号:L42)的氨基酸残基取代为Gly以外的氨基酸残基、第55位(Kabat编号:L55)的氨基酸残基取代为Ile以外的氨基酸残基、第56位(Kabat编号:L56)的氨基酸残基取代为Ser以外的氨基酸残基、第72位(Kabat编号:L72)的氨基酸残基取代为Thr以外的氨基酸残基、第74位(Kabat编号:L74)的氨基酸残基取代为Arg以外的氨基酸残基、第91位(Kabat编号:L91)的氨基酸残基取代为Thr以外的氨基酸残基、第93位(Kabat编号:L93)的氨基酸残基取代为Ser以外的氨基酸残基、第100位(Kabat编号:L100)的氨基酸残基取代为Ser以外的氨基酸残基、第103位(Kabat编号:L103)的氨基酸残基取代为Arg以外的氨基酸残基、和第106位(Kabat编号:L106)的氨基酸残基取代为Ile以外的氨基酸残基的1或2个以上的取代的氨基酸序列。
(4) 包含作为重链可变区的SEQ ID NO: 44的氨基酸序列或含有选自SEQ ID NO:44的第3位(Kabat编号:H3)的氨基酸残基取代为Gln以外的氨基酸残基、第10位(Kabat编号:H10)的氨基酸残基取代为Glu以外的氨基酸残基、第16位(Kabat编号:H16)的氨基酸残基取代为Thr以外的氨基酸残基、第19位(Kabat编号:H19)的氨基酸残基取代为Lys以外的氨基酸残基、第24位(Kabat编号:H24)的氨基酸残基取代为Val以外的氨基酸残基、第30位(Kabat编号:H30)的氨基酸残基取代为Thr以外的氨基酸残基、第31位(Kabat编号:H31)的氨基酸残基取代为Arg以外的氨基酸残基、第57位(Kabat编号:H56)的氨基酸残基取代为Thr以外的氨基酸残基、第66位(Kabat编号:H65)的氨基酸残基取代为Lys以外的氨基酸残基、第67位(Kabat编号:H66)的氨基酸残基取代为Lys以外的氨基酸残基、第74位(Kabat编号:H73)的氨基酸残基取代为Ala以外的氨基酸残基、第77位(Kabat编号:H76)的氨基酸残基取代为Asn以外的氨基酸残基、第80位(Kabat编号:H79)的氨基酸残基取代为Tyr以外的氨基酸残基、第83位(Kabat编号:H82)的氨基酸残基取代为Phe以外的氨基酸残基、第85位(Kabat编号:H82B)的氨基酸残基取代为Gly以外的氨基酸残基、第89位(Kabat编号:H85)的氨基酸残基取代为Glu以外的氨基酸残基、和第91位(Kabat编号:H87)的氨基酸残基取代为Thr以外的氨基酸残基的1或2个以上的取代的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 76的氨基酸序列或含有选自SEQ ID NO: 76的第13位(Kabat编号:L13)的氨基酸残基取代为Thr以外的氨基酸残基、第22位(Kabat编号:L22)的氨基酸残基取代为Arg以外的氨基酸残基、第25位(Kabat编号:L25)的氨基酸残基取代为Ala以外的氨基酸残基、第28位(Kabat编号:L28)的氨基酸残基取代为Asn以外的氨基酸残基、第31位(Kabat编号:L31)的氨基酸残基取代为Ser以外的氨基酸残基、第69位(Kabat编号:L69)的氨基酸残基取代为Thr以外的氨基酸残基、第79位(Kabat编号:L79)的氨基酸残基取代为Gln以外的氨基酸残基、和第80位(Kabat编号:L80)的氨基酸残基取代为Pro以外的氨基酸残基的1或2个以上的取代或缺损的氨基酸序列。
(5) 包含作为重链可变区的选自SEQ ID NO: 52、SEQ ID NO: 36、或SEQ ID NO:48的氨基酸序列;
包含作为轻链可变区的选自SEQ ID NO: 84、SEQ ID NO: 68、或SEQ ID NO: 80的氨基酸序列。
上述方案中的SPNS2中和抗体更优选作为重链可变区和轻链可变区具有以下的(1)~(5)的任一特征。
(1) 包含作为重链可变区的SEQ ID NO: 42的氨基酸序列或含有选自SEQ ID NO:42的第1位(Kabat编号:H1)的氨基酸残基由Glu取代为Ala、第6位(Kabat编号:H6)的氨基酸残基由Gly取代为Glu、第23位(Kabat编号:H23)的氨基酸残基由Glu取代为Ala、第43位(Kabat编号:H43)的氨基酸残基由Lys取代为Arg、第50位(Kabat编号:H50)的氨基酸残基由Thr取代为Ser、第75位(Kabat编号:H74)的氨基酸残基由Ala取代为Thr、第76位(Kabat编号:H75)的氨基酸残基由Arg取代为Lys、第78位(Kabat编号:H77)的氨基酸残基由Thr取代为Ile、第80位(Kabat编号:H79)的氨基酸残基由Ser取代为Tyr、第97位(Kabat编号:H93)的氨基酸残基由Ala取代为Thr、和第102位(Kabat编号:H98)的氨基酸残基由Ser取代为Thr的1或2个以上的取代的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 88的氨基酸序列或含有选自SEQ ID NO: 88的第23位(Kabat编号:L24)的氨基酸残基由Thr取代为Lys、第26位(Kabat编号:L27)的氨基酸残基由Ile取代为Thr、第38位(Kabat编号:L37)的氨基酸残基由Lys取代为Gln、第48位(Kabat编号:L47)的氨基酸残基由Met取代为Leu、第80位(Kabat编号:L77)的氨基酸残基由Asn取代为Ser、第86位(Kabat编号:L83)的氨基酸残基由Glu取代为Gly、第96位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第98位(Kabat编号:L95)的氨基酸残基由Met取代为Ile、第102位(Kabat编号:L99)的氨基酸残基由Gly取代为Ala、和第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr或Gln的1或2个以上的取代的氨基酸序列。
(2) 包含作为重链可变区的SEQ ID NO: 46的氨基酸序列或SEQ ID NO: 46的第82位(Kabat编号:H81)的氨基酸残基由Gln取代为Lys而得的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 78的氨基酸序列或SEQ ID NO: 78的第48位(Kabat编号:L47)的氨基酸残基由Leu取代为Met和/或第106位(Kabat编号:L103)的氨基酸残基由Lys取代为Thr而得的氨基酸序列。
(3) 包含作为重链可变区的SEQ ID NO: 58的氨基酸序列或含有选自SEQ ID NO:58的第13位(Kabat编号:H13)的氨基酸残基由Gln取代为Arg、第23位(Kabat编号:H23)的氨基酸残基由Ala取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Asp取代为Glu、第49位(Kabat编号:H49)的氨基酸残基由Ala取代为Gly、第58位(Kabat编号:H55)的氨基酸残基由Tyr取代为Ser、第66位(Kabat编号:H63)的氨基酸残基由Val取代为Ile、第79位(Kabat编号:H76)的氨基酸残基由Arg取代为Ser、第86位(Kabat编号:H82A)的氨基酸残基由Phe取代为Tyr或Asn、第100位(Kabat编号:H94)的氨基酸残基由Ser取代为Arg、第109位(Kabat编号:H100C)的氨基酸残基由Ser取代为Gly、和第117位(Kabat编号:H105)的氨基酸残基由His取代为Gln的1或2个以上的取代的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 90的氨基酸序列或含有选自SEQ ID NO: 90的第9位(Kabat编号:L9)的氨基酸残基由Ala取代为Pro、第39位(Kabat编号:L39)的氨基酸残基由Lys取代为Arg、第42位(Kabat编号:L42)的氨基酸残基由Gly取代为Glu、第55位(Kabat编号:L55)的氨基酸残基由Ile取代为Met、第56位(Kabat编号:L56)的氨基酸残基由Ser取代为Ala、第72位(Kabat编号:L72)的氨基酸残基由Thr取代为Ile、第74位(Kabat编号:L74)的氨基酸残基由Arg取代为Ser、第91位(Kabat编号:L91)的氨基酸残基由Thr取代为Ser、第93位(Kabat编号:L93)的氨基酸残基由Ser取代为Asn、第100位(Kabat编号:L100)的氨基酸残基由Ser取代为Pro、第103位(Kabat编号:L103)的氨基酸残基由Arg取代为Lys、和第106位(Kabat编号:L106)的氨基酸残基由Ile取代为Val的1或2个以上的取代的氨基酸序列。
(4) 包含作为重链可变区的SEQ ID NO: 44的氨基酸序列或含有选自SEQ ID NO:44的第3位(Kabat编号:H3)的氨基酸残基由Gln取代为His、第10位(Kabat编号:H10)的氨基酸残基由Glu取代为Ala或Gly、第16位(Kabat编号:H16)的氨基酸残基由Thr取代为Ala、第19位(Kabat编号:H19)的氨基酸残基由Lys取代为Arg、第24位(Kabat编号:H24)的氨基酸残基由Val取代为Ile、第30位(Kabat编号:H30)的氨基酸残基由Thr取代为Ser、第31位(Kabat编号:H31)的氨基酸残基由Arg取代为Ala、第57位(Kabat编号:H56)的氨基酸残基由Thr取代为Ser、第66位(Kabat编号:H65)的氨基酸残基由Lys取代为Asn、第67位(Kabat编号:H66)的氨基酸残基由Lys取代为Arg、第74位(Kabat编号:H73)的氨基酸残基由Ala取代为Val、第77位(Kabat编号:H76)的氨基酸残基由Asn取代为Asp或Ser、第80位(Kabat编号:H79)的氨基酸残基由Tyr取代为Ser、第83位(Kabat编号:H82)的氨基酸残基由Phe取代为Leu、第85位(Kabat编号:H82B)的氨基酸残基由Gly取代为Ser、第89位(Kabat编号:H85)的氨基酸残基由Glu取代为Asp、和第91位(Kabat编号:H87)的氨基酸残基由Thr取代为Ser的1或2个以上的取代的氨基酸序列;
包含作为轻链可变区的SEQ ID NO: 76的氨基酸序列或含有选自SEQ ID NO: 76的第13位(Kabat编号:L13)的氨基酸残基由Thr取代为Ala、第22位(Kabat编号:L22)的氨基酸残基由Arg取代为Ser、第25位(Kabat编号:L25)的氨基酸残基由Ala取代为Pro、第28位(Kabat编号:L28)的氨基酸残基由Asn取代为Ser、第31位(Kabat编号:L31)的氨基酸残基由Ser取代为Asn、第69位(Kabat编号:L69)的氨基酸残基由Thr取代为Ser、第79位(Kabat编号:L79)的氨基酸残基由Gln取代为Arg、和第80位(Kabat编号:L80)的氨基酸残基由Pro取代为Ala的1或2个以上的取代或缺损的氨基酸序列。
(5) 包含作为重链可变区的选自SEQ ID NO: 52、SEQ ID NO: 36、或SEQ ID NO:48的氨基酸序列;
包含作为轻链可变区的选自SEQ ID NO: 84、SEQ ID NO: 68、或SEQ ID NO: 80的氨基酸序列。
上述方案中的SPNS2中和抗体进一步优选下述的抗体:包含作为重链可变区的选自SEQ ID NO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO: 40、SEQ ID NO: 42、SEQID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO:54、SEQ ID NO: 56、SEQ ID NO: 58、SEQ ID NO: 60或SEQ ID NO: 62的氨基酸序列;包含作为轻链可变区的选自SEQ ID NO: 66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQ ID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ IDNO: 84、SEQ ID NO: 86、SEQ ID NO: 88、SEQ ID NO: 90、SEQ ID NO: 92、或SEQ ID NO:94的氨基酸序列。
另外,作为本发明中的SPNS2中和抗体的一个方案,是包含以下的(1)~(15)的重链可变区和轻链可变区的抗体。
(1) 包含作为重链可变区的SEQ ID NO: 34的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 66的氨基酸序列。
(2) 包含作为重链可变区的SEQ ID NO: 36的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 68的氨基酸序列。
(3) 包含作为重链可变区的SEQ ID NO: 38的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 70的氨基酸序列。
(4) 包含作为重链可变区的SEQ ID NO: 40的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 72的氨基酸序列。
(5) 包含作为重链可变区的SEQ ID NO: 42的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 74的氨基酸序列。
(6) 包含作为重链可变区的SEQ ID NO: 44的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 76的氨基酸序列。
(7) 包含作为重链可变区的SEQ ID NO: 46的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 78的氨基酸序列。
(8) 包含作为重链可变区的SEQ ID NO: 48的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 80的氨基酸序列。
(9) 包含作为重链可变区的SEQ ID NO: 50的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 82的氨基酸序列。
(10) 包含作为重链可变区的SEQ ID NO: 52的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 84的氨基酸序列。
(11) 包含作为重链可变区的SEQ ID NO: 54的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 86的氨基酸序列。
(12) 包含作为重链可变区的SEQ ID NO: 56的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 88的氨基酸序列。
(13) 包含作为重链可变区的SEQ ID NO: 58的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 90的氨基酸序列。
(14) 包含作为重链可变区的SEQ ID NO: 60的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 92的氨基酸序列。
(15) 包含作为重链可变区的SEQ ID NO: 62的氨基酸序列;包含作为轻链可变区的SEQ ID NO: 94的氨基酸序列。
需要说明的是,作为鉴定抗体中的CDR-H1、CDR-H2、CDR-H3、CDR-L1、CDR-L2、或CDR-L3的各序列的方法,例如可举出:Kabat法(Kabat等人、The Journal of Immunology、1991、Vol.147、No.5、1709-1719页)或Chothia法(Al-Lazikani等人、Journal ofMolecular Biology、1997、Vol.273、No.4、927-948页)。这些方法对于该领域的本领域技术人员而言是技术常识,例如也可由Dr. Andrew C.R. Martin‘s Group的互联网主页(http://www.bioinf.org.uk/abs/)获知概要。
作为本发明的抗体的免疫球蛋白的框架序列优选为脊椎动物的免疫球蛋白的各类中的框架序列。特别是,优选为人或包括小鼠或大鼠的非人动物的免疫球蛋白的各类中的框架序列。
通过将人抗体的重链和轻链的各框架区和/或各恒定区的氨基酸序列与以上的重链和轻链的各CDR和/或各可变区的氨基酸序列适当组合,本领域技术人员即可设计本发明的人源化SPNS2中和抗体。人源化抗体的重链和轻链的各框架区和/或各恒定区的氨基酸序列例如可选自人的IgG、IgA、IgM、IgE、IgD的各类或其突变体。
关于本发明的SPNS2中和抗体,优选本发明的抗体或其抗原结合片段为人IgG类或其突变体、优选人IgG4亚类或人IgG1亚类或它们的突变体。在1个例子中,通过Kabat的体系,稳定化IgG4恒定区在铰链区的位置241中包含脯氨酸。关于该位置,依据EU编号方式(Kabat等人)、免疫学有关的蛋白的序列(Washington DC United States Department ofHealth and Human Services、2001 and Edelman等人、Proc. Natl. Acad. Sci USA、63、78-85、1969),是对应于铰链区的位置228。在人IgG4中,该残基通常为丝氨酸,可通过将丝氨酸取代为脯氨酸来诱导稳定化。在1个例子中,可将N297A突变掺入至IgG1的恒定区中,以尽可能地抑制与Fc受体的结合和/或固定补体的能力。
[竞争性结合]
与本发明的SPNS2中和抗体对SPNS2进行竞争性结合的抗体也包含在本发明的范围内。在本发明中,“竞争性结合”是指,在多种单克隆抗体与抗原共存时,一种抗体与抗原的结合被另一种抗体与抗原的结合抑制的现象。一般而言,对于一定量(浓度)的单克隆抗体,在将另外的单克隆抗体的量(浓度)进行改变而加入的情况下,可通过测定前者的一定量的单克隆抗体与抗原的结合量降低的添加量(浓度)来进行测定。其抑制的程度,能够以IC
[SPNS2中和抗体的制造方法]
本发明中的抗体可使用本领域技术人员所周知的技术而得到。本发明中的抗体为多克隆抗体或单克隆抗体(米尔斯坦(Milstein)等、自然(Nature)(England)1983年10月6日发行、305卷5934号、537~540页)。例如,关于多克隆抗体,能够以SEQ ID NO: 1的SPNS2的表达细胞、包含SEQ ID NO: 3、SEQ ID NO: 4、SEQ ID NO: 5、SEQ ID NO: 6、SEQ ID NO: 7、或SEQ ID NO: 8的肽为抗原、或将SEQ ID NO: 2的SPNS2的核苷酸对哺乳动物的肌肉或皮下进行给予,在致敏动物表达抗原而致敏,并从该动物的血清等中进行回收。另外,在使用肽作为抗原的情况下,可使用与BSA或KLH等的载体蛋白或聚赖氨酸等结合的形态的抗原。
关于该发明中的单克隆抗体,可通过将SEQ ID NO: 2的SPNS2的核苷酸给予该动物,在该动物的体内产生抗原,从经所产生的抗原致敏的哺乳动物取出免疫细胞,并与骨髓瘤细胞等进行细胞融合,由此克隆所得的杂交瘤,从其培养物中进行回收。作为这样的单克隆抗体的获取方法,记载于实施例6中,作为由此得到的单克隆抗体,可举出:具有SEQ IDNO: 34、SEQ ID NO: 36、SEQ ID NO: 38、SEQ ID NO: 40、SEQ ID NO: 42、SEQ ID NO: 44、SEQ ID NO: 46、SEQ ID NO: 48、SEQ ID NO: 50、SEQ ID NO: 52、SEQ ID NO: 54、SEQ IDNO: 56、SEQ ID NO: 58、SEQ ID NO: 60、和SEQ ID NO: 62的VH氨基酸序列;SEQ ID NO:66、SEQ ID NO: 68、SEQ ID NO: 70、SEQ ID NO: 72、SEQ ID NO: 74、SEQ ID NO: 76、SEQID NO: 78、SEQ ID NO: 80、SEQ ID NO: 82、SEQ ID NO: 84、SEQ ID NO: 86、SEQ ID NO:88、SEQ ID NO: 90、SEQ ID NO: 92、和SEQ ID NO: 94的VL氨基酸序列的单克隆抗体,但不限于这些。
所得的单克隆抗体也可得到具有编码该抗体的蛋白的氨基酸的基因序列的核酸分子。作为这样的基因序列的获取方法,记载于实施例8中,作为由此得到的单克隆抗体,可举出:编码SEQ ID NO: 35、SEQ ID NO: 37、SEQ ID NO: 39、SEQ ID NO: 41、SEQ ID NO:43、SEQ ID NO: 45、SEQ ID NO: 47、SEQ ID NO: 49、SEQ ID NO: 51、SEQ ID NO: 53、SEQID NO: 55、SEQ ID NO: 57、SEQ ID NO: 59、SEQ ID NO: 61、和SEQ ID NO: 63的VH氨基酸序列的基因;编码SEQ ID NO: 67、SEQ ID NO: 69、SEQ ID NO: 71、SEQ ID NO: 73、SEQ IDNO: 75、SEQ ID NO: 77、SEQ ID NO: 79、SEQ ID NO: 81、SEQ ID NO: 83、SEQ ID NO: 85、SEQ ID NO: 87、SEQ ID NO: 89、SEQ ID NO: 91、SEQ ID NO: 93、和SEQ ID NO: 95的VL氨基酸序列的基因,但不限于这些。
也可使用这样的核酸分子基因工程学地制作抗体。该抗体的基因信息使用H链、L链;它们的可变区使用CDR序列等的信息,进行用于提高抗体的结合性或特异性的修饰等,或通过从小鼠等动物的抗体修饰成人型抗体来制作适合用于治疗剂的结构的抗体,这对在该领域的本领域技术人员而言是熟知的技术。另外,作为将抗原致敏的动物,通过使用导入有人抗体基因的非人-转基因动物,也可获取人型的单克隆抗体。除此之外,作为不需要对动物致敏的方法,本领域技术人员也可适当进行如下技术:使用表达人抗体的可变区或其一部分的噬菌体文库(人抗体噬菌体展示),获取与所对应的抗原进行特异性结合的抗体或由特定的氨基酸序列构成的噬菌体克隆,并根据该信息制作人抗体(例如,参照TaketoTanaka等、Keio J. Med.、60卷、37-46页的评论等)。
另外,作为制造上述单克隆抗体的方法,可分别培养产生欲获取的抗体的杂交瘤,从所得的培养上清中通过常规方法纯化抗体而获取。另外,作为其他的制造方法,也可从产生欲获取的抗体的杂交瘤或从人抗体噬菌体展示中所得的噬菌体克隆等中获取编码抗体的基因、更详细而言获取编码免疫球蛋白的重链和/或轻链的基因,制作用于表达该基因的载体,并导入至宿主细胞(哺乳类细胞、昆虫细胞、微生物等),而产生该抗体。此时,对于编码免疫球蛋白的重链和/或轻链的基因,实施用于导入所期望性质的基因修饰、使用免疫球蛋白的重链和/或轻链的可变区或CDR区的结构信息来制作人源化抗体、抗体嵌合蛋白、低分子抗体或支架抗体,这可由本领域技术人员使用公知的技术来实施。另外,以提高抗体的性能或避免副作用为目的,对抗体的恒定区的结构加入修饰、或进行在糖链部分的修饰,这也可通过本领域技术人员所熟知的技术来适当进行。
本发明的SPNS2中和抗体可使用本领域技术人员所周知的技术而得到。具体而言,本发明的SPNS2中和抗体通常为单克隆抗体(Milstein等人、Nature、1983、Vol.305、No.5934、537-540页),所述单克隆抗体例如可通过以下的方法制作。
例如,制作编码本发明的SPNS2中和抗体的免疫球蛋白的重链和/或轻链的氨基酸序列的核酸分子。在此,通过将所述核酸分子导入至各种的载体或质粒,可制作包含该核酸分子的载体或质粒。然后,用上述的核酸分子、载体、或质粒转化宿主细胞。作为宿主细胞,例如可举出:哺乳动物细胞、昆虫细胞、酵母细胞、或植物细胞等的真核细胞、或者细菌细胞。其次,将该经转化的宿主细胞在用于产生本发明的SPNS2中和抗体的适当条件下进行培养。在此,根据需要,也可将所得的本发明的SPNS2中和抗体从宿主细胞中分离。这些程序中所用的各种方法,均是本领域技术人员所周知的。
另外,作为使用对动物致敏的方法,可使用导入有人抗体基因的非人-转基因动物作为将抗原致敏的动物,使SPNS2和/或其部分肽等致敏,取出免疫细胞,并与骨髓瘤细胞等进行细胞融合,将由此所得的杂交瘤进行克隆,从所得的培养上清中通过常规方法纯化抗体并回收,由此而得到。作为这样的单克隆抗体的获取方法,例如记载于国际公开第2013/180238号中。
除此之外,还可使用下述的技术:使用表达所期望的人源化抗体的可变区或其一部分的噬菌体文库(人抗体噬菌体展示),获取由与对应的抗原特异性结合的抗体或特定的氨基酸序列构成的噬菌体克隆,并根据该信息制作人源化抗体(例如,参照Taketo Tanaka等人、The Keio Journal of Medicine、Vol.60、37-46页的评论等)。
在此,通过对于编码免疫球蛋白的重链和/或轻链的基因,进行用于导入所期望性质的基因修饰、或者使用免疫球蛋白的重链和/或轻链的可变区或CDR区的结构信息来制作抗体嵌合蛋白、低分子抗体、支架抗体等,这是本领域技术人员使用公知的技术可以实施的。另外,以提高抗体的性能或避免副作用为目的,对抗体的恒定区的结构加入修饰、或进行在糖链部分的修饰,这也可通过本领域技术人员所熟知的技术来适当进行。
[含有SPNS2中和抗体的药物]
本发明的SPNS2中和抗体可用作起因于与S1P相关的状态或对S1P受体的作用的疾病的进展、复发或转移的抑制药、治疗药或预防药。具体而言,作为起因于与S1P相关的状态或对S1P受体的作用的疾病,可举出:显示自身免疫疾病的病态的、多发性硬化、类风湿性关节炎、牛皮癣、溃疡性结肠炎、克罗恩病、系统性红斑狼疮、狼疮性肾炎、哮喘、特应性皮炎、移植排斥反应、全身性关节僵直症、1型糖尿病、视神经炎、葡萄膜炎、中风、精神分裂症、肌萎缩性侧索硬化、皮肌炎、多发性肌炎、肺纤维化、桥本甲状腺炎、重症肌无力、自身免疫性甲状腺炎、和贝切特氏病;作为可期待作为癌症治疗药的疾病,可举出:神经母细胞瘤、横纹肌肉瘤、骨肉瘤、儿童癌症、卵巢癌、胰腺癌、乳腺癌、前列腺癌、骨癌、肺癌、结肠直肠癌、颈部癌、滑膜肉瘤、膀胱癌、胃癌、维尔姆斯瘤、转移性类癌、和与血管活性肠肽分泌肿瘤相关的腹泻、血管活性肠肽瘤(VIPoma,舒血管肠肽瘤)、Verner-Morrison综合征、贝克威思-威德曼综合征(Beckwith-Wiedemann syndrome)、肾癌、肾细胞癌、移行上皮癌、尤文肉瘤(Ewing's sarcoma)、白血病、急性成淋巴细胞性白血病、脑肿瘤、胶质母细胞瘤、非胶质母细胞瘤性脑肿瘤、脑脊膜瘤、垂体腺瘤、前庭神经鞘瘤、未分化神经外胚层肿瘤、髓母细胞瘤、星形细胞瘤、少突胶质瘤、脑室管膜瘤、和脉络丛乳头状瘤。特别是,本发明的SPNS2中和抗体优选用作癌症转移和/或多发性硬化复发的预防或它们的抑制药。另外,本发明的SPNS2中和抗体的优异之处在于通过给予该抗体不会产生心率波动。
含有本发明的SPNS2中和抗体的药物也可作为除了本发明的SPNS2中和抗体之外还含有医药上可接受的载体和/或其他添加剂的药物组合物的形式来进行制剂化。使用医药上可接受的载体和/或其他添加剂的制剂,例如可通过University of the Sciences inPhiladelphia、“Remington: The Science and Practice of Pharmacy、20th EDITION”,Lippincott Williams & Wilkins、2000中记载的方法进行实施。作为这样的药物的一个形式,以通过在无菌的水性液或油性液中溶解、悬浮或乳化而调制的液剂或冻干剂的方式供给。作为这样的溶剂或溶解液,作为水性液可举出注射用蒸馏水、生理盐水等,除此之外,在添加浸透压调节剂(例如,D-葡萄糖、D-山梨糖醇、D-甘露糖醇、氯化钠等)的情况下,有时也并用适当的助溶剂、例如醇(例如,乙醇)、多元醇(例如,丙二醇、聚乙二醇)、非离子性表面活性剂(例如,聚山梨醇酯80、聚氧乙烯氢化蓖麻油50)等。另外,作为溶剂或溶解液,有时也使用油性液,作为该油性液的例子,可举出:芝麻油、大豆油等,作为助溶剂,有时也并用苯甲酸苄酯、苄醇等。在这样的制剂中,有时适当使用缓冲剂(例如,磷酸盐类缓冲剂、乙酸盐类缓冲剂)、无痛化剂(例如,苯扎氯铵、盐酸普鲁卡因等)、稳定剂(例如,人血清白蛋白、聚乙二醇等)、保存剂(例如,抗坏血酸、异抗坏血酸和它们的盐等)、着色剂(例如,叶绿素铜、
另外,作为其他药物的形式,可举出:散剂、片剂、颗粒剂、胶囊剂、丸剂、栓剂、锭剂等固体制剂。在以口服用制剂的形式给予的固体制剂的情况下,作为添加剂,可使用:赋形剂(例如,结晶纤维素、乳糖、淀粉等)、润滑剂(例如,硬脂酸镁、滑石等)、粘合剂(羟丙基纤维素、羟丙基甲基纤维素、聚乙二醇等)、崩解剂(例如,淀粉、羧甲基纤维素钙等)等。另外,根据需要,可使用防腐剂(例如,苄醇、氯丁醇、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯等)、抗氧化剂、着色剂、甜味剂等的添加剂。而且,作为其他的形式,还可举出粘膜应用药,在该制剂中,以赋予对粘膜的吸附性、滞留性等为主要目的,有时还含有粘着剂、粘着增强剂、粘稠剂、粘稠化剂等(例如,粘蛋白、琼脂、明胶、果胶、角叉菜胶、海藻酸钠、刺槐豆胶、黄原胶、黄蓍胶、阿拉伯胶、壳聚糖、支链淀粉(Pullulan)、蜡质淀粉、硫糖铝、纤维素及其衍生物(例如,羟丙基甲基纤维素、聚甘油脂肪酸酯、丙烯酸(甲基)丙烯酸烷基酯共聚物或其盐、聚甘油脂肪酸酯等)作为添加剂。然而,供给至生物体的药物的形式和溶剂或添加剂并不限定于这些,本领域技术人员可适当选择。
含有本发明的SPNS2中和抗体的药物除了本发明的SPNS2中和抗体之外还可包含现有的其他药物(活性成分)。另外,也可将包含本发明的SPNS2中和抗体的药物与现有的其他药物组合,而作为试剂盒的形式。作为与SPNS2中和抗体组合的活性成分,可举出:免疫抑制剂或其类似物、抗癌剂或其类似物、SPNS2中和抗体或其类似物、氮卓斯汀(Azelastine)、苯咪唑嗪(Oxatomide)、美喹他嗪(Mequitazine)、非索非那定(Fexofenadine)、依匹斯汀(Epinastine)、依巴斯汀(Ebastine)、西替利嗪(Cetirizine)、左西替利嗪(Levocetirizine)、贝他斯汀(Bepotastine)、依美斯汀(Emedastine)、奥洛他定(Olopatadine)、氯雷他定(Loratadine)、左卡巴斯汀(Levocabastine)、奥扎格雷(Ozagrel)、塞曲司特(Seratrodast)、雷马曲班(Ramatroban)、普鲁司特(Pranlukast)、孟鲁司特(Montelukast)、扎鲁司特(Zafirlukast)、甲磺司特(Suplatast)、苯海拉明(Diphenhydramine)、茶苯海明(Dimenhydrinate)、双苯比拉林(Diphenylpyraline)、氯马斯汀(Clemastine)、氯苯那敏(Chlorpheniramine)、曲普利啶(Triprolidine)、异丙嗪(Promethazine)、阿利马嗪(Alimemazine)、羟嗪(Hydroxyzine)、高氯环嗪(Homochlorcyclizine)、赛庚啶(Cyproheptadine)、美沙拉嗪(Mesalazine)、干扰素
本发明中的药物,以症状的改善为目的,可胃肠外给予。在胃肠外给予的情况下,例如可为经鼻剂,可选择液剂、悬浮剂、固体制剂等。另外,作为其他的胃肠外给予的形式,可为注射剂,作为注射剂,可选择皮下注射剂、静脉注射剂、点滴注射剂、肌肉注射剂、脑室内注射剂、或腹腔内注射剂等。另外,作为用于其他的胃肠外给予的制剂,也可举出:栓剂、舌下剂、经皮剂、除了经鼻剂以外的经粘膜给予剂等。而且,也能够以在支架或血管内栓塞剂中含有或涂布的方案进行血管内局部给予。
本发明中的药物的给予量根据患者的年龄、性别、体重、症状、治疗效果、给予方法、处理时间、或该药物组合物所含的活性成分的种类等而不同,通常成人每1人、每1次能够以1mg~1g的范围、优选以0.1mg~300mg的范围、且1周~4周1次、或1个月~2个月1次来给予主剂。然而,由于给予量和给予次数根据各种条件而变化,因此,也有以少于上述给予量和次数的量和次数即足够的情况,而且也有必需超过上述范围的给予量和给予次数的情况。另外,本发明中的药物以较短的给予期间即可得到效果。
实施例
[实施例1] 基因克隆
以市售的人cDNA(Human MTC Panel II Takara Bio、636743)为模板,通过使用KOD -Plus-Ver.2(东洋纺Life Science、KOD-211)的PCR反应,来扩增编码人SPNS2的全长cDNA。
即,将包含1
将包含人SPNS2的cDNA的pCR Blunt II-TOPO用HindIII、NotI消化而得的片段插入至pcDNA5/FRT(Thermo Fisher Scientific、V601020)的多克隆位点HindIII、NotI位点。
获取cDNA克隆文库(Open Biosystems、MHS1010-7507992),将其用作模板,通过使用KOD-Plus Ver.2(东洋纺Life Science、KOD-211)的PCR反应,来扩增人SphK1。
即,将包含1
将包含人SphK1的cDNA的pCR Blunt II-TOPO用EcoRI、NotI消化而得的片段插入至pIRESpuro3(Takara Bio、631619)的多克隆位点EcoRI、NotI位点。
以市售的人cDNA(Human MTC Panel II Takara Bio、636743)为模板,通过使用KOD-Plus Ver.2(东洋纺Life Science、KOD-211)的PCR反应,来扩增人S1PR3。
即,将包含1
将包含人S1PR3的cDNA的pCR Blunt II-TOPO用EcoRI、NotI消化而得的片段插入至pIRESpuro3(Takara Bio、631619)的多克隆位点EcoRI、NotI位点。
关于小鼠SPNS2,将人工合成基因序列而得的序列插入至pcDNA5/FRT(ThermoFisher Scientific、V601020)的多克隆位点HindIII、NotI位点。以SEQ ID NO: 20表示的序列显示小鼠SPNS2基因的核苷酸序列,以SEQ ID NO: 19表示的序列显示小鼠SPNS2蛋白的氨基酸序列。
[实施例2] 稳定表达细胞的制作
人SphK1稳定表达细胞是利用脂质转染法导入掺入有人SphK1基因的pIRESpuro3表达载体,用含嘌呤霉素的选择培养基制作了稳定表达细胞系。人和小鼠SPNS2表达细胞是利用脂质转染法对人SphK1稳定表达Flp-In-293 Cell细胞(Thermo Fisher Scientific、R75007)导入掺入有人和小鼠的SPNS2基因的pcDNA5/FRT表达载体与Flp重组酶表达载体的pOG44(Thermo Fisher Scientific、V600520),用含潮霉素的选择培养基制作了稳定表达细胞系。人S1PR3稳定表达细胞是利用脂质转染法对CHO细胞导入掺入有人S1PR3基因的pIRESpuro3表达载体,用含嘌呤霉素的选择培养基制作了稳定表达细胞系。将在此制作的稳定表达株用于Cell ELISA、S1P产生抑制评价。
[实施例3] 稳定表达细胞的功能确认
一般而言,在生物体试样中的S1P的定量中使用质谱法。将人SPNS2、SphK1双重稳定表达细胞系或Mock载体(pcDNA5/FRT)、SphK1双重稳定表达细胞系以2mL/孔(8×10
[实施例4] N末端、C末端的定位确认
一般而言,SLC转运蛋白为12次跨膜型蛋白,但SPNS2的详细的结构域结构尚不明确。在使用跨膜区预测程序TMHMM (HTTP://www.cbs.dtu.dk/services/TMHMM/)server的预测中,预测到存在11个的跨膜结构域。因此,制作在SPNS2的N末端、C末端添加有FLAG序列的SPNS2构建体,研究了N末端、C末端的定位。以插入在pcDNA5/FRT的人SPNS2为模板,利用PCR在SPNS2的cDNA序列的N末端、C末端添加了FLAG序列。PCR条件是:将包含1
不进行膜透过处理的方法的详情:去除培养基,将孔用PBS洗涤后,以200
膜透过处理方法的详情:去除培养基,将孔用PBS洗涤后,添加4%多聚甲醛,在室温下放置5分钟后,去除4%多聚甲醛,添加含0.5%Triton X-100的PBS,在室温下放置15分钟后,去除溶液。用含3%BSA、0.2%血清的PBS在室温下放置30分钟,将孔用PBS洗涤后,以200
N末端、C末端均仅以膜透过处理的条件检测到FLAG的信号,可知N末端、C末端均在细胞内(图4)。根据该结果推测,SPNS2的跨膜结构域有偶数个。在由使用SOUSI(http://harrier.nagahama-i-bio.ac.jp/sosui/)server的跨膜区预测得到的预测跨膜区中,在TMHMM中预测不为跨膜区的最接近N末端的区域被添加为第1次的跨膜区作为推定细胞外区(图1、2)。
[实施例5] 大鼠抗人SPNS2抗体的制作
将人SPNS2的基因序列掺入至pIRESpuro3(Takara Bio、631619)的EcoRI、NotI。在人SPNS2表达载体的大量调制中,使用了EndoFree Plasmid Giga Kit(QIAGEN公司)。
免疫中使用了SLC/wisher的雌性大鼠(日本SLC公司)。首先,在大鼠胫骨前肌处肌肉注射了将人SPNS2掺入至pIRESpuro3而得的表达载体。接着,使用ECM830(BTX公司),使用2针电极(双极针电极),在同部位实施了体内电穿孔。每两周1次,共重复4次同样的体内电穿孔后,将人SPNS2、SphK1双重稳定表达细胞系给予至腹腔内,3天后采取大鼠的脾脏,用于杂交瘤制作。
[实施例6] 产生大鼠单克隆抗体的杂交瘤的制作
大鼠单克隆抗体可通过Kohler等人(Nature 256:495-497、1975)的杂交瘤法进行制作。将人SPNS2以DNA质粒和表达细胞的形式对大鼠进行免疫,将从大鼠采取的淋巴细胞和小鼠骨髓瘤细胞系(P3U1)通过电细胞融合法进行融合。具体而言,将1.8×10
[实施例7] 抗体同型的确定
为了确定抗SPNS2抗体的抗体同型,使用对抗体的同型特异性的抗体,实施了ELISA。将用PBS稀释为1
[表1]
[实施例8] 抗体序列的确定
使用RNeasy Mini Kit(Qiagen、74106),根据产品所附的方法,由产生抗SPNS2抗体的杂交瘤提取总RNA。将RNA浓度通过吸光度法进行定量后,使用Omniscript RT Kit(Qiagen、205113),根据产品所附的方法,由1
即,将包含1
将用于确定杂交瘤克隆的抗体基因的引物组所含的引物的序列示于表2中,将用于确定各杂交瘤克隆的抗体基因的引物的组合示于表3中。关于未用引物组扩增的、表3中记载的一部分克隆,使用SMARTer
使用Zero Blunt TOPO PCR Cloning Kit(Thermo Fisher Scientific、K280020),根据产品所附的方法,将PCR产物插入至克隆载体。转化为E. coli DH5
[表2]
[表3]
[表4]
[表5]
[实施例9] 对SPNS2的结合活性(Cell ELISA)
为了研究抗SPNS2抗体对人SPNS2和小鼠SPNS2的结合活性,使用表达SPNS2的细胞,实施了Cell ELISA。
将人和小鼠SPNS2、人SphK1双重稳定表达Flp-In-293细胞以1×10
[表6]
[实施例10] 抗SPNS2抗体的结合部位的分析(流式细胞术)
为了鉴定抗SPNS2抗体对SPNS2的结合部位,测定了抗SPNS2抗体对在人SPNS2的细胞外环序列中插入有FLAG标签序列(SEQ ID NO: 22)的突变体的结合性。
具体而言,制作了在人SPNS2的细胞外环序列中插入有FLAG标签序列的、以下的4个突变体。
(突变体1) 使人SPNS2的细胞外环1序列(SEQ ID NO: 3)突变而得的突变体1(SEQID NO: 160)。
(突变体2) 使人SPNS2的细胞外环5序列(SEQ ID NO: 5)突变而得的突变体2(SEQID NO: 164)。
(突变体3) 使人SPNS2的细胞外环7序列(SEQ ID NO: 6)突变而得的突变体3(SEQID NO: 166)。
(突变体4) 使人SPNS2的细胞外环11序列(SEQ ID NO: 8)突变而得的突变体4(SEQ ID NO: 170)。
利用脂质转染法,在HEK293细胞中导入了分别掺入有上述4种SPNS2的突变体1~4的基因(SEQ ID NO: 161、165、167、171)的pcDNA5/FRT(Thermo Fisher Scientific、V601020)。在脂质转染后,从培养皿中回收经过夜培养的HEK293细胞,使其于含有各20
[表7]
各抗体主要与细胞外环1序列和细胞外环5序列结合。具备SPNS2中和活性的抗体主要与细胞外环1序列和细胞外环5序列结合,由于没有中和活性的抗体与细胞外环7序列和细胞外环11序列结合,因此明确了:为了得到SPNS2中和活性,识别细胞外环1序列和细胞外环5序列是重要的。需要说明的是,未观察到SPNS2抑制活性的82-1109A保有CDR-H1(SEQ IDNO: 107)、CDR-H2(SEQ ID NO: 119)、CDR-H3(SEQ ID NO: 128)、CDR-L1(SEQ ID NO:139)、CDR-L2(SEQ ID NO: 148)、CDR-L3(SEQ ID NO: 159)作为CDR,不与细胞外环1序列、细胞外环5序列结合。
[实施例11] SPNS2中和抗体的表位的确定
为了更详细地限定结合部位,制作了对于结合有SPNS2中和抗体的细胞外环1及细胞外环5、和在FLAG序列插入突变体见不到抗FLAG抗体的反应性的细胞外环3将氨基酸取代而得的突变体。制作了细胞外环1的丙氨酸突变体(SEQ ID NO: 1的序列的第127位亮氨酸取代体L127A(SEQ ID NO: 172)、第128位天冬氨酸取代体D128A(SEQ ID NO: 173)、第129位异亮氨酸取代体I129A(SEQ ID NO: 174)、第130位谷氨酰胺取代体Q130A(SEQ ID NO: 175)、第131位谷氨酰胺取代体Q131A(SEQ ID NO: 176)、第132位组氨酸取代体H132A(SEQ IDNO: 177)、第133位苯丙氨酸取代体F133A(SEQ ID NO: 178)、第134位甘氨酸取代体G134A(SEQ ID NO: 179)、第135位缬氨酸取代体V135A(SEQ ID NO: 180)、第136位赖氨酸取代体K136A(SEQ ID NO: 181)、第137位天冬氨酸取代体D137A(SEQ ID NO: 182)、第138位精氨酸取代体R138A(SEQ ID NO: 183)、第139位甘氨酸取代体G139A(SEQ ID NO: 184));细胞外环3的丙氨酸突变体(SEQ ID NO: 1的序列的第189位脯氨酸取代体P189A(SEQ ID NO:185)、第190位谷氨酰胺取代体Q190A(SEQ ID NO: 186)、第191位谷氨酰胺取代体Q191A(SEQ ID NO: 187)、第192位酪氨酸取代体Y192A(SEQ ID NO: 188)、第193位苯丙氨酸取代体F193A(SEQ ID NO: 189)、第194位色氨酸取代体W194A(SEQ ID NO: 190)、第195位亮氨酸取代体L195A(SEQ ID NO: 191)、第196位亮氨酸取代体L196A(SEQ ID NO: 192)、第197位缬氨酸取代体V197A(SEQ ID NO: 193)、第198位亮氨酸取代体L198A(SEQ ID NO: 194)、第199位丝氨酸取代体S199A(SEQ ID NO: 195)、第200位精氨酸取代体R200A(SEQ ID NO:196)、第201位甘氨酸取代体G201A(SEQ ID NO: 197)、第202位亮氨酸取代体L202A(SEQ IDNO: 198));细胞外环5的丙氨酸或苯丙氨酸突变体(SEQ ID NO: 1的序列的第252位缬氨酸取代体V252A(SEQ ID NO: 199)、第253位赖氨酸取代体K253A(SEQ ID NO: 200)、第254位谷氨酰胺取代体Q254A(SEQ ID NO: 201)、第255位丙氨酸取代体A255F(SEQ ID NO: 206)、第256位丙氨酸取代体A256F(SEQ ID NO: 207)、第257位甘氨酸取代体G257A(SEQ ID NO:202)、第258位天冬氨酸取代体D258A(SEQ ID NO: 203)、第259位色氨酸取代体W259A(SEQID NO: 204)、第260位组氨酸取代体H260A(SEQ ID NO: 205))。人工合成了L127A突变体的基因(SEQ ID NO: 208)、D128A突变体的基因(SEQ ID NO: 209)、I129A突变体的基因(SEQID NO: 210)、Q130A突变体的基因(SEQ ID NO: 211)、Q131A突变体的基因(SEQ ID NO:212)、H132A突变体的基因(SEQ ID NO: 213)、F133A突变体的基因(SEQ ID NO: 214)、G134A突变体的基因(SEQ ID NO: 215)、V135A突变体的基因(SEQ ID NO: 216)、K136A突变体的基因(SEQ ID NO: 217)、D137A突变体的基因(SEQ ID NO: 218)、R138A突变体的基因(SEQ ID NO: 219)、G139A突变体的基因(SEQ ID NO: 220)、P189A突变体的基因(SEQ IDNO: 221)、Q190A突变体的基因(SEQ ID NO: 222)、Q191A突变体的基因(SEQ ID NO: 223)、Y192A突变体的基因(SEQ ID NO: 224)、F193A突变体的基因(SEQ ID NO: 225)、W194A突变体的基因(SEQ ID NO: 226)、L195A突变体的基因(SEQ ID NO: 227)、L196A突变体的基因(SEQ ID NO: 228)、V197A突变体的基因(SEQ ID NO: 229)、L198A突变体的基因(SEQ IDNO: 230)、S199A突变体的基因(SEQ ID NO: 231)、R200A突变体的基因(SEQ ID NO: 232)、G201A突变体的基因(SEQ ID NO: 233)、L202A突变体的基因(SEQ ID NO: 234)、V252A突变体的基因(SEQ ID NO: 235)、K253A突变体的基因(SEQ ID NO: 236)、Q254A突变体的基因(SEQ ID NO: 237)、A255F突变体的基因(SEQ ID NO: 242)、A256F突变体的基因(SEQ IDNO: 243)、G257A突变体的基因(SEQ ID NO: 238)、D258A突变体的基因(SEQ ID NO: 239)、W259A突变体的基因(SEQ ID NO: 240)、H260A突变体的基因(SEQ ID NO: 241)。利用脂质转染法,在HEK293T细胞中导入了插入有上述36种SPNS2之1个氨基酸突变体的基因的pcDNA5/FRT(Thermo Fisher Scientific、V601020)。在脂质转染后,从培养皿中回收经过夜培养的HEK293T细胞,并悬浮于含有20
[表8]
已知SPNS2中和抗体具有对跨细胞外环与SPNS2结合而言为重要的氨基酸,由该结果提示SPNS2中和抗体是识别SPNS2的立体结构的抗体。综合考察各SPNS2中和抗体所需的氨基酸残基时,显示出细胞外环1是至少包含从SEQ ID NO: 3的N末端起第1位的Leu(SEQ IDNO: 1的第127位的Leu)~第13位的Gly(SEQ ID NO: 1的第139位的Gly)的序列,细胞外环3是至少包含从SEQ ID NO: 4的N末端起第2位的Gln(SEQ ID NO: 1的第190位的Gln)~第12位的Arg(SEQ ID NO: 1的第200位的Arg)的序列,细胞外环5是至少包含从SEQ ID NO: 5的N末端起第1位的Val(SEQ ID NO: 1的第252位的Val)~第9位的His(SEQ ID NO: 1的第260位的His)的序列。另外,认为抑制SPNS2的S1P转运的抗体,通过与细胞外环1、细胞外环3或细胞外环5结合,来抑制S1P转运所需的结构变化。
[实施例12] 使用S1P检测生物测定法来评价抗SPNS2抗体对SPNS2介导的S1P转运能力所带来的影响
为了检测抗SPNS2抗体对SPNS2介导的S1P转运的抑制作用,以S1P受体的下游信号的活化为指标构建了生物测定法。
作为产生S1P的细胞,使用了人或小鼠的SPNS2、人SphK1基因双重稳定表达Flp-In-293细胞。作为检测S1P的细胞,使用了人S1PR3稳定表达CHO细胞。为了测定SPNS2的S1P转运能力,将SPNS2、SphK1双重稳定表达细胞系的培养上清添加至S1PR3稳定表达细胞系,用Ca
将人或小鼠SPNS2、人SphK1双重稳定表达细胞系以100
作为结果,在18-0211B、33-0503E、37-0511F、49-0703G、50-0704C、53-0707E、64-0807A、65-0810G、80-1104A、83-1110B、84-1111F、89-1207D、93-1310F、94-1311E和96-1403F的15个克隆的抗体中,观察到SPNS2介导的S1P转运能力的抑制活性。
另一方面,在82-1109A中未观察到该抑制活性。
[表9]
[实施例13] 使用基于质谱的S1P检测法来评价抗SPNS2抗体对SPNS2介导的S1P转运能力所带来的影响
一般而言,在生物体试样中的S1P的定量中使用质谱法。
将人或小鼠SPNS2、人SphK1双重稳定表达细胞系以100
将对人SPNS2的抑制结果示于图7中,将对小鼠SPNS2的抑制结果示于图8中。另外,计算出显示各抗体的50%抑制活性的浓度的对数值(pIC50),并示于表10中。作为结果,在18-0211B、33-0503E、37-0511F、49-0703G、50-0704C、53-0707E、64-0807A、65-0810G、80-1104A、83-1110B、84-1111F、89-1207D、93-1310F、94-1311E和96-1403F的15个克隆的抗体中,观察到SPNS2介导的S1P转运能力的抑制活性。另一方面,在82-1109A中未观察到该抑制活性。
[表10]
[实施例14] SPNS2中和抗体克隆之间的相似性分析
在实施例12和13中,18-0211B、33-0503E、37-0511F、49-0703G、50-0704C、53-0707E、64-0807A、65-0810G、80-1104A、83-1110B、84-1111F、89-1207D、93-1310F、94-1311E和96-1403F的15个克隆的抗体,由于具有SPNS2的S1P转运能力的抑制活性(中和活性),因此显示出其为SPNS2中和抗体。因此,对于该15个克隆的重链(H链)可变区和轻链(L链)可变区,进行了克隆之间的相似性的分析。相似性分析是对于各克隆的重链(H链)可变区和轻链(L链)可变区的氨基酸序列(与SEQ ID NO的对应参照表5),利用Needleman-Wunsch algorithm(Journal of Molecular Biology, 1970 Vol.48 pp443-453)的方法,在Matrix:EBLOSUM62、Gap open:100、Gap extend:0.5、End Gap Penalty:false、End Gap OpenPenalty:100和End Gap Extension Penalty:0.5的条件下来进行。另外,PhylogeneticTree分析是使用PRRN法(http://www.genome.jp/tools-bin/prrn)来进行。将各克隆的重链(H链)可变区和轻链(L链)可变区的氨基酸的相似性分析结果示于图9-1(重链可变区)和图9-2(轻链可变区)中。在图中,在右上半的部分以%表示的值,从上起表示对应的氨基酸序列之间的同一性(Identity:完全一致的氨基酸残基的比例)、相似性(Similarity:一致或类似的氨基酸残基的比例)、空隙(Gap:在对应的位置无氨基酸残基)。另外,在图中的左下半的部分以分数表示的是,对于将所对应的氨基酸排列的(序列比对的)情况的整体长度(分母),从上起分别表示在同一性、相似性和空隙的计算中所计数的氨基酸残基数(分子)。
根据所得的相似性分析结果可知,关于重链可变区的氨基酸序列,在18-0211B、33-0503E、49-0703G、50-0704C、64-0807A、65-0810G、84-1111F和89-1207D的8个克隆;80-1104A、93-1310F和96-1403F的3个克隆;37-0511F、53-0707E、83-1110B和94-1311E的4个克隆的抗体之间显示80%以上的相似性,而且,在18-0211B、49-0703G、50-0704C和89-1207D的4个克隆;64-0807A和84-1111F的2个克隆;80-1104A、93-1310F和96-1403F的3个克隆;37-0511F、53-0707E、和94-1311E的3个克隆之间的抗体中显示90%以上相似性且87%以上的同一性。可知,关于轻链可变区的氨基酸序列,在18-0211B、33-0503E、49-0703G、50-0704C、64-0807A、65-0810G、84-1111F和89-1207D的8个克隆;80-1104A、93-1310F和96-1403F的3个克隆;37-0511F、53-0707E、83-1110B和94-1311E的4个克隆的抗体之间显示80%以上的相似性,而且,在18-0211B、49-0703G、50-0704C和89-1207D的4个克隆;64-0807A和84-1111F的2个克隆;80-1104A、93-1310F和96-1403F的3个克隆;37-0511F、53-0707E、和94-1311E的3个克隆之间的抗体中显示95%以上的相似性且90%以上的同一性。
关于该重链可变区和轻链可变区的氨基酸序列的类似性的结果,在图10-1(重链可变区)和图10-2(轻链可变区)所示的Phylogenetic Tree分析的结果中也同样地,显示18-0211B、49-0703G、50-0704C和89-1207D的4个克隆;64-0807A和84-1111F的2个克隆;80-1104A、93-1310F和96-1403F的3个克隆;37-0511F、53-0707E、和94-1311E的3个克隆之间的抗体其氨基酸序列接近。根据该结果,将所得的15个克隆的抗体分类为组1:18-0211B、49-0703G、50-0704C和89-1207D的4个克隆;组2:64-0807A和84-1111F的2个克隆;组3:80-1104A、93-1310F和96-1403F的3个克隆;组4:37-0511F、53-0707E、和94-1311E的3个克隆。需要说明的是,33-0503E、65-0810G和83-1110B分类为不属于组1~4的抗体。在图11-1~图11-5中,分别排列并比较所分类的组之间的抗体中的重链可变区和轻链可变区的氨基酸序列(单字母符号),同时显示与Kabat编号(Kabat No.)的对比。将各克隆的对应的重链可变区或轻链可变区的氨基酸序列在纵向显示,将在组内与其他克隆不同的氨基酸残基的部分用网点显示。
[实施例15] SPNS2中和抗体所致的血液中淋巴细胞的减少作用的评价
已知SPNS2缺损小鼠与野生型小鼠进行比较,血液中淋巴细胞减少。调制94-1311E的小鼠IgG1嵌合抗体,通过对小鼠给予SPNS2中和抗体,确认了体内的中和抗体的药效。
94-1311E的小鼠IgG1嵌合抗体(重链:SEQ ID NO: 345和轻链:SEQ ID NO: 346)通过使用ExpiCHO细胞的一过性表达体系进行调制。制作将94-1311E的重链和轻链的可变区分别掺入至小鼠IgG1的重链恒定区和小鼠轻链
对8周龄的C57BL/6J小鼠(雄性)以每3天1次的频率皮下给予94-1311E的小鼠IgG1嵌合抗体28天。在给予28日后实施采血,将血液中淋巴细胞数利用流式细胞仪(BDLSRFortessa, Becton Dickinson)进行测定。
在经肝素处理的25
[表11]
与溶剂给予组进行比较,SPNS2中和抗体使血液中的CD4
- SPNS2中和抗体
- 第552位点发生突变的SPNS2突变基因及其检测方法
