一种用于荧光成像导航肿瘤切除和光热治疗的纳米复合体及其制备方法
文献发布时间:2023-06-19 10:11:51
技术领域
本发明设计生物医用材料技术领域,尤其设计肿瘤分子影像诊断和治疗探针分子的技术领域,特别是一种用于荧光成像导航肿瘤切除和光热治疗的纳米复合体及其制备方法。
背景技术
在临床诊疗中,与现有的临床医学影像检查方式相比,分子荧光成像具有低成本、简单易行、安全、实时、分辨率高、特异性强的优势。因此,迫切需要发展新的荧光成像引导肿瘤切除的新策略,借助相应的荧光探针的帮助,实现术中对肿瘤病灶的非侵入式、高穿透、高分辨、高灵敏和低噪声实时成像,指导外科医师在术中对肿瘤病灶进行精准定位和完全手术切除。近年来,新近发展的近红外二区(the Second Near-infrared Window,NIRII,900-1700nm)荧光,尤其是近红外二区b(NIR IIb,1500-1700nm)荧光在探测深层肿瘤方面,大大克服了近红外一区(the First Near-infrared Window,NIR I,650-900nm)荧光在探测肿瘤时组织穿透深度低和信噪比不高的限制;因此发射在NIR IIb区的探针成为荧光成像引导手术切除的理想造影剂。据此,发展肿瘤高灵敏性、高分辨率、高穿透深度的NIRIIb荧光探针,开展荧光成像引导的手术切除,对提高病人的生存率、降低肿瘤复发率具有重要意义。
然而,由于肿瘤经常表现为弥漫浸润性生长,肿瘤组织与正常组织往往缺乏明显边界,NIR IIb荧光探针对肿瘤成像的特异性仍有待提高。随着肿瘤生物学研究的不断进展,逐步认识到:肿瘤是一种非正常组织,有着非常复杂的结构和独特的微环境。肿瘤微环境与正常组织微环境之间的存在着很多差异,例如,弱酸性、酶过度表达、高还原性以及缺氧等。据此,设计肿瘤微环境刺激响应的NIR IIb智能纳米探针,可以提高其在肿瘤部位的特异性,有助于手术前对肿瘤进行精准定位。大部分肿瘤被发现时,已经存在癌细胞的潜在扩散,即使有些手术完全切除的肿瘤仍然不能避免转移和复发。光热治疗(PhotothermalTherapy,PTT)由于其具备创伤小、光照区域选择性高、对不同类型的肿瘤细胞均有杀伤效果等诸多优势。因此,手术切除联合光热治疗可以进一步增加肿瘤治疗的彻底性,有望成为彻底的根治肿瘤的新手段和新方法。
发明内容
本发明的目的在于提供一种用于荧光成像导航肿瘤切除和光热治疗的纳米复合体及其制备方法,以实现对肿瘤区域的特异性近红外二区b荧光成像,进而引导原位肿瘤的手术切除和转移灶的光热治疗,增加肿瘤治疗的彻底性,以期提高肿瘤的长期疗效。
为实现上述技术目的,达到上述技术效果,本发明公开了一种用于荧光成像导航肿瘤切除和光热治疗的纳米复合体,纳米复合体为QD@SiO
其中,纳米复合体在1650nm处有强荧光发射信号,处于水分子较低吸收峰和最适宜的深组织光学成像峰之间。
优选的,有机硅层状结构为病毒硅、介孔硅、多巴胺掺杂的硅球中的一种。
优选的,靶向蛋白为跨膜肽、RGD肽、叶酸、卵泡刺激素受体中的一种。
本发明还公开了一种用于荧光成像导航肿瘤切除和光热治疗的纳米复合体的制备方法,制备方法如下:
步骤1:合成QD量子点核心;
步骤2:在QD量子点核心的外层均匀包裹有机硅层状结构,并通过刻蚀的方法形成容纳近红外染料IR的介孔孔洞和/或空腔;
步骤3:采用物理或化学修饰方法将靶向蛋白TP复合于有机硅层,形成纳米复合体。
优选的,步骤1具体为通过高温溶剂热法合成PbS@CdS量子点。
优选的,步骤2具体为以PbS@CdS量子点为核心,通过反向微乳液法在其表面包裹无定型硅后,再通过两相法包裹病毒介孔无机硅;刻蚀无定型硅形成空腔后,最终获得空心的病毒介孔有机硅包裹的量子点,其空腔用于近红外染料IR820的负载。
优选的,步骤3具体为在步骤2得到的纳米载体壳层上化学修饰氨基,通过氨基与羧基缩合的方式将跨膜肽。
本发明具有以下有益效果:
本发明的优点之一是高量子产率NIR IIb荧光探针的构筑用作荧光成像引导的手术切除:高量子产率NIR IIb荧光探针的极高的穿透性和信噪比,可以高灵敏的对深层肿瘤进行精准的探测和高效切除,防止了肿瘤的原位复发。
本发明的优点之二是NIR IIb复合探针的低毒性,肿瘤细胞粘附性:空心病毒介孔有机硅的包裹可以降低NIR IIb复合探针中量子点的毒性,粗糙的类病毒表面可以进一步增加肿瘤细胞的粘附性。
本发明的优点之三是肿瘤微环境响应的NIR IIb复合探针用于荧光成像引导的手术切除:该复合探针的空心病毒介孔有机硅壳层可以对肿瘤微环境的GSH响应发生降解,释放出具有竞争吸收的近红外染料IR820,NIR IIb复合探针中量子点可以发出1650nm荧光用于荧光成像引导原发肿瘤的手术切除;释放出的IR820可以对转移灶进行光热治疗,两方面彻底的抑制肿瘤复发和肿瘤转移,大大提高病人的生存期。
附图说明
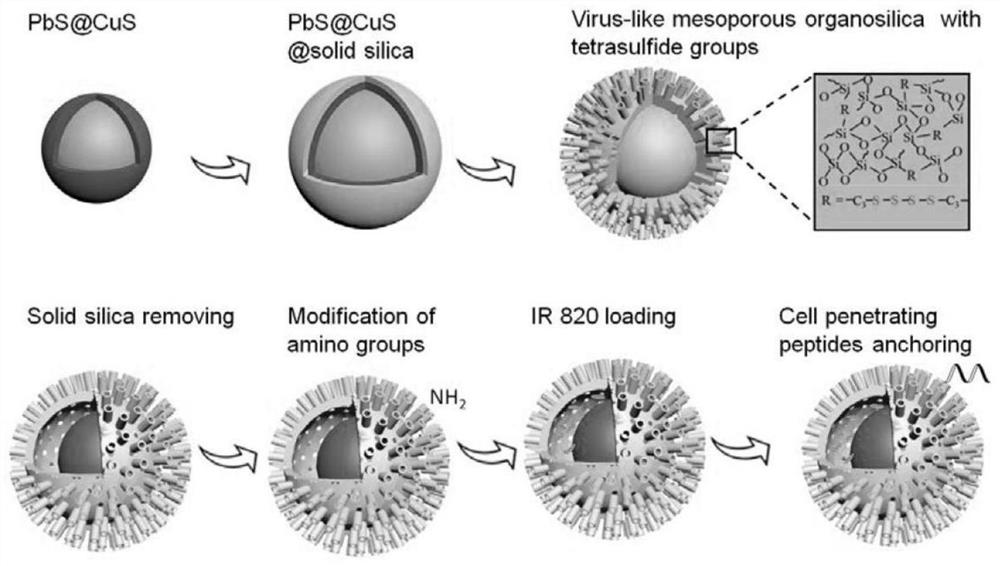
图1近红外二b区荧光复合探针逐级构筑示意图。
图2PbS@CdS,PbS@CdS@Silica,QD@HVMO的透射电镜图(A-C)以及动态光散射测量的三者的粒径分布(D-E),插入图为与透射电镜相对应的示意图,标尺为40nm。
图3(A)PbS@CdS,PbS@CdS@Silica,QD@HVMO在808nm激发下的发射光谱;(B)QD@HVMO的发射光谱和水分子的透射率光谱。
图4分散在水、PBS、血液、培养基中QD@HVMO在808nm激光连续照射不同时间后,1650nm处发射光的强度变化;(B)QD@HVMO在水、PBS、血液、培养基中孵育不同时间后,1650nm处发射光的强度变化。
图5近红外二b区复合探针尾静脉注射后不同小时的近红外二b区荧光成像图以及在注射后12h,通过近红外二b区荧光成像导航手术切除后肿瘤的H&E染色图。
图6复合纳米探针用于表皮瘤的热疗。(A)肿瘤大小的变化;(B)不同处理组在治疗4天后肿瘤部位的H&E和TUNNEL染色。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。
实施例1
如图1所示,本发明公开了以PbS@CdS量子点、病毒有机介孔硅为例进行说明,包括如下步骤:
通过高温溶剂热合成PbS@CdS量子点,考察不同核壳大小比例等因素对该量子点808nm激发下的发射波段和发射强度的影响。
以PbS@CdS量子点为核,通过反向微乳液法在其表面包裹无定型硅后,再通过两相法包裹病毒介孔无机硅;刻蚀无定型硅形成空腔后,最终获得空心的病毒介孔有机硅包裹的NIR IIb量子点(QD@HVMO)。其空腔用于近红外染料IR820的负载,在壳层最外修饰氨基以嫁接靶向多肽。
对QD@HVMO内部空腔负载IR820,构筑QD@HVMO-IR820;通过氨基羧基缩合嫁接跨膜肽,合成QD@HVMO-IR820-CPP,以利于癌细胞靶向吞噬。
具体合成方法如下:
通过溶剂热(油胺体系)首先合成PbS量子点:硫的前驱体主要是以0.08g硫粉和7.5mL的油胺,在120℃氩气氛围保护下,在160℃条件下保持30min,再加入10mL冰冷的环己烷和20mL乙醇停止反应。通过环己烷离心洗涤三次后分散在十八烯中。PbS@CdS量子点:1.2g CdO,8mL油酸,20mL十八烯,在氩气氛围下加热到200℃,然后冷却至100℃,制备Cd前驱体。5mL分散在十八烯中上述合成的PbS在氩气下鼓泡10min后,加入到上述Cd前驱体当中。在100℃下保持30min后,加入5mL冰冷的环己烷。最后PbS@CdS量子点通过乙醇离心洗涤三次后分散在环己烷当中。
实心硅和病毒介孔有机硅的包裹:实心硅球的包裹采用反向微乳液法,这里的硅源采用的是正硅酸四乙酯TEOS),病毒介孔有机硅采用TEOS和双-[3-(三乙氧基硅)丙基]-四硫化物(BTES)作为硅源(比例为5:4),采用两相法进行包裹。
实心硅球的刻蚀和纳米复合探针表面氨基基团的修饰:实心硅球的去除采用0.1MNa
实施例2
为了进一步表征所获得的复合探针其荧光光谱和荧光稳定性,本实施例以实施例1中所获得的PbS@CdS,PbS@CdS@Silica,QD@HVMO在808nm激发下的发射光谱进行了测定。
如图3所示,从发射光谱可以看出,PbS@CdS在NIR IIb有很强的发射(1650nm),在包裹实心硅和空心病毒介孔有机硅后,发射强度并无明显下降。同时在该处的发射可以规避水的最大吸收峰,因此可以用于高效的NIR IIb荧光成像。
如图4所示,对空心病毒介孔有机硅包裹的量子点的荧光的稳定性进行了测定,从结果可以看出,在808nm激光的连续照射下,无论在水、PBS、血液、培养基中,该复合纳米探针的发射光一直可以保持稳定,具有很强的抗光漂白的能力。同时在水、PBS、血液、培养基中做到长达96小时的保存之后,荧光强度也不会发生改变。
实施例3
为了进一步表征所获得复合探针在生物体中的荧光成像效果,本实施例以实施例1所获得的QD@HVMO-IR820-CPP进行原位肿瘤小鼠荧光成像表征。
NIR IIb荧光成像:取10只原位肿瘤小鼠,分成2组(每组5只),分别以尾静脉注射QD@HVMO-IR820-CPP,然后通过InGaAs CCD在不同时间段(2h,4h,6h,8h,12h,18h,24h,48h),1500nm滤光片,808nm激光照射下拍摄小鼠全身NIR IIb荧光图像。得出不同时间点肿瘤处信号强度的变化和信噪比,如图5所示,实验结果看出,在注射后12小时肿瘤最亮。
NIR IIb荧光成像引导的手术切除:在原位肿瘤和腘窝淋巴结模型中,在肿瘤最大时间点内,利用NIR IIb荧光成像引导,进行肝脏原位肿瘤的手术切除;对切除肿瘤进行甲醛(10%)固定24h后,依次经过酒精梯度脱水、二甲苯透明、石蜡包埋后制成切片、H&E染色,观察组织病理结构进行病理学切片,确定肿瘤组织是否切除干净,如图5所示,肿瘤和正常组织有明显的边界,证明肿瘤已经被切除干净。
实施例4
为了进一步表征所获得的纳米复合体对生物体肿瘤抑制生长的效果,本实施例以实施例1所获得的材料对小鼠表皮瘤进行不同组的光热治疗。
取10只带瘤小鼠,分成2组(每组5只),尾静脉注射QD@HVMO组、QD@HVMO-IR820-CPP组、QD@HVMO-IR820、IR820组、PBS组、激光照射组,对腘窝淋巴结进行NIR IIb荧光成像,探测肿瘤最大富集时间点,在此时间点内,通过808nm激光照射,分别检测测量后肿瘤的大小变化,治疗5天后,对肿瘤进行H&E和TUNNEL染色,结果如图6所示,QD@HVMO-IR820-CPP有及其明显的抗肿瘤优势性,可以大大的抑制肿瘤的生长。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。
- 一种用于荧光成像导航肿瘤切除和光热治疗的纳米复合体及其制备方法
- 一种用于肿瘤光热治疗联合免疫治疗的抗体偶联硒化铋纳米颗粒及其制备方法
