一种短肽在制备具有消除吗啡耐受性作用的产品中的应用
文献发布时间:2023-06-19 10:21:15
技术领域
本发明属于生物医药技术领域,具体涉及一种短肽在制备具有消除吗啡耐受性作用的产品中的应用。
背景技术
吗啡(Morphine),为阿片受体激动剂,在鸦片中的含量为4%-21%,平均 10%左右。IUPAC名称为7,8-Didehydro-4,5-epoxy-17-methyl-mor phinan-3,6-diol。分子式为C17H19NO3,分子量为285.3。1806年德国化学家泽尔蒂纳首次将其从鸦片中分离出来,并使用希腊梦神Morpheus的名字将其命名为吗啡。其衍生物盐酸吗啡是临床上常用的麻醉剂,有极强的镇痛作用,而且它的镇痛作用有较好的选择性,多用于创伤、手术、烧伤等引起的剧痛,也用于心肌梗死引起的心绞痛,还可作为镇痛、镇咳和止泻剂。
吗啡是临床疼痛治疗中重要的选择,但反复使用,会产生生理耐受性和依赖性。其临床表现主要是镇痛效果降低,表现为持续给予阿片类药物后镇痛效果逐渐减弱甚至消失,需要增加阿片类药物剂量才能获得同等的镇痛效果。
发明内容
本部分的目的在于概述本发明的实施例的一些方面以及简要介绍一些较佳实施例。在本部分以及本申请的说明书摘要和发明名称中可能会做些简化或省略以避免使本部分、说明书摘要和发明名称的目的模糊,而这种简化或省略不能用于限制本发明的范围。
鉴于上述的技术缺陷,提出了本发明。
因此,本发明提供一种短肽在制备具有消除吗啡耐受性作用的产品中的应用,其中,所述短肽,其氨基酸序列为:WKCNPNDDKCCRPKLKC。
作为本发明所述的短肽在制备具有消除吗啡耐受性作用的产品中的应用的一种优选方案:所述短肽,为低剂量短肽,其作用浓度为0.05μg/Kg以上。
作为本发明所述的短肽在制备具有消除吗啡耐受性作用的产品中的应用的一种优选方案:所述低剂量短肽,其作用浓度为0.05~0.1μg/Kg。
作为本发明所述的短肽在制备具有消除吗啡耐受性作用的产品中的应用的一种优选方案:所述短肽,其作用浓度在2μg/Kg以上时,既能够发挥镇痛作用又不发生耐受性。
作为本发明所述的短肽在制备具有消除吗啡耐受性作用的产品中的应用的一种优选方案:所述产品,其使用方式包括腹腔注射、静脉注射、鞘内注射。
本发明的有益效果:本发明研究发现,短肽P10581能够基本完全翻转由角叉菜胶诱导的炎性疼痛阈值,并且这种镇痛效果能够持续12h以上不变,表明短肽P10581对机械疼痛的镇痛效果不产生耐受性。并且低剂量合成短肽 P10581也能够消除吗啡镇痛作用的耐受性。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其它的附图。其中:
图1为合成短肽P10581和吗啡对大鼠痛觉过敏抑制效果耐受性比较图。
图2为低剂量短肽P10581对大鼠机械痛觉过敏的作用效果。
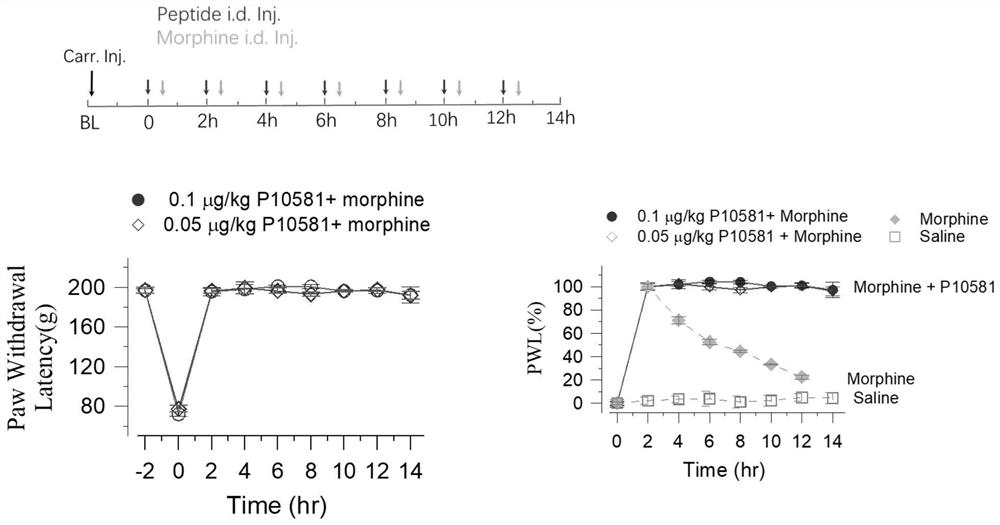
图3为低剂量短肽P10581对吗啡镇痛作用的耐受性。
具体实施方式
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合具体实施例对本发明的具体实施方式做详细的说明。
在下面的描述中阐述了很多具体细节以便于充分理解本发明,但是本发明还可以采用其他不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似推广,因此本发明不受下面公开的具体实施例的限制。
其次,此处所称的“一个实施例”或“实施例”是指可包含于本发明至少一个实现方式中的特定特征、结构或特性。在本说明书中不同地方出现的“在一个实施例中”并非均指同一个实施例,也不是单独的或选择性的与其他实施例互相排斥的实施例。
实验动物、仪器和试剂:
选择健康成年雄性SD大鼠(8周以上),体重180g-220g,购于徐州医科大学实验动物中心。
角叉菜胶(Carrageenan,简写为Carr)为美国sigma公司产品,配制 1%角叉菜胶(0.1g角叉菜胶溶于10ml 0.9%生理盐水溶液中,分装至10个EP 管),于-20℃保存,使用前半小时取出放置冰上。
38500-PAM压力应用测量系统(Ugo Basile Biological Research Apparatus,Comerio–Varese,Italy)由两部分组成,一部分为手持单元,另一部分为综合电子单元。手持单元为力传感器,该力传感器是根据 Randall-Selitto测痛仪而设计,综合电子单元可自动记录施加在大鼠左侧后足足底最大的机械缩足反射阈值。
大鼠炎性痛模型的制备:
6μl 1%角叉菜胶炎性痛模型:按照文献(Alessandri-Haber N,et al.Neurosci.Vol 29(19),pp 6217-6288,2009);介绍的方法制备角叉菜胶炎性痛模型。该法用于足底注射给药方式药物镇痛效果的检测。从大鼠左后足 2、3趾之间进针,注射1%角叉菜胶,注射量为6μl,该注射浓度可诱导产生痛觉过敏,即:在注射后1小时内大鼠足底即出现肿胀和痛觉阈值的降低。机械缩足反射阈值在100gf以下者作为角叉菜胶炎性痛造模成功大鼠。炎性阈值在100gf以上的炎性模型大鼠给予剔除。
机械性痛觉过敏检测:
实验一:测定合成短肽P10581和吗啡对大鼠痛觉过敏抑制效果的耐受性。选取180g-220g健康成年雄性SD大鼠,在其尾巴编号后放入同一鼠笼中(共 18只)。在测量房间适应2h,待大鼠安静后用38500-PAM压力应用测量系统(Ugo Basile Biological ResearchApparatus,Comerio–Varese,Italy)的锥形尖端对准大鼠左后足足底中心部位,以恒定的力率(30gf/s)测量大鼠的机械性缩足阈值,最大测量时间设定为15s(当测量值大于450gf时,会对大鼠造成损伤)。记录大鼠左后足缩时的机械性缩足阈值,若受试大鼠15s后仍未出现缩足反射,停止测量。每只大鼠重复测量3-5次,每次间隔5-10min,取平均值。测量完毕后足底皮内注射6μl 1%角叉菜胶,建立大鼠炎性疼痛模型。注射角叉菜胶1小时后检测大鼠左侧后足机械性缩足阈值,剔除阈值大小异常的大鼠(造模失败)。将炎性阈值较高与阈值较低的大鼠混合平均分为3组,每组6只,使得两组大鼠炎性阈值分布相似,A组注射生理盐水,B组注射 5mg/Kg吗啡,C组左后足底皮内注射2μg/Kg P10581,1h后记录各组大鼠左后足缩时的机械性缩足阈值,每只大鼠均重复测试3-5次(每次测试时间间隔为5-10min),取缩足反射阈值的平均值为该大鼠实际缩足反射阈值(单位为:g)。此后按照上述给药剂量和给药时间每2h注射药物,并记录大鼠机械性缩足阈值,共计6次。
实验二:测定低剂量短肽P10581对大鼠机械痛觉过敏不具有抑制效果。低剂量短肽P10581对大鼠机械痛觉过敏抑制效果的测定的方法步骤与实验一相似:
(1)实验二选取共计12只180g-220g健康成年雄性SD大鼠,1%角叉菜胶造模后,剔除造模失败大鼠,剩余大鼠分为2组,每组6只,A组注射生理盐水,B组左后足底皮内注射0.1μg/Kg的合成短肽P10581。
(2)按第一次给药剂量每2h注射药物,并记录大鼠机械性缩足阈值,反复给药共计7次。
实验三:测定低剂量合成短肽P10581对吗啡镇痛作用的耐受性的影响。低剂量合成短肽P10581对吗啡镇痛作用耐受性的影响的测定方法步骤与实验一相似,但有几点不同:
(1)实验三选取共计12只180g-220g健康成年雄性SD大鼠,1%角叉菜胶造模后,大鼠随机分为2组,每组6只,A、B组左后足底皮内先分别注射 0.1μg/Kg P10581和0.05μg/KgP10581,30min后两组大鼠于左后足底皮内注射5mg/Kg吗啡,1h后记录各组大鼠左后足缩时的机械性缩足阈值,每只大鼠均重复测试3-5次(每次测试时间间隔为5-10min)。
(2)按照第一次给药剂量和给药时间每2h注射药物,并记录大鼠机械性缩足阈值,共计7次。
上述实验设计均遵循随机、双盲的实验设计原则。
本发明的短肽序列:WKCNPNDDKCCRPKLKC(命名为P10581),含17个氨基酸序列(如图1),来源于蜘蛛毒素GsMTx4位于loop2和loop3的两个环状结构域。图1为合成短肽P10581和吗啡对大鼠痛觉过敏抑制效果耐受性比较图。其中,A图显示合成肽P10581序列;B.合成肽P10581和吗啡对大鼠痛觉过敏镇痛效果比较,多肽和吗啡每2小时通过足底皮内注射给药。C.P10581和吗啡对大鼠痛觉过敏镇痛标准化耐受性比较;实验结果表明,本发明短肽P10581 (2μg/kg)能够基本完全翻转由角叉菜胶诱导的炎性疼痛阈值,并且这种镇痛效果持续12h以上不变,表明短肽P10581对大鼠机械疼痛的镇痛效果不产生耐受性。但吗啡(5mg/kg)的镇痛效果随着注射次数的增加逐渐减弱,即吗啡对镇痛效果逐渐产生耐受性。
图2显示低剂量短肽P10581对大鼠机械痛觉过敏失去作用。短肽P10581 (0.1μg/Kg)每2小时通过足底皮内注射给药,结果表明低剂量P10581(0.1 μg/Kg)对大鼠痛觉过敏无镇痛效果,并且随着给药次数的增加始终无明显镇痛作用。
图3显示低剂量合成短肽P10581消除了吗啡镇痛作用的耐受性。事先在大鼠左后足底皮内注射6μl 1%角叉菜胶(Carr)诱导大鼠炎性痛模型,然后在大鼠左足底肿胀部位注射低剂量(0.1μg/Kg或0.05μg/Kg)合成短肽 P10581,30min后两组大鼠于左后足底皮内注射吗啡(5mg/Kg),1h后记录各组大鼠左后足缩时的机械性缩足阈值。此后按照上述给药剂量和给药时间每 2h注射药物,并记录大鼠机械性缩足阈值,共计7次。结果表明低剂量(0.1 μg/Kg或0.05μg/Kg)合成短肽P10581基本完全消除了吗啡镇痛作用的耐受性,且短肽的这种作用效果在实验过程中持续存在。图3低剂量合成短肽 P10581和吗啡对大鼠痛觉过敏镇痛效果标准化耐受性比较,可以看出:在没有多肽P0581共同用药情况下,吗啡的疼痛效果持续下降,表明吗啡镇痛效果产生了耐受性;但在低剂量多肽P10581(0.1μg/Kg或0.05μg/Kg)共同用药情况下,吗啡的镇痛效果持续不变,表明多肽P10581几乎可以完全消除吗啡镇痛的耐受性。
应说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,其均应涵盖在本发明的权利要求范围当中。
- 一种短肽在制备具有消除吗啡耐受性作用的产品中的应用
- 一种短肽在制备具有消除吗啡耐受性作用的产品中的应用
