具有温度监测的导管消融设备
文献发布时间:2023-06-19 10:32:14
技术领域
本发明涉及导管消融设备和使用这种设备的方法。本设备可以是微波消融设备,其应用于血管内交感神经切除或去神经(例如肾动脉去神经)的领域。本发明还可应用于包括治疗房性心律失常和室性心律失常在内的其他医疗消融领域。
背景技术
高血压是由于终末器官损伤(诸如中风、心脏病和肾衰竭)而导致发病和死亡的严重的医学疾病。许多患者需要多种药物来控制血压,而且对一些患者来说,药物耐受性差或完全无效。对于难治疗的或不耐受药物治疗的患者来说,通过射频导管消融进行肾动脉去神经已成为控制高血压的一种可能的治疗选择。该过程旨在消除在肾脏与中枢神经系统之间传递神经信息的传出神经和传入神经,因为它们构成了使血压升高的神经激素反射的重要组成部分。传出神经和传入神经在肾动脉的外层(即外膜)和肾周脂肪中行进,通常距离肾动脉内(腔)表面在1至6mm之间,这些神经可能被血管内导管消融破坏。
最近,提出了微波消融技术用于血管去神经,并且本发明的发明人已经在如WO2016/197206所述的微波消融设备的试验中证明了非常有效的结果,其全部内容通过引用包括在本文中。
这一概念的发展证实了使用血管内导管的微波消融在高血压治疗中用于肾脏去神经,以及在心律不齐的治疗中用于心脏消融。微波加热具有辐射性,可以深入地穿透到组织中,产生比射频消融更均匀温度分布的大的热损伤。该技术不需要任何导管尖端与组织接触来产生热量。
本说明书中包含对文件、行为、材料、设备、物品等的任何讨论仅是为了提供本发明背景的目的。其并未建议或表示这些事项中的任何一个构成如同在本申请的每个权利要求的优先权日之前存在于澳大利亚或其他地方的现有技术基础的一部分或是与本发明相关的领域的公知常识。
发明内容
在一种形式中,本发明提供了一种用于将能量输送到选定组织区域的导管消融设备,该设备具有天线部,该天线部包括可经由电馈线电连接到能量源的辐射天线,该天线被配置为产生能够消融所述选定组织区域中的组织的电磁场,该设备包括热电偶,该热电偶具有由热电偶导体与电馈线的导电部分之间的电连接形成的热接点。
这样,无需通过专用的热电偶导体对来实现热电偶,因为热电偶的第二导体由用于向设备天线提供消融能量的馈线提供。
优选地,该设备是用于输送微波能量的微波消融设备,能量源包括微波发生器,并且电馈线的导电部分是同轴微波馈线的屏蔽编织层。
优选地,所述热接点电连接点位于所述馈线连接到所述辐射天线的位置处或接近所述馈线连接到所述辐射天线的位置。
优选地,所述热电偶导体和所述馈线的所述导电部分电连接到热电偶温度监测装置,所述热电偶温度监测装置被配置成向所述设备的用户提供所述天线部中的温度的指示。
所述热电偶导体可以由热电偶导线(诸如康铜导线)提供。优选地,导管消融设备包括具有外鞘的细长导管,导线从所述导管鞘内的导管的近侧部分延伸至热接点电连接。
在一种形式中,所述热电偶导线布置为拉线,使得其从所述导管的近侧部分的操纵引起导管在所述天线部处的选择性操纵,所述热接点电连接提供所述拉线与所述电馈线之间的机械连接点以实现所述操纵。
以这种形式,该设备可包括在所述电馈线的远端处或邻近所述电馈线的远端的弯曲结构,所述拉线被布置成在被施加牵引时引起或允许所述弯曲结构的弯折,从而引起所述天线部的操纵。
弯曲结构可以包括围绕所述电馈线布置的套管,所述套管具有以定向布置配置的一个或多个能压缩元件,所述导线在所述套管内延伸,使得拉线的牵引引起套管的定向压缩,从而引起天线部的定向操纵。
优选地,所述导线以从所述导管的近侧部分到所述热接点电连接保持相对靠近电馈线的方式被容纳在所述导管鞘内。
因此,本发明的实施方式改善了消融过程的功效和安全性。
附图说明
现在将参考附图通过非限制性示例的方式描述本发明的各个方面的说明性实施例。在附图中:
图1示出微波消融设备的局部剖视图;
图2和图3示出了在替代实施例中包括热电偶布置的微波消融设备;
图4A和图4B以两种配置更详细地示出了图3的设备的一部分;
图5和图6示出了本发明的设备的试验的时间-温度图;
图7示意性地示出了包括阻抗传感器布置的微波消融设备;
图8和图9示出了图7的感测电极的替代实施例;以及
图10A和10B示出了图7的设备的试验的不同阶段的血管造影,图11示出了试验的时间-阻抗图。
具体实施方式
在图1中,示出了用于肾动脉去神经的微波消融设备10,其包括适于穿过脉管系统的细长柔性导管。特别地,设备10被示出位于肾动脉12中,其中由附图标记64指示消融区域。
在WO 2016/197206中更详细地描述了设备10和动脉12的各种部件以及周围神经。在该公开文献中还讨论了其他特征,包括可选的部件、材料、尺寸、功能、过程步骤和操作参数。
在本发明的背景中特别注意的是以下部件:
馈线22,由同轴缆线形成,包括绝缘外鞘26、外部传导屏蔽层28(例如编织铜线)、绝缘内鞘30和传导芯32。
微波辐射器24,具有辐射元件(天线)34,形成为馈线22的同轴缆线的端子部分,其屏蔽层和外部绝缘鞘被剥去。天线34被定位在设备10的远侧部分内并且被封装在管状鞘36中以使其与其环境绝缘。
馈线22和辐射器24被容纳在外导管鞘46内,外导管鞘的尺寸被制定为围绕馈线22提供足够的内部自由空间,以允许泵送的盐溶液从设备的近端流动到远端,以用作灌注剂和冷却剂。天线鞘36的远端和导管鞘46的远端在尖端42处粘合在一起。
为了提供用于设备的固定和定心功能以及供灌注流体离开设备的路径,导管鞘46包括一个或多个定位结构48,所述定位结构由围绕鞘布置成环的纵向狭缝50(例如6个狭缝)形成。设备的中心芯(包括馈线22和天线34)相对较硬,而鞘46由更柔软的材料制成。在近侧位置处相对于鞘46拉动馈线22,会使得鞘46的位于狭缝50之间的材料条向外变形为凸状突起,以抵靠动脉12的内壁14。在沿着设备的远侧部分的一个或多个位置处设置结构48,所述位置被选择为根据具体应用确保辐射器24被保持在所需的方位。在图1中,示出了靠近导管尖端42的单个远侧结构48。
图1还示出了结构支撑盖部40,其终止并密封外部传导屏蔽层28并提供外层以密封地覆盖馈线外鞘26与天线鞘36之间的过渡部,以及为该部分中的辐射器24提供结构支撑。
如本领域技术人员所理解的,设备10可以包括附加部件和功能,包括在WO 2016/197206中讨论的那些。
图1还图解地示出了设备10的近端,其连接到经皮进入位置PAL的外部,具有柄部H,柄部H提供与患者缆线52的连接。柄部H被设计成允许操作者通过两个轴向分开的柄部部分之间的相对旋转来致动和控制定位结构48,从而引起馈线22相对于鞘46的牵引。如图1所示,柄部H的左手部分设置有刻度标记,以向操作者指示相对于右手部分上的标记物(indicium)的旋转程度,刻度标记指示定位结构48的打开程度(例如5mm扩张)。柄部H还提供了相对较细的同轴馈线22(其延伸至导管远侧部分)和较粗的电馈线22’(其延伸至微波发生器)之间的互连,以及导管鞘46的内腔与流体管路54之间的流体互连。
在患者缆线52的近端处,流体管路54连接到流体控制系统56,该流体控制系统56提供通过鞘46的盐水灌注流,而患者缆线馈线22’连接到电源/控制单元60。流体控制系统56包括适当的泵、控制和流量测量装置,允许选择性地调节流体流量参数,并且还可以用于将其它流体(诸如药物和标记物)引入到流体流中,以便输送到导管设备的远端。电气单元60包括用于向天线34输送功率(power,动力)的可调谐微波产生源。电缆线58将设备10的其它电气部件(如下所述)连接到包括在电气单元60中的功率、监测和控制电路。可以理解,患者缆线52将来自柄部H的所有芯封(jacket,套)在一起,以便于实施该设备。
设备10还包括用于测量导管远侧部的温度的装置。
已知在医疗导管设备中包括一个或多个温度传感器,例如热电偶或热敏电阻。例如,为了使用热电偶进行温度监测,导管配备有由两种不同金属构成的热电偶导线对,所述热电偶导线对从近端延伸,穿过导管轴并进入远侧部分,其中导线对的热电偶热接点(温度测量点)位于该远侧部分。每个线的端部通常被剥离其覆盖绝缘层、被绞合、被焊接和被封装到远侧尖端电极中。然而,关于在微波消融设备中使用这种设备产生了特定的问题。
如从WO 2016/197206中可以理解的,微波加热是辐射的并且可以在没有天线-组织接触的情况下深入地穿透到组织中。导管的这种设计意味着辐射天线与周围环境电绝缘并且通过流动的灌注流体(盐水)的区域与周围环境隔开。这防止了欧姆加热导致的导管尖端的温度升高,并且减少了沿着导管柄的任何介电加热,从而能够使用更高的微波功率,而不会在导管内产生不希望或不可控的高温。在这点上,导管尖端的温度应被限制到最大约50℃左右,因为高于该温度的话会有形成凝结物、组织炭化和蒸汽爆裂的风险,这可能引起不良临床结果。因此,监测导管的远侧部分中的温度可能非常重要。另外,在微波肾动脉去神经过程中,在导管尖端附近的温度传感器可以使用热稀释法提供肾动脉血流速度的测量。这使得能够监测动脉通畅性(这是安全输送微波能量所必需的),并且如果患者具有较高的肾交感神经紧张度(由于先天生理或其他原因),则在成功进行肾去神经时会按期望发生肾微血管阻力的降低。
围绕微波天线的电隔离和流体的自然后果导致无法通过测量天线尖端的温度来近似计算局部组织温度。
如图2和图3所示,设备10使用热电偶来测量馈线22的外部传导屏蔽层28的端子部分处的温度。这是通过在该点108处电连接导线以形成热电偶热接点来实现的。导线由塞贝克系数(Seebeck coefficient,热电系数)不同于屏蔽层28的材料制成,使得在该接合点处的温度变化提供可用于确定温度的电流。特别地,使用T型铜-康铜材料,馈线屏蔽层28的编织导线被镀铜。已发现在消融过程期间遇到的温度范围内提供了约0.5℃的精度内的温度的测量。可以理解,对于导管来说最高温度的区域将位于该点108的远侧,更靠近天线34的纵向中心,然而,馈线屏蔽编织层28的远端38足够接近,以提供该最高温度的准确的相对测量值,如下面进一步讨论的。
重要的是,这种布置消除了为了提供热电偶而对第二导线(以及相关元件,如粘合剂)的需要。温度测量是对外部屏蔽材料本身进行的,靠近或位于编织层结束的点处,中心馈线芯从该点延伸。
特别地,通过从康铜导线的端部剥离绝缘物并将其焊接到屏蔽编织层28的短端部106(更详细地参见图4B中)来制造热接点,外鞘26已经从该短端部移除。在图3所示的变型中,导线100的端部在焊接之前缠绕在屏蔽编织层28的端子部分上,以形成在电气上和结构上都坚固、牢固的接头。
导线100沿着导管的长度延伸并经由柄部H中的适当的连接器连接到患者缆线52,并从那里通过电缆线58连接到电源/控制单元60,该电源/控制单元包括适当的电路和处理装置以根据测量的电压来计算温度。在图中,附图标记150表示引导鞘,导管设备10被引入穿过该引导鞘。
该热电偶系统提供了与导管天线相邻的监测加热的装置,特别是为了使用户能够避免消融期间温度过高,所述温度过高诸如可由过高的功率或导管灌注流的故障而引起。此外,监测温度提供了对天线处的微波辐射的测量。随着更高的电功率到达天线,或者当天线与其周围介质之间的频率匹配提高时,局部温度增加。因此,除了测量微波发生源处的反射功率以外,温度还提供了微波发射的独立测量。
作为示例,在测试本发明的设备时,通过施加80W微波功率(在发生器处测量到10W反射功率,这是选择较差匹配频率的结果),在有意的次优条件下执行消融过程。利用热电偶系统在点108处测量的温度为38℃。用相同正向功率的重复测试并选择最佳频率(将在发生器处测得的反射功率降低到零),测量到温度为44℃。
如上所述,在消融期间馈线编织点108处的温度与来自天线的微波发射相关。设备的测试还证明了由微波发生器检测到的反射功率与测量的温度之间的反比关系,从而提供了微波能量发射的附加独立测量。
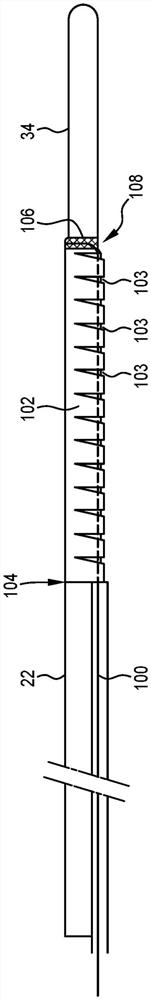
根据本发明的另一实施例,热电偶导线可用于提供温度监测和导管转向的双重功能。图4A和图4B中所示的细节图示了将热电偶导线100用作拉线,用于在插入期间使设备的远端弯曲并因此使其转向。
为此,微波馈线22的一部分设置有由相对不可压缩的材料制成的弯曲鞘102。弯曲鞘102从天线34的近端处的点108(在传导屏蔽层28的端子处)到其被锚固到馈线的外鞘26的点104包裹馈线,距离例如为30mm,其定义了导管所需弯曲部分的纵向长度。如下所述,弯曲鞘102的内径大于馈线鞘26的外径,以提供容纳热电偶导线100进行纵向移动的空间。
弯曲鞘102沿着其一侧的长度包括一系列规则间隔的柔性条纹103,柔性条纹可以是材料中的横向切口,或者可以沿着弯曲区段的长度包括插入的柔软且柔性的材料。在任一形式中,这些条纹允许弯曲鞘102仅在该侧容易地压缩(在相反侧保持对压缩的抵抗)。因此,这种布置提供了一种机构,该机构包括相对不可压缩的“脊部”以及在与脊部相反的方向上能够弯曲的可压缩的“肋部”的布置。
在馈线22的同一侧上,从点104起,相对不可压缩材料(为了防止在轴向方向上的压缩,但是通常能够在侧向方向上相对容易地偏转)的中空缆线101延伸到导管的近侧部分,通过封在馈线内而被固定到外部馈线鞘26,或者可替代地固定在外鞘46的内腔内。缆线101的内孔的尺寸被设计成容纳热电偶导线100,并且这种布置确保导线保持在导管的馈线芯附近。
如图4A所示,康铜导线100沿着缆线101的孔并且沿着弯曲鞘102的内部延伸,然后其端子部分缠绕在馈线屏蔽层28的导电编织层的远端106上(一次或多次),并且在点108处电连接(通过固定焊接)到其上,以产生热电偶热接点。在这一点,弯曲鞘102的远端被密封在该电接头之上,使得其两端均围绕馈线22固定(在点104和108处)。因此,导线100可自由地从该结点108自由地延伸到导管的近侧部分,在该近侧部分处导线100被布置用于由操作者进行接近和操纵。选择具有足够的拉伸强度的康铜导线以处理相对较大的张力,从而允许其可靠地将力传递到导管尖端。
因此,导线100提供拉线功能,如在偏转尖端导管的一般领域中已知的。当沿着方向A拉动导线100时,沿着该弯曲部分的导线长度110缩短,通过闭合或压缩条纹103而产生鞘102的弯折,并导致图4B所示的弯曲。在最大弯曲的构造112中,条纹103完全闭合或压缩。可以理解,可通过选择弯曲鞘102的条纹103的特定布置和尺寸来选择弯曲半径,从而根据特定应用来提供“急弯(tight curve,小半径曲线)”或“缓弯(wide curve,平缓曲线)”的导管。
当释放导线100时,导管的材料的自然弹性导致其恢复到原始的笔直构造。可以理解,导线总是沿着其长度保持平行于导管的轴向方向,从而使导线在任何点处疲劳的风险降至最低。
以这种方式,可以通过操纵热电偶导线100来使导管的尖端转向,从而将导管引导到期望的消融位置,而不需要在导管组件中包含单独的拉线。
提供导管的期望方向柔性的替代手段当然也是可行的,诸如使用线圈增强的外鞘和/或使用不锈钢条(或类似的相对不可压缩的材料)来提供弯曲部分的脊部,导管该部分的其余部分是根据需要能够压缩的弹性体材料,因此导管能够在与脊部的位置相反的方向上弯曲。
图5以图表方式示出了在110W试验消融过程(包括动脉注入和灌注失败)期间使用本发明的设备的测量的温度波动。这些结果证明,该设备提供了对导管远侧部分中的条件的可靠反馈测量。
该过程的参考点和阶段是:
A 肾血管造影;
B 通过注入室温造影剂产生的热稀释曲线;
C 导管灌注中断;
D 导致温度的急剧上升;
E 停止微波消融。
如上所述,如图5所示(阶段B),本发明提供的温度监测还可以帮助提供血流速度的测量。在微波肾动脉去神经期间,将室温流体从引导鞘注入到肾动脉中会导致导管温度的瞬时降低。随时间变化监测温度提供了有关传输时间(从引导鞘出口到热电偶位置)以及肾动脉血流的有用信息,并且可以与血压的测量一起用于估计肾微血管阻力。
图6提供了大型动物模型中的体内微波去神经过程的示例,并且特别地示出了在微波发生源在2400-2500MHz的调谐期间的温度变化,以便找到具有最大编织层(braid,屏蔽层)温度上升的频率(因此最小反射功率),从而优化组织联接。
该处理的参考点和阶段是:
A’初始基线(血液温度),约37℃;
B’导管灌注开始(30ml/m);
C’微波消融开始(110W,2400MHz),从该点施加的微波频率在10秒的时间自动增加到2500MHz;温度迅速上升;
D’峰值温度,其在2450MHz(与在发生器处测量的0W反射功率相关联)下实现;
E’最低测量温度,表明联接不良(与在发生器处测量的12W反射功率相关联);
F’在达到2500MHz时完成的调谐,此时消融在2450MHz的选定频率下继续。
微波加热具有辐射性,可以深入地穿透到组织,因此WO 2016/197206中所述类型的导管设备可以执行深周向消融(deep circumferential ablation),而很少对与流动血池相邻的组织造成损伤。
在微波肾脏去神经过程中,重要的是能够监测肾动脉口径。肾动脉口径的减小会增加热动脉损伤的风险,这是因为动脉壁会更接近微波天线,因此会受到更迅速的加热,而血管收缩会引起动脉血流量减少,从而降低冷却速率。另一方面,肾动脉扩张可以提供成功的肾神经消融的证明并提供生理终点以确保有效的治疗传递。
发明人已经确定,监测微波消融导管设备10周围的血池的阻抗可以提供对血管口径的测量。尽管阻抗监测在心血管过程中是已知的,但是这通常用于当组织加热时测量组织阻抗的变化。
如图7所示,设备10的实施例包括两个电极204、206,这两个电极分别位于导管外鞘46的外侧和内侧,在导管辐射器部分的近侧的大致相同的轴向位置处。在第一形式中,这些电极被设置为导线200和202的剥离端,其从近端起延伸导管的长度。
导线200和202经由柄部H中的适当连接器连接到患者缆线52,并从那里通过电缆线58连接到电源/控制单元60,该电源/控制单元包括适当的电路和处理装置来测量、记录和显示电极204和206之间的阻抗。
一旦对导线200和202施加交变电势(其中导管在血池内且盐水灌注流体填充导管远侧部分),就从电极206开始、沿着围绕馈线22和辐射器24的流体体积中的导管的内部、穿过六个狭缝孔50中的一个或多个、以及沿着血液中的导管的外部返回到电极204而形成离子导电路径210。因此,测量电流可提供电极204和206之间的阻抗(即,电路径所通过的血液体积和盐水体积的阻抗)的测量,并且该阻抗的变化可以提供血管口径的变化的表示。可以理解,当动脉12在去神经过程期间扩张时,导管内部的电路的部分的电特性基本上不改变,但是导管外部的电路的部分的较低电阻路径对整体阻抗具有显著影响。
因此,外部电极204必须位于血流中,图8和图9提供了实现电极的适当替代方式的细节。在这些图中,附图标记S表示导线200和202的端子部分的起点,其绝缘层被移除。
在图8中,导线202沿着导管在导管鞘46与馈线鞘26之间的空间中延伸,其剥离的端部202’向其自身回弯180°,然后其尖端电连接并固定到围绕馈线鞘26的环形电极206。导线200类似地沿着导管在导管鞘46和馈线鞘26之间的空间中延伸,其剥离的端部200’穿过鞘46中的穿孔,向其自身回弯,然后其尖端电连接并固定到围绕导管鞘46的外部环形电极204,使得这两个环形电极在距馈线编织层28的端部(天线34的近端)约10-15mm的位置处纵向重合。使用适当的粘合剂来密封穿孔。
在替代形式中,可以以独立于设备10的方式提供外部电极204。例如,其可设置在引导鞘150的远端处或附近(例如,与不透射线环通常所处的位置相邻),或者其可作为参考患者返回电极设置在适当位置处。通常,这样的解决方案不是优选的方法,因为它们需要使用单独的电连接引线来连接到电源/控制单元60的阻抗测量电路。然而,这样的布置可以具有减小和简化设备10的部件部分的优点,从而使导管鞘46的口径最小化。
可以理解,为了确保任何金属部件都位于微波场之外并避免对场应用和阻抗电路两者的干扰,在导管的辐射器部分之前使导线200和202终止是很重要的(否则会导致干扰)。此外,环形电极204和206优选地不是完整的传导环,即优选是C形的而不是O形的,以避免闭合电路径,从而潜在地使它们成为微波场中的寄生电感器,这可能导致不需要的加热。
图9中的替代电极布置包括内部电极206,作为导线202的端子部分202’,向自身回弯180°,其尖端通过热缩部220简单地围绕馈线鞘26固定。导线200穿过鞘46中的穿孔,并且外部电极204包括剥离导线端部200’的环201,围绕导管鞘46的外部穿过,并通过热缩部或粘合剂固定到其上。在图8和图9中示出的两个变型中,电极204的回路形式确保了与血池的电接触,并且回路不会电连接回到其自身(图9中所示的返回点在剥离绝缘物的起点附近),以避免闭合环路周围的电路径和微波场感应加热的相关风险,如上文参考图8的实施例所讨论的。
在沿着馈线鞘26的外部的其路线过程中,导线200、202可以通过胶接点或热缩带固定到其上。
在本发明的另一实施例中,发明人开发和测试了导管10的替代形式,其中在制造时导线200、202被集成在导管鞘46的壁材料内,因此完全与鞘的内部或外部电绝缘。在该方案中,电极204和206形成为不完整的环形结构(是与图8中所示的实施例中的那些类似的形式),一个(通过熔融嵌入)集成在导管鞘壁的外表面中,一个集成在内表面中。类似于导线,这些电极在制造鞘46时形成,以分别呈现与鞘壁的对应表面齐平的外表面和内表面,以防止任何不期望的表面不连续性。
在导管鞘46上设置两个电极的一个优点是,不管馈线在其内的任何相对移动如何,确保介入距离在功能上恒定,从而避免任何相关联的测量伪像。
发明人在动物试验中测试了在去神经导管中使用阻抗电路来监测血管扩张的概念,阻抗随时间变化的图表输出如图11所示。
该过程的参考点和阶段是:
A”基线(与呼吸和腹内压的变化相对应的动脉大小的波动);
B”消融开始;
C”血管造影1(图10A);
D”球囊闭塞;
E”血管造影(图10B)。
阻抗下降由对流体的微波辐射的加热效应引起,但是由于室温盐水的冷却效应,阻抗随着灌注速率的增加而增加。从阶段A”结束时微波消融开始,由于微波辐射器周围的盐水的加温,阻抗下降约30秒。
在约72秒时,冷造影介质的注入引起测量的阻抗急剧瞬变到点C”,在此取得第一血管造影。图10示出了辐射器24、导管尖端42和电极204、206在肾动脉12中的位置。
此时,肾上降主动脉的球囊闭塞(图10B中所示的球囊闭塞设备210)导致血压下降,并因此导致肾动脉12的轻度收缩。该血管收缩在该过程的阶段D”期间清楚地转化为阻抗的上升。
第二血管造影与图11中的点E”对应,也显示了收缩的动脉12。
在该实施例中,观察到大约250欧姆的阻抗变化,血管口径从大约6mm减小到5mm。
本实验清楚地证明了阻抗监测作为血管口径的测量的价值,因此也证明了在血管去神经治疗中作为反馈机构的价值。
除了提供上述过程中的点和阶段的指示之外,本发明还可以提供(一个或多个)定位结构48的部署的指示,前提是流体路径横穿结构的位置。一旦部署了定位结构,则任何观察到的阻抗变化应当仅由于血管口径变化而引起。但是在部署期间,阻抗对定位结构的扩张是敏感的,因此本发明可以用于确认成功的部署。
可以理解,本说明书中公开和限定的本发明延伸到从文本或附图提及或显而易见的单个特征中的两个或更多个的所有替代组合。所有这些不同的组合构成本发明的各种替代方案。
如本文所使用的,除非上下文另有要求,否则术语“包括”和该术语的变型(诸如“包含(comprising)”、“含有(comprises)”和“具有(comprised)”)不旨在排除进一步的添加物、部件、整体或步骤。
- 具有温度监测的导管消融设备
- 用于在心脏消融过程中监测组织温度的光学高温测量导管
