用于预防或治疗肥胖或非酒精性脂肪性肝炎的包含氢醌衍生物的药物组合物
文献发布时间:2023-06-19 11:21:00
技术领域
本发明涉及用于预防或治疗肥胖或非酒精性脂肪性肝炎的包含氢醌(hydroquinone)衍生物的药物组合物。
背景技术
肥胖是指,由于能量的摄入和消耗的不平衡,脂肪在体内过度积聚,而导致脂肪组织异常增加的状态。肥胖分为:没有特定病因的因摄取过度热量和缺乏运动而导致的单纯性肥胖;以及由遗传因素、内分泌疾病、下丘脑食欲调节中枢异常以及药物副作用而继发的症状性肥胖。在所有肥胖患者中,单纯性肥胖约占95%。
与肥胖自身的风险相比,因肥胖可能引起的各种并发症,其严重性被进一步认识。众所周知,肥胖会增加发生如高血压、高脂血症、糖尿病等的代谢综合征、脂肪肝、关节异常以及癌症的风险。
目前,市售中的代表性的肥胖治疗剂包括以奥利司他(Orlistat)为主原料的罗氏鲜(Xenical)
最近,由于肥胖人口的增加而导致的代谢综合征患病率增加,非酒精性脂肪肝病的患病率也随之增加。据报道,脂肪肝是由如上所述的肥胖的并发症引起,或者也可由其他多种原因引起,例如,酒精、糖尿病、营养不良、药物滥用等,其被定义为在组织检查中脂肪沉积在5%以上的肝细胞上的情况。尤其,将在没有显著的酒精摄取、没有导致脂肪肝的药物的服用、没有伴随其他原因的肝疾病等的情况下,在影像检查或组织检查中显示出肝内脂肪沉积迹象的疾病称为“非酒精性脂肪肝病(non-alcoholic fatty liver disease,NAFLD)”,其包括单纯性脂肪肝(simple steatosis)以及非酒精性脂肪性肝炎(nonalcoholic steatohepatitis,NASH)。单纯性脂肪肝的预后相对较好,而非酒精性脂肪性肝炎是一种可致命的疾病,具体地,其在10~20%的非酒精性脂肪性肝病(NAFLD)患者中发病的疾病,表现出肝内脂肪沉积以及伴随肝细胞损伤的炎症,9~25%的患者进展为肝硬化,而其中的30~40%死于肝病的并发症。
非酒精性脂肪性肝炎与肥胖、胰岛素抗性等代谢综合征密切相关,但未报导病理机制和治疗方法。非酒精性脂肪性肝炎的诊断主要通过组织病理学检查来进行,诊断为非酒精性脂肪性肝炎的最低限度的必要的发现包括脂肪症、肝细胞的气球样变性、肝小叶炎症。为了有效治疗这种非酒精性脂肪性肝炎,重要的是通过抑制非酒精性脂肪肝进展到脂肪肝炎的同时改善脂肪肝炎,从而抑制进展到下一阶段。进而,通过运动疗法或药物治疗来减少与非酒精性脂肪性肝炎相关的胰岛素抗性和内脏脂肪蓄积等是治疗中非常重要的管理项目。
随着因非酒精性脂肪性肝炎导致的社会性费用增加,许多研究人员已尝试开发治疗剂,但目前为止,尚没有已证明对非酒精性脂肪肝病的临床效果的药物治疗,尤其尚未开发出可以防止非酒精性脂肪性肝炎的发生或进展的治疗药。全世界尚无获批的非酒精性脂肪性肝炎治疗剂,仅存在考虑到对患者的安全性和有效性而作为第二方案的标签外(off-label)药物。虽然胰岛素抗性改善剂(例如,PPARs(Peroxisome proliferator-activatedreceptors)激动剂(agonists))或法尼酯X受体激动剂(Farnesoid X Receptor(FXR)agonist)等正在临床开发中,但尚无证明有治疗效果的药物,而且还存在引起血脂异常等的副作用的药物。另外,由于非酒精性脂肪性肝炎涉及各种病理生理,因而在许多情况下,仅靠一般的抗氧化、抗炎效果是无法在实际动物实验、临床试验中显示充分的治疗效果。
已证实,现有的特定氢醌衍生物在四氯化碳(CCl4)诱导的肝硬化模型中表现出对肝纤维化的抑制作用,在对乙酰氨基酚及α-萘异硫氰酸酯(ANIT)诱导的急性肝损伤模型中显示出肝功能改善效果(日本公开专利第1996-67627号及韩国授权专利第10-1042697号)。然而,上述任意现有文献中没有指出其记载的氢醌衍生物对肥胖、非酒精性脂肪肝或非酒精性脂肪性肝炎是否具有直接效果。
本发明人发现所述氢醌衍生物对如肥胖、内脏脂肪蓄积、或胰岛素抗性等的非酒精性脂肪性肝炎的危险因素具有改善效果,还发现组织病理学上对肝组织内脂肪的蓄积及肝小叶炎症的改善起到综合性作用,从而对非酒精性脂肪性肝炎的预防或治疗也具有效果,从而完成了本发明。
发明内容
发明要解决的问题
本发明的目的在于,提供用于预防或治疗肥胖或非酒精性脂肪性肝炎的包含氢醌衍生物的药物组合物。
用于解决问题的手段
本发明涉及用于预防或治疗肥胖或非酒精性脂肪性肝炎的、包含式1的氢醌衍生物作为有效成分的药物组合物。
式1
所述R
在所述药物组合物中,优选地,式1的氢醌衍生物为2,3,5-三甲基氢醌-1-己醚(2,3,5-trimethyl hydroquinone-1-hexylether)(化合物1)或2,3,5-三甲基氢醌-1-己醚-4-乙酸酯(2,3,5-trimethyl hydroquinone-1-hexylether-4-acetate)(化合物2)。
在所述药物组合物中,优选地,非酒精性脂肪性肝炎为肥胖型非酒精性脂肪性肝炎(obese NASH)。
根据本发明的另一方面,涉及用于预防或改善肥胖或非酒精性脂肪性肝炎的包含所述式1的氢醌衍生物作为有效成分的食品组合物。
在所述食品组合物中,优选地,式1的氢醌衍生物为2,3,5-三甲基氢醌-1-己醚(化合物1)或2,3,5-三甲基氢醌-1-己醚-4-乙酸酯(化合物2)。
在所述食品组合物中,优选地,非酒精性脂肪性肝炎为肥胖型非酒精性脂肪性肝炎。
以下,更详细说明本发明。
本发明涉及用于预防或治疗肥胖或非酒精性脂肪性肝炎的、包含式1的氢醌衍生物作为有效成分的药物组合物。
式1
所述R
由所述R
另外,R
在所述药物组合物中,优选地,式1的氢醌衍生物为2,3,5-三甲基氢醌-1-己醚或2,3,5-三甲基氢醌-1-己醚-4-乙酸酯。
根据本发明,具有通过抑制体重增加或内脏脂肪蓄积来预防、改善或治疗肥胖的效果。
另外,尤其是,根据本发明不仅能抑制肝组织内脂肪的蓄积及肝小叶炎症,还通过改善胰岛素抗性来获得预防、改善或治疗非酒精性脂肪性肝炎的效果。本发明可适用于表现出非酒精性脂肪性肝炎的组织病理学特征,即脂肪症、肝细胞的气球样变性及肝小叶内炎症等的所有非酒精性脂肪性肝炎的治疗,优选地,可适用于肥胖型非酒精性脂肪性肝炎的治疗。
已证实,所述式1的氢醌衍生物是安全性极高的化合物。尤其,2,3,5-三甲基氢醌-1-己醚在临床试验中,对每个成人单次最多给药2000mg也不会引起异常反应。并且,在反复给药14天的情况下,即使对每个成人单日给药1000mg也不会引起异常反应,即其被证实为是一种安全性极高的化合物。因此,本发明的组合物具有可以有效地用于治疗慢性且需要长期治疗的肥胖或非酒精性脂肪性肝炎的优点。
本发明的药物组合物可以口服给药或肠胃外给药,优选适用口服给药方式。
本发明的药物组合物的合适剂量可以根据制剂化方法、给药方式、患者的年龄、体重、性别、病情、饮食状况、给药时间、给药途径、排泄速率及反应敏感性等因素,以多种方式给药。通常,作为上述氢醌衍生物,每日肠胃外剂量为约0.01~100mg/kg体重,优选为约0.05~50mg/kg体重。另外,作为上述氢醌衍生物,本发明的组合物的每日口服剂量为约0.1~500mg/kg体重,优选为约0.5~200mg/kg体重,可将其分成1~3次给药。
本发明的药物组合物可以通过常规使用的方法制备成各种形式。在此情况下,可利用常规制剂用载体或赋形剂等允许作为医药品添加剂的添加剂来制剂化。另外,为了提高本化合物的生物利用率或稳定性,可以使用药物递送系统,其包括微胶囊、微粉化、使用环糊精的包合化等的制剂技术。
在将所述组合物用作口服给药制剂的情况下,可以以片剂、颗粒剂、胶囊剂或口服液等的形式使用,但优选以适合在消化道吸收的形态使用。另外,基于运输性、储存性等原因以所期望的形态提供制剂的情况下,也可以使用现有的制剂技术。另外,在用作肠胃外给药制剂的情况下,可以以注射剂、栓剂、贴片(tape)和巴布剂(湿布剂)等的透皮吸收剂等形态使用,在基于运输性、储存性等原因以固体制剂的形态使用的情况下,还可以以适当的溶剂溶解使用,也可以通过现有制剂技术以液体剂及半固体剂的形态提供。
根据本发明的另一方面,本发明涉及包含式1的氢醌衍生物作为有效成分的食品组合物。
本发明的食品组合物可以以如片剂、胶囊、颗粒剂、糖浆等的补充物形式、如饮料、饼干、面包、粥、谷物、面类、果冻、汤、乳制品、调味料、食用油等的所有形态使用。另外,当用作食品组合物时,在不影响本发明的有效成分的效果的范围内,也可以以各种组合方式组合其他有效成分或维生素、矿物质或氨基酸等的营养素等。基于本发明的食品组合物开发出的食品包括补充物、健康食品、功能食品、特定保健食品等。另外,本发明的食品组合物中氢醌衍生物的摄取量优选为约0.1~500mg/kg体重,更优选为约0.5~200mg/kg体重,且优选分成1~3次摄取。
发明的效果
本发明的组合物作为包含式1的氢醌衍生物作为有效成分的药物组合物,具有抑制内脏脂肪蓄积并预防、改善或治疗肥胖的效果。
另外,本发明的组合物尤其具有抑制肝组织内脂肪的蓄积且治疗肝小叶炎症的效果,还具有通过改善胰岛素抗性来预防、改善或治疗非酒精性脂肪肝或非酒精性脂肪性肝炎的效果。
附图说明
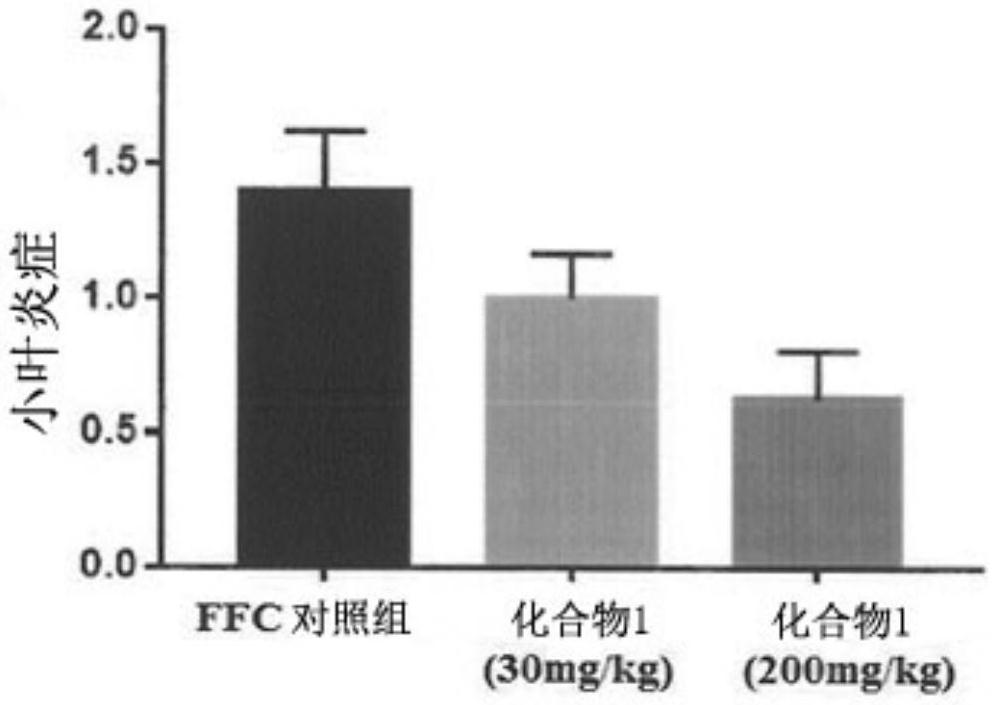
图1是示出对高脂/高果糖/高胆固醇饮食(Fat,fructose-and cholesterol-richdiet,FFC)喂养模型中的肝小叶炎症的本发明的化合物1的作用的图。
图2是示出对FFC饮食喂养模型中的脂肪肝的化合物1的作用的图。
图3是对FFC饮食喂养模型中的非酒精性脂肪肝病活性指数的化合物1的作用的图。
图4是示出对蛋氨酸/胆碱缺乏饮食(Methionine and choline deficient diet,MCD)喂养8周的模型中的肝小叶炎症的化合物1的作用的图。
图5是示出对MCD饮食喂养8周的模型中的非酒精性脂肪肝病活性指数的化合物1的作用的图。
图6是示出对MCD饮食喂养8周的模型中的谷丙转氨酶(ALT)数值的化合物1的作用的图。
图7是示出对MCD饮食喂养12周的模型中的肝小叶炎症的化合物1的作用的图。
图8是示出对MCD饮食喂养12周的模型中的非酒精性脂肪肝病活性指数的化合物1的作用的图。
图9是示出对高脂饮食(High fat diet)喂养模型中的动物体重的化合物1的作用的图。
图10是对高脂饮食喂养模型中的饮食摄取量的化合物1的作用的图。
图11是对高脂饮食喂养模型中的附睾脂肪重量的化合物1的作用的图。
图12是示出13周重复进行毒性试验时的基于化合物1的各种日剂量的体重变化的图。
图13是示出胰岛素抗性检查时血糖随着时间的变化的图。
图14是将胰岛素抗性检查结果数值化为胰岛素曲线下面积(iAUC)值来示出基于化合物1处理的胰岛素感受性增加的图。
图15是示出对高脂饮食喂养模型中的肝小叶炎症的化合物1的作用的图。
图16是示出对高脂饮食喂养模型中的非酒精性脂肪肝病活性指数的化合物1的作用的图。
图17是示出对高脂饮食喂养模型中的ALT数值的化合物1的作用的图。
图18是示出对高脂饮食喂养模型中的谷草转氨酶(AST)数值的化合物1的作用的图。
图19是示出对高脂饮食喂养模型中的血液胆固醇数值(A)及血液中性脂肪(TG)数值的化合物1的作用的图。
具体实施方式
以下,详细说明本发明的优选实施例。但是,本发明不限于在这里说明的实施例,可以以其他形式实施。而且,其用于使在这里说明内容更彻底且完整的理解,并将本发明的思想充分地传递给本领域技术人员。
给6~7周龄雄性C57BL/6小鼠喂食FFC饮食(高脂、高果糖、高胆固醇饮食)(RESEARCH DIETS,Product No.:D12079B)16周,以诱导非酒精性脂肪肝后,进行活检,仅分离出非酒精性脂肪肝活性指数(NAS score)为3.2以上的动物。活检2周后,以仅给药0.5%甲基纤维素(Methyl cellulose,MC)水溶液的阴性对照组(FFC control)、溶解在0.5%MC水溶液的化合物1(2,3,5-三甲基氢醌-1-己醚化合物各30mg/kg及200mg/kg给药组)给药组的方式分为三个试验组。化合物1总共给药2个月,通过组织病理学检查评价了对非酒精性脂肪性肝炎的改善效果。
为了组织病理学检查,处死小鼠,分离肝组织,并制作了苏木精-伊红(Hematoxylin-Eosin,H&E)染色载玻片。即将分离的肝组织在4℃下,用4%多聚甲醛(paraformaldehyde)固定24小时后,用流水洗涤,用石蜡包埋,并将组织切成3~4μm的厚度。将切下的组织附着在涂覆载玻片上后,用二甲苯(xylene)去除石蜡,按照顺序使用乙醇(99%、95%、90%、80%及70%的乙醇(EtOH))经过水合过程后,进行组织学染色。将切下的组织用苏木精染色液染色5分钟后,用流水洗涤5分钟,用1%盐酸乙醇及氨脱色。之后,用流水洗涤10分钟后,再用伊红染色液复染1分钟,向水合过程的方向相反的方向进行脱水后密封。
将H&E染色的载玻片置于显微镜下,进行组织病理学评价,根据表1的基准,对非酒精性脂肪肝病活性指数(NAFLD activity score:NAS)进行数值化并进行记录。非酒精性脂肪肝病活性指数是通过合算对1)脂肪变性(steatosis)、2)肝小叶内炎症等病变(lobularinflammation)、3)肝细胞的气球样变性(bal looning)的变化的评价分数来计算出的,并广泛用于评价非酒精性脂肪性肝炎的严重程度。
表1
如图1所示,与仅给药0.5%MC(Methyl cellulose)水溶液作为赋形剂的阴性对照组(FFC control)相比,化合物1给药组减少了肝小叶炎性细胞浸润,从而证实了具有优异的炎症改善效果。另外,化合物1给药组表现出浓度依赖性的脂肪肝改善效果(图2),并证实了能够降低非酒精性脂肪肝病活性指数(图3)。
因此,证实了本发明在预防或治疗非酒精性脂肪性肝炎方面具有优异的效果。
MCD饮食(缺乏蛋氨酸和胆碱的饮食,Methionine and choline deficient diet)模型为通过供应没有对起到β氧化和VLDL(Very low-density lipoprotein,极低密度脂蛋白)合成起到重要作用的蛋氨酸和胆碱的饮食来诱导脂肪肝的试验模型,由于其在组织病理学中严重引起肝小叶内炎症,因而广泛用于观察非酒精性脂肪性肝炎的改善效果。
给7周龄的雄性C57BL/6小鼠喂食MCD饮食(RESEARCH DIETS,Prod uct No:A02082002B)4周,以诱导非酒精性脂肪肝,之后再喂养MCD饮食4周,同时以如下表2的G3~G8试验组组成所示,将相当于本发明的氢醌衍生物化合物的2,3,5-三甲基氢醌-1-己醚(化合物1)以及作为比较对照组的其他药物以特定剂量向小鼠重复口服给药4周,并通过临床病理学检查及组织病理学检查来评价了对非酒精性脂肪性肝炎的改善效果。
表2
正常对照组是用正常饮食(RESEARCH DIETS,Product No:A02082003B)喂养,而不是MCD饮食,阴性对照组是用MCD饮食喂养后,仅用作为赋形剂的0.5%MC(Methylcellulose)水溶液进行给药。作为比较对照组,如表2所示,使用作为FXR激动剂的奥贝胆酸(Obeticholic acid,OCA)、作为PPARγ激动剂的吡格列酮(Pioglitazone,PGZ)、作为抗氧化剂的白藜芦醇(Resveratrol,RSV)以及联苯二甲酸二甲酯(Biphenyl DimethylDicarboxylate,DDB)系列肝功能保护剂(DDB复合体,DDB complex),进行了效果对比实验。白藜芦醇及DDB系列肝功能保护剂的给药剂量设定为200mg/kg。奥贝胆酸及吡格列酮的每日给药剂量如表2所示,分别设定为30mg/kg/天及10mg/天,该剂量是参照通过美国食品和药物管理局(FDA)及欧洲药品管理局(EMA)提出的批准资料报告的毒性剂量和论文等报告的有效剂量及副作用剂量来设定的。
据报道,利用CD-1(ICR)小鼠进行7天反复给药毒性试验(3、50、175、300mg/kg的浓度)时,在175mg/kg的浓度,奥贝胆酸可产生动物死亡等的严重的副作用(FDA obeticholicacid(INT-747)NDA package pharmacology revi ews;Application number:207999Orig1s000)。另外,据报道,在对西方饮食(western diet)NASH小鼠模型进行效果试验时,在40mg/kg以上的剂量中反而使非酒精性脂肪肝病的进程恶化(使肝纤维化严重、ALT数值上升)(Front Phar macol.2018 May 1;9:410)。因此,将试验剂量设定为在许多小鼠非酒精性脂肪肝研究论文中使用的20~30mg/kg剂量范围中的最高剂量30mg/kg。
据报道,在对小鼠进行13周反复毒性试验时,吡格列酮在320mg/kg以上的剂量发生个体死亡,在100mg/kg以上产生心脏副作用(FDA Pioglitazone(ACTOS)NDA packagepharmacology reviews:021073)。另外,虽然有研究论文报道了对小鼠非酒精性脂肪肝的效果剂量范围为10~30mg/kg,然而还参照吡格列酮在25mg/kg的剂量下反而会使脂肪肝恶化的研究结果(Int.J.Mol.Sci.2015,16,12213-12229,PPAR Res.2014:38183),将试验剂量设定为作为最常报道剂量的10mg/kg。
将MCD饮食喂养时间延长至共12周,以提高非酒精性脂肪性肝炎的诱导水平。为此,给7周龄的雄性C57BL/6小鼠喂食缺乏蛋氨酸-胆碱的饮食8周,以诱导非酒精性脂肪肝后,用与表2相同的试验组以相同的剂量反复口服给药4周。
与试验例1的组织病理学检查方法相同,从进行MCD饮食8周喂养试验的小鼠分离肝组织,制作H&E染色载玻片后,基于表1的基准,分析对1)脂肪变性(steatosis)、2)肝小叶内炎症等病变(lobular inflammation)、3)肝细胞的气球样变性(ballooning)的变化并合算评价分数,以计算出非酒精性脂肪肝病活性指数,由此评价了非酒精性脂肪性肝炎的治疗效果。
小鼠肝组织的组织病理学肝小叶炎症、以及非酒精性脂肪肝病活性指数如图4及图5所示,作为代表性肝功能临床病理数值的ALT数值如图6所示。
如图4所示的肝小叶的炎症细胞浸润指数是非酒精性脂肪性肝炎的组织病理学评价中最重要的指数之一。另外,由于非酒精性脂肪性肝炎的药物治疗的最大目的是防止从脂肪肝发展为脂肪肝炎或从脂肪肝炎发展为肝硬化等的下一阶段,病理组织学肝小叶炎症的改善是非常重要的效果改善指标。
在本发明的化合物1给药组的情况下,与阴性对照组(MCD control)相比,肝小叶炎性细胞浸润的改善效果显著(图4)。尤其,与现在在临床中作为非酒精性脂肪性肝炎的一次治疗剂使用的胰岛素抗性改善药物的吡格列酮(Pioglitaz one,PGZ)相比,显示出优异的抗炎效果,与目前临床3期开发中的奥贝胆酸(Obeticholic acid,OCA)相比,也显示出优异的抗炎效果。
另外,已证实本发明的化合物1的非酒精性脂肪肝病活性指数降低(图5),并且观察到,与阴性对照组及比较对照组相比,在化合物1的200mg/kg给药组中,作为临床病理学肝功能指标的ALT数值显著降低(图6)。
另一方面,就已知具有抗氧化、抗炎效果的白藜芦醇(RSV)及DDB系列肝功能保护剂(DDB compelx)而言,与阴性对照组相比,不显示出非酒精性脂肪性肝炎的改善效果,这意味着仅靠一般抗氧化、抗炎效果对具有复杂的病理机制的非酒精性脂肪性肝炎没有抑制效果。据此,与现有将非酒精性脂肪性肝炎作为适应症开发的各种作用机制的药物组相比,证实了本发明的化合物1显示出优异的非酒精性脂肪性肝炎的抑制效果。
对于MCD饮食12周喂养试验的小鼠肝组织的肝小叶炎性细胞浸润的改善效果、及非酒精性脂肪肝病活性指数示于图7及图8。
如图7及图8所示,就化合物1给药组而言,与阴性对照组(MCD control)相比,显示出对肝小叶炎性细胞浸润的改善效果,且使得非酒精性脂肪肝病活性指数降低,这种效果以化合物1的浓度依赖性地方式增加。尤其,现在临床中,与用作非酒精性脂肪性肝炎的一次治疗剂的胰岛素抗性改善药物的吡格列酮(PGZ)相比,显示出优异的抗炎效果,与目前临床3期开发中的奥贝胆酸(Obeticholic acid,OCA)相比,也显示出优异的抗炎效果。
在本试验例中,就已知具有抗氧化、抗炎效果的白藜芦醇(RSV)及DDB系列肝功能保护剂(DDB compelx)而言,与阴性对照组相比,也未显示出非酒精性脂肪性肝炎的改善效果,这意味着仅靠一般抗氧化、抗炎效果对具有复杂的病理机制的非酒精性脂肪性肝炎无法实现充分的抑制效果。
给7周龄雄性C57BL/6小鼠喂食60kcal%高脂饮食(RESEARCH DIETS,Product No:D12492)16周,以诱导非酒精性脂肪肝,高脂饮食的第17周至第25周,利用试验物质反复口服给药9周,通过临床病理学检查及组织病理学检查评价了对非酒精性脂肪性肝炎的改善效果。
作为试验组设定了喂养正常饮食(10kcal%脂肪饮食,RESEARCH DIETS,ProductNo:D12450B)而并非是HFD饮食的正常对照组、喂养HFD饮食后仅给药作为赋形剂的0.5%MC(Methyl cellulose)水溶液的阴性对照组、以及化合物1(2,3,5-三甲基氢醌-1-己醚)给药组(30、100、200mg/kg)、比较对照组(30mg/kg的奥贝胆酸、10mg/kg的吡格列酮、200mg/kg的DDB系列肝功能保护剂)。
与所述(1)的试验方法相同,利用试验物质反复口服给药9周,并观察、记录了9周的体重增加量、饮食摄取量及一般症状。
如图9所示,就化合物1给药组而言,与阴性对照组(HFD control)相比,由于喂养高脂饮食而导致的体重增加率显著降低。尤其,就化合物1给药组而言,饮食摄取量与其他给药组没有差异(图10),由此可知化合物1给药组中的体重减少效果不是由于饮食摄取量的减少而导致的。
另外,如图11所示,在对小鼠的尸体进行剖检时测定附睾脂肪重量的结果,化合物1具有优异的抑制附睾脂肪等的内脏脂肪蓄积的效果。据报道,就这种如附睾脂肪等的内脏脂肪而言,由于比皮下脂肪动员起来更快,通过肝门静脉直接流入肝,因此与非酒精性脂肪性肝炎的进展及预后密切相关。
像这样,由于化合物1具有非常优异的体重及内脏脂肪量减少效果,因而证实了其对肥胖的预防、改善或治疗有效果。
进而,就化合物1给药组而言,以在正常动物中也产生副作用的代谢途径作为目标(target)的药物不同,大鼠单次口服毒性试验时,2000mg/kg的高剂量给药也没产生死亡个体。另外,在500mg/kg的高浓度下,也没有产生死亡、器官衰竭等的严重的副作用,体重(图12)及饮食摄取量、尿检及血液学检查中也没有出现因给药化合物1而产生的变化。
在化合物1的化合物给药第7周进行了胰岛素抗性检查,观察了化合物1对因高脂饮食而导致胰岛素抗性增加所产生的影响。
通过对禁食4小时的小鼠覆膜内给药胰岛素(0.7IU/kg),并以30分钟的间隔测定血糖来执行了胰岛素抗性检查。另外,为了将胰岛素抗性数值化,将胰岛素给药前的血糖为基线值(baseline),将减少的血糖数值曲线面积数值化为iAUC值,以定量比较胰岛素抗性(图14)。其中,iAUC值越小,胰岛素抗性越高,iAUC值越大,胰岛素感受性越大。
如图13所示,通过胰岛素抗性检测结果可确认,就化合物1给药组而言,与阴性对照组及其他药物对照组相比,给药胰岛素时,血糖降低的更快。即就阴性对照组而言,由于末梢组织的胰岛素抗性增加,血糖缓慢降低,但是观察到在给药化合物1时,因对胰岛素的感受性增加,血糖降低地更快。如图14所示,在将其数值化为iAUC值并进行比较的情况下,可以确认与阴性对照组及其他药物对照组相比,对因高脂饮食而产生的胰岛素抗性的抑制效果大。
与试验例1的组织病理学检查方法相同,从高脂饮食喂养试验的小鼠分离肝组织,制作H&E染色载玻片后,基于表1的基准,分析对1)脂肪变性(ste atosis)、2)肝小叶内炎症等病变(lobular inflammation)、3)肝细胞的气球样变性(ballooning)的变化并合算评价分数,以计算出非酒精性脂肪肝病活性指数,由此评价了非酒精性脂肪性肝炎的治疗效果。
如图15及图16所示,在组织病理学评价中,也证实了化合物1显示出优于其他药物的非酒精性脂肪性肝炎的治疗效果。如图15及图16所示,观察到就化合物1给药组而言,与阴性对照组(HFD control)相比,显示出对肝小叶炎性细胞浸润及脂肪肝的改善效果,改善效果以化合物1处理浓度依赖性地方式增加。另外,就200mg/kg的化合物1给药组而言,显示出明显高于其他对照药物的肝小叶炎症抑制效果。
在临床病理学评价中,证实了因化合物1的给药,作为肝功能及肝损伤指标的ALT及AST数值恢复至正常水平。尤其,ALT、AST数值比其他药物对照组降低了更多(图17及图18)。
进一步地,证实了使脂肪肝及脂肪肝炎恶化的血液中胆固醇及中性脂肪数值比阴性对照组降低(图19的(A)部分及图19的(B)部分)。就奥贝胆酸而言,在本动物实验中显示出了高胆固醇抑制作用,然而,已知在临床试验时,即使在低浓度(每个成人10~25mg)下,在正常人和非酒精性脂肪肝患者中也会发生总胆固醇及低密度脂蛋白(LDL)胆固醇升高的副作用(Diabetes,Obes ity and Metabolism 18:936-940,2016)。相反,本发明的化合物1在临床1期试验时,即使以每个成人1000mg的剂量反复给药14天,也没有报告血脂异常症等的异常反应。
通过所述高脂饮食喂养动物模型试验,证实了本发明的化合物1具有优异的减少体重增加及内脏脂肪量的蓄积的效果,因此可用作肥胖的预防、改善或治疗剂。
另外,与已开发的非酒精性脂肪性肝炎治疗剂相比,本发明的化合物1具有优异的体重及内脏脂肪蓄积抑制、胰岛素感受性增加、以及肝组织炎症抑制效果,因此对复杂且多样的因子起作用的非酒精性脂肪性肝炎的治疗非常有效。
不仅如此,证实了本发明的化合物1在大鼠中的半数致死剂量超过2000mg/kg,在比格犬中的最大耐受剂量为2000mg/kg以上,是非常安全的化合物,在使用大鼠的反复给药13周的毒性试验中,即使在500mg/kg的高浓度下,也没有发生死亡、体重减少、器官衰竭等副作用。并且,通过临床1期试验,即使以每个成人2000mg的方式单次给药、以每个成人1000mg的剂量反复给药14天也没有报告异常反应,因此所述化合物为安全性高的化合物,其可以有效地用作需要长期治疗的非酒精性脂肪性肝炎治疗剂。
- 用于预防或治疗肥胖或非酒精性脂肪性肝炎的包含氢醌衍生物的药物组合物
- 用于预防或治疗非酒精性脂肪性肝炎的药物组合物
