KRAS基因突变的检测试剂盒及其应用
文献发布时间:2023-06-19 11:34:14
技术领域
本发明属于基因突变检测技术领域,具体涉及KRAS基因突变的检测试剂盒及其应用。
背景技术
RAS基因家族与人类肿瘤密切相关的基因有三种HRAS、KRAS和NRAS,这三种基因编码的蛋白质有约90%的氨基酸序列同源,又称为RASp21蛋白。KRAS信号通路是EGFR和其他信号转导的下游通路,当RAS基因发生突变时,其编码的RAS蛋白水解GTP-RAS能力下降,使得信号转导通路一直处于持续激活状态,刺激细胞不断增殖分化,最终导致细胞恶变。KRAS突变基因是一种常见的致癌基因,多见于恶性肿瘤,结直肠癌患者中约有30%~40%存在KRAS基因突变,肺腺癌患者中约有15%~30%存在KRAS突变。
研究表明,KRAS基因突变与NSCLC对吉非替尼、厄洛替尼等靶向治疗药物的原发性耐药有关。有研究发现KRAS基因的突变使结直肠癌患者对西妥昔单抗的治疗产生耐药性,NCCN(非小细胞肺癌临床实践指南2016版)指出KRAS基因突变会使肺癌患者对EGFR酪氨酸激酶抑制剂(EGFT-TKI)产生耐药,使结直肠癌患者对抗EGFR抗体类药物产生耐药。因此对KRAS基因突变进行风险预测,是EGFR靶向治疗耐药性产生与否的重要预测指标。
目前临床检测DNA中基因突变的方法主要有:1)直接测序法,是目前应用最多的一种检测方法,主要是Sanger测序,当突变基因得到有效富集之后,才能被测序,在突变基因含量低的情况下检测不准确,即灵敏度低。2)高通量测序技术法,但其富集特异性和有效性在不同的实验平台差距大,并且建库流程繁杂,周期长,成本高。3)常规的ARMS-PCR法:其灵敏度只能稳定达到1%突变检测,但血浆样本中游离的DNA往往碎片化并且总量非常少,导致需要采集的血液样本量过大,对患者伤害较大且操作繁琐。目前临床上推荐采集患者5-10ml全血用于后续检测,即所提取的游离DNA浓度有限,因此亟需一种灵敏度更高,能够兼容组织和血浆这两种样本类型的检测方法和检测试剂盒。
发明内容
本发明的目的在于克服现有技术的缺陷,提供一种KRAS基因突变的检测试剂盒及其应用,通过对荧光PCR检测上游引物进行特殊设计,提高了识别效率和特异性,进一步将该引物与双淬灭探针结合,显著提高了引物探针与靶标片段的结合能力,提高了检测的扩增效率和信号值,以满足血检的高灵敏度高特异性要求,可兼容组织和血浆两种样本类型并同时检测KRAS基因7种类型的突变,而且操作过程简单快速,成本低,检测结果清晰明了易分析。
为实现上述目的,本发明采用的技术方案是:
本发明提供了一种KRAS基因突变的检测试剂盒,所述检测试剂盒中包括:突变位点的特异性上游引物、下游引物和双淬灭探针;
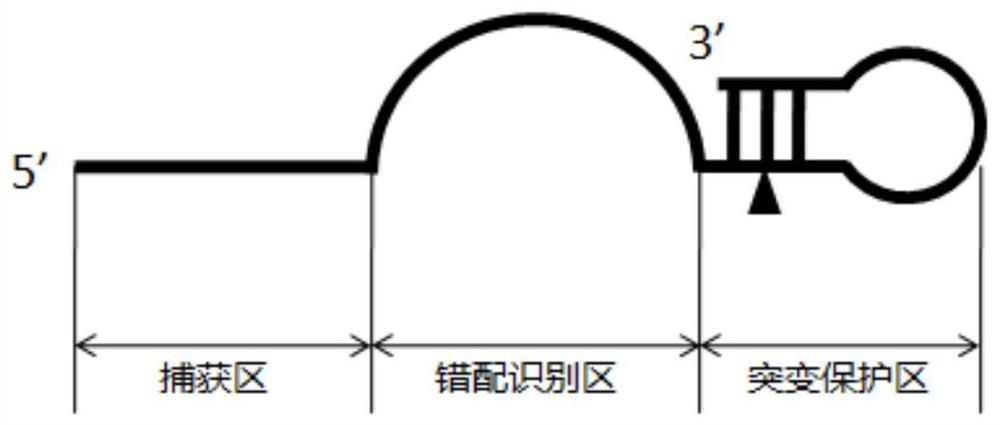
其中所述的特异性上游引物结构依次为:捕获区:长度为12-21bp,与目的片段完全配对;错配识别区:长度为3-6bp,与目的片段错配;突变保护区:包含突变识别位点,以及与所述突变识别位点配对形成发卡结构的3’端;
所述下游引物与KRAS基因突变位点的下游配对;
所述双淬灭探针上带有两个淬灭基团。
本发明中的特异性上游引物中包含一个发卡结构的突变保护区,当低于解链温度时,引物的发卡结构关闭,将突变识别保护起来避免与其他序列错配结合;当达到变性温度时,发卡结构打开,随着引物捕获区与目的片段的结合,错配识别区和打开的发卡结构对目的突变位点形成的双重识别开始发挥作用:在检测时,如果待检测片段为野生型,则错配区、突变位点以及发夹结构3’端区域均无法与目的片段结合,形成一个超强错配,使扩增无法进行下去;当目的片段为突变型时,引物上的捕获区以及突变位点区域能够与靶标结合,扩增反应能够顺利进行下去,进一步地,结合双荧光淬灭探针,使突变型被成功检测出来。
进一步的,所述突变位点的特异性上游引物包括:
①Gly12Cys突变位点的特异性上游引物:其序列如SEQ ID NO.1所示;
②Gly12Ser突变位点的特异性上游引物:其序列如SEQ ID NO.2所示;
③Gly12Arg突变位点的特异性上游引物:其序列如SEQ ID NO.3所示;
④Gly12Val突变位点的特异性上游引物:其序列如SEQ ID NO.4所示;
⑤Gly12Asp突变位点的特异性上游引物:其序列如SEQ ID NO.5所示;
⑥Gly12Ala突变位点的特异性上游引物:其序列如SEQ ID NO.6所示;
⑦Gly13Asp突变位点的特异性上游引物:其序列如SEQ ID NO.7所示。
进一步的,所述下游引物为通用下游引物,其序列如SEQ ID NO.8所示。
进一步的,所述双淬灭探针序列的5’端标记有荧光报告基团,3端标记有连接了MGB修饰基团的荧光淬灭基团。其中MGB修饰基团本身不产生荧光,因此可以大大降低本底信号的强度,进而提高检测特异性。
进一步的,所述荧光报告基团选自FAM、VIC、ROX、Cy3、Cy5、HEX、JOE中的任意一种;
所述荧光淬灭基团选自TAMRA、BHQ1、BHQ2、NFQ、LFN中的任意一种。
进一步的,所述双淬灭探针的序列为:
5’FAM-CAAGAGTGC-LFN-CTTGACGATA-MGB 3’。
进一步的,所述检测试剂盒中还包括:DNA聚合酶、UNG酶、dNTPs和Mg
进一步的,所述检测试剂盒中的PCR反应体系为每25μL含:DNA聚合酶0.5U~1.0U,UNG酶0.1U-0.5U,MgCl
进一步的,在PCR反应体系中,上游引物、下游引物和探针的浓度比为0.2μM:0.2μM:0.1μM。
进一步的,在PCR反应体系中,MgCl
进一步的,在PCR反应体系中,所述DNA聚合酶为Taq酶,所述Taq酶和UNG酶的总量比为0.5U:0.1U、0.5U:0.5U、1.0U:0.1U或1.0U:0.5U。
进一步的,在PCR反应体系中,dNTP中dATP、dUTP、dGTP和dCTP的浓度分别为0.15mM、0.15mM、0.15mM、0.3mM。
进一步的,所述检测试剂盒中还包括:阳性对照液和/或空白对照液。
进一步的,所述检测试剂盒中还包括可用于监控点样的内标引物,其上游引物序列为:GGGCCACTAGGCGCTCA,下游引物序列为:AGCCACCCGCGAACTCA,荧光探针序列为:5’VIC-CTCTCCCTCCGCGCAGCCG-3’MGB
进一步地,在本发明的一些实施方案中,所述引物组还包括用于监控样本质量的质控引物,所述质控引物的碱基序列,其上游引物序列为:GACTGAATATAAACTTGTGGTAGTTGGA,下游引物序列为:CATATTCGTCCACAAAATGATTCTG,荧光探针序列为:5’FAM-CTGTATCGTCAAGGCACT-3’MGB
本发明还提供了上述检测试剂盒在检测KRAS基因突变的非疾病诊断和治疗目的上的用途。
与现有技术相比,本发明的有益效果是:
本发明提供了一种用于检测KRAS基因突变的检测试剂盒及应用,本发明基于KRAS基因的7种突变位点,设计了特殊的上游引物,即在引物中增加有错配识别区和突变保护区,从而提高了引物对于目的片段的识别效率和识别特异性,进一步的,本发明发现该引物与双淬灭探针结合,具有协同增效作用,可显著提高引物探针与靶标片段的结合能力,提高检测的扩增效率和信号值,即显著提高了检测灵敏度和特异性,可实现40ng DNA样本中1copy突变(1/12000)的准确检出,满足了血检的高灵敏度高特异性要求,2-5ml血浆提取ctDNA原液可以直接用于检测;对于组织样本则可以耐受50ng的基因组DNA背景干扰。即本发明的检测试剂盒可同时检测KRAS基因7种类型的突变,实现对EGFR靶向治疗耐药性的辅助诊断治疗,灵敏度和特异性均显著提高,可兼容组织和血浆两种样本类型,满足临床需求;同时成本低,操作过程简单快速,100min内即可完成检测;并且可直接根据反应液的检测Ct值判断检测结果,不需要额外使用质控Ct值计算相关ΔCt值,检测结果的判读简单直观。
附图说明
图1为本发明实施例1中特异性上游引物的结构;
图2为本发明实施例1中特异性上游引物的工作原理;
图3为本发明实施例1和对比例1灵敏度检测时的扩增曲线图。
具体实施方式
下面将结合本发明中的实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动条件下所获得的所有其它实施例,都属于本发明保护的范围。
实施例1
本实施例提供了一种KRAS基因突变检测试剂盒,其中包括针对KRAS基因7个突变位点的特异性上游引物、通用下游引物、双淬灭探针、Taq酶、UNG酶、dNTPs和Mg
KRAS基因7个突变位点及序列如表1所示,其中加粗的碱基即为突变位点。
表1 KRAS基因的7个突变位点及序列
根据表1所述的7个突变位点,分别设计用于荧光定量PCR检测的特异性上游引物,其结构从5’端到3’端依次为:捕获区:长度为12-21bp,与目的片段完全配对;错配识别区:长度为3-6bp,与目的片段错配;突变保护区:包含突变识别位点,以及与所述突变识别位点配对形成发卡结构的3’端(如图1所示)。该引物的工作原理是:(1)当低于解链温度时,引物的发卡结构关闭,将突变识别保护起来避免与其他序列错配结合;当达到变性温度时,发卡结构打开,随着引物捕获区与目的片段的结合,错配识别区和打开的发卡结构对目的突变位点形成双重识别。(2)在检测时,如果待检测片段为野生型,则错配区、突变位点以及发夹结构3’端区域均无法与目的片段结合,形成一个超强错配,无法进行扩增;当目的片段为突变型时,引物上的突变位点能够与之结合,并扩增突变基因。基于此设计的7个特异性上游引物及序列如表2所示,其中下划线为错配序列,加粗碱基为突变识别位点。
表2特异性上游引物
进一步的,根据表1所述的序列,设计了通用下游引物KRAS-R,其序列为:TTCGTCCACAAAATGATTCTGAAT(如SEQ ID NO.8所示);
更进一步的,本实施例所采用的双淬灭探针为KRAS-P1,其序列具体为:5’FAM-CAAGAGTGC-LFN-CTTGACGATA-MGB 3’。
对比例1
本对比例与实施例1的不同之处在于:本对比例中所采用的探针为常规设计探针,仅有一个淬灭基团,具体序列为:
KRAS-P2:5’FAM-CAAGAGTGCCTTGACGATA-MGB 3’
对比例2
本对比例与实施例1的不同之处在于:本对比例中所采用的上游引物为常规的ARMS引物,各上游引物序列表3所示。
表3常规ARMs引物
对比例3
本对比例与实施例1的不同之处在于:本对比例中所采用的上游引物为常规的ARMS引物,其序列如对比例2中的表3所示;同时本对比例所采用的探针为常规设计探针,仅有一个淬灭基团,其序列与对比例1中的探针相同,即:KRAS-P2:5’FAM-CAAGAGTGCCTTGACGATA-MGB 3’
评价方法
为验证实施例1和对比例1-3中各引物组和探针的检测效果,首先建立参考品体系,即采用常规方法,将表1中所示的7个突变基因的DNA片段分别克隆到pEASY-T1质粒载体上,并分别转化到DH5α菌株内,菌株经培养后分别提取质粒,其A
另外提取HT-29细胞系基因组DNA,将上述所得到的突变质粒进行定量并梯度稀释,和基因组DNA混合形成含有不同比例突变质粒的混合样本。
(1)特异性评价
分别取浓度为10ng/μL和20ng/μL的基因组DNA作为待测样本(不含突变质粒)。取实施例1和对比例1-3的检测体系分别进行荧光定量PCR检测,以验证不同的检测体系的检测特异性。PCR检测体系如表4所示。
表4荧光定量PCR检测体系
PCR扩增条件为:37℃、10min;95℃、5min;95℃、15s,60℃、60s,45个循环。使用实时荧光定量PCR仪读取不同浓度样本和不同检测体系的循环数,即CT值,结果如表5所示。
表5特异性评价检测结果
根据表5的特异性检测结果,其中对比例2和对比例3在待测样本中不含有突变质粒的情况下仍能读取出CT值,说明其特异性较差,检测结果不准确,而实施例1和对比例1均无法读取相应的CT值,即在待测样本中不含突变的情况下未进行扩增,说明采用本发明特殊设计的上游引物可增强检测特异性,能够耐受高达20ng/μL背景DNA的干扰,避免了非特异性扩增导致的假阳性结果。
(2)灵敏度评价
将上述制得的7种突变质粒和基因组DNA混合分别按照一定浓度混合,形成含有不同比例突变质粒的混合样本。每种突变质粒包含3个浓度:20ng/μL样本中含有1%、0.1%或0.01%拷贝数的突变质粒(其中浓度为20ng/μL的样本中DNA拷贝数为6000copies/μL)。取实施例1和对比例1-3的检测体系分别进行荧光定量PCR检测,以验证不同的检测体系的检测灵敏度。PCR检测体系和扩增条件与特异性检测中相同,分别读取不同样本不同检测体系的CT值,结果如表6和图3所示。
表6灵敏度评价检测结果
根据表6的检测结果,其中当40ng样本中含有0.01%拷贝数(约1copy)的突变质粒时,对比例2和对比例3存在部分或完全无法读取CT值的情况,即灵敏度偏低,无法满足临床上血浆样本的高灵敏度检测。即采用本发明特殊设计的上游引物可增强检测灵敏度。更进一步的,根据表6,本发明实施例1和对比例1的CT值也存在差异,实施例1相较于对比例1提前了约1个CT值,扩增效率更高,并且根据图3,以Gly12Val位点为例,实施例1相比于对比例1,其信号高度更高,曲线线型平台期也更明显,说明本发明特殊设计的引物与双淬灭探针具有协同增效作用,可显著增加检测灵敏度,可实现40ng DNA样本中1copy突变(1/12000)的准确检出,满足了血检的高灵敏度要求,2-5ml血浆提取的ctDNA原液即可直接用于检测。
(3)精密度评价
分别将上述制得的7种突变质粒和基因组DNA混合制成突变质粒的混合样本,其浓度为10ng/μL样本中含有5%的突变质粒,采用实施例1的检测体系分别重复检测10次,读取CT值并计算平均值、标准差和变异系数CV值,通过CV值评价实施例1检测体系的精密度。检测结果如表7所示。
表7精密度评价检测结果
根据表7的检测结果可知,采用本发明实施例1的检测体系进行突变基因的检测时,其CV值均低于3%,说明该检测体系的重复性好,精密度高,可满足临床使用需求。
综合上述检测结果,采用本发明所述的KRAS基因检测体系和检测试剂盒,不仅可同时检测KRAS基因7种类型的突变,并且通过将特殊设计的上游引物与双淬灭探针结合,产生协同增效作用,显著提高了检测灵敏度和特异性,可兼容组织和血浆两种样本类型,满足临床需求,实现对EGFR靶向治疗耐药性的辅助诊断治疗,同时操作过程简单快速,100min内即可完成检测;并且检测结果的判读简单直观。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。
序列表
<110> 武汉友芝友医疗科技股份有限公司
<120> KRAS基因突变的检测试剂盒及其应用
<160> 8
<170> SIPOSequenceListing 1.0
<210> 1
<211> 40
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
gaatataaac ttgtggtagt tccgtaatgt gccccccaca 40
<210> 2
<211> 37
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
aatataaact tgtggtagtt aattaaagtg ggggact 37
<210> 3
<211> 34
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
taaacttgtg gtagttggta gccgtgaaaa acac 34
<210> 4
<211> 38
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
aatataaact tgtggtagtt gggatagttg aaaaacaa 38
<210> 5
<211> 34
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
taaacttgtg gtagttgcga taaatgtttt tcat 34
<210> 6
<211> 33
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
aacttgtggt agttggcatg actgtttttt cag 33
<210> 7
<211> 40
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 7
ataaacttgt ggtagttgga gagttctacg tgggggacgt 40
<210> 8
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
ttcgtccaca aaatgattct gaat 24
- KRAS基因突变的检测试剂盒及其应用
- KRAS基因突变检测试剂盒及其应用
