青光眼中的VE-PTP抑制
文献发布时间:2023-06-19 12:16:29
技术领域
本公开涉及青光眼,并且更具体地涉及饲养到Tie2单倍体不足小鼠的VE-PTPlacZ小鼠的小鼠模型,以及VE-PTP抑制在神经保护和减轻由升高眼内压引起的其他青光眼症状中的用途。
背景技术
青光眼是全球不可逆性失明的第二大主要原因,是无法治愈的毁灭性疾病。升高眼内压(IOP)主要由房水流出通路的缺陷引起,是疾病恶化的重要危险因素。房水流出(AHO)的减少导致前房流体稳态的改变,从而导致高眼压症、视网膜神经节细胞(RGC)死亡和青光眼。
大部分的AHO都经由常规路线,包括小梁网(TM)和位于虹膜角膜角的大型淋巴状Schlemm管(SC)。来自前房的房水通过TM进入SC,并通过一系列收集器通道排入巩膜外静脉。最近研究已确定Angpt-TEK信号传导通路在SC发育和维持中的重要性,并且在患有原发性先天性青光眼的患者中发现了Angpt受体TEK(内膜内皮细胞激酶,也称为Tie2)及其主要配体ANGPT1的功能突变丧失,原发性先天性青光眼是一种严重的青光眼,其特征是早期/儿时发作、眼球突出和视神经病变。Tek敲除小鼠完全缺乏SC,并表现出快速发展的青光眼样表型。
在美国专利9,719,135中描述了一种小鼠模型,其中双血管生成素1/血管生成素2(Angpt1/Angpt2)敲除小鼠和Tie2敲除小鼠由于眼内压升高而发展为牛眼症。Angpt1/Angpt2双敲除小鼠和Tie2敲除小鼠都缺乏Schlemm管。血管生成素信号传导对Schlemm管形成具有剂量效应。Tie2信号传导(活化)对Schlemm管形成具有剂量效应。Tie2活化促进Schlemm管形成,而活化Tie2的因素包括血管内皮磷酸酪氨酸磷酸酶(VE-PTP)抑制剂。
血管生成素-TEK信号传导对于淋巴状Schlemm管(眼前房中的一种独特血管)的发育至关重要。缺乏TEK或血管生成素配体ANGPT1和ANGPT2的敲除小鼠迅速发展为高眼压症症、牛眼症和青光眼性神经疾病。
在缺乏血管生成素配体ANGPT1或ANGPT2的小鼠中观察到了类似的效果,这证实了血管生成素-TEK信号传导是SC发育所必需的。
2017年5月4日提交的公开号为WO2017/190222、名称为“VE-PTP敲除(VE-PTPKnockout)”的PCT专利申请第PCT/CA2017/000120号描述了一种生产具有减少的VE-PTP和Tie2表达的小鼠的方法,该专利申请通过引用整体并入本文,该方法包含在小鼠基因组中用VE-PTP无效等位基因替换单个野生型VE-PTP等位基因,并用Tie2无效等位基因替换至少一个野生型Tie2等位基因。将单个VE-PTP无效等位基因引入Tie2杂合无效小鼠基因组表明相对于Tie2杂合无效小鼠的眼内压,所得小鼠中升高眼内压的表型表达降低了。在WO2017/190222中还描述了一种小鼠,其基因组包含一个VE-PTP无效等位基因、一个VE-PTP野生型等位基因、两个血管生成素1无效等位基因和两个血管生成素2无效等位基因,其中血管生成素1和/或血管生成素2无效等位基因为条件无效等位基因,其中该条件无效等位基因通过表达Cre重组酶而诱发,并且小鼠的眼内压正常。
人和小鼠中血管生成素TEK(也称为Tie2)信号传导通路的破坏会导致Schlemm管缺失、IOP升高和青光眼。在TEK杂合小鼠模型中,该通路的部分破坏揭示了SC发育中的剂量依赖性,并且杂合眼的特征在于发育不全的SC具有局灶性窄化、间隙和卷积。该畸形管不足以进行正常的引流,并且与对照组(12.30mmHg,p=0.0046)相比,杂合小鼠的IOP升高(15.39mmHg)。
实际上,Tek单倍体不足小鼠(Tek
通过增加ANGPT配体的利用率或通过抑制磷酸酶PTPRB(也称为血管内皮蛋白酪氨酸磷酸酶,VE-PTP),可以在体外和体内实现TEK受体的异位激活,从而增强TEK磷酸化。PTPRB抑制增强了所有磷酸化酪氨酸残基的TEK磷酸化,并显著增加了下游信号传导。
发明内容
在下文中将描述本公开各特征中的几个。应当理解,本发明的应用不限于在以下实施例、权利要求、说明书和附图中阐述的细节。本发明还具有其他实施例并且能够以许多其他方式来实践或进行。一些实施例如下:
1.一种减轻有此需要的受试者的高眼压症的方法,包含向所述受试者施用治疗有效量的VE-PTP抑制剂。
2.一种治疗有此需要的受试者的青光眼的方法,包含向所述受试者施用引起角膜缘血管丛、SVP和/或巩膜外静脉中的平滑肌细胞血管舒张的化合物。
3.根据实施例2所述的方法,其中所述化合物为VE-PTP抑制剂。
4.一种治疗眼部神经疾病或保护包括RGC在内的神经元细胞免于因有此需要的受试者的升高眼内压而造成的伤害的方法,包含向所述受试者施用VE-PTP抑制剂。
5.一种激活有此需要的受试者的SVP/SCP中的Tie2信号传导的方法,所述方法包含向所述患者施用VE-PTP抑制剂。
6.一种激活有此需要的受试者的角膜缘血管丛中的Tie2信号传导的方法,所述方法包含向所述受试者施用VE-PTP抑制剂。
7.根据上述实施例中任一项所述的方法,其中所述VE-PTP抑制剂被施用于眼睛。
8.根据上述实施例中任一项所述的方法,其中所述VE-PTP抑制剂是系统性施用的。
9.根据上述实施例中任一项所述的方法,其中所述VE-PTP抑制剂为小分子或生物制剂。
10.一种治疗有此需要的受试者的青光眼的方法,包含向所述受试者施用治疗有效量的VE-PTP抑制剂。
11.一种减轻有此需要的受试者的高眼压症的方法,包含向所述受试者施用引起角膜缘血管丛、SVP和/或巩膜外静脉中的平滑肌细胞血管舒张的化合物。
12.根据实施例11所述的方法,其中所述化合物为VE-PTP抑制剂。
附图说明
附图仅描述了本公开的示例实施例,因此不限制其范围。附图用于增添特征和细节。
专利或申请文件含有至少一张彩色附图。专利局将根据要求,在必要的费用支付后提供带有彩色附图的本专利或专利申请公开的副本。
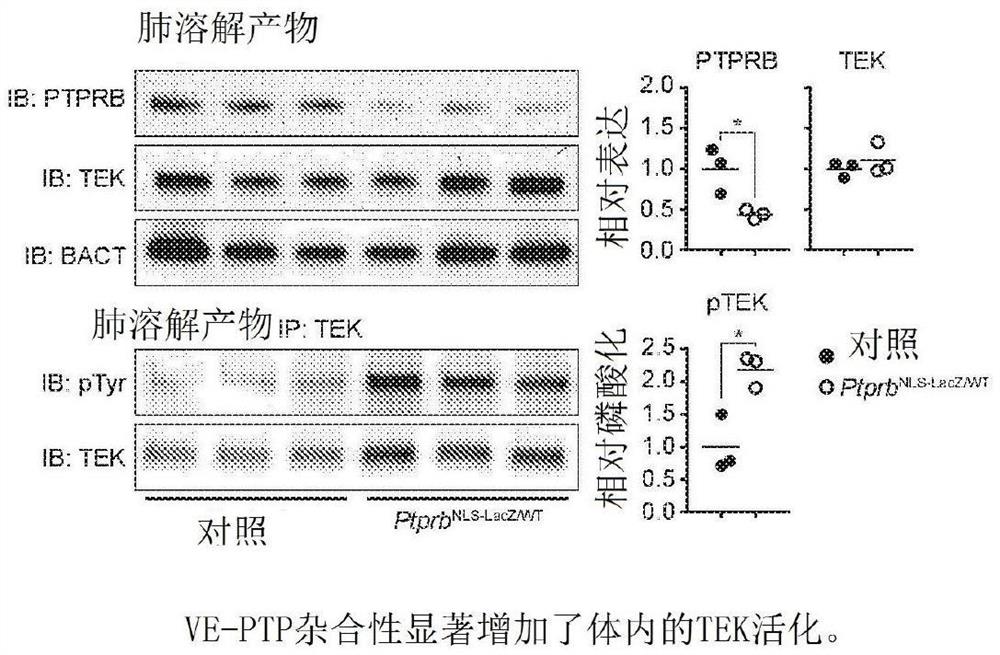
图1示出了在对照小鼠和VE-PTP/Ptprb杂合小鼠体内TEK活化的示例性蛋白质印迹分析和相应的图形表示。
图2示出了对照野生型小鼠、TEK单倍体不足小鼠和TEK单倍体不足/VE-PTP杂合小鼠的眼内压图。
图3示出了用抗BRN3B抗体(可鉴定RGC)染色的视网膜全胚胎,以及对比TEK单倍体不足小鼠的视网膜神经节细胞损失和TEK/VE-PTP双杂合小鼠中RGC挽救的相应图表。
图4示出了Schlemm管的形态比较,以及野生型对照小鼠、TEK和VE-PTP单倍体不足小鼠和TEK/VE-PTP双杂合小鼠的范围和卷积的相应图形表示。
图5示出了TEK/VE-PTP双杂合小鼠的眼内压与Schlemm管形态缺陷数量和Schlemm管范围的对比图。
图6示出了与SVP相比,Schlemm管腔内皮的免疫荧光染色(FSP对应于包括SC和浅表毛细血管丛在内的全层图像)。
具体实施方式
在本公开的实施例中,提供了一种饲养到Tie2单倍体不足小鼠的VE-PTPlacZ小鼠的小鼠模型。
在本公开的实施例中,提供了一种通过缺失Tek单倍体不足小鼠中的单个PTPRB等位基因来制作小鼠模型的方法。
在本公开的实施例中,VE-PTP抑制在角膜缘血管丛/浅表毛细血管丛中的使用提供了针对升高眼内压(青光眼症状)的神经保护。
在本公开的实施例中,提供了一种小鼠,其基因组包含Tek单倍体不足小鼠中的单个PTPRB等位基因的缺失。
在本公开的实施例中,提供了一种通过角膜缘血管丛中的针对升高眼内压(青光眼症状)神经保护的VE-PTP抑制来治疗青光眼的方法。
在本公开的实施例中,提供了一种Tek单倍体不足小鼠模型,其中缺失单个PTPRB等位基因足以增加TEK活化作用、降低眼内压(IOP)并抑制与压力有关的视网膜神经节细胞(RGC)损失。其结果是RGC保护,并且Schlemm管(SC)的管直径没有变化。
在本公开的实施例中,提供了一种饲养到Tie2单倍体不足小鼠的VE-PTPlacZ小鼠的小鼠模型,用于测量升高眼内压的青光眼症状的神经保护作用。
在本公开的另一实施例中,VE-PTP/PTPRB抑制的使用为青光眼患者提供了降低IOP的治疗策略。
在本公开的另一实施例中,VE-PTP/PTPRB抑制的使用增加了Schlemm管下游的房水流出。
在本公开的另一实施例中,眼睛中浅表毛细血管丛周围的平滑肌的血管舒张提供了神经保护,并避免了由高IOP引起的视网膜神经节细胞损失。
在本公开的另一实施例中,药理性TEK活化作用可用于治疗高眼压症和青光眼。
在本公开的实施例中,提供了一种方法,该方法通过加入VE-PTP的单倍体不足而防止青光眼中RGC的损失以及降低Tie2/TEK单倍体不足小鼠的IOP。
房水流出受到SC内壁流量和阻力的限制,并且假设SC范围的减少直接影响流出能力。但是,SC内壁的流动阻力不是影响房水流出的唯一因素,并且如Goldmann方程(方程1)所述,流出和IOP两者都与巩膜外静脉压(EVP)直接相关。本文提供的数据表明,ptprb抑制会增加Schlemm管下游流出量,从而允许更粗的血管和更多的流出量。反过来,这又具有神经保护作用,可以保护RGC。
方程1:
IOP=F/C+EVP
为避免提出的机制的束缚,通过挽救具有VE-PTP缺失的TEK单倍体不足小鼠而降低的IOP很可能是由引流血管(包括浅表血管丛)的血管舒张引起的,因为在缺失之前其表达高水平的PTPRB。通过缺失单个VE-PTP等位基因,增加了(系统性)TEK活化作用,并且避免了在Tek杂合无效小鼠中观察到的高眼压症和RGC损失。
通过VEPTP抑制进行眼部保护的机制似乎是利用VE-PTP抑制对正常表达VE-PTP的浅表静脉丛的作用。
结果表明,Schlemm管本身不表达Beta-gal VE-PTP报告基因,这表明VE-PTP不在SC中,或者如果在SC中,其水平低于周围血管的水平。产生Schlemm管的早期毛细血管丛中的发育过程似乎不表达VE-PTP,但似乎祖细胞表达VE-PTP。
可以通过VE-PTP抑制来实现IOP降低和神经保护,其可能是通过VE-PTP抑制对引流血管的直接作用(不一定是在Schlemm本身中)增加的流出量来实现。
通过使用VE-PTP-LacZ报告基因小鼠品系,确定在角膜缘血管丛中存在VE-PTP表达,该血管丛从SC排出房水,并在发育过程中生长以形成管。然而,在成熟的SC内皮中未识别出VE-PTP表达。产生了双TEK;VE-PTP杂合小鼠,并且与TEK杂合同窝仔不同,TEK;VE-PTP双杂合小鼠具有正常的IOP,并且未显露TEK缺陷小鼠的眼病表型。已确定通过抑制该负调节剂(VE-PTP)以活化TEK为先天性青光眼患者提供了治疗策略。
以下是本发明的其他实施例:
1.一种减轻有此需要的受试者的高眼压症的方法,包含向所述受试者施用治疗有效量的VE-PTP抑制剂。
2.一种治疗有此需要的受试者的青光眼的方法,包含向所述受试者施用引起角膜缘血管丛、SVP和/或巩膜外静脉中的平滑肌细胞血管舒张的化合物。
3.根据实施例2所述的方法,其中所述化合物为VE-PTP抑制剂。
4.一种治疗眼部神经疾病或保护包括RGC在内的神经元细胞免于因有此需要的受试者的升高眼内压而造成的伤害的方法,包含向所述受试者施用VE-PTP抑制剂。
5.一种激活有此需要的受试者的SVP/SCP中的Tie2信号传导的方法,所述方法包含向所述患者施用VE-PTP抑制剂。
6.一种激活有此需要的受试者的角膜缘血管丛中的Tie2信号传导的方法,所述方法包含向所述受试者施用VE-PTP抑制剂。
7.根据上述实施例中任一项所述的方法,其中所述VE-PTP抑制剂被施用于眼睛。
8.根据上述实施例中任一项所述的方法,其中所述VE-PTP抑制剂是系统性施用的。
9.根据上述实施例中任一项所述的方法,其中所述VE-PTP抑制剂为小分子或生物制剂。
10.一种治疗有此需要的受试者的青光眼的方法,包含向所述受试者施用治疗有效量的VE-PTP抑制剂。
11.一种减轻有此需要的受试者的高眼压症的方法,包含向该受试者施用引起角膜缘血管丛、SVP和/或巩膜外静脉中的平滑肌细胞血管舒张的化合物。
12.根据实施例11所述的方法,其中所述化合物为VE-PTP抑制剂。
在一实施例中,VE-PTP抑制剂为小分子。在另一实施例中,VE-PTP抑制剂为生物制剂。VE-PTP抑制剂的示例是本领域众所周知的,包括以下文章中所述示例:
Antioxid Redox Signal.2014 May 10;20(14):2130-40.doi:10.1089/ars.2013.5463.Epub 2014 Feb 4.
用于受体型蛋白酪氨酸蛋白磷酸酶β的羟基吲哚羧酸基抑制剂。
Zeng LF,Zhang RY,Bai Y,Wu L,Gunawan AM,Zhang ZY.
PMID:24180557 PMCID:PMC3995206 DOI:10.1089/ars.2013.5463
J Biol Chem.2004 Jun 4;279(23):24226-35.Epub 2004 Mar 15.
蛋白酪氨酸磷酸酶β的选择性和有效抑制剂的基于结构的设计。
Lund IK,Andersen HS,Iversen LF,Olsen OH,
PMID:15024017 DOI:10.1074/jbc.M313027200
Proc Natl Acad Sci U S A.2006 Jul 11;103(28):10606-11.Epub 2006Jun29.
通过面向生物学的合成发现蛋白磷酸酶抑制剂类别。
PMID:16809424 PMCID:PMC1502279 DOI:10.1073/pnas.0601490103
J Inorg Biochem.2003 Aug 1;96(2-3):321-30.
利用BMOV(甲基麦芽酚氧钒)的胰岛素致敏机制;非配位钒(VO4)作为活性成分。
Peters KG,Davis MG,Howard BW,Pokross M,Rastogi V,Diven C,Greis KD,Eby-Wilkens E,Maier M,Evdokimov A,Soper S,Genbauffe F.
PMID:12888267
Am J Physiol Heart Circ Physiol.2004 Jul;287(1):H268-76.Epub 2004Feb26.
酪氨酸磷酸酶的抑制增加了周围血管疾病大鼠模型的侧支血流量。
Carr AN,Davis MG,Eby-Wilkens E,Howard BW,Towne BA,Dufresne TE,PetersKG.
PMID:14988069 DOI:10.1152/ajpheart.00007.2004
Angiogenesis.2009;12(1):25-33.doi:10.1007/s10456-008-9126-0.Epub 2009Jan 1.
酪氨酸磷酸酶β调节人内皮细胞中的血管生成素-Tie2信号传导。
Yacyshyn OK,Lai PF,Forse K,Teichert-Kuliszewska K,Jurasz P,StewartDJ.
PMID:19116766 DOI:10.1007/s10456-008-9126-0
J Biol Chem.2012 Mar 16;287(12):9322-6.doi:10.1074/jbc.C111.320796.Epub2012Jan 24.
皮摩尔浓度的游离锌(II)离子调节受体蛋白酪氨酸磷酸酶β的活性。
Wilson M,Hogstrand C,Maret W.
PMID:22275360PMCID:PMC3308757 DOI:10.1074/jbc.C111.320796
J Med Chem.2009 Nov 12;52(21):6649-59.doi:10.1021/jm9008899.
用于合理的抑制剂设计的人蛋白酪氨酸磷酸酶家族中相似关系的基于知识的表征。
PMID:19810703 PMCID:PMC2786264 DOI:10.1021/jm9008899
FEBS Lett.2004May 21;566(1-3):35-8.
双过氧钒化合物是有效的PTEN抑制剂。
Schmid AC,Byrne RD,Vilar R,Woscholski R.
PMID:15147864 DOI:10.1016/j.febslet.2004.03.102
Bioorg Med Chem.2012Jul 15;20(14):4371-6.doi:10.1016/j.bmc.2012.05.040.Epub 2012 May 24.
芳基锑酸是Cdc25a和Cdc25b磷酸酶的有效且同种型选择性抑制剂。
Mak LH,Knott J,Scott KA,Scott C,Whyte GF,Ye Y,Mann DJ,Ces O,StiversJ,Woscholski R.
PMID:22705189 PMCID:PMC3389297 DOI:10.1016/j.bmc.2012.05.040
ACS Chem Biol.2006Dec 15;1(12):780-90.
一种在染色体10上缺失(PTEN)的磷酸酶和张力蛋白同源物的小分子抑制剂。
Rosivatz E,Matthews JG,McDonald NQ,Mulet X,Ho KK,Lossi N,Schmid AC,Mirabelli M,Pomeranz KM,Erneux C,Lam EW,Vilar R,Woscholski R.
PMID:17240976 DOI:10.1021/cb600352f
J Med Chem.2013 Jun 27;56(12):4990-5008.doi:10.1021/jm400248c.Epub2013Jun 6.
一种用于与自身免疫性疾病相关联的淋巴特异性酪氨酸磷酸酶(LYP)的有效且选择性的小分子抑制剂。
He Y,Liu S,Menon A,Stanford S,Oppong E,Gunawan AM,Wu L,Wu DJ,BarriosAM,Bottini N,Cato AC,Zhang ZY.
PMID:23713581 PMCID:PMC3711248 DOI:10.1021/jm400248c
J Biol Chem.2009 Apr 24;284(17):11385-95.doi:10.1074/jbc.M807241200.Epub2009 Feb 20.
GLEPP1/蛋白酪氨酸磷酸酶phi抑制剂在体内和体外阻滞趋化性,并改善小鼠溃疡性结肠炎。
Gobert RP,van den Eijnden M,Szyndralewiez C,Jorand-Lebrun C,SwinnenD,Chen L,Gillieron C,Pixley F,Juillard P,Gerber P,Johnson-Léger C,Halazy S,Camps M,Bombrun A,Shipp M,Vitte PA,Ardissone V,Ferrandi C,Perrin D,Rommel C,Hooft van Huijsduijnen R.
PMID:19233845 PMCID:PMC2670144 DOI:10.1074/jbc.M807241200
Bioorg Med Chem.2007 Aug 1;15(15):5137-49.Epub 2007May 17.
作为蛋白酪氨酸磷酸酶抑制剂的5-亚芳基-2,4-噻唑烷二酮。
Maccari R,Paoli P,OttanàR,Jacomelli M,Ciurleo R,Manao G,Steindl T,Langer T,Vigorita MG,Camici G.
PMID:17543532 DOI:10.1016/j.bmc.2007.05.027
Molecules.2018 Mar 2;23(3).pii:E569.doi:10.3390/molecules23030569.
用生物治疗剂靶向受体型蛋白酪氨酸磷酸酶:由外而内比由内而外更好吗?
Senis YA,Barr AJ.
PMID:29498714 DOI:10.3390/molecules23030569
此为靶向酪氨酸磷酸酶的抑制剂的综述:
Trends Pharmacol Sci.2017 Jun;38(6):524-540.doi:10.1016/j.tips.2017.03.004.Epub 2017 Apr 12.
靶向酪氨酸磷酸酶:是结束污名的时候了。
Stanford SM,Bottini N.
PMID:28412041 PMCID:PMC5494996 DOI:10.1016/j.tips.2017.03.004
Curr Diab Rep.2016 Dec;16(12):126.
靶向Tie2来治疗糖尿病性视网膜病变和糖尿病性黄斑水肿。
Campochiaro PA,Peters KG.
PMID:27778249 DOI:10.1007/s11892-016-0816-5
Prog Retin Eye Res.2015 Nov;49:67-81.doi:10.1016/j.preteyeres.2015.06.002.Epub 2015 Jun 23.
视网膜和脉络膜血管疾病的分子发病机理。
Campochiaro PA.
PMID:26113211 PMCID:PMC4651818 DOI:10.1016/j.preteyeres.2015.06.002
为生物制剂的VE-PTP抑制剂的示例包括抗体及以下药物:
J Exp Med.2015 Dec 14;212(13):2267-87.doi:10.1084/jem.20150718.Epub2015Dec 7.
在不存在VE-钙粘着蛋白的情况下,干扰VE-PTP会经由Tie2体内稳定内皮连接。
Frye M,Dierkes M,Küppers V,Vockel M,Tomm J,Zeuschner D,Rossaint J,Zarbock A,Koh GY,Peters K,Nottebaum AF,Vestweber D.
PMID:26642851 PMCID:PMC4689167 DOI:10.1084/jem.20150718
J Clin Invest.2014Oct;124(10):4564-76.doi:10.1172/JCI74527.Epub2014Sep 2.
靶向VE-PTP会激活TIE2并稳定眼部脉管系统。
Shen J,Frye M,Lee BL,Reinardy JL,McClung JM,Ding K,Kojima M,Xia H,Seidel C,Lima e Silva R,Dong A,Hackett SF,Wang J,Howard BW,Vestweber D,KontosCD,Peters KG,Campochiaro PA.
PMID:25180601 PMCID:PMC4191011 DOI:10.1172/JCI74527
J Cell Biol.2009 May 18;185(4):657-71.doi:10.1083/jcb.200811159.
VE-PTP通过平衡Tie2活性来控制血管发育。
Winderlich M,Keller L,Cagna G,Broermann A,Kamenyeva O,Kiefer F,Deutsch U,Nottebaum AF,Vestweber D.
PMID:19451274 PMCID:PMC2711575 DOI:10.1083/jcb.200811159
促进平滑肌细胞松弛的药物的示例包括血管松弛剂/血管扩张剂,诸如:
·α-肾上腺素受体拮抗剂(α-阻滞剂)
·血管紧张素转换酶(ACE)抑制剂
·血管紧张素受体阻滞剂(ARB)
·β2-肾上腺素受体激动剂(β2-激动剂)
·钙通道阻滞剂(CCB)
·中枢作用性抗交感神经药
·直接作用性血管扩张剂
·内皮素受体拮抗剂
·神经节阻滞剂
·硝化剂
·磷酸二酯酶抑制剂
·钾通道开放剂
·肾素抑制剂
示例
Ptprb单倍体不足小鼠的Tek磷酸化升高。本文所述的ptprb单倍体不足小鼠品系为VE-PTP-LacZ报告基因小鼠品系。为了提高体内TEK磷酸化水平,先前描述的Ptprb
在本公开中,在高眼压症的Tek单倍体不足模型中单个Ptprb等位基因的缺失降低了IOP并防止了相关的RGC损失。发现在30周龄时测量的Tek杂合小鼠的IOP升高(图2,对照:13.7±0.23,Tek
Ptprb杂合性不会改变SC形态。发现Ptprb杂合性在Tek
已确定,尽管Tek
在Tek
众所周知,房水流出受到SC内壁流量和阻力的限制,并且假设SC范围的减少直接影响流出能力。但是,已确定SC内壁的流动阻力不是影响房水流出的唯一因素,并且如Goldmann方程(方程1)所述,流出和IOP两者都与巩膜外静脉压(EVP)直接相关。
方程1:
IOP=F/C+EVP
已确定ptprb抑制(基因缺失)会增加Schlemm管下游流出量。SVP周围平滑肌的血管舒张有可能实现更粗的血管和更多的流出量,这反过来又具有神经保护作用,从而不破坏RGC。
Angpt-TEK信号传导对于Schlemm管的发育和维持至关重要,并且该信号传导通路的失调会导致小鼠和人类罹患青光眼。除血管生成素配体外,TEK受体的活化还受内皮特异性受体型磷酸酶PTPRB(VE-PTP)的调节。已确定Ptprb杂合性会导致(系统性)TEK过度活化,并为虹膜角膜角中TEK信号传导不足引起的发育表型提供了部分补偿。
图1是对照小鼠和VE-PTP杂合小鼠体内TEK活化的凝胶和相应图表。
已确定Ptprb杂合性会导致系统性TEK过度活化,并为虹膜角膜角中TEK信号传导不足引起的发育表型提供了部分补偿。图2显示,VE-PTP杂合性避免在TEK单倍体不足小鼠模型中观察到的高眼压症。在小鼠中缺失单个Ve-ptp等位基因防止在青光眼的Tek单倍体不足模型中观察到的高眼压症。
图3显示VE-PTP/TEK双杂合小鼠没有表现出在TEK单倍体不足动物中观察到的RGC损失。与Tie2
图4显示,尽管VE-PTP单倍体不足改善了SC的生理功能,但对SC范围或形态没有影响。尽管VE-PTP单倍体不足会增加TEK磷酸化、降低眼内压并防止视网膜神经节细胞损失,但通过共聚焦显微镜未观察到其对Schlemm管范围或形态的影响。
图5显示VEPTP-TEK双杂合小鼠中SC形态缺陷的数量或SC范围似乎与IOP不相关。
图6显示在SC内皮中未表达VE-PTP,并且确定了VEPTP缺失对改善Schlemm管引流的影响位于SC自身的下游,作用于浅表毛细血管丛和/或巩膜外静脉。FSP对应于包括SC和浅表毛细血管丛在内的全层图像。
尽管已经在详细描述中描述了本公开的实施例,但权利要求书的范围不应由示例中阐述的优选实施例来限制,而应给出与整个说明书一致的最宽泛的解释。
在本申请中引用的所有出版物、专利、专利申请和其他文件,用于所有目的通过引用整体并入本文,如同分别指出每个单独的出版物、专利、专利申请或其他文件用于所有目的通过引用并入。
- 青光眼中的VE-PTP抑制
- N-乙酰-L-半胱氨酸在治疗原发性闭角型青光眼中的应用
