CUL9作为标志物在结直肠癌预后评价上的应用
文献发布时间:2023-06-19 12:18:04
技术领域
本发明属于结直肠癌预后评价技术领域,尤其是涉及一种CUL9作为标志物在结直肠癌预后评价上的应用。
背景技术
结直肠癌作为常见的消化道恶性肿瘤,对人民的健康威胁不容小视。根据世界卫生组织国际癌症研究机构(IARC)发布的全球肿瘤流行病统计数据(GLOBOCAN 2020)估计,2020年全球结直肠癌新发病例193.16万,死亡病例93.52万,分别位于所有恶性肿瘤的第三位和第二位。近几十年来,随着人民生活水平的提高及饮食结构的改变,结直肠癌的发生比例亦逐渐增多。
随着对结直肠癌研究的不断深入,结直肠癌预后已经较过去几十年呈改善趋势。然而,对于结直肠癌临床诊治而言,肿瘤分期依旧是重要的预后因素,早期结直肠癌和中晚期结直肠癌的预后存在较大异质性。
中国专利CN107622800A公开了一种用于结直肠癌肝转移疗效预测的数学模型,其给出了一个公式,公式涉及的因素包括ATP6V1B1、CUL9、ERBB2、LY6G6D、RBMXL3、PTCH1这六个基因的基因型,该专利说明对西妥昔单抗敏感人群进行筛选后,客观反应率提升显著,从而可以更好的用于治疗方式的预测。
中国专利CN103954757B公开了一种通过TEAD4细胞核阳性表达情况对结直肠癌评价的方法,即首先制成肿瘤组织芯片,然后进行免疫组化实验、免疫评分,根据免疫评分进行分组,最后按照TEAD4的细胞核着染情况将患者分为TEAD4细胞核阳性表达组和TEAD4细胞核阴性表达组,然后运用统计学方法分析两组病人的临床特征以及总生存期的差异。该种通过结直肠癌免疫学指标TEAD4细胞核阳性表达情况对结直肠癌患者的临床特征和总体预后进行评价的方法,即根据结直肠癌患者肿瘤组织中TEAD4细胞核阳性表达的情况可以直接确定患者的临床特征和预后信息。
然而现有技术中,并没有通过结直肠癌标志物CUL9细胞浆阳性表达情况对结直肠癌患者的临床特征和预后进行评价的方法。
发明内容
本发明的目的就是为了克服上述现有技术存在的缺陷而提供一种CUL9作为标志物在结直肠癌预后评价上的应用。
本发明的目的可以通过以下技术方案来实现:
本发明提供一种CUL9作为标志物在结直肠癌预后评价上的应用,所述CUL9作为标志物,基于CUL9细胞浆阳性表达情况对结直肠癌患者的临床特征和预后进行评价。
本发明提供一种CUL9作为标志物在结直肠癌预后评价上的应用,具体方法为:
a.制作蜡块和组织芯片;
b.组织芯片包埋;
c.脱蜡水化;
d.抗原修复并封闭;
e.CUL9一抗抗体过夜孵育;
f.洗片后二抗室温孵育,显色放大液;
g.孵育后DAB显色;
h.苏木精染核,固定;
i.脱水至腊,切片保持;
j.结果读片;
k.统计分析:所有数据均使用SPSS统计软件包(22.0;SPSS Inc.,Chicago,Illinois,USA)进行统计分析,OS的计算及分析使用Kaplan-Meier方法进行,危险因素表示为危险比[HR,95%置信区间(Confidence interval,CI)],P值小于0.05被定义为有统计显著性。
在本发明的一个实施方式中,抗原修复并封闭的方法为:将组织切片浸于由EDTA配制的抗原修复液中,加热,取出后室温下冷却,洗涤,将组织切片浸泡在灭活液中灭活后,洗涤,将组织切片擦洗干净,在每张组织切片上滴加5%的BSA水溶液作为封闭液,孵育,封闭非特异性抗原。
在本发明的一个实施方式中,步骤j所述的结果读片的方法为:
CUL9阳性染色为细胞胞浆上呈现棕黄色颗粒,由两人分别独立进行免疫组化评分,评分结果有异议时重新评估,对染色结果进行评分,包括两个指标:1)染色强度:0分(-):0%细胞染色;1分(+):0-10%细胞不完全染色;2分(++):10%细胞弱至中等完全染色;3分(+++):10%细胞中度至强烈完整的染色;2)阳性染色占全部视野的比例;
两个指标的乘积为最终的免疫组化评分,即表达量,Cut-off值取表达量的中位数,大于cut-off值为高表达,小于等于Cut-off值为低表达。
本发明还提供一种验证CUL9细胞浆高表达和低表达情况与结直肠癌患者的临床特征和预后生存率的关系的方法,
首先制成肿瘤组织芯片,然后进行免疫组化实验、免疫评分,根据免疫评分进行分组,最后按照CUL9的细胞浆着染情况将患者分为CUL9细胞浆高表达组和CUL9细胞浆低表达组,然后运用统计学方法分析两组病人的临床特征以及总生存期的差异。
在本发明的一个实施方式中,对于结直肠癌患者,在手术切除标本后,首先制作基于石蜡切片的组织芯片,通过免疫组织化学的实验方式验证CUL9的表达水平。
在本发明的一个实施方式中,具体方法为:
a.制作蜡块和组织芯片;
b.组织芯片包埋;
c.脱蜡水化;
d.抗原修复并封闭;
e.CUL9一抗抗体过夜孵育;
f.洗片后二抗室温孵育,显色放大液;
g.孵育后DAB显色;
h.苏木精染核,固定;
i.脱水至腊,切片保持;
j.结果读片;
k.统计分析:所有数据均使用SPSS统计软件包进行统计分析,OS的计算及分析使用Kaplan-Meier方法进行,危险因素表示为危险比[HR,95%置信区间(Confidenceinterval,CI)],P值小于0.05被定义为有统计显著性,统计分析数据为CUL9免疫组化评分数据和及结直肠癌临床病理特征的相关性分析。
在本发明的一个实施方式中,抗原修复并封闭的方法为:将组织切片浸于由EDTA配制的抗原修复液中,加热,取出后室温下冷却,洗涤,将组织切片浸泡在灭活液中灭活后,洗涤,将组织切片擦洗干净,在每张组织切片上滴加5%的BSA水溶液作为封闭液,孵育,封闭非特异性抗原。
在本发明的一个实施方式中,步骤j所述的结果读片的方法为:
CUL9阳性染色为细胞胞浆上呈现棕黄色颗粒,由两人分别独立进行免疫组化评分,评分结果有异议时重新评估,对染色结果进行评分,包括两个指标:1)染色强度:0分(-):0%细胞染色;1分(+):0-10%细胞不完全染色;2分(++):10%细胞弱至中等完全染色;3分(+++):10%细胞中度至强烈完整的染色;2)阳性染色占全部视野的比例;
两个指标的乘积为最终的免疫组化评分,即表达量,Cut-off值取表达量的中位数,大于cut-off值为高表达,小于等于Cut-off值为低表达。
在本发明的一个实施方式中,本发明数据提示:CUL9高表达与肿瘤直径>4cm(P=0.001),肿瘤低分化(P=0.037),N1/2(P=0.028)和M1(P=0.001)正相关;CUL9蛋白高表达(P=0.001,HR=1.71,95%CI:1.45-2.34)都是OS较差相关。
多因素回归分析结果显示:T3/T4分期(P=0.001,HR=1.23,95%CI:1.03-1.67),N1/2分期(P=0.001,HR=1.51,95%CI:1.47-2.57),M1分期(P=0.001,HR=3.75,95%CI:2.83-4.56)以及CUL9蛋白高表达(P=0.001,HR=1.55,95%CI:1.38-2.04)都是影响CRC总生存期的独立危险因素。
本发明通过结直肠癌CUL9细胞浆阳性表达情况对结直肠癌患者的临床特征和总体预后进行评价的方法,即根据结直肠癌患者肿瘤组织中CUL9细胞浆表达的情况可以直接确定患者的临床特征和预后信息。
免疫组织化学方法为现今较为成熟的评估肿瘤组织表达的一种实验方式。基于前期实验及样本的积累,本发明旨在通过免疫组织化学的实验提供一种评估结直肠癌预后的方法。实验证明,通过本发明的方法进行统计与分析,CUL9在结直肠癌细胞浆的表达可以显著反映结直肠癌患者的预后,并具有统计学差异。
附图说明
图1:结直肠癌标本取材图示;
图2:CUL9不同表达量的代表性图片;
图3:CUL9高表达和低表达的代表性图片;
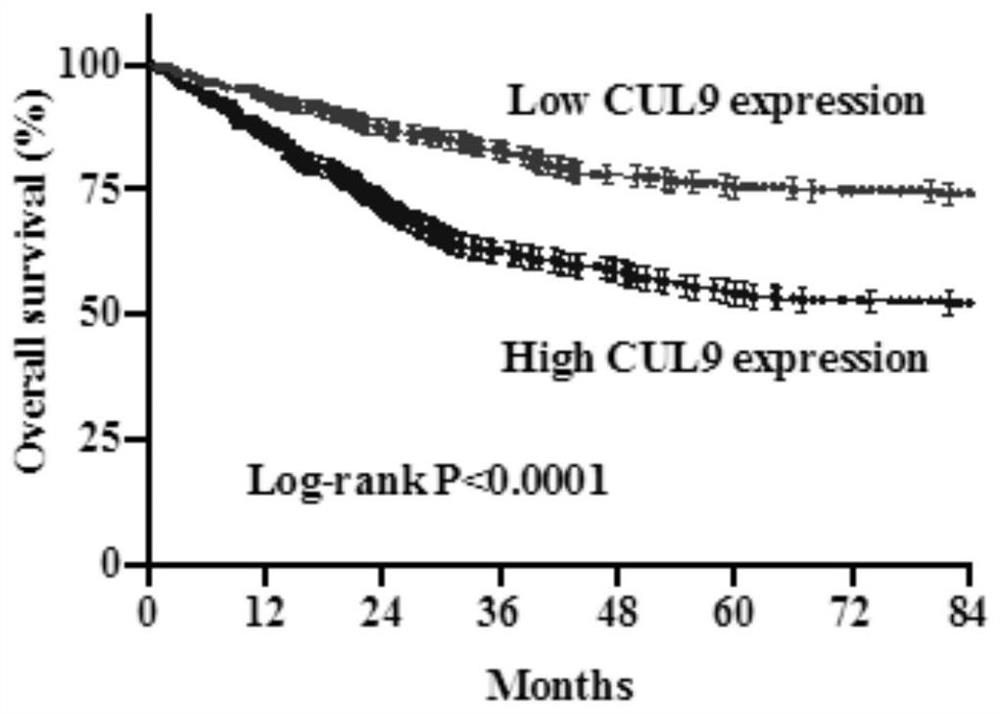
图4:CUL9表达量与结直肠癌患者预后的相关性。
具体实施方式
下面结合附图和具体实施例对本发明进行详细说明。
实施例1
本实施例的方法步骤如下:
a、本实施例中所用的911个结直肠癌组织的蜡块都来自复旦大学附属中山医院普外科。本实验通过了中山医院伦理委员会,每位患者都签订了知情同意。
b、取材:将实验所需的911个标本进行蜡块制作,911个结直肠癌组织取材位置如图1所示,蜡块具体制作方式如下:材料新鲜;所取的组织块的大小约为2.0cm×2.0cm×0.3cm;用刀片切取大小约为0.8cm×0.8cm×0.3cm的组织块。放入一次性塑料包埋框中,记号笔做好标记,脱水步骤是将含有组织的塑料包埋框依顺序放入不同浓度梯度的乙醇中;通常组织先经纯酒精和透明剂各半的混合液浸渍1~2小时,再转入纯透明剂中浸渍;组织经透明后在熔化的石蜡内浸渍的过程称浸蜡。将塑料包埋框放入烘箱中含有熔化石蜡的容器内。融化后的石蜡倒入不锈钢包埋框,打开塑料包埋框,用加温的镊子将浸蜡后的组织材料块切面朝下放入不锈钢包埋框,待蜡液表层凝固即迅速冷却,完全凝固后即做成含有组织块的蜡块。制作的蜡块应平整,自此蜡块制作完成。
c、组织芯片制备:在构建组织芯片之前,应该预先计划检测多少样本,然后相应地进行设计(一般在一个常规的载玻片上放置60~100个样本已经足够);收集病例及相关蜡块:挑选出具有随访资料的不同发展阶段的肿瘤组织蜡块,根据HE切片对石蜡标本中有代表性的点进行标记,包括典型的肿瘤和相应的正常组织,以构建肿瘤组织芯片;TMA受体蜡块制备:取97.5克莱卡石蜡+2.5克蜂蜡(2.5%)混合,制成长36mm*宽26mm*高17mm的空白蜡块,在该蜡块20mm×16mm范围内设计10×7点组织陈列。组织四周预留0.5cm-0.7cm空间,用组织仪打孔制成TMA蜡块;在组织芯片制作机上用细针对受体蜡块打孔,孔径以1~1.5mm比较适宜,同样在供体蜡块上标记的相应部位打孔采集组织芯。孔径同样为1~1.5mm;将组织芯转移到受体模块的孔中,每个组织芯之间的间距以0.2mm为佳;为了防止在打点、切片、染色或免疫组化过程中出现漏点,滑片及掉片现象,每个样本可以上样1-2个点;将构建好的TMA芯片蜡块放在相宜的塑料盒子内,并严密固定防止移位。放入55℃温箱中约10分钟,在蜡将要完全溶解前,取出室温下冷却,使受体模块的蜡与新插入的小圆柱状组织溶为一体,取下蜡块,于4℃冰箱中保存备用;切片前,蜡块需在4℃中预冷4h左右,然后夹在切片机上进行修正,等修到全部组织完整为止。用-20℃预冷冰袋贴在蜡块上5-10min左右,快速连续切片30-50张左右,再用冰袋冷冻组织块,或直接在冰冻切片机内进行,直至将组织切完为止。将4μm连续切片分别漂在凉水中,让其自然展开,按顺序将切片转移至45℃的温水中展片2min左右,将其贴在浸有APES切片黏合剂的载玻片上晾干,60℃中烤片3min左右,58℃中继续烤片18h,-20℃保存备用。
d、将切片脱蜡并水化,脱蜡利用二甲苯,水化通过梯度的酒精进行,具体为:组织切片依次经过二甲苯洗涤2次,每次10分钟、无水乙醇洗涤2次,每次5分钟、95%酒精洗涤2次,每次5分钟、75%酒精洗涤2次,每次5分钟,使组织切片表面的石蜡脱掉并充分水化,之后用自来水冲洗切片1min,用PBS缓冲液洗1分钟×3次;
e、EDTA抗原修复并封闭,将组织切片浸于由EDTA配制的抗原修复液(货号:P0085,碧云天,抗原修复液是根据试剂盒配置的,主要用于对福尔马林固定石蜡包埋的组织切片进行抗原修复,去除醛类固定试剂导致的蛋白之间的交联,充分暴露石蜡切片等样品中的抗原表位,从而大大改善免疫染色效果)中,于微波炉中高火档加热3分钟,然后中低档火加热4分钟×2次,取出后室温下冷却,用PBS缓冲液洗涤,5分钟×3次;用30%过氧化氢和甲醇配成的灭活液,将组织切片浸泡在灭活液中30分钟,以灭活内源性过氧化物酶后,用PBS缓冲液洗涤,5分钟×3次;将组织切片擦洗干净,在每张组织切片上滴加50微升的封闭液即5%的BSA水溶液,孵育30分钟,封闭非特异性抗原;
f、用抗人CUL9单克隆抗体(货号:NBP1-02783,NOVUS抗体公司),按照1:200稀释于PBS(磷酸缓冲盐溶液)后在4℃下过夜孵育,4℃PBS洗片后二抗(兔二抗:货号:ab6721;Abcam抗体公司,按照1:1000的比例稀释)室温孵育2小时;
g、室温下孵育30min,用DAB显色,然后使用苏木精染核,固定;
h、将组织切片依次经过75%酒精洗涤2次,每次5分钟、95%酒精洗涤2次,每次5分钟、无水乙醇洗涤2次,每次5分钟、二甲苯洗涤2次,每次10分钟;通风橱内放置5min,使组织切片上的二甲苯挥发,然后用中性树胶(货号:S30509,源叶生物)封片,封片之后在烘箱内放置1小时,使树胶尽快凝固;
i、结果分析:CUL9阳性染色为细胞胞浆上呈现棕黄色颗粒,由两人分别独立进行免疫组化评分,评分结果有异议时重新评估。对染色结果进行评分,包括两个指标:1)染色强度:0分(-):0%细胞染色;1分(+):0-10%细胞不完全染色;2分(++):10%细胞弱至中等完全染色;3分(+++):10%细胞中度至强烈完整的染色;2)阳性染色占全部视野的比例。两个指标的乘积为最终的免疫组化评分(表达量)(图2为代表性图片)。Cut-off值取表达量(免疫组织化学评分)的中位数。大于cut-off值为高表达,小于等于Cut-off值为低表达。
j、统计分析:此研究的所有数据均使用SPSS统计软件包(22.0;SPSS Inc.,Chicago,Illinois,USA)进行统计分析。OS的计算及分析使用Kaplan-Meier方法进行。危险因素表示为危险比[HR,95%置信区间(Confidence interval,CI)]。P值小于0.05被定义为有统计显著性。统计分析数据为CUL9免疫组化评分数据和及结直肠癌临床病理特征的相关性分析。
k、分析CUL9表达与结直肠癌患者临床相关性,结果如表1所示。
表1:CUL9表达与结直肠癌临床特征相关性分析
表1附录:CEA(癌胚抗原)检测为实施肿瘤手术之前检测血液而得。组织学类型,肿瘤大小,T分期,N分期,M分期均根据AJCC国际分期标准基于患者手术标本检测而得。
卡方检验分析了911例结直肠癌标本中CUL9表达与结直肠癌临床特征的相关性。结果显示CUL9高表达与肿瘤直径>4cm(P=0.001),肿瘤低分化(P=0.037),N1/2(P=0.028)和M1(P=0.001)正相关(肿瘤大小为手术标本的尺寸,取最长径;分化程度,T分期,N分期,M分期根据AJCC国际分期标准进行统计分析)。图3显示CUL9低表达与高表达的代表性图片。继续分析CUL9表达对于结直肠癌患者预后的评估作用,表2和图4显示生存分析显示CUL9高表达的CRC患者预后较差。
表2对于CRC的总生存期的单因素及多因素分析
表2附录:生存分析采用采用Kaplan-Meier法绘制生存曲线,采用Log-Rank比较差异。单因素/多因素分析采用Logistic回归计算风险比(Hazard ratio,OR)和相应的95%置信区间(Confidence interval,CI)。
单因素分析发现肿瘤低分化(P=0.001,HR=1.24,95%CI:1.05-1.46),T3/T4(P=0.001,HR=1.98,95%CI:1.62-2.24),N1/2(P=0.001,HR=1.83,95%CI:1.32-2.54),M1(P=0.001,HR=4.55,95%CI:3.69-5.66)以及CUL9蛋白高表达(P=0.001,HR=1.71,95%CI:1.45-2.34)都是导致OS缩短的因素。将以上有统计学差异的结果,多因素回归分析结果显示:T3/T4分期(P=0.001,HR=1.23,95%CI:1.03-1.67),N1/2分期(P=0.001,HR=1.51,95%CI:1.47-2.57),M1分期(P=0.001,HR=3.75,95%CI:2.83-4.56)以及CUL9蛋白高表达(P=0.001,HR=1.55,95%CI:1.38-2.04)都是影响CRC总生存期的独立危险因素。
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
- CUL9作为标志物在结直肠癌预后评价上的应用
- GPX4、NOX1和ACSL4在结直肠癌预后评价上的应用
