经涂布的药物组成物和其制备方法
文献发布时间:2023-06-19 18:32:25
技术领域
本公开内容关于经涂布的药物组成物和制备经涂布的药物组成物的方法。
背景技术
对于医药行业而言,开发活性医药成分(active pharmaceutical ingredient;API)的改进调配物是非常受关注的。调配物可以影响API的稳定性及生物利用度以及其他特性。调配物亦可以影响药物产品(drug product;DP)制造的各个方面,例如,制造工艺的容易性和安全性。
许多API的溶解性差。在批准的药物之中,约40%含有溶解性差的API。在开发中的化合物中溶解性差的化合物的百分比要高得多。溶解性差导致生物利用度差。非晶形式的API通常比结晶形式更易溶。因此,经常期望生产其中API是非晶而非结晶的并且在储存期间保持非晶的药物调配物。通常在聚合物中的API的非晶固体分散体(amorphous soliddispersion;ASD)可以稳定化API的非晶形式以防止结晶。ASD在过饱和溶解度、溶解、和改进的生物利用度方面具有优点。与API的结晶形式相比,ASD是热力学不稳定的。然而,聚合物基质例如通过在低于玻璃转变温度(Tg)时呈现较高黏度或经由药物聚合物相互作用来抑制重新结晶。ASD最经常通过热熔挤出、喷雾干燥或抗溶剂衬垫来产生。理想地,ASD将在ASD预期的保存期限期间是动力学稳定的,但大部分恢复到结晶形式。暴露于高湿度或高温显著增加ASD中的API的流动性并且降低聚合物抑制重新结晶的能力。在ASD中的API的结晶可以经由大量结晶和表面结晶两者发生。
发明内容
本文描述了一种制备包含经涂布的颗粒的医药组成物的方法,这些经涂布的颗粒包含由一个或多个金属氧化物层包封的活性药物成分(ASD颗粒)的非晶固体分散体,该方法包含以下顺序步骤:(a)提供包含活性医药成分和聚合物的非晶固体分散体的颗粒;(b)执行原子层沉积以将金属氧化物层施加到包含活性医药成分和聚合物的非晶固体分散体的颗粒上,从而制备包含由一个或多个金属氧化物层包封的活性医药成分的经涂布的颗粒;和(c)处理经涂布的颗粒以制备医药组成物。
在各个实施方式中:颗粒是至少50%、60%、65%、70%wt/wt的药物;颗粒具有基于空间平均值的0.1μm至200μm(例如,0.1μm至10μm或0.1μm至5μm)的D50;颗粒具有基于空间平均值的200μm至2000μm的D90;在经涂布的颗粒中的活性医药成分的玻璃转变温度高于在所提供的颗粒中的活性医药成分的玻璃转变温度;聚合物选自由以下组成的群组:羟丙基甲基纤维素、羟丙基甲基纤维素乙酸琥珀酸酯(HPMCAS)、和聚乙烯吡咯烷酮(PVP)、聚乙烯吡咯烷酮/乙酸乙烯酯(PVPVA)、聚乙二醇(PEG)、聚丙烯酸酯和聚甲基丙烯酸酯;步骤(a)包含通过热熔挤出来制备ASD颗粒;步骤(a)包含通过喷雾干燥制备ASD颗粒;
在各个实施方式中:执行原子层沉积的步骤包含:
(b1)将包含药物的颗粒装载到反应器中;
(b2)将蒸气或气态金属前驱物施加到反应器中的颗粒;
(b3)使用惰性气体执行反应器的一次或多次泵送净化循环;
(b4)将蒸气或气态氧化剂施加到反应器中的颗粒;和
(b5)使用惰性气体执行反应器的一次或多次泵送净化循环。
在各个实施方式中,在执行步骤(c)之前执行步骤(b2)至(b5)两次或更多次以增加金属氧化物层的总厚度;在步骤(a)之前和/或期间,搅拌反应器内容物;在步骤(b1)、步骤(b2)、和/或步骤(b4)之后使反应器压强稳定化;在步骤(b1)、步骤(b3)、和/或步骤(b5)之前和/或期间,搅拌反应器内容物;在步骤(b3)和/或步骤(b5)之前,泵出蒸气或气态内容物的子集;金属氧化物层具有在0.1nm至100nm(例如,0.1nm至50nm)的范围中的厚度;步骤(c)包含将经涂布的颗粒与一种或多种医药学上可接受的赋形剂组合;金属氧化物选自由以下组成的群组:氧化锌、氧化铝、氧化硅和氧化钛;步骤(b)在25℃与50℃之间的温度下发生;步骤(b)在25℃与100℃之间的温度下发生。
亦描述了包含经涂布的颗粒的医药组成物,这些经涂布的颗粒包含由一个或多个金属氧化物层包封的活性医药成分的非晶固体分散体,该医药组成物通过包含以下顺序步骤的方法制备:
(a)提供包含活性医药成分和聚合物的非晶固体分散体的颗粒;
(b)执行原子层沉积以将金属氧化物层施加到包含活性医药成分和聚合物的非晶固体分散体的颗粒,从而制备包含由一个或多个金属氧化物层包封的活性医药成分的经涂布的颗粒;和
(c)处理经涂布的颗粒以制备医药组成物。
在组成物的各个实施方式中,执行原子层沉积的步骤包含:
(b1)将包含药物的颗粒装载到反应器中;
(b2)将蒸气或气态金属前驱物施加到反应器中的颗粒;
(b3)使用惰性气体执行反应器的一次或多次泵送净化循环;
(b4)将蒸气或气态氧化剂施加到反应器中的颗粒;和
(b5)使用惰性气体执行反应器的一次或多次泵送净化循环。
在组成物的各个实施方式中:颗粒是至少50%、60%、65%、70%wt/wt的药物;颗粒具有基于空间平均值的0.1μm至200μm(例如,0.1μm至10μm或0.1μm至5μm)的D50;颗粒具有基于空间平均值的200μm至2000μm的D90;在经涂布的颗粒中的活性医药成分的玻璃转变温度高于在所提供的颗粒中的活性医药成分的玻璃转变温度;聚合物选自由以下组成的群组:羟丙基甲基纤维素、羟丙基甲基纤维素乙酸琥珀酸酯、和聚乙烯吡咯烷酮、聚乙烯吡咯烷酮/乙酸乙烯酯、聚乙二醇(PEG)、聚丙烯酸酯和聚甲基丙烯酸酯;步骤(a)包含通过热熔挤出制备ASD颗粒;步骤(a)包含通过喷雾干燥制备ASD颗粒;
在各个实施方式中:执行原子层沉积的步骤包含:
(b1)将包含药物的颗粒装载到反应器中;
(b2)将蒸气或气态金属前驱物施加到反应器中的颗粒;
(b3)使用惰性气体执行反应器的一次或多次泵送净化循环;
(b4)将蒸气或气态氧化剂施加到反应器中的颗粒;和
(b5)使用惰性气体执行反应器的一次或多次泵送净化循环。
在各个实施方式中,在执行步骤(c)之前执行步骤(b2)至(b5)两次或更多次以增加金属氧化物层的总厚度;在步骤(a)之前和/或期间,搅拌反应器内容物;在步骤(b1)、步骤(b2)、和/或步骤(b4)之后使反应器压强稳定化;在步骤(b1)、步骤(b3)、和/或步骤(b5)之前和/或期间,搅拌反应器内容物;在步骤(b3)和/或步骤(b5)之前,泵出蒸气或气态内容物的子集;金属氧化物层具有在0.1nm至100nm的范围中的厚度;步骤(c)包含将经涂布的颗粒与一种或多种医药学上可接受的赋形剂组合;金属氧化物选自由以下组成的群组:氧化锌、氧化铝、氧化硅和氧化钛;步骤(b)在25℃与50℃之间的温度下发生;步骤(b)在25℃与50℃之间的温度下发生。
在涂布之前,颗粒可具有基于空间平均值的在0.01μm与1000μm之间的中值粒度。
医药组成物可从反应器移除并且与一种或多种医药学上可接受的稀释剂或载剂混合。
在涂布之前,颗粒可基本上由API组成。
一种或多种氧化物材料包括氧化硅和各种金属氧化物,包括:氧化铝、氧化钛、氧化铁、氧化镓、氧化镁、氧化锌、氧化铌、氧化铪、氧化钽、氧化镧、和/或二氧化锆。
氧化剂可选自水、臭氧、和有机过氧化物的群组。
除非另外定义,否则本文使用的所有技术和科学术语具有与本发明所属领域中的技术人员通常理解的相同的含义。本文描述了用于本发明的方法和材料;亦可以使用本领域中已知的其他适宜方法和材料。材料、方法、和实例仅是说明性并且不意欲为限制性。
本发明的其他特征结构和优点将从以下详细描述和附图,并且从权利要求显而易见。
附图说明
图1是用于颗粒(例如,ASD颗粒)的ALD涂布的旋转反应器的示意图。
图2描绘了未涂布和金属氧化物涂布的ASD颗粒的x射线衍射分析的结果。
图3描绘了未涂布和金属氧化物涂布的ASD颗粒的测量差示扫描量热(differential scanning calorimetry;DSC)分析的结果。
图4描绘了未涂布和金属氧化物涂布的ASD颗粒的扫描电子显微镜影像。
图5描绘了未涂布和金属氧化物涂布的ASD颗粒的体积密度和振实密度分析的结果。
图6描绘了未涂布和金属氧化物涂布的ASD颗粒的吸湿分析的结果。
图7描绘了在加速稳定性测试下的未涂布和金属氧化物涂布的ASD颗粒的x射线衍射分析的结果。
图8描绘了在加速稳定性测试下的未涂布的ASD颗粒的x射线衍射分析的结果。
图9描绘了在加速稳定性测试下的未涂布和金属氧化物涂布的ASD颗粒的测量差示扫描量热(DSC)分析的结果。
图10A至图10B描绘了在加速稳定性测试下的未涂布和金属氧化物涂布的ASD颗粒的扫描电子显微镜影像。
图11A至图11B描绘了在加速稳定性测试下的未涂布和金属氧化物涂布的ASD颗粒的扫描电子显微镜影像。
图12描绘了在加速稳定性测试下的未涂布和金属氧化物涂布的ASD颗粒的溶解分析的结果。
图13描绘了在加速稳定性测试下的未涂布和金属氧化物涂布的ASD颗粒的溶解分析的结果。
图14描绘了在40℃和75%相对湿度下储存8个月之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的外观。
图15描绘了在40℃和75%相对湿度下储存不同时间段(12天、47天、210天、240天和270天)之后的未涂布和金属氧化物涂布的50%DL(药物装载的)ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的扫描电子显微镜影像。
图16描绘了在40℃和75%相对湿度下储存不同时间段(12天、61天、180天、210天、240天和270天)之后的未涂布和金属氧化物涂布的70%DL ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的扫描电子显微镜影像。
图17描绘了在40℃和75%相对湿度下储存9个月之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的x射线衍射分析的结果。如图17所示,对于具有50%API装载的未涂布的ASD,存在约25%的结晶度,对于具有70%API装载的未涂布的ASD,存在约50%的结晶度,并且对于大部分经涂布的样品不存在结晶。
图18描绘了在40℃和75%相对湿度下储存各个持续时间之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的释放研究的结果。
图19描绘了在40℃和75%相对湿度下储存一年之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的扫描电子显微镜影像。
图20描绘了在40℃和75%相对湿度下储存一年之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的x射线衍射分析的结果。
图21A和图21B描绘了在40℃和75%相对湿度下储存各个持续时间之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的溶解分析的结果。图21C描绘了在室温或40℃和75%相对湿度下储存一年之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的溶解分析的结果。
图22描绘了具有60%药物装载的金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的SEM和TEM/FIB截面影像。
图23描绘了具有60%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的粉末流动性表征。
图24描绘了具有60%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的x射线衍射分析的结果。
图25A和图25B描绘了具有60%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的FTIR分析的结果。
图26A至图26C描绘了具有50%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)的涂层厚度、氧化物含量、SEM影像、和TEM影像。图26B描绘了未涂布的ASD(EP50-15)、薄涂布的ASD(B3-284A)和厚涂布的ASD(B3-284B)的SEM影像。图26C描绘了未涂布的ASD(EP50-15)的截面的TEM影像。
图27描绘了在40℃下具有50%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)的吸湿。
图28描绘了在40℃和43%相对湿度下在加盖玻璃瓶中储存4周的具有50%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)的x射线衍射分析的结果。
图29描绘了在40℃和43%相对湿度下在开口瓶中储存4周的具有50%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)的扫描电子显微镜影像。
图30A描绘了新鲜制备的具有50%(SF20000521)和70%(SF20000611)药物装载的各种未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的硝苯地平和水含量的测定。图30B描绘了经涂布的50%和70%的DL ASD颗粒的截面的TEM影像。
图31描绘了具有50%(SF20000521)和70%(SF20000611)药物装载的新鲜制备的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的外观。
图32A至图32F描绘了具有50%(SF20000521)及70%(SF20000611)药物装载的PVP、硝苯地平、未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的x射线衍射分析的结果。
图33A至图33D描绘了在加盖的琥珀色玻璃瓶中、用感应密封的加盖的HDPE瓶、或无盖的开口HDPE瓶中储存的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的测定、吸湿和杂质分析。
图34描绘了在40℃和75%相对湿度下在无盖的开口HDPE瓶中储存各个持续时间的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的外观。
图35描绘了在用加盖的感应密封的HDPE瓶中储存各个持续时间的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的外观。
图36描绘了在加盖的琥珀色瓶中储存各个持续时间的具有50%(SF20000521)及70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的外观。
图37描绘了在25℃和60%相对湿度下在加盖的琥珀色瓶中储存3个月的具有50%(SF20000521)及70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的x射线衍射分析的结果。
图38描绘了在40℃和75%相对湿度下在加盖的用感应密封的HDPE瓶中储存3个月的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的x射线衍射分析的结果。
图39描绘了在40℃和75%相对湿度下在无盖的开口HDPE瓶中储存3个月的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的x射线衍射分析的结果。
图40A至图40C描绘了在40℃和75%相对湿度下在无盖的开口HDPE瓶中新鲜制备的、储存2个月之后、或储存3个月之后的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/HPMCAS)的扫描电子显微镜影像。图40A描绘了未涂布的ASD的影像,观察到完全胶凝和结晶。图40B描绘了具有涂布的50%药物装载的ASD且图40C描绘了具有70%药物装载的经涂布的ASD。在40℃和75%相对湿度下储存3个月之后,对于具有50%或70%药物装载的经涂布的ASD两者,没有观察到结晶。
具体实施方式
本公开提供了制备包含用一层或多层氧化物(例如,金属氧化物)涂布的非晶固体分散体(ASD)的颗粒(“ASD颗粒”)的医药组成物的方法。涂布层是保形的且具有受控的厚度。本文所述的涂布工艺可以提供ASD颗粒,其中API的结晶被显著抑制。重要的是,涂层可以降低对ASD中的聚合物的高重量百分比的需要。这允许制备具有高药物装载的ASD颗粒。例如,ASD颗粒可以具有50%、60%、或70%wt/wt的药物装载。颗粒的此高药物装载连同氧化物涂层的相对厚度允许制备医药组成物。因为涂层相对较薄,可以生产具有高药物装载的药物产品。例如,金属氧化物层可以具有在0.1nm至100nm的范围中的厚度。此外,氧化物涂层可以改进与药物产品制造的各个方面有关的ASD颗粒的特性。例如,与其他相同的未涂布的ASD颗粒相比,经涂布的ASD颗粒可以具有改进的流动性和可压缩性。此外,与其他相同的未涂布的ASD颗粒相比,经涂布的ASD颗粒可以具有降低的附聚趋势。最后,因为多个涂层可以在相同反应器中施加,所以存在关于成本和制造容易性的益处。
药物
术语“药物”在它的最广义上包括所有小分子(例如,非生物学的)API,特别是作为有机分子的API。药物可以选自由下列组成的群组:镇痛剂、麻醉剂、消炎剂、驱虫剂、抗心律失常剂、抗哮喘剂、抗生素、抗癌剂、抗凝血剂、抗抑郁药、抗糖尿病剂、抗癫痫剂、抗组胺剂、镇咳剂、抗高血压剂、抗毒蕈碱剂、抗分枝杆菌剂、抗肿瘤剂、抗氧化剂、退热剂、免疫抑制剂、免疫刺激剂、抗甲状腺剂、抗病毒剂、抗焦虑镇静剂、催眠药、精神抑制药、收敛剂、抑菌剂、β-肾上腺素受体阻断剂、血液制品、血液替代物、支气管扩张剂、缓冲剂、心脏正性肌力剂、化学治疗剂、造影剂、皮质类固醇、咳嗽抑制剂、祛痰剂、黏液溶解剂、利尿剂、多巴胺能、抗帕金森剂、自由基清除剂、生长因子、止血剂、免疫剂、脂质调节剂、肌肉松弛剂、拟副交感神经剂、甲状旁腺降钙素、双膦酸盐、前列腺素、放射性药物、激素、性激素、抗过敏剂、食欲刺激剂、食欲抑制剂、类固醇、拟交感神经剂、甲状腺剂、疫苗、血管扩张剂和黄嘌呤。
小分子药物的示例性类型包括但不限于对乙酰胺基酚、克拉霉素、阿奇霉素、布洛芬、丙酸氟替卡松、沙美特罗、盐酸帕唑帕尼、帕博西尼、和阿莫西林克拉维酸钾。
金属氧化物材料
术语“金属氧化物材料”在它的最广义上包括由被认为是金属或类金属的元素与基于氧的氧化剂的反应形成的所有材料。示例性金属氧化物材料包括但不限于氧化铝、二氧化钛、氧化铁、氧化镓、氧化镁、氧化锌、氧化铌、氧化铪、氧化钽、氧化镧、和二氧化锆。氧化硅是通过类金属与基于氧的氧化剂之间的反应产生的金属氧化物的实例。示例性氧化物包括但不限于水、臭氧、和无机过氧化物。
原子层沉积(ALD)
原子层沉积是薄膜沉积技术,其中元素或化合物的自限制单层的顺序添加允许沉积厚度和均匀性控制在原子或分子单层的水平的膜。自限制意味着一次仅形成单个原子层,并且需要后续处理步骤来再生表面且允许进一步的沉积。
反应器系统
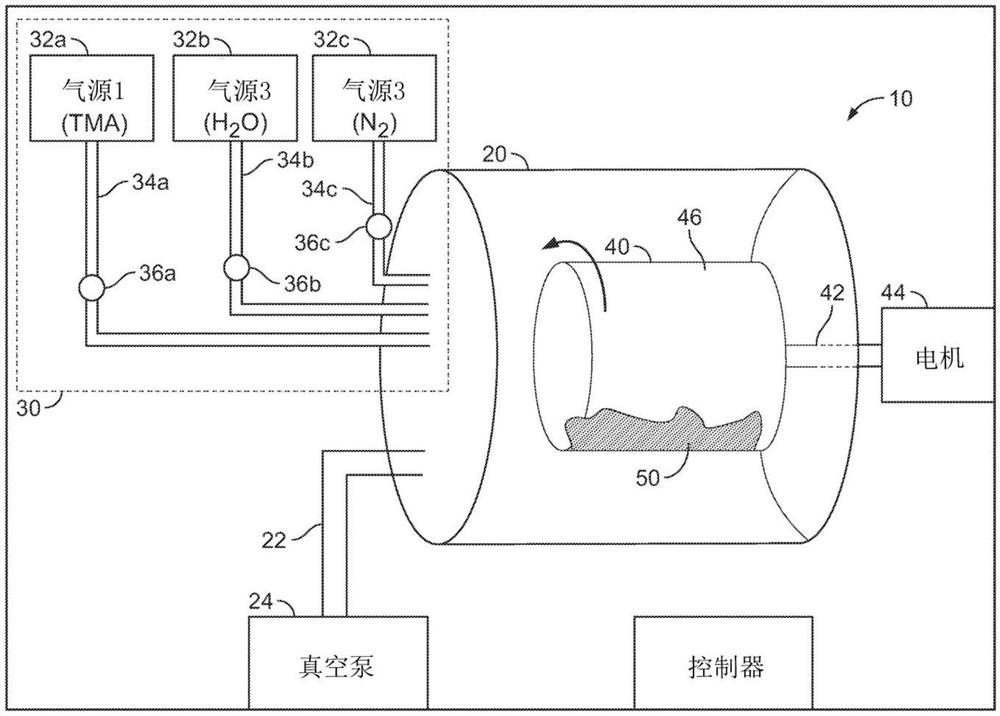
术语“反应器系统”在它的最广义上包括可以用于执行ALD的所有系统。示例性反应器系统在图1中示出并且在下文进一步描述。
图1示出了用于执行用薄膜涂层涂布颗粒的反应器系统10。反应器系统10可以执行ALD涂布。反应器系统10允许在较高(高于50℃,例如,50-100℃或更高)或较低处理温度(例如,低于50℃,例如,处于或低于35℃)下执行ALD涂布。例如,反应器系统10可以主要在22至35℃(例如,25至35℃、25至30℃、或30至35℃)的温度下通过ALD在颗粒上形成薄膜金属氧化物。通常,颗粒可以保持或维持在此种温度下。这可以通过使反应物气体和/或反应器腔室(例如,下文论述的腔室20和滚筒40)的内表面保持或维持在这种温度下来实现。
再者,在说明ALD工艺的情况下,反应器系统10包括通过真空管22耦接到真空泵24的固定真空腔室20。真空泵24可以是足以建立小于1Torr(例如,1至100mTorr,例如,50mTorr)的压强的工业真空泵。真空泵24允许将腔室20维持在期望压强下并且允许移除反应副产物和未反应的处理气体。
在操作中,反应器10通过将涂层的气态前驱物引入腔室20中来执行ALD薄膜涂布工艺。气态前驱物交替地掺加到反应器中。这允许ALD工艺是无溶剂工艺。ALD工艺的半反应是自限制的,此可以提供沉积的埃级控制。此外,ALD反应可以在低温条件下执行,诸如低于50℃,例如,低于35℃。
腔室20亦耦接到化学递送系统30。化学递送腔室30包括通过相应的递送管34a、34b、34c和可控阀36a、36b、36c耦接到真空腔室20的三个或多个气源32a、32b、32c。化学递送系统30可以包括限流器、气流控制器、压强传感器和超声流量计的组合,以提供到腔室20中的各种气体的可控流动速率。化学递送系统30亦可以包括一个或多个温度控制部件,例如,热交换器、电阻式加热器、热灯等,用于在各种气体流入腔室20中之前加热或冷却该等气体。尽管图1示出了与每个气源的腔室平行延伸的分离的气体管线,在组合的管线到达腔室20之前,两个或多个气体管线可以例如通过一个或多个三通阀连接。此外,尽管图1示出了三个气源,使用四个气源可以实现原位形成具有两种不同金属氧化物的交替层的层压结构。
两个气源将用于涂布工艺的两种化学上不同的气态反应物提供到腔室20。用于ALD方法的适宜反应物包括以下各项的任何一个或组合:单体蒸气、金属有机物、金属卤化物、氧化剂(诸如臭氧或水蒸气)、和聚合物或纳米颗粒气溶胶(干的或湿的)。例如,第一气源32a可以提供气态三甲基铝(TMA)或四氯化钛(TiCl
气源之一可以提供净化气体。特定而言,第三气源可以提供对反应物、涂层、和所处理的颗粒化学惰性的气体。例如,净化气体可以是N
可旋转涂布滚筒40固持在腔室20内部。滚筒40可以通过驱动轴件42连接,驱动轴件42穿过腔室20的侧壁中的密封口延伸到电机44。电机44可以1至100rpm的速度旋转滚筒。或者,滚筒可以穿过旋转接头直接连接到真空源。
待涂布的颗粒(图示为颗粒床50)放置在滚筒40的内部空间46中。滚筒40和腔室20可以包括可密封口(未示出)以允许将颗粒放置到滚筒40中并且从滚筒40移除。
滚筒40的主体由多孔材料、实体金属、和穿孔金属中的一种或多种提供。穿过滚筒40的圆柱形侧壁的孔可以具有10μm的尺寸。
在操作中,随着滚筒40旋转,气体之一从化学递送系统30流入腔室20中。涂布滚筒40中的孔(pore)(1至100μm)、孔洞(hole)(0.1至10mm)、或大的开口(opening)的组合用于将颗粒限制在涂布滚筒40中,同时允许快速递送前驱物化学物质和泵送副产物或未反应的物质。归因于滚筒40中的孔,气体可以在滚筒40的外部(亦即,反应器腔室20)与滚筒40的内部之间流动。此外,滚筒40的旋转搅拌颗粒以保持颗粒分离,从而确保颗粒的大表面积保持暴露。这允许颗粒表面与处理气体的快速、均匀的相互作用。
在一些实施方式中,一个或多个温度控制部件整合到滚筒40中以允许控制滚筒40的温度。例如,电阻式加热器、热电冷却器、或其他部件可以在滚筒40的侧壁中或侧壁上。
反应器系统10亦包括耦接到各种可控部件(例如,真空泵24、气体分配系统30、电机44、温度控制系统等)以控制反应器系统10的操作的控制器60。控制器60亦可以耦接到各种传感器,例如,压强传感器、流量计等,以提供对腔室20中的气体压强的闭合循环控制。
通常,控制器60可以根据“制作方法”操作反应器系统10。制作方法为每个可控元件指定随时间变化的操作值。例如,制作方法可以指定真空泵24操作的持续时间,每个气源32a、32b、32c的时间和流动速率,电机44的旋转速率等。控制器60可以接收制作方法作为计算机可读数据(例如,储存在非暂时性计算机可读介质上)。
本文描述的系统的控制器60和其他计算装置可以在数字电子电路系统中、或者在计算机软件、韧体、或硬件中实施。例如,控制器可以包括处理器,用于执行在计算机程序产品中(例如,在非暂时性机器可读储存介质中)储存的计算机程序。这种计算机程序(亦称为程序、软件、软件应用、或代码)可以任何形式的可程序化语言写入,包括编译或解释语言,并且这种计算机程序可以任何形式部署,包括作为独立式程序或作为适于在计算环境中使用的模块、部件、子例程、或其他单元。在一些实施方式中,控制器60是通用可程序化计算机。在一些实施方式中,控制器可以使用专用逻辑电路实施,例如,FPGA(现场可程序化门阵列)或ASIC(特殊应用集成电路)。
操作
最初,将颗粒装载到反应器系统10中的滚筒40中。颗粒可以具有包含药物(例如,上文论述的药物之一)的实体芯(solid core)。一旦密封任何出入口,控制器60根据制作方法操作反应器系统10,以便在颗粒上形成薄膜金属氧化物层。
特定而言,两种反应物气体交替地供应到腔室20,供应反应物气体的步骤之后是净化循环,其中将惰性气体供应到腔室20以排出在先前步骤中使用的反应物气体和副产物。此外,一种或多种气体(例如,反应物气体和/或惰性气体)可以以脉冲的方式供应,其中腔室20用气体填充到指定压强,允许经过延迟时间,并且腔室在下一脉冲开始之前由真空泵24抽空。
特定而言,控制器60可以如下操作反应器系统10。
在第一反应物半循环中,在电机44旋转滚筒40以搅拌颗粒50时:
i)操作气体分配系统30以使第一反应物气体(例如,TMA)从源32a流入腔室20中,直到实现第一指定压强。指定压强可以是0.1Torr至反应物气体的饱和压强的一半。
ii)暂停第一反应物的流动,并且允许经过指定延迟时间,例如,如通过控制器中的定时器测量。这允许第一反应物流过滚筒40中的颗粒床并且与滚筒40内部的颗粒50的表面反应。
iii)真空泵50抽空腔室20,例如,抽空到低于1Torr的压强,例如,到1至100mTorr,例如,50mTorr。
这些步骤(i)至(iii)可以重复由制作方法设定的次数,例如,两次到十次,例如,六次。
接下来,在第一净化循环中,在电机44旋转滚筒以搅拌颗粒50时:
iv)操作气体分配系统30以使惰性气体(例如,N
v)暂停惰性气体的流动,并且允许经过指定延迟时间,例如,如由控制器中的定时器所测量。这允许惰性气体流过滚筒40中的孔,并且穿过颗粒50扩散以替换反应物气体和任何蒸气副产物。
vi)真空泵50抽空腔室20,例如,抽空到低于1Torr的压强,例如,到1至500mTorr,例如,50mTorr。
这些步骤(iv)至(vi)可以重复由制作方法设定的次数,例如,六次到二十次,例如,十六次。
在第二反应物半循环中,在电机44旋转滚筒40以搅拌颗粒50时:
vii)操作气体分配系统30以使第二反应物气体(例如,H2O)从源32a流入腔室20中,直到实现第三指定压强。第三压强可以是0.1Torr至反应物气体的饱和压强的一半。
viii)暂停第二反应物的流动,并且允许经过指定延迟时间,例如,如由控制器中的定时器所测量。这允许第二反应物流过滚筒40中的孔并且与滚筒40内部的颗粒50的表面反应。
ix)真空泵50抽空腔室20,例如,抽空到低于1Torr的压强,例如,到1至500mTorr,例如,50mTorr。
这些步骤(vii)至(ix)可以重复由制作方法设定的次数,例如,两次至十次,例如,六次。
接下来,执行第二净化循环。该第二净化循环可以与第一净化循环相同,或可以具有不同的步骤(iv)至(vi)的重复次数和/或不同延迟时间和/或不同压强。
第一反应物半循环、第一净化循环、第二反应物半循环和第二净化循环的循环可以重复由制作方法设定的次数,例如,一次到十次。
如上所述,涂布工艺可以在低处理温度(例如,低于50℃,例如,处于或低于35℃)下执行。特定而言,在上文所述的所有步骤(i)至(ix)期间,颗粒可以保持或维持在这种温度下。通常,在步骤(i)至(ix)期间,反应器腔室的内部空间的温度不超过35℃。此可以通过在相应循环期间在这种温度下将第一反应物气体、第二反应物气体和惰性气体注入腔室中来实现。此外,若需要,可以例如使用冷却系统(例如,热电冷却器)将腔室的实体部件保持或维持在这种温度下。
用于制备包含由一层或多层金属氧化物封装的药物的医药组成物的工艺
提供了用于包含由一种或多种金属氧化物材料包封的含药物芯(ASD颗粒)的医药组成物的两种示例性方法。第一示例性方法包括以下顺序步骤:(a)将包含药物的颗粒装载到反应器中,(b)将蒸气或气态金属前驱物施加到反应器中的基板,(c)使用惰性气体执行反应器的一次或多次泵送净化循环,(d)将蒸气或气态氧化剂施加到反应器中的基板,和(e)使用惰性气体执行反应器的一次或多次泵送净化循环。在第一示例性方法的一些实施方式中,顺序步骤(b)至(e)视情况重复一次或多次以增加包封经涂布的颗粒的实体芯的一种或多种金属氧化物材料的总厚度。在一些实施方式中,在步骤(a)、步骤(b)、和/或步骤(d)之后使反应器压强稳定化。在一些实施方式中,在步骤(b)、步骤(c)和/或步骤(e)之前和/或期间搅拌反应器内容物。在一些实施方式中,在步骤(c)和/或步骤(e)之前泵出蒸气或气态内容物的子集。
第二示例性方法包括(例如,由以下顺序步骤组合)以下顺序步骤:(a)将包含药物的颗粒装载到反应器中,(b)将反应器压强降低至小于1Torr,(c)搅拌反应器内容物,直到反应器内容物具有期望的水分含量,(d)通过添加蒸气或气态金属前驱物来将反应物加压到至少10Torr,(e)使稳定反应器压强稳定化,(f)搅拌反应器内容物,(g)泵出蒸气或气态内容物的子集并且基于反应器中的内容物的分析决定何时停止泵送,该内容物包括金属前驱物和与基板上或颗粒表面上暴露的羟基残留物反应的金属前驱物的副产物,(h)使用惰性气执行反应器的泵送净化循环的序列,(i)通过添加蒸气或气态氧化剂将反应器加压到至少10Torr,(j)使反应器压强稳定化,(k)搅拌反应器内容物,(I)泵出蒸气或气态内容物的子集,并且基于反应器中的内容物的分析决定何时停止泵送,该内容物包括金属前驱物、与基板上或颗粒表面上暴露的羟基残留物反应的金属前驱物的副产物、和未反应的氧化物,和(m)使用惰性气体执行反应器的泵送净化循环的序列。在第二示例性方法的一些实施方式中,顺序步骤(b)-(m)视情况重复一次或多次以增加包封经涂布的颗粒的实体芯的一种或多种金属氧化物材料的总厚度。
一些实施方式提供了制备包含经涂布的颗粒的医药组成物的方法,这些经涂布的颗粒包含由一个或多个金属氧化物层包封的活性医药成分的非晶固体分散体,该方法包含以下顺序步骤:(a)提供包含活性医药成分(API)和聚合物的非晶固体分散体的未涂布的颗粒;(b)执行原子层沉积以将金属氧化物层施加到包含活性医药成分和聚合物的非晶固体分散体的未涂布的颗粒,从而制备包含由一个或多个金属氧化物层包封的活性医药成分的经涂布的颗粒;和(c)处理经涂布的颗粒以制备医药组成物。
在一些实施方式中,未涂布的颗粒是至少50%wt/wt的API。在一些实施方式中,未涂布的颗粒是至少70%wt/wt的API。在一些实施方式中,经涂布的颗粒具有基于空间平均值的0.5μm至200μm的D50。在一些实施方式中,经涂布的颗粒具有基于空间平均值的200μm至2000μm的D90。
在一些实施方式中,在经涂布的颗粒中的活性医药成分的玻璃转变温度高于在所提供的颗粒中的活性医药成分的玻璃转变温度。
在一些实施方式中,聚合物选自由下列组成的群组:羟丙基甲基纤维素、羟丙基甲基纤维素乙酸琥珀酸酯(HPMCAS)、和聚乙烯吡咯烷酮(PVP)、聚乙烯吡咯烷酮/乙酸乙烯酯、聚乙二醇(PEG)、聚丙烯酸酯和聚甲基丙烯酸酯。
在一些实施方式中,步骤(a)包含热熔挤出。在一些实施方式中,步骤(a)包含喷雾干燥包含聚合物和活性医药成分的组成物。在一些实施方式中,在步骤(a)之前和/或期间搅拌聚合物和活性医药成分。
在一些实施方式中,执行原子层沉积的步骤包含:(b1)将包含药物的颗粒装载到反应器中;(b2)将蒸气或气态金属前驱物施加到反应器中的颗粒;(b3)使用惰性气体执行反应器的一次或多次泵送净化循环;(b4)将蒸气或气态氧化剂施加到反应器中的颗粒;和(b5)使用惰性气体执行反应器的一次或多次泵送净化循环。在一些实施方式中,在执行步骤(c)之前,执行步骤(b2)至(b5)两次或更多次以增加金属氧化物层的总厚度。
在一些实施方式中,在步骤(b1)、步骤(b2)、和/或步骤(b4)之后使反应器压强稳定化。在一些实施方式中,在步骤(b1)、步骤(b3)、和/或步骤(b5)之前和/或期间,搅拌反应器内容物。在一些实施方式中,在步骤(b3)和/或(b5)之前泵出蒸气或气态内容物的子集。在一些实施方式中,步骤(b)在35℃与50℃之间的温度下发生。在一些实施方式中,步骤(c)包含将经涂布的颗粒与一种或多种医药学上可接受的赋形剂组合。
在一些实施方式中,金属氧化物层具有在0.1nm至100nm的范围中的厚度。
在一些实施方式中,金属氧化物选自由下列组成的群组:氧化锌、氧化铝、氧化硅和氧化钛。在一些实施方式中,金属氧化物是氧化铝。在一些实施方式中,金属氧化物选自由氧化铝和氧化钛组成的群组。在一些实施方式中,API选自由依泽替米贝、厄洛替尼和硝苯地平组成的群组。在一些实施方式中,聚合物选自由HPMCAS、PVPVA和PVP组成的群组。
在一些实施方式中,在储存期间,步骤(b)中的经涂布的颗粒与步骤(a)中的未涂布的颗粒相比更不易于附聚。在一些实施方式中,在储存期间,步骤(b)中的经涂布的颗粒与步骤(a)中的未涂布的颗粒相比保持非晶达更长的时间。在一些实施方式中,步骤(b)中的经涂布的颗粒与步骤(a)中的未涂布的颗粒相比吸湿性较小。在一些实施方式中,在储存期间,步骤(b)中的经涂布的颗粒显示出与步骤(a)中的未涂布的颗粒相比较慢的结晶。
一些实施方式提供了包含经涂布的颗粒的医药组成物,这些经涂布的颗粒包含由一个或多个金属氧化物层包封的活性医药成分的非晶固体分散体,该医药组成物通过包含以下顺序步骤的方法制备:(a)提供包含活性医药成分和聚合物的非晶固体分散体的未涂布的颗粒;(b)执行原子层沉积以将金属氧化物层施加到包含活性医药成分和聚合物的非晶固体分散体的未涂布的颗粒,从而制备包含由一个或多个金属氧化物层包封的活性医药成分的经涂布的颗粒;和(c)处理经涂布的颗粒以制备医药组成物。
在一些实施方式中,执行原子层沉积的步骤包含:
(b1)将包含药物的颗粒装载到反应器中;(b2)将蒸气或气态金属前驱物施加到反应器中的颗粒;(b3)使用惰性气体执行反应器的一次或多次泵送净化循环;(b4)将蒸气或气态氧化剂施加到反应器中的颗粒;和(b5)使用惰性气体执行反应器的一次或多次泵送净化循环。
在一些实施方式中,在执行步骤(c)之前,执行步骤(b2)至(b5)两次或更多次以增加金属氧化物层的总厚度。在一些实施方式中,在步骤(a)之前和/或期间搅拌聚合物和活性医药成分。在一些实施方式中,在步骤(b1)、步骤(b2)、和/或步骤(b4)之后使反应器压强稳定化。在一些实施方式中,在步骤(b1)、步骤(b3)、和/或步骤(b5)之前和/或期间,搅拌反应器内容物。在一些实施方式中,在步骤(b3)和/或步骤(b5)之前泵出蒸气或气态内容物的子集。在一些实施方式中,步骤(b)在35℃与50℃之间的温度下发生。
在一些实施方式中,金属氧化物层具有在0.1nm至100nm的范围中的厚度。在一些实施方式中,未涂布的颗粒具有基于空间平均值的在0.1μm与1000μm之间的中值粒度。
在一些实施方式中,包含活性医药成分的经涂布的颗粒进一步包含一种或多种医药学上可接受的赋形剂。在一些实施方式中,未涂布的颗粒由活性医药成分组成。
在一些实施方式中,金属氧化物选自由氧化铝和氧化钛组成的群组。在一些实施方式中,API选自由依泽替米贝、厄洛替尼和硝苯地平组成的群组。在一些实施方式中,聚合物选自由HPMCAS、PVPVA和PVP组成的群组。
在一些实施方式中,在储存期间,步骤(b)中的经涂布的颗粒与步骤(a)中的未涂布的颗粒相比更不易于附聚。在一些实施方式中,在储存期间,步骤(b)中的经涂布的颗粒与步骤(a)中的未涂布的颗粒相比保持非晶达更长的时间。在一些实施方式中,步骤(b)中的经涂布的颗粒与步骤(a)中的未涂布的颗粒相比吸湿性较小。在一些实施方式中,在储存期间,步骤(b)中的经涂布的颗粒显示出与步骤(a)中的未涂布的颗粒相比较慢的结晶。
医药学上可接受的赋形剂、稀释剂、和载剂
医药学上可接受的赋形剂包括但不限于:
(1)表面活性剂和聚合物,包括:聚乙二醇(PEG)、聚乙烯吡咯烷酮(PVP)、十二烷基硫酸钠、聚乙烯醇、交联聚维酮、聚乙烯基吡咯烷酮-聚乙烯基丙烯酸酯共聚物(PVPVA)、纤维素衍生物、羟丙基甲基纤维素、羟丙基纤维素、羧基甲基乙基纤维素、羟丙基甲基纤维素邻苯二甲酸酯、聚丙烯酸酯及聚甲基丙烯酸酯、尿素、糖、多元醇、增稠剂和它们的聚合物、乳化剂、糖胶、淀粉、有机酸和它们的盐。
(2)黏合剂,诸如纤维素、交联的聚乙烯吡咯烷酮、微晶纤维素;
(3)填充剂,诸如乳糖一水合物、无水乳糖、微晶纤维素和各种淀粉;
(4)润滑剂,诸如作用于待压制的粉末的流动性的试剂,包括胶体二氧化硅、滑石、硬脂酸、硬脂酸镁、硬脂酸钙、硅胶;
(5)甜味剂,诸如任何天然或人造的甜味剂,包括蔗糖、木糖醇、糖精钠、环己胺磺酸盐、阿斯巴甜和乙酰舒泛K;
(6)调味剂;
(7)防腐剂,诸如山梨酸钾、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、苯甲酸和它的盐、对羟基苯甲酸的其他酯,诸如对羟基苯甲酸丁酯,醇,诸如乙醇或苯甲醇,酚类化学品,诸如苯酚,或四元化合物,诸如苯扎氯铵;
(8)缓冲剂;
(9)稀释剂,诸如医药学上可接受的惰性填充剂,诸如微晶纤维素、乳糖、磷酸氢钙、糖类、和/或任何前述的混合物;
(10)润湿剂,诸如小麦淀粉、马铃薯淀粉、玉米淀粉、和改性淀粉、和它们的混合物;
(11)崩解剂,诸如交联羧甲基纤维素钠、交联聚维酮、淀粉羟乙酸钠;和
(12)泡腾剂,诸如泡腾剂对,诸如有机酸(例如,柠檬酸、酒石酸、苹果酸、富马酸、己二酸、琥珀酸、和海藻酸和酸酐和酸式盐)、或碳酸盐(例如,碳酸钠、碳酸钾、碳酸镁、甘胺酸碳酸钠、L-离胺酸碳酸盐及精胺酸碳酸盐)或碳酸氢盐(例如,碳酸氢钠或碳酸氢钾)。
实例
在实例中使用以下材料和方法。
为了施加氧化铝涂层,蒸气或气态金属前驱物是三甲基铝(TMA),在TMA与颗粒上或经涂布的颗粒的表面上暴露的羟基反应之后形成副产物气态甲烷,并且氧化剂是水蒸气。
简而言之,用于产生Al
(a)将包含药物的颗粒装载到反应器中;
(b)将反应器压强降低到小于1Torr;
(c)通过执行残留气体分析(residual gas analysis;RGA)以监控反应器中的水蒸气的水平,搅拌反应器内容物,直到反应器内容物具有期望的水含量;
(d)通过添加蒸气或气态TMA将反应器加压到至少1Torr;
(e)使反应器压强稳定化;
(f)搅拌反应器内容物;
(g)泵出包括气态甲烷和未反应的TMA的蒸气或气态内容物的子集,并且通过执行RGA以监控反应器中的气态甲烷和未反应的TMA的水平来决定何时停止泵送;
(h)使用氮气对反应器执行泵送净化循环的序列;
(i)通过添加水蒸气将反应器加压到至少1Torr;
(j)使反应器压强稳定化;
(k)搅拌反应器内容物;
(I)泵出包括水蒸气的蒸气或气态内容物的子集,并且通过执行RGA以监控反应器中的水蒸气的水平来决定何时停止泵送;和
(m)使用氮气对反应器执行泵送净化循环的序列。
在一些情况下,步骤(b)至(m)重复一次以上以增加包封药物颗粒芯的金属氧化物的总厚度。TiO
实例1:与未涂布的ASD颗粒相比,金属氧化物涂布的ASD颗粒耐受结晶,呈现出较少的附聚并且具有改进的可压缩性和流动性
通过喷雾干燥制备具有50%或70%药物装载的依泽替米贝在羟丙基甲基纤维素乙酸琥珀酸酯(HPMCAS)中的ASD的颗粒。基本上如上文描述,具有50%(B3-140及B3-141)或70%(B3-139A、B3-138B及B3-139B)药物装载的颗粒在35℃下通过ALD用氧化铝涂布。ASD颗粒接受大约5nm厚(B3-140和B3-139A)、大约15至20nm厚(B3-138B)或大约20-30nm厚的涂层(B3-141和B3-139B)。各种ASD颗粒的粒度分布在表1中显示。
表1
使用x射线衍射来评估经涂布和未涂布的ASD颗粒。如图2所示,x射线衍射分析显示经涂布和未涂布的ASD颗粒是非晶的。热分析用于评估经涂布和未涂布的ASD颗粒的玻璃转变温度(Tg)和热诱导结晶。如可以图3中看到,经涂布的ASD颗粒呈现出与未涂布的ASD颗粒相比具有较高的玻璃转变温度(Tg)。亦如可以看到,特别是对于具有70%药物装载的ASD颗粒,涂层显著降低热诱导结晶。
使用扫描电子显微镜来评估经涂布和未涂布的ASD颗粒的形态。如可以在图4中看到,经涂布的ASD颗粒与未涂布的ASD颗粒相比较不附聚。
测量了经涂布和未涂布的ASD颗粒的可压缩性及流动性。如可以在图5中看到,涂层改进ASD颗粒的可压缩性和流动性。
使用等温吸湿来评估经涂布和未涂布的ASD颗粒的吸湿趋势。如可以在图6中看到,经涂布的ASD颗粒与未涂布的ASD颗粒相比吸湿性较小。
实例2:金属氧化物涂布的ASD颗粒在加速稳定性研究条件下耐受结晶
实例1的经涂布和未涂布的ASD颗粒经受加速稳定性研究。将经涂布和未涂布的ASD颗粒储存在40℃/75%相对湿度下。在第12、19、26、33、40、47、54和61天,通过x射线衍射分析经涂布和未涂布的ASD颗粒的样品。如可以在图7中看到,未涂布的ASD颗粒变得逐渐结晶,特别是70%药物装载的ASD颗粒,而经涂布的ASD颗粒保持基本上非晶。图8呈现仅未涂布的ASD颗粒的x射线衍射数据。在此可以更容易看到这些ASF颗粒的增加的结晶度。
热分析用于评估经受加速稳定性研究的经涂布和未涂布的ASD颗粒的热诱导结晶。如可以在图9中看到,经涂布的ASD样品似乎具有与未涂布的ASD样品相比较高的玻璃转变温度(Tg)。如亦可以在图9中看到,即使在50%药物装载下,未涂布的ASD颗粒在仅一个月之后呈现热诱导结晶。即使在2个月之后,经涂布的ASD颗粒几乎不呈现热诱导结晶的改变。
使用扫描电子显微镜来评估经涂布和未涂布的ASD颗粒的形态。如可以在图10A至图10B和图11A至图11B中看到,晶体在第17天在未涂布的50%药物装载的ASD颗粒的表面上和在第12天在未涂布的70%药物装载的ASD颗粒上是可见的。相比之下,在加速稳定性条件下,即使在61之后,晶体在经涂布的ASD颗粒的表面上不可见。
在开放条件下(在40℃和75%相对湿度下储存8个月),实例1的经涂布和未涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)经受加速稳定性研究。如可以在图14中看到,与经涂布的ASD颗粒相比,未涂布的ASD颗粒(50%和70%药物装载)显示出较暗的颜色(黄色)。此外,未涂布的ASD(50%和70%药物装载)与薄涂布的ASD(B3-139A)相比显示出更多附聚。中间经涂布的ASD(B3-139B)和厚涂布的ASD(B3-141和B3-139B)不存在附聚。
样品亦通过扫描电子显微镜(scanning electron microscopy;SEM)评估,以评估在40℃和75%相对湿度下储存不同时间段(12天、47天、210天、240天和270天)之后的未涂布和金属氧化物涂布的50%DL(药物装载)的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的颗粒形态。如图15所示,尽管结晶在未涂布的ASD的第47天之前开始,但在9个月的储存持续时间期间,ALD涂布的ASD(50%B3-140和50%B3-141)不存在结晶。
样品亦通过扫描电子显微镜(SEM)来评估,以评估在40℃和75%相对湿度下储存不同时间段(12天、61天、180天、210天、240天和270天)之后的未涂布和金属氧化物涂布的70%DL ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的颗粒形态。如图16所示,尽管结晶早在未涂布的ASD的第12天开始,但是对于薄涂布的ASD(70%B3-139A),直到7个月(第210天)仍不存在结晶,并且对于厚涂布的ASD(70%B3-138B和70%B3-139B),在9个月的储存持续时间期间,不存在结晶。
在40℃和75%相对湿度下储存9个月之后,经涂布和未涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的样品通过x射线衍射分析。如图17所示,对于具有50%API装载的未涂布的ASD,存在约25%的结晶度,对于具有70%API装载的未涂布的ASD,存在约50%结晶度,并且对于大部分经涂布的样品,不存在结晶。
样品亦通过扫描电子显微镜(SEM)来评估,以评估在40℃和75%相对湿度下储存一年之后的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的颗粒形态。如图19所示,50%和70%的未涂布的ASD皆完全结晶。对于50%DL涂布的样品,不存在结晶。对于70%涂布的ASD,观察到少量结晶。
在40℃和75%相对湿度下储存一年之后,经涂布和未涂布的ASD颗粒(氧化铝/依泽替米贝/HPMCAS)的样品通过x射线衍射分析。如图20所示,对于50%和70%未涂布的ASD两者,存在显著结晶,对于70%薄涂布的ASD(B3-139A),存在少量结晶,并且对于大部分其他经涂布的样品,存在接近零的结晶。
实例3:金属氧化物涂布的ASD颗粒抵抗API释放的劣化
结晶降低了依泽替米贝的溶解度。研究了依泽替米贝从如实例1所描述制备的经涂布和未涂布的ASD颗粒的释放。在每种情况下,溶解条件是37℃,在FaSSSIF(pH 6.5)溶液的50ml磷酸盐缓冲液中搅拌200rpm,并且使用的ASD颗粒的量相当于10mg的依泽替米贝。因此,在此释放研究中,依泽替米贝的最大可能浓度是200μg/ml。在添加相当于10mg的依泽替米贝的ASD颗粒之后,释放曲线数据通过实时原位UV溶解测量来收集。如可以在图12中看到,在40℃/75%相对湿度下1个月之后,依泽替米贝从未涂布的50%药物装载的ASD颗粒的释放速率大大减小。相比之下,从经涂布的50%药物装载的ASD颗粒的释放速率几乎没有改变。如可以在图13中看到,在40℃/75%相对湿度下1个月之后,依泽替米贝从未涂布的70%药物装载的ASD颗粒的释放速率大大减小。相比之下,从经涂布的70%药物装载的ASD颗粒的释放速率几乎没有改变。从未涂布的颗粒的释放减少可能是归因于随时间推移的结晶度和附聚的增加。如图18所示,未涂布的样品的C
实例4:具有60%药物装载的氧化铝涂布的厄洛替尼HPMCAS ASD颗粒(氧化铝/厄洛替尼/HPMCAS)
通过喷雾干燥制备具有60%药物装载的厄洛替尼在羟丙基甲基纤维素乙酸琥珀酸酯(HPMCAS)中的ASD的颗粒。基本上如上文描述,颗粒EH60-5在35℃下通过ALD用氧化铝涂布。EH60-5是具有60%药物装载的未涂布的ASD颗粒(厄洛替尼/HPMCAS)。B3-281B是具有60%药物装载的经涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)。
测试具有60%药物装载的新鲜制备的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的粉末流动性。如图23所示,基于具有60%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的粉末流动性表征,经涂布的ASD颗粒显示出与未涂布的ASD颗粒相比较高的条件体积密度(conditioned bulk density;CBD)。如图23所示,与未涂布的ASD相比,在经涂布的ASD中在15kPa(CPS@15kPa)下压缩之后通过空间改变百分比测量的可压缩性较低。如图23所示,与未涂布的ASD相比,在经涂布的ASD中在3kPa(FFc@3kPa)下压缩之后的流动功能系数较高,从而将黏结的ASD粉末改进到易流动的区域。
通过x射线衍射分析具有60%药物装载的新鲜制备的未涂布和经涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)。如图24所示,基于具有60%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的x射线衍射分析,在涂布之后不存在结晶。
亦通过傅里叶变换红外光谱来分析具有60%药物装载的新鲜制备的未涂布和经涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)。如图25A和图25B所示,基于具有60%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/厄洛替尼/HPMCAS)的FTIR分析,在涂布之后FTIR光谱不改变。
实例5:具有50%药物装载的氧化铝涂布的厄洛替尼PVPVA ASD颗粒(氧化铝/厄洛替尼/PVPVA)
通过具有以下参数的喷雾干燥来制备具有50%药物装载的厄洛替尼在聚乙烯吡咯烷酮-聚乙烯丙烯酸酯共聚物(PVPVA)中的ASD的颗粒:1)输入/输出温度:105℃/68℃;2)喷雾流动速率(设定):20%;3)抽吸器:100%;和4)气体流量:55。EP50-15是具有50%药物装载的未涂布的ASD颗粒(厄洛替尼/PVPVA)。B3-284A是具有50%药物装载的薄涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)。B3-284B是具有50%药物装载的厚涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)。
分析新鲜制备的薄涂布的ASD(B3-284A)和厚涂布的ASD(B3-284B)以评估涂层厚度和氧化物含量。如图26A所示,薄涂布的ASD(B3-284A)具有约4.4至5.5nm的涂层厚度,并且厚涂布的ASD(B3-284B)具有约8.8至9.4nm的涂层厚度。薄涂布的ASD(B3-284A)具有约1.6%的氧化物含量,并且厚涂布的ASD(B3-284B)具有约3.31%的氧化物含量。
等温吸湿用于评估经涂布和未涂布的ASD颗粒的吸湿趋势。如可以在图27中看到,具有50%药物装载的未涂布和经涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)具有相当的等温线。
通过x射线衍射来分析在40℃和43%相对湿度下在开口瓶中储存4周的具有50%药物装载的未涂布和经涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)的样品。如图28所示,尽管未涂布的ASD颗粒(EP50-15)在约2至3周内开始结晶,对于经涂布的ASD颗粒(B3-284A和B3-284B),未观察到结晶。
亦通过SEM来分析在40℃和43%相对湿度下在开口瓶中储存4周的具有50%药物装载的未涂布和经涂布的ASD颗粒(氧化铝/厄洛替尼/PVPVA)的样品。如图29所示,尽管未涂布的ASD颗粒(EP50-15)在约1至2周内开始结晶,对于经涂布的ASD颗粒(B3-284A和B3-284B),未观察到结晶。
实例6具有50%和70%药物装载的金属氧化物涂布的硝苯地平PVP ASD(氧化铝/硝苯地平/PVP或氧化钛/硝苯地平/PVP)
根据表2通过喷雾干燥制备具有50%(SF20000521)或70%(SF20000611)的聚乙烯吡咯烷酮(PVP)中的硝苯地平的ASD的颗粒。基本上如上文描述,颗粒在35℃通过ALD用氧化铝涂布。
表2
具有50%(SF20000521)和70%(SF20000611)药物装载的各种未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的粒度分布、体积密度和振实密度在表3中显示。
表3
分析具有50%(SF20000521)和70%(SF20000611)药物装载的新鲜制备的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的硝苯地平含量和水含量。如图30A所示,与经涂布的颗粒(SF20000521B和SF20000611B)相比,未涂布的颗粒(SF20000521A和SF20000611A)具有较高的硝苯地平含量和较高的水含量。
如图31所示,具有50%(SF20000521)和70%(SF20000611)药物装载的新鲜制备的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的目视检查没有显示出显著附聚。
通过x射线衍射来分析具有50%(SF20000521)和70%(SF20000611)药物装载的新鲜制备的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)。如图32A至图32F所示,不存在结晶。
在加盖的琥珀色玻璃瓶中、加盖的用感应密封的HDPE瓶、和无盖的开口HDPE瓶中储存各个持续时间之后,具有50%和70%药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)经受吸湿分析。如图33A至图33B所示,对于50%药物装载的样品(SF20000521),在各种条件下储存之后,与未涂布的ASD颗粒相比,经涂布的ASD颗粒显示出较少杂质。如图33C至图33D所示,对于70%药物装载的样品(SF20000611),对于经涂布和未涂布的ASD颗粒存在相当的杂质和水分含量。
在40℃和75%相对湿度下在无盖的开口HDPE瓶中储存各个持续时间的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的样品经受目视检查。如图34所示,具有50%药物装载(SF20000521A)和70%药物装载(SF20000611A)的未涂布的ASD显示出显著附聚(结块形成)和颜色改变。在3个月之后,对于具有50%药物装载(SF20000521B)和70%药物装载(SF20000611B)的经涂布的ASD,没有观察到附聚。
在用加盖的感应密封的HDPE瓶中储存各种持续时间的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的样品经受目视检查。如图35所示,具有50%药物装载(SF20000521A)和70%药物装载(SF20000611A)的未涂布的ASD显示出显著附聚(结块形成)。对于具有50%药物装载(SF20000521B)和70%药物装载(SF20000611B)的经涂布的ASD,未观察到附聚。
在加盖的琥珀色瓶中储存各个持续时间的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的样品经受目视检查。如图36所示,具有50%药物装载(SF20000521A)和70%药物装载(SF20000611A)的未涂布的ASD显示出显著附聚(结块形成)。在三个月之后,对于具有50%药物装载(SF20000521B)和70%药物装载(SF20000611B)的经涂布的ASD,未观察到附聚。
在25℃和60%相对湿度下在加盖的琥珀色瓶中储存3个月的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的样品经受X射线衍射分析。如图37所示,对于经涂布或未涂布的样品,未观察到结晶。
在40℃和75%相对湿度下在用加盖的感应密封的HDPE瓶中储存3个月的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的样品经受X射线衍射分析。如图38所示,对于70%药物装载的样品,在未涂布的样品(20000611A)中存在显著结晶并且在经涂布的样品(20000611B)中不存在结晶。
在40℃和75%相对湿度下在无盖的开口HDPE瓶中储存3个月的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/PVP)的样品经受X射线衍射分析。如图39所示,对于50%和70%药物装载的样品,在未涂布的样品(20000521A和20000611A)中存在显著结晶并且在经涂布的样品(20000521B和20000611B)中存在相对较小量的结晶。
亦通过扫描电子显微镜(SEM)来评估样品,以评估在40℃和75%相对湿度下在无盖的开口HDPE瓶中储存3个月之后的具有50%(SF20000521)和70%(SF20000611)药物装载的未涂布和金属氧化物涂布的ASD颗粒(氧化铝/硝苯地平/HPMCAS)的颗粒形态。如图40A所示,未涂布的50%和70%药物装载的ASD颗粒在开口瓶中储存3个月之后显示出显著结晶(完全胶凝)。实际上,归因于附聚,在将样品研磨/压碎成小片之后拍摄SEM影像。相比之下,如图40B至图40C所示,经涂布的50%和70%药物装载的ASD颗粒在开口瓶中储存3个月之后不显示出结晶或形态改变。
- 核酸-药物结合物、药物递送系统及其制备方法和应用
- 用于制备治疗肝癌药物的芳基钌配合物及其制备方法和用途
- 一类檀香内生真菌来源的二苯酚酸类化合物及其制备方法和在制备抗菌药物中的应用
- 化合物lithocarolsA-F及其制备方法和在制备抗肿瘤药物中的应用
- 一种红树内生真菌来源的1,4-萘醌类化合物及其制备方法和在制备抗炎药物中的应用
- 化学增幅型光阻组成物、使用该组成物的光阻膜、涂布光阻的空白光罩、光阻图案形成方法、光罩及聚合化合物
- 预防以及治疗糖尿病伴发的心血管疾病的药物组成物、其包含氨氯地平、络舒坦以及瑞舒伐他汀、以及包含所述组成物的复合物制备
