EGFR蛋白磷酸化的抑制试剂及抑制方法和用途
文献发布时间:2024-01-17 01:15:20
技术领域
本发明涉及生物分析及医学领域,具体涉及一种针对EGFR蛋白磷酸化的特异性抑制试剂及抑制方法和用途。
背景技术
表皮生长因子受体(Epidermal Growth Factor Receptor,EGFR)是一类具有酪氨酸激酶活性的细胞膜表面受体,EGFR是肿瘤细胞促有丝分裂和转化的一个重要靶点,在许多肿瘤细胞中过度表达,其介导的信号转导与肿瘤细胞的生长、增殖、转移等过程密切相关。
EGFR在细胞增殖、存活、迁移、粘附和分化方面发挥着重要作用,具有酪氨酸激酶活性。EGFR自磷酸化后可与生长因子受体结合蛋白的复合物结合,从而激活Ras蛋白。活化的Ras激活下游丝/苏氨酸蛋白激酶Raf,从而使Erk(细胞外调节蛋白激酶)磷酸化,将信号传至细胞核内,导致核内转录因子的磷酸化,从而启动靶基因的转录,最终导致细胞增殖、扩散等生物学效应。
通过抑制EGFR可有效抑制肿瘤的生长,因此有一些研究针对EGFR为靶点开发药物,靶向抑制EGFR酪氨酸激酶。可见,寻找EGFR抑制剂,阻断EGFR的信号转导,对于肿瘤的治疗至关重要。
发明内容
本发明首次发现,当细胞的碘钠转运体(NIS)表达高时,碘化钠可以显著抑制EGFR蛋白磷酸化;当细胞的NIS表达低时,可通过辅助剂KT5823提高细胞NIS摄碘功能,从而碘化钠可以正常进入细胞并显著抑制EGFR蛋白磷酸化。基于此,碘化钠处理可作为EGFR蛋白磷酸化抑制剂,为EGFR的磷酸化抑制和疾病的治疗提供新的手段。
具体地,本发明采用的技术方案如下:
第一方面,本发明提供一种EGFR蛋白磷酸化的抑制试剂,其包含碘化钠。
进一步地,所述EGFR蛋白磷酸化的抑制试剂还包含辅助剂KT5823。
第二方面,本发明提供一种EGFR蛋白磷酸化的抑制试剂的制备方法,其步骤包括:
将碘化钠溶解于超纯水,制得碘化钠母液,作为EGFR蛋白磷酸化的抑制试剂;
将KT5823溶解于DMSO,制得KT5823母液,作为EGFR蛋白磷酸化的抑制试剂的辅助剂。
进一步地,准确称取纯度大于99.9%的碘化钠,将其溶解于超纯水,制得浓度为200mM的碘化钠母液,作为EGFR蛋白磷酸化的抑制试剂;准确称取纯度大于98%的KT5823,将其溶解于DMSO,制得浓度为2mM的KT5823母液,作为EGFR蛋白磷酸化的抑制试剂的辅助剂。
第三方面,本发明提供一种EGFR蛋白磷酸化的抑制方法,包括以下步骤:
将碘化钠溶解于超纯水,制得碘化钠母液;
将碘化钠母液加入细胞培养基中,配制成EGFR磷酸化抑制培养基;
对于NIS高表达细胞,直接利用含有碘化钠的EGFR磷酸化抑制培养基抑制EGFR蛋白的磷酸化;
对于NIS低表达细胞,将EGFR蛋白的磷酸化抑制试剂辅助剂加入含有碘化钠的EGFR磷酸化抑制培养基,再用其抑制EGFR蛋白的磷酸化。
其中,NIS表达的“高”与“低”,可以通过现有技术或本领域公知常识来确定,例如甲状腺细胞中NIS表达量高,其他类型细胞中NIS的表达量低;可以设定一个阈值,大于等于该阈值的认为是NIS高活性细胞,小于该阈值的认为是NIS低活性细胞。
进一步地,NIS高表达细胞的EGFR蛋白的磷酸化抑制方法的具体步骤为:
1)以B-CPAP、Hth-7、SW579和Nthy-Ori-3-1的NIS高表达细胞为例,首先对以上细胞进行传代培养,将培养好的细胞种板至96孔板,每孔2×10
2)配制EGFR磷酸化抑制培养基:向各细胞培养基中加入适量200mM的碘化钠母液,配制成EGFR磷酸化抑制培养基;
3)细胞种板过夜培养后,小心将细胞培养基吸出,并加入EGFR磷酸化抑制培养基,置于37℃、5%二氧化碳细胞培养箱继续培养24小时。
更为优选地,所述EGFR磷酸化抑制培养基是碘化钠浓度为100μM的细胞培养基。
进一步地,上述NIS高表达细胞的EGFR蛋白的磷酸化抑制方法还包括对EGFR蛋白的磷酸化程度进行检测的步骤。在对EGFR蛋白的磷酸化程度进行检测前还包括:
将EGFR磷酸化抑制培养基培养好的细胞用磷酸缓冲液PBS进行清洗2-3次;加入适量固定-破膜液,常温避光固定30分钟或37℃避光固定10分钟;
再将固定后的细胞加入1×破膜液进行清洗2-3次;向清洗后的细胞中加入适量EGFR一抗溶液,室温避光孵育30分钟;
一抗孵育后,加入1×破膜液进行清洗3次;向清洗后的细胞中加入适量的荧光二抗溶液,室温避光孵育60分钟;
荧光二抗孵育后,加入1×破膜液进行清洗3次;加入200μL的加有细胞核染色液Horchest的Flurbrite DMEM,避光,立即进行高内涵细胞成像分析系统检测。
优选地,所述固定-破膜液采用新鲜配置的eBioscience
优选地,所述1×破膜液采用新鲜配置的eBioscience
优选地,所述EGFR一抗溶液采用Cell Signaling Technology公司Phospho-EGFReceptor(Tyr1068)(D7A5)
优选地,所述荧光二抗溶液采用Cell Signaling Technology公司Anti-rabbitIgG(H+L)(#4412)二抗,并用1×破膜液进行1:1000稀释。
进一步地,NIS低表达细胞的EGFR蛋白的磷酸化抑制方法的具体步骤为:
1)以BeWo、TE-1和MKN-45低NIS表达细胞为例,首先对以上细胞进行传代培养,将培养好的细胞种板至96孔板,每孔2×10
2)配制含有辅助剂KT5823的EGFR磷酸化抑制培养基:向各细胞培养基中加入适量2mM的KT5823和200mM的碘化钠母液,配制成含有辅助剂KT5823的EGFR磷酸化抑制培养基;
3)细胞种板过夜培养后,小心将细胞培养基吸出,加入含有辅助剂KT5823的EGFR磷酸化抑制培养基,置于37℃、5%二氧化碳细胞培养箱继续培养24小时。
更为优选地,所述含有辅助剂KT5823的EGFR磷酸化抑制培养基是KT5823浓度为2μM,碘化钠浓度为10μM的细胞培养基。
进一步地,上述NIS低表达细胞的EGFR蛋白的磷酸化抑制方法还包括对EGFR蛋白的磷酸化程度进行检测的步骤。在对EGFR蛋白的磷酸化程度进行检测前还包括:
将含有辅助剂KT5823的EGFR磷酸化抑制培养基培养好的细胞用磷酸缓冲液PBS进行清洗2-3次;加入适量固定-破膜液,常温避光固定30分钟或37℃避光固定10分钟;
再将固定后的细胞加入1×破膜液进行清洗2-3次;向清洗后的细胞中加入适量EGFR一抗溶液,室温避光孵育30分钟;
一抗孵育后,加入1×破膜液进行清洗3次;向清洗后的细胞中加入适量的荧光二抗溶液,室温避光孵育60分钟;
荧光二抗孵育后,加入1×破膜液进行清洗3次;加入200μL的加有细胞核染色液Horchest的Flurbrite DMEM,避光,立即进行高内涵细胞成像分析系统检测。
优选地,所述固定-破膜液采用新鲜配置的eBioscience
优选地,所述1×破膜液采用新鲜配置的eBioscience
优选地,所述EGFR一抗溶液采用Cell Signaling Technology公司Phospho-EGFReceptor(Tyr1068)(D7A5)
优选地,所述荧光二抗溶液采用Cell Signaling Technology公司Anti-rabbitIgG(H+L)F(ab')2Fragment(Alexa
进一步地,对EGFR蛋白的磷酸化程度进行检测的具体方法包括:
高内涵细胞成像分析系统选择DAPI和FITC两个通道进行检测,其中DAPI通道的曝光时间为5ms,FITC通道的曝光时间为100ms。采用20x的镜头,每孔9个视野进行采集。并通过系统自带的分析软件对EGFR表达水平进行分析。
第四方面,本发明提供上述EGFR蛋白的磷酸化抑制试剂即碘化钠在抗肿瘤药物中的用途。
本发明的有益效果如下:
本发明首次发现,碘化钠可以显著抑制EGFR蛋白的磷酸化,其磷酸化位点845和1068均可显著地被碘化钠抑制,因此碘化钠可作为EGFR的抑制剂。即加入碘化钠能够对酪氨酸进行碘化修饰,形成空间位阻,从而抑制酪氨酸的磷酸化。
本发明中的EGFR磷酸化抑制方法,可潜在地应用于抗肿瘤药物的研发。EGFR是肿瘤细胞促有丝分裂和转化的一个重要靶点,在许多肿瘤细胞中过度表达,与肿瘤的发生发展及转移密切相关。抑制EGFR磷酸化激活可抑制肿瘤细胞的增殖、侵袭、转移和血管再生,诱导肿瘤细胞凋亡。
附图说明
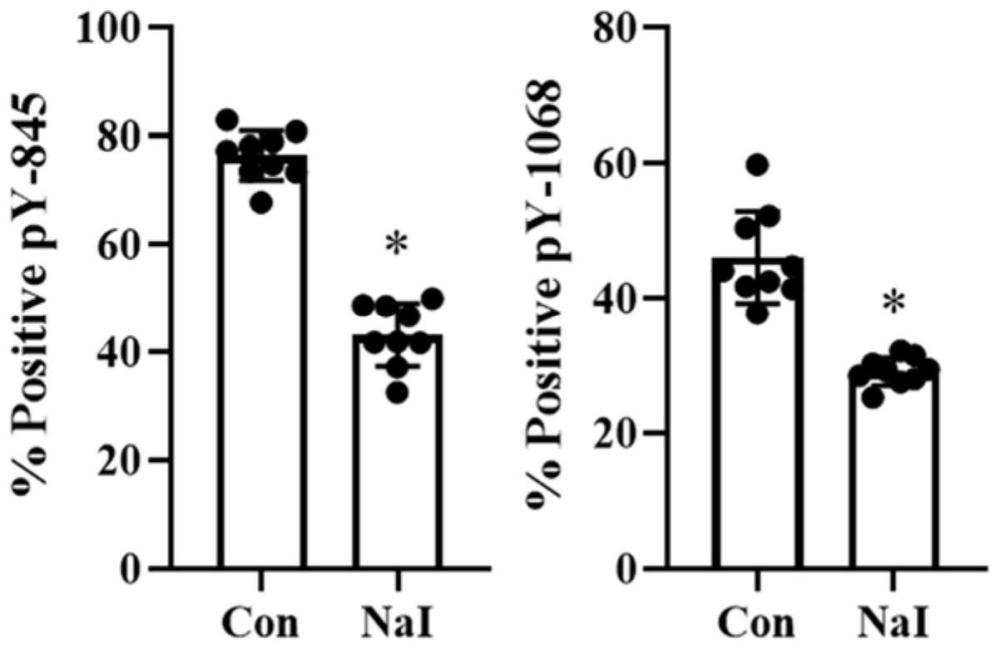
图1为B-CPAP细胞磷酸化抑制剂100μM处理后磷酸化位点845和1068磷酸化结果图;
图2为Hth-7细胞磷酸化抑制剂100μM处理后磷酸化位点845和1068磷酸化结果图;
图3为SW579细胞磷酸化抑制剂100μM处理后磷酸化位点845和1068磷酸化结果图;
图4为Nthy-Ori-3-1细胞磷酸化100μM抑制剂处理后磷酸化位点845和1068磷酸化结果图。
图5为BEWO细胞2μM KT5823和磷酸化抑制剂10μM处理后磷酸化位点845和1068磷酸化结果图;
图6为TE-1细胞2μM KT5823和磷酸化抑制剂100μM处理后磷酸化位点845和1068磷酸化结果图;
图7为MKN-45细胞2μM KT5823和磷酸化抑制剂10μM处理后磷酸化位点845和1068磷酸化结果图;
图1~图7中,横坐标处的Con表示经碘化钠处理前各细胞的EGFR磷酸化845和1068位点,NaI表示经碘化钠处理后各细胞的EGFR磷酸化845和1068位点,纵坐标处的Positive表示细胞中EGFR蛋白磷酸化的阳性率。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。
实施例1:甲状腺癌细胞B-CPAP的磷酸化抑制效果测定
1、仪器与试剂:
高内涵细胞成像分析系统(Molecular Devices公司);碘化钠;超纯水;eBioscience
2、B-CPAP细胞的培养和磷酸化抑制处理
(1)B-CPAP细胞复苏-传代:将含有1mL细胞悬液的冻存管在37℃水浴中迅速摇晃解冻,加入5mL的培养基(RPMI-1640+10%FBS+1%Penicillin-Streptomycin Solution)混合均匀。在500RPM条件下离心5分钟,弃去上清液,补加4-6mL完全培养基后吹匀。然后将所有细胞悬液加入培养瓶中培养过夜(或将细胞悬液加入6cm皿中),培养过夜。第二天换液并检查细胞密度。
细胞密度达80%-90%,即可进行传代培养。将0.25%胰酶-0.53mM EDTA消化液置于37°预热,倒掉培养瓶中的培养基,往培养瓶中加入3-5ml PBS,轻晃洗涤后弃去。往瓶中加1-2ml预热好的胰酶,置于37°孵育消化,消化好后加入3ml完全培养基终止消化。用移液枪轻轻吹打瓶壁上的细胞,使之完全脱落,然后收集细胞悬液,1200rpm离心3min,弃上清,加入完全培养基重悬细胞,进行传代。
(2)待细胞长至足够量,收集细胞,并测定细胞密度,细胞种板至96孔板,每孔2×10
(3)磷酸化抑制剂处理:配制EGFR磷酸化抑制培养基,向各细胞培养基中加入适量200mM的碘化钠母液,配制成碘化钠浓度为100μM的细胞培养基。细胞种板过夜培养后,小心将细胞培养基吸出,并加入EGFR磷酸化抑制培养基,置于37℃、5%二氧化碳细胞培养箱继续培养24小时。
(4)细胞固定:将EGFR磷酸化抑制培养基培养好的细胞用磷酸缓冲液PBS进行清洗2-3次;加适量入固定-破膜液,常温避光固定30分钟或37℃避光固定10分钟。
(5)细胞染色:固定后的细胞加入1×破膜液进行清洗2-3次;向清洗后的细胞中加入50μL的1:500稀释的EGFR一抗溶液(抗体Phospho-EGF Receptor(Tyr1068)(D7A5)
(6)荧光二抗孵育:一抗孵育后,加入1×破膜液进行清洗3次;向清洗后的细胞中加入适量的荧光二抗1:1000稀释的Anti-rabbit IgG(H+L)(#4412)溶液,室温避光孵育60分钟;
(7)高内涵检测:荧光二抗孵育后,加入1×破膜液进行清洗3次;加入200μL的加有细胞核染色液Horchest的Flurbrite DMEM,避光,立即进行高内涵细胞成像分析系统检测。高内涵细胞成像分析系统选择DAPI和FITC两个通道进行检测,其中DAPI通道的曝光时间为5ms,FITC通道的曝光时间为100ms。采用20x的镜头,每孔9个视野进行采集。并通过系统自带的分析软件对EGFR表达水平进行分析。
实施例2:甲状腺癌细胞Hth-7的磷酸化抑制效果测定
1、仪器与试剂:
同实施例1。
2、Hth-7细胞的培养和磷酸化抑制处理
(1)Hth-7细胞复苏-传代:将含有1mL细胞悬液的冻存管在37℃水浴中迅速摇晃解冻,加入5mL的培养基(DMEM+10%FBS+1%Penicillin-Streptomycin Solution)混合均匀。在500RPM条件下离心5分钟,弃去上清液,补加4-6mL完全培养基后吹匀。然后将所有细胞悬液加入培养瓶中培养过夜(或将细胞悬液加入6cm皿中),培养过夜。第二天换液并检查细胞密度。
其他步骤同实施例1。
实施例3:甲状腺癌细胞SW579的磷酸化抑制效果测定
1、仪器与试剂:
同实施例1。
2、SW579细胞的培养和磷酸化抑制处理
(1)SW579细胞复苏-传代:将含有1mL细胞悬液的冻存管在37℃水浴中迅速摇晃解冻,加入5mL的培养基(DMEM+10%FBS+1%Penicillin-Streptomycin Solution)混合均匀。在500RPM条件下离心5分钟,弃去上清液,补加4-6mL完全培养基后吹匀。然后将所有细胞悬液加入培养瓶中培养过夜(或将细胞悬液加入6cm皿中),培养过夜。第二天换液并检查细胞密度。
其他步骤同实施例1。
实施例4:永生化甲状腺细胞Nthy-Ori-3-1的磷酸化抑制效果测定
1、仪器与试剂:
同实施例1。
2、Nthy-Ori-3-1细胞的培养和磷酸化抑制处理
同实施例1。
实施例5:人胎盘绒毛癌细胞BeWo的磷酸化抑制效果测定
1、仪器与试剂:
高内涵细胞成像分析系统(Molecular Devices公司);碘化钠;超纯水;KT5823;DMSO;eBioscience
2、BeWo细胞的培养和磷酸化抑制处理
(1)BeWo细胞复苏-传代:将含有1mL细胞悬液的冻存管在37℃水浴中迅速摇晃解冻,加入5mL的培养基(DMEM+10%FBS+1%Penicillin-Streptomycin Solution)混合均匀。在500RPM条件下离心5分钟,弃去上清液,补加4-6mL完全培养基后吹匀。然后将所有细胞悬液加入培养瓶中培养过夜(或将细胞悬液加入6cm皿中),培养过夜。第二天换液并检查细胞密度。
(2)待细胞长至足够量,收集细胞,并测定细胞密度,细胞种板至96孔板,每孔2×10
(3)磷酸化抑制剂处理:配制含有辅助剂KT5823的EGFR磷酸化抑制培养基,向各细胞培养基中加入适量200mM的碘化钠母液和适量2mM的KT5823母液,配制成KT5823浓度为2μM碘化钠浓度为100μM的细胞培养基。细胞种板过夜培养后,小心将细胞培养基吸出,并加入含有辅助剂KT5823的EGFR磷酸化抑制培养基,置于37℃、5%二氧化碳细胞培养箱继续培养24小时。
其他步骤同实施例1。
实施例6:人食管癌细胞TE-1的磷酸化抑制效果测定
1、仪器与试剂:
同实施例5。
2、TE-1细胞的培养和磷酸化抑制处理
(1)TE-1细胞复苏-传代:将含有1mL细胞悬液的冻存管在37℃水浴中迅速摇晃解冻,加入5mL的培养基(RPMI-1640+10%FBS+1%Penicillin-Streptomycin Solution)混合均匀。在500RPM条件下离心5分钟,弃去上清液,补加4-6mL完全培养基后吹匀。然后将所有细胞悬液加入培养瓶中培养过夜(或将细胞悬液加入6cm皿中),培养过夜。第二天换液并检查细胞密度。
其他步骤同实施例5。
实施例7:人胃癌细胞MKN-45的磷酸化抑制效果测定
1、仪器与试剂:
同实施例6。
2、MKN-45细胞的培养和磷酸化抑制处理
同实施例6。
综合实施例1和实施例7中的检测结果即图1~图7,可以看出,经碘化钠处理后B-CPAP、Hth-7、SW579、Nthy-Ori-3-1、BeWo、TE-1和MKN-45细胞的EGFR磷酸化845和1068位点均显著受到抑制。因此,本发明中的EGFR蛋白磷酸化抑制方法可为癌症药物的研发提供依据。
以上公开的本发明的具体实施例,其目的在于帮助理解本发明的内容并据以实施,本领域的普通技术人员可以理解,在不脱离本发明的精神和范围内,各种替换、变化和修改都是可能的。本发明不应局限于本说明书的实施例所公开的内容,本发明的保护范围以权利要求书界定的范围为准。
- EGFR和HER2双靶点酪氨酸激酶抑制剂及制备方法和用途
- 分析血红蛋白的毛细管电泳方法,用于毛细管电泳的试剂盒,和流动抑制剂在所述方法中的用途
- 分析血红蛋白的毛细管电泳方法,用于毛细管电泳的试剂盒,和流动抑制剂在所述方法中的用途
