一种药品包装的无菌检测方法及系统
文献发布时间:2024-01-17 01:26:37
技术领域
本发明涉及智能检测相关技术领域,具体涉及一种药品包装的无菌检测方法及系统。
背景技术
药品包装的无菌检测是指对药品包装进行无菌性的检测,以确保药品包装的内部没有被微生物污染,药品包装的无菌检测可以保证药品的质量和安全性,避免患者因微生物污染而引发感染。
通常情况下,是通过培养和发现药品包装中是否存在微生物来进行的,常见的无菌检测方法包括菌落计数法、膜过滤法、直接培养法等。但菌落计数法、膜过滤法、直接培养法的检测周期长,无法大规模推广使用。
综上所述,现有技术中存在药品包装无菌检测精度低,无法及时发现微生物污染,无菌检测结果可信度低的技术问题。
发明内容
本申请通过提供了一种药品包装的无菌检测方法及系统,旨在解决现有技术中的药品包装无菌检测精度低,无法及时发现微生物污染,无菌检测结果可信度低的技术问题。
鉴于上述问题,本申请实施例提供了一种药品包装的无菌检测方法及系统。
本申请公开的第一个方面,提供了一种药品包装的无菌检测方法,其中,所述方法应用于药品包装检测系统,所述药品包装检测系统内置一微孔检测单元,所述方法包括:在对目标药品进行包装之前,获取所述目标药品的包装用材料、包装用容器;以及在药品包装无尘清洁车间中,对所述目标药品的消毒灭菌环节进行监测,获取第一无菌检测分量;在药品包装无尘清洁车间中,对所述目标药品的包装用材料的消毒灭菌环节进行监测,获取第二无菌检测分量;在药品包装无尘清洁车间中,对所述目标药品的包装用容器的消毒灭菌环节进行监测,获取第三无菌检测分量;将所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量发送至药品包装机组,判断是否进行组合包装,所述组合包装即目标药品其及包装的组合封装;若进行组合包装,在所述目标药品包装完成后,通过所述微孔检测单元进行密封性检测,获取密封性检测结果;将所述密封性检测结果反馈至药品包装机组,基于所述密封性检测结果、所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量构造组合特征,获取目标药品的无菌检测结果。
本申请公开的另一个方面,提供了一种药品包装的无菌检测系统,其中,所述系统包括:材料、容器获取模块,用于在对目标药品进行包装之前,获取所述目标药品的包装用材料、包装用容器;以及第一无菌检测分量获取模块,用于在药品包装无尘清洁车间中,对所述目标药品的消毒灭菌环节进行监测,获取第一无菌检测分量;第二无菌检测分量获取模块,用于在药品包装无尘清洁车间中,对所述目标药品的包装用材料的消毒灭菌环节进行监测,获取第二无菌检测分量;第三无菌检测分量获取模块,用于在药品包装无尘清洁车间中,对所述目标药品的包装用容器的消毒灭菌环节进行监测,获取第三无菌检测分量;组合封装模块,用于将所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量发送至药品包装机组,判断是否进行组合包装,所述组合包装即目标药品其及包装的组合封装;密封性检测模块,用于若进行组合包装,在所述目标药品包装完成后,通过微孔检测单元进行密封性检测,获取密封性检测结果;无菌检测结果获取模块,用于将所述密封性检测结果反馈至药品包装机组,基于所述密封性检测结果、所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量构造组合特征,获取目标药品的无菌检测结果。
本申请中提供的一个或多个技术方案,至少具有如下技术效果或优点:
由于采用了目标药品包装之前,获取包装用材料、包装用容器;监测消毒灭菌环节,获取第一无菌检测分量、第二无菌检测分量、第三无菌检测分量,发送至药品包装机组,判断是否进行组合包装;若进行组合包装,在目标药品包装完成后,通过微孔检测单元进行密封性检测,获取密封性检测结果,反馈至药品包装机组,基于密封性检测结果、第一无菌检测分量、第二无菌检测分量与第三无菌检测分量构造组合特征,获取目标药品的无菌检测结果,实现了分别从药品、材料、容器出发,提高药品包装无菌检测精度,全面落实药品包装无菌检测,及时确定微生物污染,维护无菌检测结果可信度的技术效果。
上述说明仅是本申请技术方案的概述,为了能够更清楚了解本申请的技术手段,而可依照说明书的内容予以实施,并且为了让本申请的上述和其它目的、特征和优点能够更明显易懂,以下特举本申请的具体实施方式。
附图说明
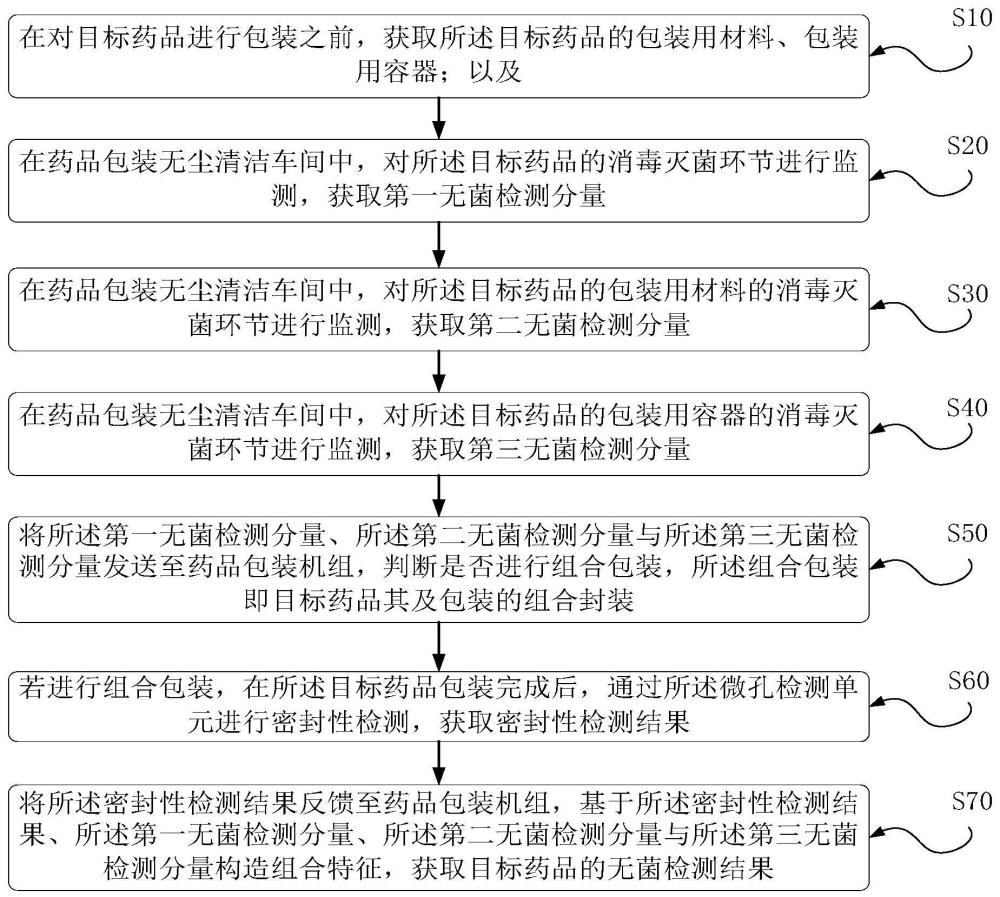
图1为本申请实施例提供了一种药品包装的无菌检测方法可能的流程示意图;
图2为本申请实施例提供了一种药品包装的无菌检测方法中生成第一无菌检测分量可能的流程示意图;
图3为本申请实施例提供了一种药品包装的无菌检测方法中温度升高曲线优化结果可能的流程示意图;
图4为本申请实施例提供了一种药品包装的无菌检测系统可能的结构示意图。
附图标记说明:材料、容器获取模块100,第一无菌检测分量获取模块200,第二无菌检测分量获取模块300,第三无菌检测分量获取模块400,组合封装模块500,密封性检测模块600,无菌检测结果获取模块700。
具体实施方式
本申请实施例提供了一种药品包装的无菌检测方法及系统,解决了药品包装无菌检测精度低,无法及时发现微生物污染,无菌检测结果可信度低的技术问题,实现了分别从药品、材料、容器出发,提高药品包装无菌检测精度,全面落实药品包装无菌检测,及时确定微生物污染,维护无菌检测结果可信度的技术效果。
在介绍了本申请基本原理后,下面将结合说明书附图来具体介绍本申请的各种非限制性的实施方式。
实施例一
如图1所示,本申请实施例提供了一种药品包装的无菌检测方法,其中,所述方法应用于药品包装检测系统,所述药品包装检测系统内置一微孔检测单元,所述方法包括:
S10:在对目标药品进行包装之前,获取所述目标药品的包装用材料、包装用容器;以及
具体而言,所述药品包装检测系统内置一微孔检测单元,所述微孔检测单元与药品包装检测系统通信连接,所述通信连接简单来说就是通过信号的传输交互,在所述微孔检测单元与药品包装检测系统之间构成通讯网络,为进行药品包装无菌检测提供硬件支持;
目标药品为进行药品包装无菌检测的对象,在对目标药品进行包装之前,获取所述目标药品的包装用材料(可以是塑料、玻璃或金属)、包装用容器(常见如塑料瓶、玻璃瓶、药用铝箔),所述包装用材料与所述包装用容器相互对应,为后续分析提供基础。
S20:在药品包装无尘清洁车间中,对所述目标药品的消毒灭菌环节进行监测,获取第一无菌检测分量;
如图2所示,步骤S20包括步骤:
S21:对所述目标药品进行缺陷检测,获取第一初始检测分量,所述第一初始检测分量包括产品破损检测分量、产品缺块检测分量、产品裂缝检测分量;
S22:在所述目标药品的消毒灭菌环节过程进行物理或化学监测,获取第二初始检测分量,所述第二初始检测分量包括目标药品的灭菌温度和灭菌时间;
S23:基于所述第一初始检测分量与所述第二初始检测分量,生成所述第一无菌检测分量。
具体而言,在药品包装无尘清洁车间中,对所述目标药品的消毒灭菌环节进行监测,获取第一无菌检测分量,包括,须知的,片剂、胶囊、栓剂、丸剂等固体制剂药品一般要经过压封、切割等一系列作业,容易产生破损、缺块、裂缝等情况,基于此,对所述目标药品进行缺陷检测(缺陷检测:使用AI视觉检测设备,利用深度学习算法框架结合自主研发的外观检测模型成功智能识别产生破损、缺块、裂缝,获取目标药品对应的出厂标准,目标药品对应的出厂标准中附有的目标药品的药品外观样图,将药品外观样图作为标准,对目标药品与所述药品外观样图进行视觉检测比对),获取第一初始检测分量,所述第一初始检测分量包括产品破损检测分量、产品缺块检测分量、产品裂缝检测分量;
须知的,消毒、杀菌方法有物理方法(常见如高温灭菌)、化学方法(常见比如使用化学消毒剂),消毒杀菌技术包括但不限于热力、化学(液体或气体)、辐射(γ辐射和紫外线)、过滤技术,在所述目标药品的消毒灭菌环节过程进行物理或化学监测,比如利用化学指示卡、生物指示剂等监测压力灭菌器的灭菌温度和时间,获取第二初始检测分量,所述第二初始检测分量包括目标药品的灭菌温度和灭菌时间;组合所述第一初始检测分量与所述第二初始检测分量,获取所述第一无菌检测分量,从第一个污染源头进行无菌检测,为全面落实药品包装无菌检测提供基础。
S30:在药品包装无尘清洁车间中,对所述目标药品的包装用材料的消毒灭菌环节进行监测,获取第二无菌检测分量;
步骤S30包括步骤:
S31:对所述目标药品的包装用材料进行缺陷检测,获取第三初始检测分量,所述第三初始检测分量包括材料黏合缺陷检测分量、材料张力缺陷检测分量、材料固化缺陷检测分量;
S32:在所述目标药品的包装用材料的消毒灭菌环节过程进行物理或化学监测,获取第四初始检测分量,所述第四初始检测分量包括所述目标药品的包装用材料的灭菌温度和灭菌时间;
S33:基于所述第三初始检测分量与所述第四初始检测分量,生成所述第二无菌检测分量。
具体而言,在药品包装无尘清洁车间中,对所述目标药品的包装用材料的消毒灭菌环节进行监测,获取第二无菌检测分量,包括,须知的,在进行药品包装过程还需要粘合剂,粘合剂固化后,用于起到固定药品包装(常用于固体药品袋装情况),同时,非PVC复合膜软袋由三层共挤膜制成的,不使用黏合剂,具有很低的透水性、透气性及迁移性,非PVC复合膜软袋为输液包装,不同规格的非PVC复合膜软袋的内部液体量不同,要在材料张力限定范围内,基于此,对所述目标药品的包装用材料进行缺陷检测(缺陷检测:粘合剂的上胶量不够-材料黏合缺陷检测分量、薄膜和铝箔表面张力不够-材料张力缺陷检测分量、粘合剂固化交联不完全-材料固化缺陷检测分量),获取第三初始检测分量,所述第三初始检测分量包括材料黏合缺陷检测分量、材料张力缺陷检测分量、材料固化缺陷检测分量;
在所述目标药品的包装用材料的消毒灭菌环节过程进行物理或化学监测,利用化学指示卡、生物指示剂等监测压力灭菌器的灭菌温度和时间,获取第四初始检测分量,所述第四初始检测分量包括所述目标药品的包装用材料的灭菌温度和灭菌时间;组合所述第三初始检测分量与所述第四初始检测分量,获取所述第二无菌检测分量,从第二个污染源头进行无菌检测,为全面落实药品包装无菌检测提供基础。
S40:在药品包装无尘清洁车间中,对所述目标药品的包装用容器的消毒灭菌环节进行监测,获取第三无菌检测分量;
步骤S40包括步骤:
S41:对所述目标药品的包装用容器进行缺陷检测,获取第五初始检测分量,所述第五初始检测分量包括容器破损检测分量、容器畸形检测分量、容器裂缝检测分量;
S42:在所述目标药品的包装用容器的消毒灭菌环节过程进行物理或化学监测,获取第六初始检测分量,所述第六初始检测分量包括所述目标药品的包装用容器的灭菌温度和灭菌时间;
S43:基于所述第五初始检测分量与所述第六初始检测分量,生成所述第三无菌检测分量。
具体而言,在药品包装无尘清洁车间中,对所述目标药品的包装用容器的消毒灭菌环节进行监测,获取第三无菌检测分量,包括,须知的,使用玻璃瓶在灌装前需要判断瓶口与瓶身是否存在破损、裂缝等问题,使用橡胶塞前确定是否出现畸形等问题,基于此,对所述目标药品的包装用容器进行缺陷检测(缺陷检测:获取所述目标药品的包装用容器对应的出厂标准,目标药品的包装用容器对应的出厂标准中附有的目标药品的包装用容器的包装用容器外观样图,将包装用容器外观样图作为标准,使用AI视觉检测设备,对目标药品的包装用容器与所述包装用容器外观样图进行视觉检测比对),获取第五初始检测分量,所述第五初始检测分量包括容器破损检测分量、容器畸形检测分量、容器裂缝检测分量;
在所述目标药品的包装用容器的消毒灭菌环节过程进行物理或化学监测,利用化学指示卡、生物指示剂等监测压力灭菌器的灭菌温度和时间,获取第六初始检测分量,所述第六初始检测分量包括所述目标药品的包装用容器的灭菌温度和灭菌时间;组合所述第五初始检测分量与所述第六初始检测分量,获取所述第三无菌检测分量,从第三个污染源头进行无菌检测,为全面落实药品包装无菌检测提供基础。
S50:将所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量发送至药品包装机组,判断是否进行组合包装,所述组合包装即目标药品其及包装的组合封装;
S60:若进行组合包装,在所述目标药品包装完成后,通过所述微孔检测单元进行密封性检测,获取密封性检测结果;
S70:将所述密封性检测结果反馈至药品包装机组,基于所述密封性检测结果、所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量构造组合特征,获取目标药品的无菌检测结果。
具体而言,将所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量打包发送至药品包装机组,判断是否满足《药品生产质量管理规范(2021年修订)》等相关标准性规范,在满足相关标准性规范的情况下进行组合包装,所述组合包装即目标药品其及包装的组合封装,在所述目标药品包装完成后,通过所述微孔检测单元对组合包装进行密封性检测,获取密封性检测结果;将所述密封性检测结果反馈至药品包装机组,基于所述密封性检测结果、所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量构造组合特征,获取目标药品的无菌检测结果;
基于所述密封性检测结果、所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量构造组合特征:对所述密封性检测结果、所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量进行标准化处理,通过TOPSIS法(Techniquefor Order Preference by Similarity to ideal Sulution,优劣解距离法),进行相关性分析,具体的,采用余弦法找出标准化处理的密封性检测结果与标准化处理的第一无菌检测分量、标准化处理的密封性检测结果与标准化处理的第二无菌检测分量、标准化处理的密封性检测结果与标准化处理的第三无菌检测分量的最优匹配特征和最劣匹配特征,然后计算剩余的一个指标与最优匹配特征和最劣匹配特征间的距离,获得密封性检测结果与第一无菌检测分量、密封性检测结果与第二无菌检测分量、密封性检测结果与第三无菌检测分量的相对接近程度,以此作为权重值,对第一无菌检测分量、第二无菌检测分量与第三无菌检测分量进行加权融合,获取目标药品的无菌检测结果,为保证目标药品的无菌检测结果的稳定性提供基础。
步骤S60包括步骤:
S61:在目标药品包装完成后,判断目标药品的组合包装方式;
S62:若目标药品的组合包装方式为液体瓶/软袋且存在绝缘瓶装封口/绝缘软袋封口,进行液体泄漏检测,获取密封性检测结果。
如图3所示,本申请实施例还包括:
S621:在绝缘瓶装封口/绝缘软袋封口的第一面与液体瓶/软袋的内部液体充分接触的情况下,在绝缘瓶装封口/绝缘软袋封口的第二面的两端设置发射极与接收极,所述发射极与接收极为所述微孔检测单元的构件;
S622:通过所述微孔检测单元的发射极与接收极,进行感应微电流检测,获取感应微电流I;
S623:比较感应微电流I与初设感应微电流I
步骤S623包括步骤:
S623-1:获取初设感应微电流I
S623-2:若感应微电流I≤初设感应微电流I
S623-3:若感应微电流I≥初设感应微电流I
具体而言,通过所述微孔检测单元进行密封性检测,获取密封性检测结果,包括,在目标药品包装完成后,判断目标药品的组合包装方式(组合包装方式与目标药品的物理形态对应,若为液体一般为瓶装或是袋装、若为固体一般也是至压片瓶装、压片板装、小颗粒胶囊板装、小颗粒胶囊瓶装等多种包装方式),须知的,液体泄露造成的药品污染问题最为常见,基于此,若目标药品的组合包装方式为液体瓶/软袋且存在绝缘瓶装封口/绝缘软袋封口,进行液体泄漏检测,获取密封性检测结果;
进行液体泄漏检测,获取密封性检测结果:在绝缘瓶装封口/绝缘软袋封口的第一面(若为橡胶塞,常见的一端为圆筒状,另一端为圆片状,使用橡胶塞对瓶口进行密封,圆筒状与圆片状相接处与瓶口上端处于同一个平面,在这种状态下,将瓶口倒置,将这种情况定义为绝缘瓶装封口/绝缘软袋封口的第一面与液体瓶/软袋的内部液体充分接触,第一面:绝缘瓶装封口/绝缘软袋封口与内部液体接触的面)与液体瓶/软袋的内部液体充分接触的情况下,在绝缘瓶装封口/绝缘软袋封口的第二面(第二面:圆片状的圆周面)的两端设置发射极与接收极,所述发射极与接收极为所述微孔检测单元的构件;
须知的,发射极的电容值为C
在设置发射极与接收极后,利用所述微孔检测单元的发射极与接收极,进行感应微电流检测,获取感应微电流I,比较感应微电流I与初设感应微电流I
本申请实施例还包括:
S623-4:若初设感应微电流I
S623-5:所述故障检测预警对应的故障检测预警内容包括发射极接触故障与发射极液体残留、接收极接触故障与接收极液体残留。
具体而言,若发射极/接收极存在液体残留、发射极/接收极接触不佳,会发生检测故障:比较感应微电流I与初设感应微电流I
综上所述,本申请实施例所提供的一种药品包装的无菌检测方法及系统具有如下技术效果:
1.由于采用了目标药品包装之前,获取包装用材料、包装用容器;监测消毒灭菌环节,获取第一无菌检测分量、第二无菌检测分量、第三无菌检测分量,发送至药品包装机组,判断是否进行组合包装;若进行组合包装,在目标药品包装完成后,通过微孔检测单元进行密封性检测,获取密封性检测结果,反馈至药品包装机组,基于密封性检测结果、第一无菌检测分量、第二无菌检测分量与第三无菌检测分量构造组合特征,获取目标药品的无菌检测结果,本申请通过提供了一种药品包装的无菌检测方法及系统,实现了分别从药品、材料、容器出发,提高药品包装无菌检测精度,全面落实药品包装无菌检测,及时确定微生物污染,维护无菌检测结果可信度的技术效果。
2.由于采用了设置发射极与接收极;进行感应微电流检测,获取感应微电流I;比较感应微电流I与初设感应微电流I
实施例二
基于与前述实施例中一种药品包装的无菌检测方法相同的发明构思,如图4所示,本申请实施例提供了一种药品包装的无菌检测系统,其中,所述系统包括:
材料、容器获取模块100,用于在对目标药品进行包装之前,获取所述目标药品的包装用材料、包装用容器;以及
第一无菌检测分量获取模块200,用于在药品包装无尘清洁车间中,对所述目标药品的消毒灭菌环节进行监测,获取第一无菌检测分量;
第二无菌检测分量获取模块300,用于在药品包装无尘清洁车间中,对所述目标药品的包装用材料的消毒灭菌环节进行监测,获取第二无菌检测分量;
第三无菌检测分量获取模块400,用于在药品包装无尘清洁车间中,对所述目标药品的包装用容器的消毒灭菌环节进行监测,获取第三无菌检测分量;
组合封装模块500,用于将所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量发送至药品包装机组,判断是否进行组合包装,所述组合包装即目标药品其及包装的组合封装;
密封性检测模块600,用于若进行组合包装,在所述目标药品包装完成后,通过微孔检测单元进行密封性检测,获取密封性检测结果;
无菌检测结果获取模块700,用于将所述密封性检测结果反馈至药品包装机组,基于所述密封性检测结果、所述第一无菌检测分量、所述第二无菌检测分量与所述第三无菌检测分量构造组合特征,获取目标药品的无菌检测结果。
进一步的,所述系统包括:
第一初始检测分量获取模块,用于对所述目标药品进行缺陷检测,获取第一初始检测分量,所述第一初始检测分量包括产品破损检测分量、产品缺块检测分量、产品裂缝检测分量;
第二初始检测分量获取模块,用于在所述目标药品的消毒灭菌环节过程进行物理或化学监测,获取第二初始检测分量,所述第二初始检测分量包括目标药品的灭菌温度和灭菌时间;
第一无菌检测分量生成模块,用于基于所述第一初始检测分量与所述第二初始检测分量,生成所述第一无菌检测分量。
进一步的,所述系统包括:
第三初始检测分量获取模块,用于对所述目标药品的包装用材料进行缺陷检测,获取第三初始检测分量,所述第三初始检测分量包括材料黏合缺陷检测分量、材料张力缺陷检测分量、材料固化缺陷检测分量;
第四初始检测分量获取模块,用于在所述目标药品的包装用材料的消毒灭菌环节过程进行物理或化学监测,获取第四初始检测分量,所述第四初始检测分量包括所述目标药品的包装用材料的灭菌温度和灭菌时间;
第二无菌检测分量生成模块,用于基于所述第三初始检测分量与所述第四初始检测分量,生成所述第二无菌检测分量。
进一步的,所述系统包括:
第五初始检测分量获取模块,用于对所述目标药品的包装用容器进行缺陷检测,获取第五初始检测分量,所述第五初始检测分量包括容器破损检测分量、容器畸形检测分量、容器裂缝检测分量;
第六初始检测分量获取模块,用于在所述目标药品的包装用容器的消毒灭菌环节过程进行物理或化学监测,获取第六初始检测分量,所述第六初始检测分量包括所述目标药品的包装用容器的灭菌温度和灭菌时间;
第三无菌检测分量生成模块,用于基于所述第五初始检测分量与所述第六初始检测分量,生成所述第三无菌检测分量。
进一步的,所述系统包括:
组合包装方式判断模块,用于在目标药品包装完成后,判断目标药品的组合包装方式;
液体泄漏检测模块,用于若目标药品的组合包装方式为液体瓶/软袋且存在绝缘瓶装封口/绝缘软袋封口,进行液体泄漏检测,获取密封性检测结果。
进一步的,所述系统包括:
发射极与接收极设置模块,用于在绝缘瓶装封口/绝缘软袋封口的第一面与液体瓶/软袋的内部液体充分接触的情况下,在绝缘瓶装封口/绝缘软袋封口的第二面的两端设置发射极与接收极,所述发射极与接收极为所述微孔检测单元的构件;
感应微电流检测模块,用于通过所述微孔检测单元的发射极与接收极,进行感应微电流检测,获取感应微电流I;
密封性检测结果获取模块,用于比较感应微电流I与初设感应微电流I
进一步的,所述系统包括:
感应微电流比较模块,用于比较感应微电流I与初设感应微电流I
第一个密封性检测结果确定模块,用于若感应微电流I≤初设感应微电流I
第二个密封性检测结果确定模块,用于若感应微电流I≥初设感应微电流I
进一步的,所述系统包括:
故障检测预警发送模块,用于若初设感应微电流I
故障检测预警内容确定模块,用于所述故障检测预警对应的故障检测预警内容包括发射极接触故障与发射极液体残留、接收极接触故障与接收极液体残留。
综上所述的方法的任意步骤都可作为计算机指令或者程序存储在不设限制的计算机存储器中,并可以被不设限制的计算机处理器调用识别用以实现本申请实施例中的任一项方法,在此不做多余限制。
进一步的,综上所述的第一或第二可能不止代表次序关系,也可能代表某项特指概念,和/或指的是多个元素之间可单独或全部选择。显然,本领域的技术人员可以对本申请进行各种改动和变型而不脱离本申请的范围。这样,倘若本申请的这些修改和变型属于本申请及其等同技术的范围之内,则本申请意图包括这些改动和变型在内。
