一种可快速降解的聚乙二醇水凝胶及应用
文献发布时间:2024-04-18 20:00:50
技术领域
本发明属于生物医药技术领域,具体涉及一种可快速降解的可注射原位化学交联聚乙二醇水凝胶及其应用。
背景技术
聚乙二醇(PEG)因良好的生物相容性,作为合成类高分子材料在生物医药领域广泛应用。PEG水凝胶因富含水分,与组织接近,生物相容性良好,在组织工程,药物缓释,细胞培养等领域受到研究者和医疗企业的青睐。对于某些特殊的临床需求,例如临床某器官、血管即时止血,皮肤创面的保护,肿瘤器官的临时封堵等,需要成胶速度快,强度高且无需长期停留人体的水凝胶体系。在实现功能的同时,快速降解减轻对机体的炎症反应。
以止血、封堵材料为例,近年来,已经陆续开发数款水凝胶产品,例如美国的Coseal、Duraseal、赛脑宁等,均成功应用于临床并上市。在止血、密封功能上,他们都展示的快速凝胶化且强度高的优点。然而这些凝胶降解时间普遍偏慢,在体内停留数周到数个月会引发持续的炎症反应,限制了其更广泛的应用。因临床使用不当需要去除时,传统水凝胶材料必须通过外科手术取出,增加手术风险。
发明内容
为了克服现有技术不足,本发明目的在于提供一种可快速降解的可注射原位化学交联水凝胶及其应用。
本发明具体技术方案如下:
一种快速降解的聚乙二醇水凝胶,由单臂分子量1250~5000Da、4~8臂苯醛基封端的星形多臂聚乙二醇和分子量600~10000Da的聚乙烯亚胺原位交联而成。所述醛基与星形多臂聚乙二醇之间以酯键、醚键、酰胺键、氨酯键、亚胺键或脲键化学键连接。
优选的,所述聚乙二醇水凝胶采用分子量为600~1800Da聚乙烯亚胺,可实现24小时内的快速降解。
本发明所述聚乙二醇水凝胶,采用将苯醛基封端的星形多臂聚乙二醇溶解在pH4.0-6.0(更优选pH4.0)缓冲液中,配置苯醛基封端的星形多臂聚乙二醇溶液;将聚乙烯亚胺溶解在pH7.0-10.0(更优选pH8.0-9.5)缓冲液中,配置聚乙烯亚胺溶液;将两者混合得到聚乙二醇水凝胶,凝胶中苯醛基封端的星形多臂聚乙二醇的浓度为4-60%,聚乙烯亚胺浓度为0.4-40%。
本发明另一目的在于提供所述聚乙二醇水凝胶在制备器官/血管止血、创面修复、器官封合、血管封堵、药物释放、医用植入物涂层、组织防粘连材料中的应用。
本发明优点:本发明通过调节聚乙二醇链结构、分子量以及多氨基交联剂的比例,实现降解时间从2小时到数天的可快速降解的可注射水凝胶。所述聚乙二醇水凝胶在物体表面能快速凝胶化,在体内、体表能快速降解,生物相容性好,强度高,在快速体内器官、血管止血、体表创面修复、器官封合、血管封堵、药物释放、医用内置物涂层、组织防粘连等领域有潜在医学应用。
附图说明
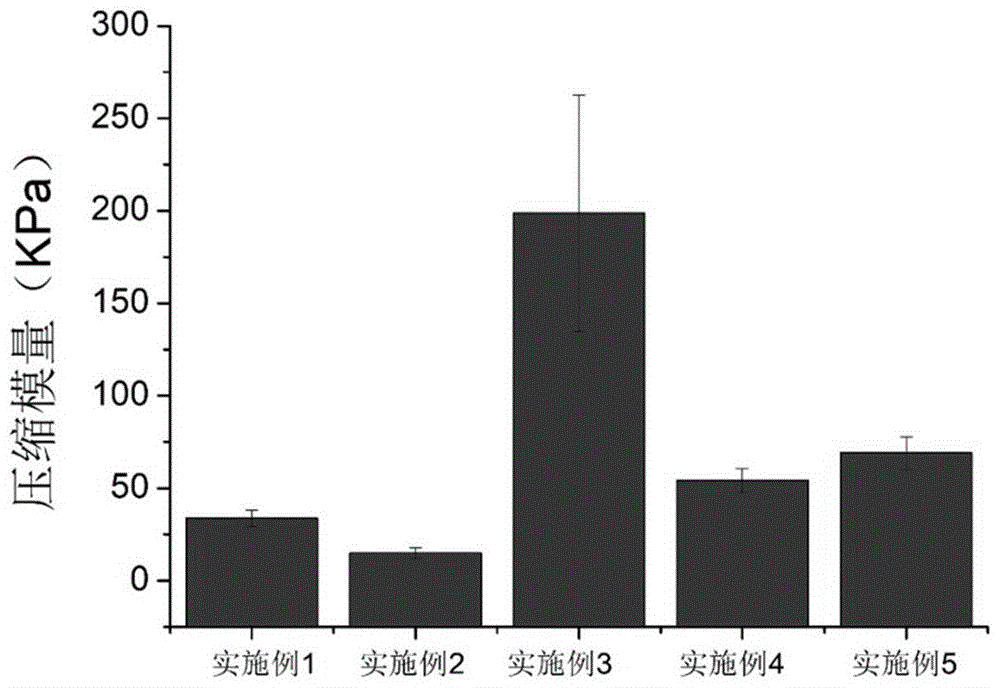
图1实施例1-5水凝胶的压缩模量测试结果。
图2实施例1~5水凝胶体外降解时间。
图3不同分子量聚乙烯亚胺对水凝胶体外降解时间的影响。
图4聚乙二醇溶液浓度对凝胶降解性能的影响。
图5聚乙烯亚胺溶液pH对凝胶降解速率的影响。
图6大鼠皮下植入实施例1凝胶6小时后维持凝胶形态。
图7大鼠皮下植入实施例2凝胶6小时后凝胶降解。
具体实施方式
以下通过实施例说明本发明的具体步骤,但不受实施例限制。
在本发明中使用的术语,除非另有说明,一般具有本领域普通技术人员通常理解的含义。下面结合具体实施例并参照数据进一步详细描述本发明,应理解,这些实施例只是为了举例说明本发明,而非以任何方式限制本发明的范围。
在以下实施例中,未详细描述的各种过程和方法是本领域中公知的常规方法。
实施例1
将1g的4臂苯醛基封端聚乙二醇(10K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(1.8K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.15作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例2
将1g的4臂苯醛基封端聚乙二醇(20K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(1.8K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.15作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例3
将1g的8臂苯醛基封端聚乙二醇(10K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(1.8K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至9.16作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例4
将1g的6臂苯醛基封端聚乙二醇(15K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(1.8K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.15作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例5
将1g的8臂苯醛基封端聚乙二醇(20K Da)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(1.8K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.15作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例6
将1g的8臂苯醛基封端聚乙二醇(10K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(10KDa)溶解在5mL去离子水中,加少量10M磷酸调节pH至9.13作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例7
将1g的8臂苯醛基封端聚乙二醇(20K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(0.6K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.14作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例8
将1g的8臂苯醛基封端聚乙二醇(20K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(10KDa)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.16作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例9
将0.5g的8臂苯醛基封端聚乙二醇(20K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4)溶液中,作为A溶液;取0.09g聚乙烯亚胺(1.8KDa)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.15作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例10
将1.5g的8臂苯醛基封端聚乙二醇(20K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.28g聚乙烯亚胺(1.8K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至8.15作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例11
将1g的8臂苯醛基封端聚乙二醇(20K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(1.8K)溶解在5mL去离子水中,加少量10M氢氧化钠调节pH至7.0作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例12
将1g的8臂苯醛基封端聚乙二醇(20K Da,苯醛基与星形多臂聚乙二醇之间以酯键连接)溶解在5mL的0.02M磷酸缓冲液(pH4.0)溶液中,作为A溶液;取0.19克聚乙烯亚胺(1.8K Da)溶解在5mL去离子水中,加少量10M磷酸调节pH至10.0作为B溶液。通过双联注射器等体积混合A/B两种溶液,形成PEG水凝胶。
实施例13考察实施例1-12制备的PEG水凝胶性能
1.水凝胶成胶时间测试
分别将实施例1~12的A液和B液于37℃恒温水浴锅恒温10min,用移液枪吸取200μl的A液于透明西林瓶中,再用移液枪加入200μlB液时同时掐表计时,加入B液迅速左右摇晃两三秒,倒置观察,不流动则为凝胶状态,记录成胶时间。再向西林瓶中加入2ml去离子水,24h后取浸提液测试pH值,即为凝胶pH。实施例1-12的凝胶成胶时间如表1所示,结果显示实施例1-8、10和12中的水凝胶能在5-25秒内快速凝胶化,而实施例9和实施例11的凝胶固化速率较慢,表明当B液pH较低(pH7)时和A/B溶液浓度降低时凝胶固化速率显著减慢。
表1:水凝胶成胶时间及凝胶pH
2.水凝胶力学性能测试
将实施例1-5制备得到的凝胶10×10×5(长×宽×高,mm),放于拉力仪待测区中央,打开拉力仪仪器进行参数设置,然后对凝胶进行压缩测试,通过数据处理得到凝胶压缩模量,结果如图1所示,凝胶压缩模量在15Kpa-200KPa,可匹配人体不同软硬器官对凝胶强度的要求。
3.水凝胶37℃体外模拟降解
将实施例1-12制备好的凝胶样品于玻璃瓶中,加入凝胶质量10倍的PBS溶液密封,放入37℃恒温水浴振荡里,每半小时观察凝胶状态,记录凝胶形态变化及降解时间。实施例1~5的结果如图2所示。结果显示聚乙二醇的分子量及臂数对凝胶的降解时间有明显影响,在臂数相同的情况下,单臂分子量越大降解时间越短,单臂分子量相同的情况下,臂数越多降解时间越长,除八臂10K分子量PEG,其它四种苯醛基封端多臂聚乙二醇制备凝胶在体外模拟降解均可在6-24小时内凝胶完全降解。不同分子量的聚乙烯亚胺(PEI)对凝胶降解也有明显影响(如图3所示),对于PEG 8-20kDa体系,凝胶降解随着PEI分子量提高而显著变慢,分子量为0.6kDa时,凝胶在2小时左右完全降解,而当分子量增加到10kDa时,凝胶降解时间延长到5天左右。
溶液pH以及星形多臂聚乙二醇和聚乙烯亚胺的浓度对凝胶的降解也有一定的影响。当A/B溶液浓度升高时,降解有一定的加速(如图4所示);当溶液pH过低或者过高时,凝胶降解速率都会加快(如图5所示)。
4.水凝胶体内降解测试
取3只大鼠,水合氯醛麻醉,剔除背部毛发,碘伏消毒,确定大鼠背部皮下的5个点,分别注射实施例1-5制备的水凝胶,每点0.3ml溶液,每2h、6h、12h、24h解剖观察记录凝胶状态,凝胶在6-24小时内完全降解(结果如表2和图6、7所示)。
表2:水凝胶大鼠体内降解观察
- 一种负极片及含有该负极片的金属锂电池
- 一种钛酸锂负极极片、制备方法及钛酸锂电池
- 一种锂电池回收用废旧钛酸锂负极片分离装置
- 复合负极材料及其制备方法、锂离子二次电池负极极片和锂离子二次电池
- 一种可快速嵌锂的负极片及包括该负极片的电池
- 一种锂离子电池负极片快速预嵌锂的方法
