用于防治中性粒细胞活性相关疾病的组方药物
文献发布时间:2024-04-18 20:02:18
技术领域
本发明涉及中医药领域,具体地涉及用于防治中性粒细胞活性相关疾病的组方药物,尤其涉及通过调节中性粒细胞活性防治炎症相关疾病的药物和用途。
背景技术
关节炎是一类发生在人体关节及其周围组织的炎症性疾病的统称,临床特征为关节的红、肿、热、痛、功能障碍与关节畸形等。目前已知的关节炎种类超过100种,如骨关节炎、风湿性关节炎、类风湿关节炎、痛风性关节炎、化脓性关节炎、强直性脊柱炎、反应性关节炎、银屑病关节炎等。关节炎的病因复杂,常见的有退行性病变、超敏反应、代谢紊乱、感染、创伤等。中性粒细胞作为人体外周血中数量最多的白细胞,近年来被发现能够推进类风湿关节炎、痛风性关节炎等部分种类关节炎的病程进展,且中性粒细胞在其中的作用不依赖于其针对细菌感染的免疫监视作用。
类风湿关节炎(RA)是一种常见的慢性全身性自身免疫性疾病,临床特征为持续性、对称性小关节病变。经典理论认为,类风湿关节炎是由T细胞、B细胞等获得性免疫细胞驱动形成的自身免疫性疾病,表现为以免疫复合物沉积为特征的III型超敏反应。但最新研究表明,属于固有免疫系统的中性粒细胞,在类风湿关节炎发展的各个阶段均发挥作用:①该细胞可以释放中性粒细胞胞外诱捕网(NETs),上面携带的瓜氨酸化组蛋白是刺激形成免疫复合物的主要自身抗原之一;②该细胞可以通过释放趋化因子,促进Th17细胞的分化和成熟,导致炎症免疫恶性循环;③该细胞作为效应细胞,在疾病活动期直接造成骨关节无菌性炎症损伤。
急性痛风性关节炎(AGA)是由于体内嘌呤物质代谢异常、血尿酸水平升高,导致单钠尿酸盐(MSU)晶体沉积在关节滑膜、滑囊、软骨及其他组织中引起的反复发作性炎症疾病。主要表现为反复发作性关节红肿热痛与功能障碍,甚至关节畸形、尿酸性肾病等。沉积的MSU晶体通过活化单核/巨噬细胞,进而趋化中性粒细胞大量浸润至关节滑液和滑膜中,并发生爆发式级联扩增反应。浸润的中性粒细胞大量分泌IL-l、IL-8等细胞因子,以及溶酶体酶、氧自由基、花生酸类物质、骨髓相关蛋白S100A8/A9等,推动痛风急性炎症的进展。
根据病因种类与病情进展不同,治疗关节炎可采用药物治疗、辅助治疗和手术治疗等方式。除了反应性关节炎等部分种类外,很多关节炎依靠药物治疗仅能达到临床缓解,而不能自愈。类风湿关节炎的一线治疗包括常规抗炎药物和生物疾病缓解疗法,主要用于控制疼痛和炎症,但很少实现持续缓解。急性痛风性关节炎患者可长期服用别嘌醇减少尿酸合成和丙磺舒促进尿酸盐排出,预防关节炎的急性发作;非甾体类抗炎药、糖皮质激素和秋水仙碱,用于不同程度地改善症状。
已报道了传统中药对于关节炎的治疗。例如,中国专利公布CN114796438A公开一种治疗类风湿关节炎的中药组合物及其制备方法,所述治疗类风湿关节炎的中药组合物由下列重量份的原料组成:制附子10-15重量份,桂枝9-12重量份、麸炒白术12-15重量份、麻黄6-9重量份、白芍15-20重量份、威灵仙10-15重量份、木瓜10-15重量份、生知母9-12重量份、鸡血藤15-30重量份、麸炒苍术10-15重量份、茯苓10-20重量份、伸筋草15-30重量份、生姜6-9重量份、炙甘草6-9重量份、大枣3-6重量份。
中国专利公布CN112138127A公开了一种治疗四肢关节的中药组合物,包括下列重量份的中药原料:牧丹皮8-12份、艾叶10-15份、桑枝10-13份、干姜6-8份、赤芍10-12份、川芎10-13份、鸡血藤8-12份、荆芥6-10份、防风10-14份、姜黄10-12份、羌活10-12份、桂枝6-8份、泽泻10-14份、桑寄生8-12份、丹参10-12份、牛膝10-12份、威灵仙9-12份、赤芍7-12份、千年健10-12份、伸筋草10-12份、入地金牛6-9份。
中国专利公布CN113559169A公开了栀子柏皮汤在制备治疗急性痛风性关节炎药物中的应用,其研究表明,栀子柏皮汤对于急性痛风性关节炎炎症、肿胀具有明显的抑制作用,且短时间给药对小鼠无急性毒性,可进一步开发为用于抗急性痛风性关节炎的药物。
虽然公开了众多针对关节炎的中药,但是目前没有公开能够同时对类风湿关节炎、急性痛风性关节炎等中性粒细胞活性相关疾病有效的中药配方,仍然需要开发更有效的中药配方。
背景技术中的信息仅仅在于说明本发明的总体背景,不应视为承认或以任何形式暗示这些信息构成本领域一般技术人员所公知的现有技术。
发明内容
为解决现有技术中的技术问题,本发明提供组方在制备用于防治中性粒细胞活性相关疾病的药物中的用途。通过胶原诱导型关节炎(CIA)小鼠模型、急性痛风性关节炎(AGA)小鼠模型和胶原抗体诱导型关节炎(CAIA)小鼠模型验证了本申请组方对于关节炎治疗的疗效,并进一步通过组方含药血清研究发现其通过对中性粒细胞活性的调节作用来实现有效治疗。至少部分地基于此完成了本发明。具体地,本发明包括以下内容。
本发明的第一方面,提供组方在制备用于防治中性粒细胞活性相关疾病的药物中的用途,其中,所述组方由金银花、玄参、当归和甘草组成。
在某些实施方案中,根据本发明所述的用途,其中,所述中性粒细胞活性相关疾病包括炎症疾病。
在某些实施方案中,根据本发明所述的用途,其中,所述中性粒细胞活性相关疾病包括类风湿关节炎和/或急性痛风性关节炎。
在某些实施方案中,根据本发明所述的用途,其中,所述组方包括20-120重量份的金银花、50-150重量份的玄参、20-100重量份的当归和0.1-60重量份的甘草。
在某些实施方案中,根据本发明所述的用途,其中,所述组方包含金银花、玄参、当归和甘草的比例为3:3:2:1。
在某些实施方案中,根据本发明所述的用途,其中,所述组方的加工包括:使金银花、玄参、当归和甘草在中浸泡10-90分钟,然后煮沸,接下来文火煎熬10-60分钟,倒出药液,向药渣加适量水煎熬10-30分钟,合并药液,过滤得滤液;或将金银花、玄参、当归、甘草一定比例粉碎后,药粉于水中超声溶解提取得到滤液,离心取上清药液。
在某些实施方案中,根据本发明所述的用途,其中,所述组方的加工进一步包括浓缩所述滤液的步骤。
在某些实施方案中,根据本发明所述的用途,其中,所述防治包括下述中的至少一种:
1)改善或减轻关节的红斑和肿胀;
2)改善或减轻关节炎的严重程度;
3)改善或减轻关节内炎性细胞浸润、滑膜增生和破骨细胞形成;
4)改善或减轻关节组织病理损伤;
5)改善或减轻骨损伤和/或骨破坏;
6)降低或减少中性粒细胞数量;
7)抑制、降低或减少关节炎症因子和趋化因子或其表达;
8)抑制、降低或减少ROS生成。
本发明的第二方面,提供一种体外调节中性粒细胞活性的方法,其包括组方或其制剂与中性粒细胞接触的步骤,所述组方由金银花、玄参、当归和甘草加工制备得到。
在某些实施方案中,根据本发明所述的方法,其中,所述调节包括下述之一:
(1)促进、加快、提高或激活中性粒细胞的凋亡;
(2)抑制、延缓、延迟、降低、减少或减弱中性粒细胞的趋化、ROS产生、炎性因子;
(3)抑制、延缓、延迟、降低或减少中性粒细胞外诱捕网NETs的形成。
本申请通过实验验证了本申请的组方能够通过调节中性粒细胞活性有效缓解CIA、CAIA和AGA小鼠的损伤,减少中性粒细胞迁移到损伤的关节,以及由不适当激活的中性粒细胞引起的免疫损伤。本申请能够为靶向中性粒细胞治疗关节炎,如RA和AGA,提供一种新策略。
附图说明
图1示出了本申请组方减轻了AGA小鼠关节炎症。其中A为72h内AGA小鼠关节肿胀度变化;B为AGA小鼠关节组织炎性因子mRNA水平。数据显示为平均值±SEM,#与对照组相比P<0.05,##与对照组相比P<0.01,*与模型组相比P<0.05,**与模型组相比P<0.01。
图2示出了本申请组方对CAIA模型的作用。其中A为造模后CAIA小鼠关节评分及关节肿胀度变化;B为关节组织炎症因子及中性粒细胞相关趋化因子mRNA水平。数据显示为平均值±SEM,#与对照组相比P<0.05,##与对照组相比P<0.01,*与模型组相比P<0.05,**与模型组相比P<0.01。
图3-图5示出了本申请组方减轻CIA小鼠关节炎症。其中图3A为CIA小鼠爪子的红斑和肿胀症状;图3B为CIA小鼠的关节炎指数评分(每组n=6);图3C为关节组织炎症因子及中性粒细胞相关趋化因子mRNA水平(每组n=3)。图4A为CIA小鼠踝关节苏木精和伊红(H&E)染色、番红-O/固绿染色和Trap染色的代表性图像(每组n=3),比例尺为50微米;图4B为组织病理学半定量评分。图5A为CIA小鼠关节的Micro-CT扫描三维重建图像(每组n=3);图5B为骨参数分析,BMD表示骨密度,TMD表示组织骨密度,BV/TV表示骨小梁体积/总体积,Tb.Th表示骨小梁厚度,Tb.N表示骨小梁数,Tb.Sp表示小梁间隙。数据显示为平均值±SEM,#与对照组相比P<0.05,##与对照组相比P<0.01,###与对照组相比P<0.001,*与模型组相比P<0.05,**与模型组相比P<0.01,***与模型组相比P<0.001。
图6示出了本申请组方降低CIA小鼠脾脏指数及减少脾脏粒细胞,调节粒细胞的分布。其中A为各给药组小鼠的脏器指数;B为流式分析脾脏及外周血的粒细胞数。数据显示为平均值±SEM,#与对照组相比P<0.05,##与对照组相比P<0.01,*与模型组相比P<0.05,**与模型组相比P<0.01。
图7示出了本申请组方含药血清体外抑制炎性因子的表达,抑制中性粒细胞趋化。其中A为不同浓度含药血清干预对炎症因子表达的影响,筛选最佳干预剂量为20%含药血清;B为趋化因子诱导中性粒细胞趋化结果。数据显示为平均值±SEM,#与对照组相比P<0.05,##与对照组相比P<0.01,###与对照组相比P<0.001,*与模型组相比P<0.05,**与模型组相比P<0.01,***与模型组相比P<0.001。
图8示出了本申请组方含药血清体外抑制中性粒细胞NETs生成,抑制ROS产生,并促进炎症状态中性粒细胞凋亡。其中A为PMA诱导中性粒细胞NETs形成的免疫荧光染色的代表性图像,细胞用DAPI、抗CitH3和抗MPO抗体染色,比例尺为50微米,PAD4抑制剂可防止中性粒细胞释放NETs,用作阳性对照;B为PicoGreen法检测骨髓中性粒细胞培养上清中(NETs)游离DNA(cf-DNA)结果;C为流式检测中性粒细胞产生ROS水平,NADPH氧化酶抑制剂用作阳性对照;D为LPS刺激中性粒细胞凋亡的膜联蛋白V/7-AAD染色流式分析结果,FasL是一种凋亡诱导剂,作为阳性对照。数据显示为平均值±SEM,#与对照组相比P<0.05,##与对照组相比P<0.01,###与对照组相比P<0.001,*与模型组相比P<0.05,**与模型组相比P<0.01,***与模型组相比P<0.001。
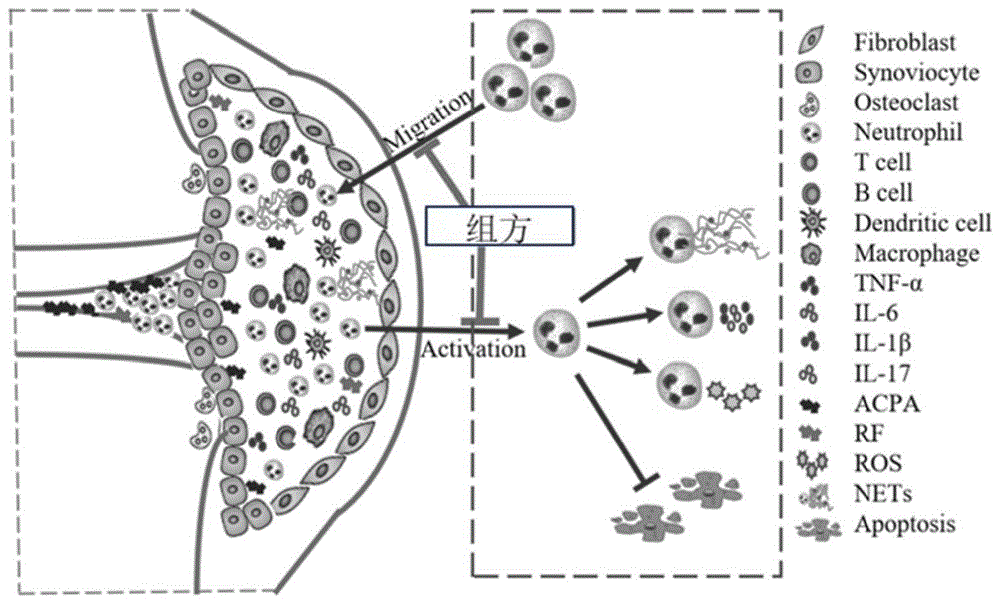
图9示例性说明RA关节中免疫细胞特别是中性粒细胞的作用,其中,示出了本申请组方通过靶向调节失调的中性粒细胞活性来治疗RA。RA的早期特征之一是持续性滑膜炎,这是由免疫细胞持续涌入关节引起的,包括T细胞、B细胞和其他先天免疫细胞,如中性粒细胞、巨噬细胞和树突状细胞,促进炎症因子和小分子介质的产生。本申请组方通过特异性中性粒细胞靶向治疗可显著改善RA。图中ACPA表示抗瓜氨酸肽抗体;RF表示类风湿因子;ROS表示活性氧;NETs表示中性粒细胞细胞外诱捕网。
具体实施方式
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为具体公开了该范围的上限和下限以及它们之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
本文中,术语“防治”指的是在疾病或机能紊乱发生之前或之后改善这种状况。与同等条件下未经治疗的参照组相比,按照任何标准技术来衡量,这种缓解或预防程度至少是5%、10%、20%、40%、50%、60%、80%、90%、95%或100%。在本发明中,防治一般包括治疗和预防。
本文中,药物包括可选的药学上可接受的赋形剂、载体或稀释剂,术语“药学上可接受的赋形剂、载体或稀释剂”指的是一种药学上可接受的材料、组合物或载体,如液体或固体填料、稀释剂、赋形剂、溶剂或封装材料,且该类药学上可接受的材料、组合物或载体参与将药剂从一个器官或身体的某一部位运载或运送至另一个器官或身体的另一部位。每种载体必须是“可接受的”,即指其与配方的其他成分相容且不损害患者。在药学上可接受的载体的部分示例如下:糖,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和马铃薯淀粉;纤维素及其衍生物和类似物,如羧甲基纤维素钠、乙基纤维素和纤维素乙酸酯;西黄蓍胶粉;麦芽;明胶;滑石粉;赋形剂,如可可油和栓剂蜡;油,如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和豆油;二醇类,如丙二醇;多元醇,如甘油、山梨醇、甘露醇和聚乙二醇;酯类,如油酸乙酯和月桂乙酯;琼脂;缓冲剂,如氢氧化镁和氢氧化铝;褐藻酸;无热原水;等渗盐水;林格氏溶液;乙醇;磷酸盐缓冲液;以及药物制剂中使用的其他无毒且相容的物质。润湿剂、乳化剂和润滑剂,如十二烷基磺酸钠、硬脂酸镁、和聚氧乙烯-聚环氧丙烷共聚物以及着色剂、脱模剂、涂层剂、甜味剂、调味剂和芳香剂、防腐剂和抗氧化剂也可存在于组合物中。
本文中,药物可制备为特定剂量。每一种治疗所需总剂量可分成多次或按一次剂量给药。本申请的药物可单独服用,或与其他治疗药物或对症药物合并使用并调整剂量。药物的施用方式没有特别限制,代表性的施用方式包括但并不限于:口服、肌肉注射、静脉注射、静脉滴注、灌肠、喷雾、外敷、或腹腔注射。
本文中,示例性地,用于口服给药的固体剂型包括片剂、丸剂、散剂、颗粒剂、或胶囊剂。在这些固体剂型中,活性成分与至少一种常规惰性赋形剂(或载体)混合,如柠檬酸钠或磷酸二钙,或与下述成分混合:(a)填料或增容剂,例如,淀粉、乳糖、蔗糖、葡萄糖、甘露醇和硅酸;(b)粘合剂,例如,羟甲基纤维素、藻酸盐、明胶、聚乙烯基吡咯烷酮、蔗糖和阿拉伯胶;(c)保湿剂,例如,甘油;(d)崩解剂,例如,琼脂、碳酸钙、马铃薯淀粉或木薯淀粉、藻酸、某些复合硅酸盐、和碳酸钠;(e)缓溶剂,例如石蜡;(f)吸收加速剂,例如,季胺化合物;(g)润湿剂,例如鲸蜡醇和单硬脂酸甘油酯;(h)吸附剂,例如,高岭土;和(i)润滑剂,例如,滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、十二烷基硫酸钠,或其混合物。胶囊剂、片剂和丸剂中,剂型也可包含缓冲剂。
固体剂型如片剂、糖丸、胶囊剂、丸剂和颗粒剂可采用包衣和壳材制备,如肠衣和其它本领域公知的材料。它们可包含不透明剂,并且,这种药物或组合物或活性组分的释放可以延迟的方式在消化道内的某一部分中释放。可采用的包埋组分的实例是聚合物质和蜡类物质。必要时,组合物、药物、单药或活性组分也可与上述赋形剂中的一种或多种形成微胶囊形式。
用于口服给药的液体剂型包括药学上可接受的乳剂、溶液、悬浮剂、糖浆或酊剂。除了活性成分外,液体剂型可包含本领域中常规采用的惰性稀释剂,如水或其它溶剂,增溶剂和乳化剂,例知,乙醇、异丙醇、碳酸乙酯、乙酸乙酯、丙二醇、1,3-丁二醇、二甲基甲酰胺以及油,特别是棉籽油、花生油、玉米胚油、橄榄油、蓖麻油和芝麻油或这些物质的混合物等。
本申请的药物可以单独给药,或者与其他治疗剂联合给药。其他治疗剂的实例包括但不限于能够用于炎症性疾病的小分子化合物或药物。
实施例1
一、实验过程
1、本申请示例性组方制备及该组方含药血清的制备
本实施例的组方为水煎液形式,其制备如下所述:金银花90g,玄参90g,当归60g,甘草30g,十剂共270g。常规方法水煎两次药液合并,过滤,浓缩至600ml(0.45g/ml)。
组方含药血清的制备如下所述:SD大鼠按临床等效剂量6倍剂量给药2.7g/kg所得水煎液。空白血清组大鼠灌胃给予生理盐水。每12h给药1次,共给药5次。末次给药1小时后取血分离血清,灭活。
2、AGA小鼠模型建立
研磨MSU晶体,过40μm筛,无菌生理盐水配制MSU晶体混悬液(50mg·mL
3、CAIA小鼠模型建立
选用7-8周龄雌性Balb/c小鼠。动物模型建立:第0d:尾静脉注射5克隆抗体合剂cocktail 150uL/只,第3d:腹腔注射LPS 70uL/只。尾静脉注射抗体后开始给药,组方组按照临床等效剂量每天给予4.5g·kg
4、CIA小鼠模型建立
牛II型胶原蛋白和完全的弗氏佐剂冰水浴条件下以1:1的比例充分乳化,以滴加水中不扩散为度,Ⅱ型胶原的终浓度为1mg/mL。二次免疫使用不完全弗氏佐剂。DBA/1小鼠分别于第0天和第21天尾根部皮内注射乳化的胶原(100μL/只)诱导建立CIA小鼠模型。初次免疫后2周开始给药。甲氨蝶呤组每3天灌胃给予0.5mg/kg甲氨蝶呤溶液。组方组小鼠每天给予4.5g/kg步骤1所得水煎液。所有动物在关节炎指数评分开始下降后取材。
5、观察及检测指标
5.1小鼠关节症状及评分
观察动物关节红肿症状。关节指数评分:0分:正常,关节无红肿;1分:足趾关节轻度红肿;2分:足趾关节和足跖肿胀;3分:踝以下足爪红肿;4分:包括踝关节在内的全足均红肿并伴功能障碍;AI=四肢关节评分之和。小鼠关节肿胀度=踝关节直径(mm)-初始踝关节直径(mm)。
5.2关节局部炎症因子及趋化因子表达变化
实时荧光定量PCR检测关节局部炎症因子和趋化因子的表达。使用Trizol提取总RNA。2
5.3关节组织病理学评价
HE染色观察关节炎症浸润情况,番红O固绿染色观察软骨破坏情况,并进行0-5级半定量评分。Trap染色观察破骨细胞形成情况,镜下随机选取5个区(×200)进行TRAP(+)细胞计数。
5.4影像学评价
小鼠踝关节Micro-CT扫描后进行三维重建成像,并对骨矿物质含量、骨密度、组织骨矿含量、组织骨密度、相对骨体积、骨小梁厚度、骨小梁分离度、骨小梁数量、骨表面积/骨体积等参数进行相关分析,进行骨破坏评价。
5.5CIA小鼠脾脏、外周血中性粒细胞变化:
小鼠眼球取血,脾脏研磨制备单细胞悬液,使用抗小鼠CD11b-PercpCy5.5、Ly6G-BV510、CD48-PE Cy7抗体标记中性粒细胞,上机前加入计数微球beads,流式检测CIA小鼠脾脏及外周血中性粒细胞数目变化。
二、实验结果
1.本申请组方减轻了AGA小鼠关节炎症
在AGA模型中,结果如图1所示。A为造模后72h内踝关节肿胀度变化,与对照组相比,AGA模型组小鼠踝关节肿胀度明显升高,本申请组方给药组24h、48h、72h与模型组比较均有统计学差异。
根据课题组前期实验结果,AGA 15h炎症高峰取材检测关节炎症因子及趋化因子表达情况,结果如图1B。AGA模型15h关节中炎症因子TNF-α、IL-1β、IL-6及中性粒细胞趋化因子IL-8的mRNA水平均显著升高,本申请组方能够降低关节中炎症因子及趋化因子mRNA水平。
2、本申请的组方减轻了CAIA小鼠关节炎症
CAIA模型结果如图2所示。尾静脉注射抗体后,CAIA模型组小鼠第3天开始出现关节红肿,腹腔注射LPS加强免疫后关节肿胀程度显著增高,关节评分明显上升,第10天关节红肿基本达到峰值,而后关节肿胀程度出现下降,评分降低。与模型组相比,本申请组方明显减轻了CAIA小鼠关节肿胀程度,降低关节评分。
实时定量PCR结果示(图2B),CAIA模型小鼠关节局部炎症因子TNF-α、IL-1β,趋化因子CXCL2、IL-8均有显著升高,本申请组方降低了炎症因子TNF-α、IL-1β及中性粒细胞相关趋化因子mRNA水平。
3、本申请的组方减轻了CIA小鼠关节炎症
CIA小鼠大约在第二次免疫后第3天出现关节炎发作。MTX和本申请组方减轻了关节炎的严重程度,表现为较轻的关节红斑和肿胀以及较低的AI评分(图3A-B)。从第二次免疫后的第3天开始,所有组小鼠的AI评分以时间依赖性模式增加,在第二次免疫后第15天AI评分基本达到峰值。与模型小鼠相比,甲氨蝶呤和本申请的组方在第二次免疫后第6天显著降低AI评分。且在早期阶段,组方药效更为突出(图3B)。
PCR结果示,CIA模型小鼠关节组织中TNF-α、IL-1β、IL-6的表达明显高于正常小鼠,与中性粒细胞募集密切相关的CXCL1、CXCL2和IL-8的表达在CIA模型小鼠中也显著增加。本申请组方抑制了炎症因子及中性粒细胞相关趋化因子的表达(图3C)。
组织病理学染色结果显示,CIA小鼠踝关节内炎性细胞浸润、滑膜增生和破骨细胞形成,并存在关节软骨结构破坏。甲氨蝶呤和本申请组方改善了关节组织病理学损伤。本申请组方在很大程度上降低了踝关节炎症和软骨损伤和/或骨破坏的严重程度和破骨细胞的形成(图4)。
Micro-CT结果所示,在CIA小鼠的踝关节中存在明显的骨破坏(图5A),并伴随着骨参数的变化,包括BMD、TMD、BV/TV、Tb.Th和Tb.N,MTX和本申请组方治疗减少了骨损伤和/或骨破坏。本申请组方在BMD、TMD、BV/TV和Tb.Th方面显示出更好的骨损伤和/或骨破坏保护作用(图5B)。
4、本申请组方能够降低脾脏指数,减少中性粒细胞数量
取材后计算心脏、肝脏、脾脏、肺、肾和脑的脏器指数。在所有这些器官中,与正常小鼠相比,CIA小鼠的脾脏指数和肾脏指数增加。据报道,MTX对CIA肾损伤具有保护作用。本申请组方降低了CIA患者的肾脏指数,但无统计学意义。作为重要的免疫器官之一,本申请组方小鼠的脾脏指数显著低于模型小鼠(图6A)。进一步分析脾脏和外周血中粒细胞的数量。结果显示,CIA模型组小鼠脾脏中性粒细胞数量显著增加,而外周血中性粒细胞数量明显减少,本申请组方减少了CIA小鼠脾脏中性粒细胞数量,增加了外周血中性粒细胞数量(图6B)。提示本申请组方有效调节CIA小鼠炎症状态下中性粒细胞的生成和分布。
实施例2
一、实验过程
1.1含组方血清最佳干预剂量确定
体外培养骨髓来源的巨噬细胞BMDMs,预先分别在含有对照血清和5%、10%、20%含组方血清的完全培养基中孵育24h,100ng/ml LPS和80ng IFN-γ刺激4h,收集细胞和培养上清。实时荧光定量PCR检测TNF-α、IL-6和IL-12的表达,确定组方含药血清体外实验最佳干预剂量。
1.2中性粒细胞趋化检测
骨髓单细胞悬液预先分别在含有对照血清及组方含药血清的培养基中孵育1h,后以3*10
1.3活化后中性粒细胞形成NETs检测
细胞培养上清cf-DNA含量测定:
将骨髓分选的中性粒细胞10
免疫荧光检测中性粒细胞形成NETs水平:
将骨髓分选的中性粒细胞分别接种在含有对照血清、组方含药血清、PAD4抑制剂的培养基中孵育1h;加入PMA刺激3h;按照Volker Brinkmann等人的方法染色,检测中性粒细胞形成NETs水平。激光共聚焦显微镜下观察、拍照。
1.4中性粒细胞凋亡检测
外周血单细胞悬液10
1.5中性粒细胞呼吸爆发功能检测
骨髓单细胞悬液接种在含有对照血清和组方含药血清的培养基孵育1h;加入PMA(0.08uM)刺激,荧光染料DCFH-DA标记;将细胞收集于流式管中,加入抗体进行中性粒细胞表面染色,流式细胞仪检测中性粒细胞产生ROS水平。
二、实验结果
1、本申请组方含药血清对中性粒细胞迁移的抑制作用
通过qRT-PCR检测炎症因子,筛选出含20%本申请组方的血清是体外实验最佳给药浓度(图7A)。中性粒细胞向炎症组织的募集是由细胞因子和趋化因子通过特定受体靶向中性粒细胞驱动的。体外中性粒细胞趋化实验结果显示,CXCL1、CXCL2刺激后,与对照组相比,更多的中性粒细胞趋化到下室。本申请组方的含药血清有效抑制趋化因子诱导的中性粒细胞迁移(图7B)。
2、本申请组方含药血清抑制中性粒细胞NETs形成
中性粒细胞活化后可将染色质DNA释放到细胞外形成NETs,NETs的形成是自身抗原的来源并且NETs中的蛋白酶释放会造成组织损伤,加重炎症反应。激光共聚焦图像显示,PMA刺激后,中性粒细胞形成NETs显著增多。本申请组方含药血清有效抑制PMA诱导的NETs形成(图8A)。此外,与对照组相比,PMA刺激后中性粒细胞培养上清液中的cf-DNA含量显著升高,本申请组方含药血清显著抑制中性粒细胞cf-DNA释放(图8B)。
3、本申请组方含药血清抑制ROS产生
据报道,ROS不仅造成组织氧化损伤,还参与多种刺激引起的NADPH氧化酶激活和NETs形成。为了评估组方对ROS生成的影响,使用DCFH-DA染色进行流式细胞分析。在正常条件下,本申请组方含药血清不影响ROS的产生,但是在PMA诱导的活化状态下,本申请组方含药血清减少了中性粒细胞的ROS产生(图8C)。
6、本申请组方含药血清促进炎症状态中性粒细胞凋亡
细胞凋亡对于炎症组织中中性粒细胞的及时清除和炎症消退至关重要。据报道,炎症关节中的中性粒细胞表现出凋亡延迟,延长了炎症反应并加剧持续的组织损伤。本发明发现,在LPS刺激的炎症状态下,中性粒细胞的凋亡减少,本申请组方含药血清显著促进了LPS刺激的中性粒细胞的早期凋亡(图8D)。
三、结论
大量免疫细胞浸润到炎症关节组织是关节炎一个重要特征,其中中性粒细胞在关节炎的发病机制中至关重要。浸润的中性粒细胞通过产生酶、炎性细胞因子、ROS和NETs来引发和维持关节炎症。本申请的组方通过调节中性粒细胞活性有效缓解AGA、CAIA、CIA三种关节炎模型小鼠的损伤,减少迁移到关节的中性粒细胞数量,以及异常激活的中性粒细胞引起的免疫损伤(图9)。本发明的发现通过靶向中性粒细胞的新策略能够有效治疗RA和AGA。
尽管本发明已经参考示例性实施方案进行了描述,但应理解本发明不限于公开的示例性实施方案。在不背离本发明的范围或精神的情况下,可对本发明说明书的示例性实施方案做多种调整或变化。权利要求的范围应基于最宽的解释以涵盖所有修改和等同结构与功能。
- 岩豆素在制备用于防治与5-脂氧合酶相关疾病的药物中的应用
- 狼毒宁B在制备用于防治神经细胞损伤相关疾病药物中的应用
