一种基于同源重组原理对耳道念珠菌进行基因敲除以及敲除株回补的方法
文献发布时间:2023-06-19 12:24:27
技术领域
本发明涉及领域,特别涉及一种基于同源重组原理对耳道念珠菌进行基因敲除以及敲除株回补的方法。
背景技术
耳道念珠菌是一种新兴病原真菌,因具有多重耐药性和对环境的强胁迫抗性被称为超级真菌。目前对耳道念珠菌的研究十分依赖于在耳道念珠菌中的对特定基因的敲除技术。现有文献中报导的基因敲除技术也是基于同源重组原理在耳道念珠菌中进行基因敲除[DAY A M,MCNIFF M M,DASILVA DANTAS A,et al.Hog1 Regulates Stress Toleranceand Virulence in the Emerging Fungal Pathogen Candida auris[J].Msphere,2018,3(5).],但存在合成敲除片段步骤繁琐,转化子阳性率低,筛选药物价格高昂等问题。目前文献中尚未报导在耳道念珠菌中成功进行过敲除株的回补,已有的在其他真菌中的回补株构建方法经过验证不适用于耳道念珠菌。
发明内容
本发明所要解决的技术问题在于针对上述现有技术中的不足,提供一种基于同源重组原理对耳道念珠菌进行基因敲除以及敲除株回补的方法。
为解决上述技术问题,本发明采用的技术方案是:一种基于同源重组原理对耳道念珠菌进行基因敲除的方法,包括以下步骤:
1)引物设计:将待敲除的目的基因的上、下游同源臂和用于替换该目的基因的敲除抗性基因作为3个片段,分别设计用于扩增上游同源臂的引物对F1与R1、用于扩增下游同源臂的引物对F2与R2,以及用于扩增敲除抗性基因的引物对F3与R3;
2)提取耳道念珠菌的基因组DNA;
3)扩增目的基因上、下游同源臂和敲除抗性基因片段:以含有目的基因的耳道念珠菌基因组DNA为模板,以F1与R1为引物对、F2与R2为引物对分别进行PCR扩增,扩增出目的基因的上、下游同源臂;以含有敲除抗性基因的质粒为模板,以F3与R3为引物进行PCR扩增,扩增出敲除抗性基因片段;
4)空载体酶切及重组质粒构建:将空载体用限制性内切酶进行酶切得到载体质粒片段,将该载体质粒片段与目的基因的上、下游同源臂和敲除抗性基因片段在重组酶反应体系中处理,构建得到重组质粒;
5)重组质粒进行转化:
6)阳性转化子筛选:对步骤5)处理后的重组质粒进行平板筛选获得阳性转化子;挑选出阳性转化子单克隆菌落,以F1、R2为引物对进行菌落PCR,将PCR产物琼脂糖凝胶电泳检测后获得有目的条带的单克隆菌株进行测序,选择序列正确的菌株提取质粒,得到基因敲除重组质粒;
7)敲除插入DNA片段扩增:以基因敲除重组质粒为模板,以F1和R2为引物对扩增出敲除插入DNA片段;
8)耳道念珠菌电转化:将敲除插入DNA片段使用电转化法插入耳道念珠菌基因组中,实现对目的基因的敲除;
9)对步骤8)处理后的耳道念珠菌使用菌落PCR筛选出敲除抗性基因正确插入到耳道念珠菌基因组目的基因位置的阳性转化子,获得耳道念珠菌敲除株。
优选的是,其中,目的基因的上、下游同源臂的长度均为0.9-1.1kb,R1和F2分别与敲除抗性基因的两端至少有15bp同源臂,F1和R2分别与空载体被限制性内切酶进行酶切后的载体质粒片段的两端至少有15bp同源臂。
优选的是,待敲除的目的基因为耳道念珠菌RIM101基因,RIM101基因的序列如SEQID NO:1所示,所述空载体为PRS316质粒,用于RIM101基因敲除的基因敲除重组质粒记为PRS316-RIM101-KNOCKOUT,其序列如SEQ ID NO:2所示。
优选的是,敲除抗性基因为NAT1基因,敲除插入DNA片段的序列如SEQ ID NO:3所示,NAT1基因的序列如SEQ ID NO:4所示;含有敲除抗性基因的质粒为抗性基因NAT1质粒bsn125。
优选的是,所述步骤1)中设计的引物序列为:
F1:CGCTCTAGAACTAGTGAGTTACGCTCAAAGTGCTGCAT;
R1:CGAGGCAAGCTTGATAACGATGTTTGAGGCGAACC;
F2:CTGTCGATTCGATACTAAGCAAAGCTTGTACCCAACGA;
R2:GCAGCCCGGGGGATCGAAGAATTGGTGGCTTGCCA;
F3:ATCAAGCTTGCCTCGTCCC;
R3:TTAGTATCGAATCGACAGCAGTAT。
优选的是,所述步骤9)中,使用菌落PCR筛选时,利用引物对vertify_up_5_RIM101for knockout和vertify_down_5_RIM101for knockout检测敲除插入DNA片段上游结合位点是否正确;利用引物对vertify_up_3_RIM101 for knockout和vertify_down_3_RIM101for knockout检测敲除插入DNA片段下游结合位点是否正确;利用引物对vertify_orf_5_RIM101和vertify_orf_3_RIM101检测目的基因是否被替换掉;当前两对引物扩增出目的片段、第三对引物扩增不出目的基因片段,即表明目的基因被成功敲除;
其中采用的引物的序列如下:
vertify_up_5_RIM101 for knockout:CTTAGTGAAATTGGCCCTTGCCAC;
vertify_up_3_RIM101 for knockout:GGATGTGATGTGAGAACTGTATCC;
vertify_down_5_RIM101for knockout:TATACGATGGTACTGCTTCCGATG;
vertify_down_3_RIM101 for knockout:GTATTGGGCTGATGTATTCACGCC;
vertify_orf_5_RIM101:GCACAATTACCAGGATGACAACCA;
vertify_orf_3_RIM101:TACCGATGTCGTAGGTACCATGGT。
本发明还提供一种基于同源重组原理对耳道念珠菌敲除株进行敲除基因回补的方法,其用于对以上方法所得到的基因敲除菌株进行敲除基因回补,具体包括以下步骤:
S1、引物设计:将被敲除的目的基因的上游同源臂以及该目的基因组成的基因片段记为片段1,分别设计用于扩增片段1的引物对F1与addback-R1,用于扩增下游同源臂的引物对addback-F2与R2,以及用于扩增回补抗性基因的引物对F4与R4;
S2、提取耳道念珠菌的基因组DNA;
S3、扩增片段1、下游同源臂和回补抗性基因片段:以含有目的基因的耳道念珠菌基因组DNA为模板,以F1与addback-R1为引物对进行PCR扩增,扩增出片段1;以addback-F2与R2为引物对分别进行PCR扩增,扩增出目的基因的下游同源臂;以含有回补抗性基因的质粒为模板,以F4与R4为引物进行PCR扩增,扩增出回补抗性基因片段;
S4、空载体酶切及重组质粒构建:将空载体用限制性内切酶进行酶切得到载体质粒片段,将该载体质粒片段与目的基因的上、下游同源臂和回补抗性基因片段在重组酶反应体系中处理,构建得到重组质粒;
S5、重组质粒进行转化:
S6、阳性转化子筛选:对步骤S5处理后的重组质粒进行平板筛选获得阳性转化子;挑选出阳性转化子单克隆菌落,以F1、R2为引物对进行菌落PCR,将PCR产物琼脂糖凝胶电泳检测后获得有目的条带的单克隆菌株进行测序,选择序列正确的菌株提取质粒,得到基因回补重组质粒;
S7、回补插入DNA片段扩增:以基因回补重组质粒为模板,以F1和R2为引物对扩增出回补插入DNA片段;
S8、耳道念珠菌电转化:将回补插入DNA片段使用电转化法插入如权利要求1-7中任意一项所获得的耳道念珠菌敲除株的基因组中,实现对被敲除的目的基因的回补;
S9、对步骤S8处理后的耳道念珠菌使用菌落PCR筛选出回补的目的基因正确插入到耳道念珠菌基因组的原位置的阳性转化子,获得耳道念珠菌敲除株的回补株。
优选的是,该方法用于对RIM101基因被敲除的耳道念珠菌敲除株进行回补,用于RIM101基因回补的基因回补重组质粒记为PRS316-RIM101-addback,其序列如SEQ ID NO:5所示;
回补抗性基因为HygR基因,回补插入DNA片段的序列如SEQ ID NO:6所示,HygR基因的序列如SEQ ID NO:7所示;含有回补抗性基因的质粒为抗性基因HygR质粒bcb299。
优选的是,所述步骤S1中设计的引物序列为:
F1:CGCTCTAGAACTAGTGAGTTACGCTCAAAGTGCTGCAT;
addback-R1:CAAGCTAAACAGATCTTTAGAATGCCGTAATCGTTGGGTA;
addback-F2:TGTCGAAAACGAGCTGGACAGCAATTCTTTCGTTGTGCG;
R2:GCAGCCCGGGGGATCGAAGAATTGGTGGCTTGCCA;
F4:AGATCTGTTTAGCTTGCCTTGTC;
R4:AGCTCGTTTTCGACACTGGATG。
优选的是,所述步骤9)中,使用菌落PCR筛选出RIM101基因正确插入到回补位置时,利用引物对vertify_up_5_RIM101 for addback和vertify_down_5_RIM101 foraddback检测回补插入DNA片段上游结合位点是否正确;利用引物对vertify_up_3_RIM101for addback和vertify_down_3_RIM101 for addback检测回补插入DNA片段下游结合位点是否正确;利用引物对vertify_orf_5_RIM101和vertify_orf_3_RIM101检测目的基因RIM101是否被正确回补;当三对引物均扩增出目的基因片段,即表明目的基因被成功回补;
其中的引物的序列如下:
vertify_up_5_RIM101 for addback:CTTAGTGAAATTGGCCCTTGCCAC;
vertify_up_3_RIM101 for addback:CCAAAACTTCAGGAATTGGTAATG;
vertify_down_5_RIM101for addback:GCTTGGGCACAAGGAAGATGTG;
vertify_down_3_RIM101 for addback:GTATTGGGCTGATGTATTCACGCC;
vertify_orf_5_RIM101:GCACAATTACCAGGATGACAACCA;
vertify_orf_3_RIM101:TACCGATGTCGTAGGTACCATGGT。
本发明的有益效果是:
本发明提供的基于同源重组原理对耳道念珠菌进行基因敲除以及对敲除株进行敲除基因回补的方法能成功实现对特定基因的敲除和敲除株的回补操作,对研究耳道念珠菌这种新兴的耐药超级真菌的研究提供了有力的技术支持。
附图说明
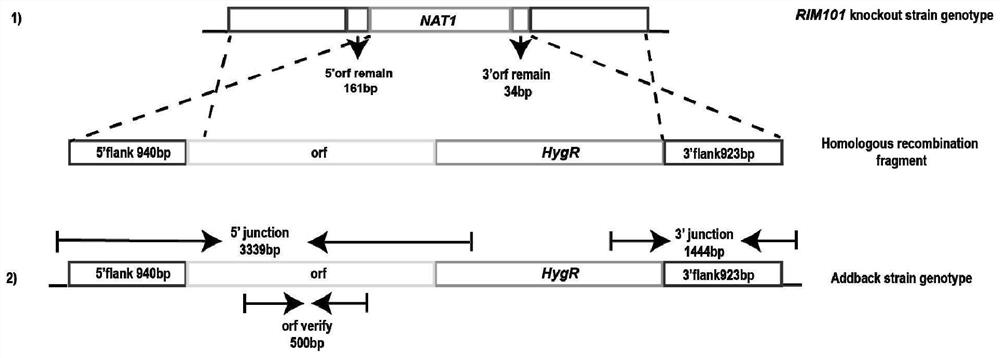
图1为本发明的实施例1的基因敲除方法的设计图;
图2为本发明的实施例2的敲除基因回补方法的设计图;
图3为本发明的实施例1的菌落PCR验证目的基因敲除结果;
图4为本发明的实施例1的RT-qPCR验证RIM101基因敲除的结果。
具体实施方式
下面结合实施例对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合具体实施例及附图对本发明的具体实施方式做详细的说明。在下面的描述中阐述了很多具体细节以便于充分理解本发明。但是本发明能够以很多不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施的限制。
实施例中采用试剂和仪器如非特别说明,均为本领域常规选择。实施例中未注明具体条件的实验方法,通常按照常规条件,例如文献、书本中的条件或者试剂盒生产厂家推荐的方法实现。实施例中所使用的试剂均为市售。
实施例1
本实施例提供一种基于同源重组原理对耳道念珠菌进行基因敲除的方法,本实施例以在耳道念珠菌中进行RIM101基因(系统命名B9J08_003060)的敲除为了进行说明,本实施例中采用的敲除抗性基因为NAT1基因。参照图1为本实施例的方法的设计图。
实验材料的准备:耳道念珠菌BJCA001(中国第一株耳道念珠菌分离株)[WANG X,BING J,ZHENG Q,et al.The first isolate of Candida auris in China:clinical andbiological aspects[J].Emerg Microbes Infect,2018,7(1):93.]、大肠杆菌(DH5α)感受态、空载体PRS316、硫酸诺尔斯菌素(Nourseothricin)、抗性基因NAT1质粒bsn125、限制性内切酶BamHI、TaKaRa Ex
F1:CGCTCTAGAACTAGTGAGTTACGCTCAAAGTGCTGCAT;
R1:CGAGGCAAGCTTGATAACGATGTTTGAGGCGAACC;
F2:CTGTCGATTCGATACTAAGCAAAGCTTGTACCCAACGA;
R2:GCAGCCCGGGGGATCGAAGAATTGGTGGCTTGCCA;
F3:ATCAAGCTTGCCTCGTCCC;
R3:TTAGTATCGAATCGACAGCAGTAT;
vertify_up_5_RIM101 for knockout:CTTAGTGAAATTGGCCCTTGCCAC;
vertify_up_3_RIM101 for knockout:GGATGTGATGTGAGAACTGTATCC;
vertify_down_5_RIM101for knockout:TATACGATGGTACTGCTTCCGATG;
vertify_down_3_RIM101 for knockout:GTATTGGGCTGATGTATTCACGCC;
vertify_orf_5_RIM101:GCACAATTACCAGGATGACAACCA;
vertify_orf_3_RIM101:TACCGATGTCGTAGGTACCATGGT;
RIM101基因的序列如SEQ ID NO:1所示,其中的下划线部分为RIM101基因ORF。
本实施例的基因敲除方法包括以下步骤:
1、引物设计:将待敲除的目的基因的上、下游同源臂和用于替换该目的基因的敲除抗性基因作为3个片段,分别设计用于扩增上游同源臂的引物对F1与R1、用于扩增下游同源臂的引物对F2与R2,以及用于扩增敲除抗性基因的引物对F3与R3,各引物序列分别如上所示;
其中,目的基因的上、下游同源臂的长度均为1kb左右,优选为0.9-1.1kb,过短的长度会降低基因敲除转化子获得数量,过长的长度会提高重组质粒构建难度。R1和F2分别与敲除抗性基因的两端至少有15bp同源臂,F1和R2分别与空载体被限制性内切酶进行酶切后的载体质粒片段的两端至少有15bp同源臂;所有同源臂的TM值应大于45℃。
2、提取耳道念珠菌的基因组DNA;
1)于10ml的YPD培养基过夜培养耳道念珠菌;
2)取1.5ml菌液到1.5ml EP管,高速离心1min,室温;
3)弃上清,加1ml ddH2O重悬,高速离心1min,室温;
4)弃去上清,加入200μL breaking buffer、200μL酸洗玻璃珠、200μL酚-氯仿(pH8.0);
5)剧烈震荡5min;
6)再加入200μL ddH2O或者TE;
7)最高速离心5min,室温;
8)将上清转移到新的1.5ml EP管,再加入200μL酚氯仿(pH 8.0),震荡混匀,最高速离心5min,室温;
9)将上清转移到新的1.5ml EP管,再加入200μL氯仿,震荡混匀,最高速离心5min,室温;
10)将上清转移到新的1.5ml EP管,再加入1ml 100%酒精,震荡混匀,-20℃沉淀20min;
11)最高速离心10min,4℃,弃去上清,加750μL75%酒精,震荡混匀。
12)10000rpm离心10min,4℃,弃去上清,超净台吹干;加入100μl ddH
3、扩增目的基因上、下游同源臂和敲除抗性基因片段:以含有目的基因的耳道念珠菌基因组DNA为模板,以F1与R1为引物对、F2与R2为引物对分别进行PCR扩增,扩增出目的基因的上、下游同源臂;以含有敲除抗性基因的质粒为模板,以F3与R3为引物进行PCR扩增,扩增出敲除抗性基因片段;
使用Takara公司的TaKaRa Ex
反应条件:98℃预变性30s;98℃变性10s,55℃复性15s,72℃延伸(延伸速度为1kb/min,延伸时间按照所需扩增片段长短计算),30个循环;72℃终延伸7min。PCR产物用1%琼脂糖凝胶电泳检测条带大小和特异性。
4、空载体酶切及重组质粒构建:将空载体PRS316质粒用限制性内切酶BamHI进行酶切得到载体质粒片段,将该载体质粒片段与目的基因的上、下游同源臂和敲除抗性基因片段在重组酶反应体系中处理,构建得到重组质粒:
将空载体PRS316质粒用限制性内切酶BamHI进行酶切后,用琼脂糖凝胶回收试剂盒对目的基因上下游同源臂片段、抗性基因NAT1片段和载体质粒片段进行胶回收,再将回收得到的片段在
5、重组质粒进行转化:
重组酶反应终止后,立即进行重组质粒的转化,从反应体系中取10μL样品在冰上与100μL大肠杆菌DH5α化学感受态混合,并冰浴30min,然后在42℃水浴锅中热激90s,立即放入冰上,5min后在体系中加入1mL无抗性LB培养基溶液,在37℃摇床中孵育1h后,将样品涂布于100μg/mL氨苄青霉素(Amp)抗性固体LB平板,在37℃培养箱中倒置培养12h。
6、阳性转化子筛选:对步骤5)处理后的重组质粒进行平板筛选获得阳性转化子;挑选出10个阳性转化子单克隆菌落,落分别放于装有100μg/mL Amp的液体LB培养基的10mL的离心管中,在37℃摇床中摇菌12h。取其中1μL菌液为PCR模板,以F1、R2为引物对进行菌落PCR。PCR产物用琼脂糖凝胶电泳检测,如有目的条带(长度为目的基因上下游同源臂长度加上抗性基因片段长度3.2kb),选取3个单克隆菌液(每个100μL菌液)送公司测序。若序列正确即可得到表达重组质粒的大肠杆菌菌株,选择序列正确的菌株提取质粒,得到基因敲除重组质粒,记为PRS316-RIM101-KNOCKOUT,其序列如SEQ ID NO:2所示。
7、敲除插入DNA片段扩增:以基因敲除重组质粒为模板,以F1和R2为引物对扩增出敲除插入DNA片段。
将上一步的测序结果比对正确的菌株接种到装有100μg/mL Amp的液体LB培养基的10mL的离心管中,在37℃摇床中摇菌12h液进行摇菌,用天根公司的快速质粒小提试剂盒提取质粒。将基因敲除重组质粒PRS316-RIM101-KNOCKOUT作为模板,以引物F1和R2为引物对进行敲除插入DNA片段扩增的扩增,扩增使用TaKaRa Ex
敲除插入DNA片段的序列如SEQ ID NO:3所示,SEQ ID NO:3所示的序列中的下划线部分为NAT1基因的序列,NAT1基因的序列如SEQ ID NO:4所示。
8、耳道念珠菌电转化:将敲除插入DNA片段使用电转化法插入耳道念珠菌基因组中,实现对目的基因的敲除。
实验中用于筛选表达了NAT1基因的耳道念珠菌的平板为加入了硫酸硫酸诺尔斯菌素的YPD平板,其中硫酸硫酸诺尔斯菌素来源于细格3%中生菌素水剂。将3%中生菌素水剂4000rpm离心5min后,用22μm的细菌过滤器过滤,以1:50的比例加入YPD平板中,即为NAT1抗性筛选平板,这种办法配制的平板对耳道念珠菌具有较高的筛选效果,同时药物成本较低。
其中,电转化方法如下:
1)接少许耳道念珠菌于50ml YPD液体培养基中,30℃过夜培养;
2)保证耳道念珠菌OD600在0.8~1.0内,转移到新的50ml离心管中,4000rpm室温离心5min;
3)弃上清,加40ml ddH2O重悬,4000rpm室温离心5min;
4)弃上清,依次加8ml ddH2O、1ml 10×TE(pH8.0)、1ml 1M LiOAC混匀,30℃,150rpm 1h;
5)加250μL 1M DTT,接着培养30min;
6)加40ml ddH2O混匀,4000rpm,4℃离心5min;
7)弃上清,加25ml冷的ddH2O重悬,4000rpm,4℃离心5min;
8)弃上清,加5ml 1M山梨醇重悬,4000rpm,4℃离心5min;
9)弃上清,加50μL 1M山梨醇混匀,放置冰上;
10)取出准备好的插入DNA片段,放置冰上待其融化;
11)取10μL酶切片段和60μL的制备好的耳道念珠菌感受态细胞混匀,冰上放置10min;
12)取出准备好的电击杯,冰上放置10min;
13)期间,准备好5ml 1M山梨醇;
14)取耳道念珠菌感受态细胞和敲除插入DNA片段混合物到电击杯中,确保无气泡,电转,用1ml 1M山梨醇吹洗,转移到新的1.5ml EP管中,3000rpm室温离心2min;弃上清,加1ml YPD,30℃培养4h;
15)3000rpm室温离心1min,弃去800μL,剩下200μL混匀,涂在含NAT的YPD平板上;30℃培养两天,即可得到单克隆菌株。
9、对步骤8)处理后的耳道念珠菌使用菌落PCR筛选出敲除抗性基因正确插入到耳道念珠菌基因组目的基因位置的阳性转化子,获得耳道念珠菌敲除株。
其中,利用引物对vertify_up_5_RIM101 for knockout和vertify_down_5_RIM101for knockout检测敲除插入DNA片段上游结合位点是否正确;利用引物对vertify_up_3_RIM101 for knockout和vertify_down_3_RIM101 for knockout检测敲除插入DNA片段下游结合位点是否正确;利用引物对vertify_orf_5_RIM101和vertify_orf_3_RIM101检测目的基因是否被替换掉;当前两对引物扩增出目的片段、第三对引物扩增不出目的基因片段,即表明目的基因被成功敲除。
其中,菌落PCR具体步骤如下。
1)用无菌移液器吸头挑取在抗性平板中长出来的单菌落(50个),接种到新的NAT抗性平板中,30℃培养一天等待菌体长出;
2)用无菌移液器吸头刮取少量的菌体,轻轻地吹打几次将菌重悬在装有15μLZymolyase缓冲液的PCR管中;
3)低速离心1-2秒将PCR管中的液体甩至管底;
4)放入PCR仪中,启动程序:37℃,15min;95℃,10min;4℃保存;
5)取出PCR管,加入135μL无菌去离子水,混匀后取5μL作为DNA模板进行普通的PCR反应;
6)PCR反应,使用诺唯赞2×Taq Master Mix(Dye Plus)反应体系;
7)用琼脂糖凝胶电泳检测扩增片段;
8)将上一步获得的敲除株用按1000μl菌液加入500μL灭菌50%甘油,混匀后用液氮速冻贮存于-80℃冰箱,得到目的基因敲除菌株。并用RT-qPCR进一步验证了敲除基因不表达。参照图3,为菌落PCR验证目的基因敲除结果,相对于野生型菌株(WT Up Down ORF),敲除株(rim101ΔUp Down ORF)可以扩增出抗性基因NAT1和被敲除基因的上下游DNA的接合片段,证明NAT1插入了目的基因的位点。敲除株扩增不出目的基因的片段,证明目的基因片段已被成功替换。
参照图4,为RT-qPCR验证RIM101基因敲除的结果,将野生型耳道念珠菌和RIM101基因敲除株接种到YPD液体培养基中30℃培养6h至对数期,每组菌株取三个重复样抽提RNA,反转录成cDNA之后通过RT-qPCR来检测RIM101基因转录水平表达情况。RT-qPCR验证了RIM101基因在敲除株中无表达,表明敲除结果是可靠的。图中的横坐标WT表示野生型耳道念珠菌,rim101Δ表示RIM101基因敲除株。
实施例2
本实施例提供一种基于同源重组原理对耳道念珠菌敲除株进行敲除基因回补的方法,本实施例中以对实施例1所得到的耳道念珠菌RIM101基因敲除菌株进行回补为例作出具体说明。本实施例中采用的回补抗性基因为HygR基因,参照图2,为本实施例的方法的设计图。
实验材料的准备:实施例1得到的耳道念珠菌RIM101基因敲除株、大肠杆菌(DH5α)感受态、空载体PRS316、潮霉素(hygromycin)抗性基因HygR质粒bcb299、限制性内切酶BamHI、TaKaRa Ex
F1:CGCTCTAGAACTAGTGAGTTACGCTCAAAGTGCTGCAT;
addback-R1:CAAGCTAAACAGATCTTTAGAATGCCGTAATCGTTGGGTA;
addback-F2:TGTCGAAAACGAGCTGGACAGCAATTCTTTCGTTGTGCG;
R2:GCAGCCCGGGGGATCGAAGAATTGGTGGCTTGCCA;
F4:AGATCTGTTTAGCTTGCCTTGTC;
R4:AGCTCGTTTTCGACACTGGATG;
vertify_up_5_RIM101 for addback:CTTAGTGAAATTGGCCCTTGCCAC;
vertify_up_3_RIM101 for addback:CCAAAACTTCAGGAATTGGTAATG;
vertify_down_5_RIM101for addback:GCTTGGGCACAAGGAAGATGTG;
vertify_down_3_RIM101 for addback:GTATTGGGCTGATGTATTCACGCC;
vertify_orf_5_RIM101:GCACAATTACCAGGATGACAACCA;
vertify_orf_3_RIM101:TACCGATGTCGTAGGTACCATGGT。
其中的部分引物与实施例1相同。
本实施例的方法包括以下步骤:
S1、引物设计:将被敲除的目的基因的上游同源臂以及该目的基因组成的基因片段记为片段1,分别设计用于扩增片段1的引物对F1与addback-R1,用于扩增下游同源臂的引物对addback-F2与R2,以及用于扩增回补抗性基因的引物对F4与R4;
其中,上、下游同源臂为1kb左右的长度,过短的长度会降低基因敲除转化子获得数量,过长的长度会提高重组质粒构建难度。同时addback-R1和addback-F2与回补抗性基因HygR两端至少有15bp同源臂,RIM101-F1和RIM101-R2分别与载体PRS316被BamHI酶切之后的两端有15bp同源臂,所有同源臂的TM值应大于45℃。
S2、提取耳道念珠菌的基因组DNA,具体操作步骤同实例1。
S3、扩增片段1、下游同源臂和回补抗性基因片段:以含有目的基因的耳道念珠菌基因组DNA为模板,以F1与addback-R1为引物对进行PCR扩增,扩增出片段1;以addback-F2与R2为引物对分别进行PCR扩增,扩增出目的基因的下游同源臂;以含有回补抗性基因的质粒为模板,以F4与R4为引物进行PCR扩增,扩增出回补抗性基因HygR;
其中的PCR扩增体系同实例1。
S4、空载体酶切及重组质粒构建:将空载体用限制性内切酶进行酶切得到载体质粒片段,将该载体质粒片段与目的基因的上、下游同源臂和回补抗性基因片段在重组酶反应体系中处理,构建得到重组质粒;具体操作步骤同实例1。
S5、重组质粒进行转化,具体操作步骤同实例1。
S6、阳性转化子筛选:对步骤S5处理后的重组质粒进行平板筛选获得阳性转化子;挑选出阳性转化子单克隆菌落,以F1、R2为引物对进行菌落PCR,将PCR产物琼脂糖凝胶电泳检测后获得有目的条带的单克隆菌株进行测序,选择序列正确的菌株提取质粒,得到基因回补重组质粒。其中,目的条带长度为目的基因上下游同源臂长度+RIM101基因长度+抗性基因片段长度,共5.2kb,其他步骤同实例一。基因回补重组质粒记为PRS316-RIM101-addback,其序列如SEQ ID NO:5所示。
S7、回补插入DNA片段扩增:以基因回补重组质粒为模板,以F1和R2为引物对扩增出回补插入DNA片段;具体操作步骤同实例1。
回补插入DNA片段的序列如SEQ ID NO:6所示,SEQ ID NO:5所示的序列中的下划线部分为HygR基因的序列,HygR基因的序列如SEQ ID NO:7所示;
S8、耳道念珠菌电转化:将回补插入DNA片段使用电转化法插入实施例1所获得的耳道念珠菌RIM101基因敲除株的基因组中,实现对被敲除的目的基因的回补。实验中用于筛选表达了HygR基因的耳道念珠菌的平板为加入了1mg/ml潮霉素的YPD平板,这个浓度的平板对耳道念珠菌具有较高的筛选效果。具体电转化操作步骤同实例1。
S9、对步骤S8处理后的耳道念珠菌使用菌落PCR筛选出回补的目的基因正确插入到耳道念珠菌基因组的原位置的阳性转化子,获得耳道念珠菌敲除株的回补株。其中使用菌落PCR筛选出RIM101基因是否正确插入到回补位置时:利用引物对vertify_up_5_RIM101for addback和vertify_down_5_RIM101 for addback检测回补插入DNA片段上游结合位点是否正确;利用引物对vertify_up_3_RIM101 for addback和vertify_down_3_RIM101 foraddback检测回补插入DNA片段下游结合位点是否正确;利用引物对vertify_orf_5_RIM101和vertify_orf_3_RIM101检测目的基因RIM101是否被正确回补;当三对引物均扩增出目的基因片段,即表明目的基因被成功回补。
S10、将上一步获得的回补株用按1000μl菌液加入500μL灭菌50%甘油,混匀后用液氮速冻贮存于-80℃冰箱,得到敲除菌株的回补株;并用RT-qPCR进一步验证回补基因的表达。
1、RIM101基因的序列SEQ ID NO:1如下(其中的下划线部分为RIM101基因ORF):
GCCTACGCTCTCACATTGTTCTTCACCGGTGGCCTTTGCGTGGCGTTACTCTCTATTTACGCCATTGGCTCTTTGGATGAAAGCAGAGATGCTCCAGGCACATTTTTGGTGCTGAAATTTTGGAGGGTTTCTTGGAGGTTACCGGCTGCAATCGCTATCCTTGCTCTCGGATTCTTGAACATTGGAATCACCGCGGTGATGGCCTCTACAGCGGCAATTCTCATTGCTCTTTACTTTTACGAAAGTGTTGTTTCGACTCCCAAACGCTACCTTGCTTTTGGCGAGTATTTCAATGGTACTGCTGCTAATTAGTACTTTTATATGCTGTTGAACTATGAAAAAGTTTGTAATACAGCTGTAGTTGACTTCTACAAATCTGTAAATTCTATCACTATTGTGATATTCCCTTCAGACATTATCGACCAAATGCGATCACTATACTCCACTCGAGGTTGAGCGAATGACAAGAATTACATAGTACAAAGCAGTCTATTGAATGATCGACATACTTTTAGTAATACAATGTATTCTTCATATGGAATTACGCGTGTTTGACGTTTGGGAGGTGACGAAGATTACCACACTTGGACCAAGAAATTCGTAGCGCTTAGCCAAGAATCCAAAATCATGGGGATACAATCTCATAGCACCAAGATTAGGCGAGCAATTTTCTAAAGCAAATGATAGAGATGAGGGATTTTGTCACTGTCACAGGCTCAAATAAATGGTAATTCAAGTAAATGATGGTAACTTGTGACATTTTTTTTCTTGTATGCATATGTGTACACGAATTTGTATTCTTACGGACTATATATAACGAGTACGGCATTGCACCAGTGCCTTCTCTCTCTCTCTCTATATATATATATGTTTTGTTTTCTTTGTCGAATACGTTGATTGAGGGTCGCTAGGGTCAAGATGTTTGACACATCTCTTCCTCAGCTTTCAAACTATACAAATCTATATAGTAAAACCAATTGCAACATAAAAAAAAAAGGACTTTTCATCATCATAAAGGATACCTAGTGTTCCTAACGAGAAATGCAAACCTCCCCTTCTGAAATTAAAAATGTGGAGTTCTTCTGTGATTATCTTGTCTTAGTGAAATTGGCCCTTGCCACCGCCTATTGGCTATTTTTTTGGGTTTATTCGGTCTTCAAAAGGATATGAGGGATAGAAGAAGTGTGAGATTCCAGAAAAGCAAAGAAGGTCCTGCATATTAGTTACGCTCAAAGTGCTGCATGTCATGAAGCGTGCAAGACTTTTTATAAGGAGTTCCTCTCGGTGGCCAAGCTGGCTAAGGCGCGAGACTGTAATGTGTGATTGTAATCTTGAGATCGGGTGTTCGACTCACCCCCGGGAGACTTCTTTCTATTGCCTTTATGGCCAAGTTGGTAAGGCACCTCACTAGTAATGAGGAGATCGTCAGTTCGAATCTGGCTGAAGGCAATATTTAGTTTTTTTGCCGCTTTTCACGTACAGATCACCAAAAGATTAGATCCTGTCAAGATATTTGGCAGAATGCAACGTTAGATTTGTAGGTGAAGTGACTCGGCTCCGATACCGAGGAAAAAAATCCAGATCTTGTGCAGTCTGTGGGCGTGGACCGACAGTGTGCAGGCTACTTTTTTCTTAACTATGAGGAAAAGCGCAACAAGATGGGCAGACAGTCGCACACTTTACTTTTTCGTACAATTTCTTTTCTCAATTTCTTGGGAACAAGGAGTTAATGGGTCGCTGAAGATATATGCAGTACGCTTTTACTTGGCGACAAACTTCTTGGCAAGCTTTTATCAAATGACCATCCTGCCTCAGCCTTTGGACAGATAAATAAATCTGGCGCCAAATCCGCAGAGAAAGAGTAACCCTCATTTACTTTTTTCCACGCACGTTCATCACGCTCTCCACCGAATTTTAACCAGTATCATCATATTACAATAGCACACACGAAGATTCAAGAGAGCAAAAAAATAAAGGGAGAGTTCAATATAAAGCAAAAC
2、敲除插入DNA片段的序列SEQ ID NO:3如下(其中,下划线部分为NAT1基因的序列):
AGTTACGCTCAAAGTGCTGCATGTCATGAAGCGTGCAAGACTTTTTATAAGGAGTTCCTCTCGGTGGCCAAGCTGGCTAAGGCGCGAGACTGTAATGTGTGATTGTAATCTTGAGATCGGGTGTTCGACTCACCCCCGGGAGACTTCTTTCTATTGCCTTTATGGCCAAGTTGGTAAGGCACCTCACTAGTAATGAGGAGATCGTCAGTTCGAATCTGGCTGAAGGCAATATTTAGTTTTTTTGCCGCTTTTCACGTACAGATCACCAAAAGATTAGATCCTGTCAAGATATTTGGCAGAATGCAACGTTAGATTTGTAGGTGAAGTGACTCGGCTCCGATACCGAGGAAAAAAATCCAGATCTTGTGCAGTCTGTGGGCGTGGACCGACAGTGTGCAGGCTACTTTTTTCTTAACTATGAGGAAAAGCGCAACAAGATGGGCAGACAGTCGCACACTTTACTTTTTCGTACAATTTCTTTTCTCAATTTCTTGGGAACAAGGAGTTAATGGGTCGCTGAAGATATATGCAGTACGCTTTTACTTGGCGACAAACTTCTTGGCAAGCTTTTATCAAATGACCATCCTGCCTCAGCCTTTGGACAGATAAATAAATCTGGCGCCAAATCCGCAGAGAAAGAGTAACCCTCATTTACTTTTTTCCACGCACGTTCATCACGCTCTCCACCGAATTTTAACCAGTATCATCATATTACAATAGCACACACGAAGATTCAAGAGAGCAAAAAAATAAAGGGAGAGTTCAATATAAAGCAAAACATGTCCAGCAACTACAACCTCCATCCGGTGACATACCTCAATGCCACTGCCGAAAAGGTGATGGACTCTGAAGTCGACTTTGACCTTGACGCTGTTAGCGACGCTGTTTCGACCAACTCCCCCACAACCCAACTGCTGAACGGTTCGCCTCAAACATCGTT
3、回补插入DNA片段的序列SEQ ID NO:6如下(其中,下划线部分为HygR基因的序列):
CGCTCTAGAACTAGTGAGTTACGCTCAAAGTGCTGCATGTCATGAAGCGTGCAAGACTTTTTATAAGGAGTTCCTCTCGGTGGCCAAGCTGGCTAAGGCGCGAGACTGTAATGTGTGATTGTAATCTTGAGATCGGGTGTTCGACTCACCCCCGGGAGACTTCTTTCTATTGCCTTTATGGCCAAGTTGGTAAGGCACCTCACTAGTAATGAGGAGATCGTCAGTTCGAATCTGGCTGAAGGCAATATTTAGTTTTTTTGCCGCTTTTCACGTACAGATCACCAAAAGATTAGATCCTGTCAAGATATTTGGCAGAATGCAACGTTAGATTTGTAGGTGAAGTGACTCGGCTCCGATACCGAGGAAAAAAATCCAGATCTTGTGCAGTCTGTGGGCGTGGACCGACAGTGTGCAGGCTACTTTTTTCTTAACTATGAGGAAAAGCGCAACAAGATGGGCAGACAGTCGCACACTTTACTTTTTCGTACAATTTCTTTTCTCAATTTCTTGGGAACAAGGAGTTAATGGGTCGCTGAAGATATATGCAGTACGCTTTTACTTGGCGACAAACTTCTTGGCAAGCTTTTATCAAATGACCATCCTGCCTCAGCCTTTGGACAGATAAATAAATCTGGCGCCAAATCCGCAGAGAAAGAGTAACCCTCATTTACTTTTTTCCACGCACGTTCATCACGCTCTCCACCGAATTTTAACCAGTATCATCATATTACAATAGCACACACGAAGATTCAAGAGAGCAAAAAAATAAAGGGAGAGTTCAATATAAAGCAAAACATGTCCAGCAACTACAACCTCCATCCGGTGACATACCTCAATGCCACTGCCGAAAAGGTGATGGACTCTGAAGTCGACTTTGACCTTGACGCTGTTAGCGACGCTGTTTCGACCAACTCCCCCACAACCCAACTGCTGAACGGTTCGCCTCAAACATCGTTCACATCGCAATCATCTGCTAATTCTCCCGTGCTGCAAACCGCCAACTTCGGCAAAGATTTCACTAACGCCCATTTTGGTGCCCGTGCTACTGGGTTCGCCGGCACAGCTTTCGACATGAAGCAAGAAAACCAACAACATGATAAGCTGCAAACCGCTCCGCACAATTACCAGGATGACAACCACTCGTGTGGAGCGAGCGCGGGGGAAAAGAAGAAGCCTAAGAAAACTTACAGAAAAGTTCGCGATGCCGACATGAAGGGTCCCTTCAACTGCCAGTGGAGTGGGTGCCTGTTGATCTTTGACACTCCAGAGGAGTTATACGATCACTTGTGCAACGAGCACGTTGGGCGCAAGCTGTCGAACAACTTGTCTTTGACATGCGATTGGGATAACTGCGGTGTTACCACCGTAAAGAGAGACCACATCACCTCGCACTTGCGTGTACATGTTCCTTTGAAGCCATACCGCTGCAACTTGTGCACAAAGAGCTTCAAGAGGCCTCAGGATTTAAAGAAGCACTCGAGAACGCACGAGGATGAACACCAGCGCAAGTTGAAGAAGTCTCAGAAGATGAACGATAGGGACGAGAGTGGGTTGAACAAAGCGGTCTACCCAATGCCCATGTTGCCTGCTCACCATGGTACCTACGACATCGGTAGCGCTTACTACCCTACGTTGGGCAATGAAATGACCCAACGCCAGGAGGTCTTTGACCTCAATTCCAGTCTCCAAGCTCCTCATGGTACGGCTGGTGCCTCAGACACCAAGAAGAGAACTTTGGACCACAACATGCACATGATGAACGGTATACTTTCCGACTTCAACTTCTATGGCCAGCAAGACCAGAACAAGAGACTGAAGTTGGAACCCTCGTACAACATGGAGGTGTACAACCGCTTGAACCACTTGGACTCCTTTATGTCCTCCCAGCAGGCCAACCCTGCTCACGTTTCGTCCACCTCCAGTCAAGGCTCTGCGCTCCACTCCCAAAGCATGATTCCAAATCCAAACTCACACTACTCTTACGGTGCTAATCCTCAAGCCAACTTGTACGAGGCTGAGAAGTTCTTTAACAACTTGTCCTCGTCCATCGAGTTGCAATACCAGAACATGGTTTCATCTGTTCCCAACCAGCAATTCCCTGTCCAACAATCTCACCAGCAGCTGTTATATCCAATGTTACCTCAATACCAAGGTAAACCTTATGACAGTCATAGCAACCACTTTGTCAACAACCACAACTCCGGCTTTACTCCTAAGTTCCCTCAGGTCAACAGACAACTCAATGGTCAAGTTGGTGCCAACCCATTCGGCTCCGTTGAATTTGACTCGATCAGCAACAACCAGAAGTCTGCTAAGAAGCTCAATGAGGAGCCTGCCAAGGAAACTGGTAAGGAGGAGGAAGACGTCTTGGCCAACTTTAACCAATTGTCTATTAAGGATGGTAAGAATGATGTCAACTTTGACATTAAGACCGTTCAGAAGCACCGCGAGTTAATCAAGTTCGTTTGCGAACAATTGGCAATCATGAAAAAGTCCATGAAGGAGCAGGAACAAGGGCAGGAGCAACAGAAGAACACCACAGAGGCAGCTTCTAAGACAAATGAGACCAAGCAAAGCTTGTACCCAACGATTACGGCATTCTAA
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节。
序列表
<110> 上海大学 中国科学院上海巴斯德研究所
<120> 一种基于同源重组原理对耳道念珠菌进行基因敲除以及敲除株回补的方法
<160> 27
<170> SIPOSequenceListing 1.0
<210> 1
<211> 38
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
<210> 2
<211> 35
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
<210> 3
<211> 38
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
<210> 4
<211> 35
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
<210> 5
<211> 19
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
<210> 6
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
<210> 7
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 7
<210> 8
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
<210> 9
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 9
<210> 10
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 10
<210> 11
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 11
<210> 12
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 12
<210> 13
<211> 40
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 13
<210> 14
<211> 39
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 14
<210> 15
<211> 23
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 15
<210> 16
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 16
<210> 17
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 17
<210> 18
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 18
<210> 19
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 19
<210> 20
<211> 24
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 20
<210> 21
<211> 5809
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 21
<210> 22
<211> 7952
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 22
<210> 23
<211> 3059
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 23
<210> 24
<211> 1196
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 24
<210> 25
<211> 10037
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 25
<210> 26
<211> 5181
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 26
<210> 27
<211> 1667
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 27
- 一种基于同源重组原理对耳道念珠菌进行基因敲除以及敲除株回补的方法
- 一种基于盐酸刺激的哈维弧菌同源重组基因敲除的方法
