一种基于金属有机框架材料构建比色免疫传感器检测新型冠状病毒的方法
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及一种比色免疫生物传感器的制备及新型冠状病毒的检测方法,涉及了一种基于酶联免疫法及金属有机框架材料的比色传感器的制备方法及其应用,属于功能材料和生物传感技术领域。
背景技术
严重急性呼吸综合征冠状病毒2(SARS-CoV-2)为单股正链RNA病毒,属套病毒目(Nidovirales)冠状病毒科(Coronaviridae)冠状病毒属(Coronavirus)β属,呈圆形或椭圆形,有包膜,直径60-140nm。基因组全长29903bp(GenBank accession number MN908947)。基因组排列顺序是5‘-ORF1ab-S-ORF3a-E-M-ORF6-ORF7a-ORF8-N-ORF10,5′端约2/3区域编码病毒RNA聚合酶蛋白后1/3区域编码4个结构蛋白,刺突蛋白(spike,S)、包膜蛋白(envelope,E)、膜蛋白(membrane,M)、核衣壳蛋白(nucleocapsid,N),以及一些非结构蛋白和辅助。2019年12月,该病毒暴发。患者的临床表现以发热、乏力、干咳为主,鼻塞、流涕等上呼吸道症状少见,会出现缺氧低氧状态。约半数患者多在一周后出现呼吸困难,严重者快速进展为急性呼吸窘迫综合征、脓毒症休克、难以纠正的代谢性酸中毒和出凝血功能障碍。
目前检测新型冠状病毒的“金标准”法为实时荧光RT-PCR检测。呼吸道样本的实时荧光PCR(polymerase chain reaction,PCR)检测是急性呼吸道传染病的常规检测手段,灵敏度高、特异性好且在病原检测中应用成熟。实时荧光RT-PCR检测法在早期诊断和筛查中都发挥了重要作用。美中不足是该方法会受到因样本类型及采集时间、样本质量、样本运输保存时间与条件、仪器设备、试剂、人员操作方法因素等多方面影响,不适用于床旁检测及现场快速筛查。免疫学检测包括对抗原的检测和对抗体的检测,SARS-CoV-2表面的S蛋白、N蛋白等可作为抗原表位,已有公司发布基于胶体金免疫层析法的2019-nCoV新型冠状病毒抗原检测试剂以及双抗体夹心的新型冠状病毒蛋白快速检测检测试剂盒,但其依赖于温度敏感的抗体试剂,灵敏度和稳定性都有待提升。
发明内容
本发明正是为了解决上述问题缺陷,提供一种基于金属有机框架材料构建比色免疫传感器检测新型冠状病毒的方法。
适配体(Aptamers,APT),又称为人工抗体,是一种人工筛选出来,能够特异性识别靶标的核酸或多肽。相较于常规抗体,适配体有稳定、成本低、易于合成和修饰等优点。
本发明的目的在于通过金属有机框架(MOF)作为纳米酶,筛选出可特异性识别S蛋白的APT,通过在其3’端修饰巯基,与其相结,制备出一种酶活性和稳定性高可识别S蛋白的纳米材料。利用酶联免疫法原理,形成“抗体—抗原—适配体”的三明治夹心结构,无需核酸提取与扩增,直接识别新型冠状病毒颗粒表面的S蛋白,构成一种可快速有效检测新型冠状病毒的比色免疫传感器。
在本发明中,金属有机框架材料(MOF)作为新一代纳米材料,自身具有不同的拓扑结构、稳定且作为纳米酶具有较高的酶活性。本发明选择具有特异性识别新型冠状病毒表面刺突蛋白(S蛋白)的APT,通过在其3’端修饰巯基,即可与纳米酶结合,再结合可特异性识别SARS-CoV-2的抗体作为一抗,构建出夹心式的SARS-CoV-2比色传感器。该检测方法无需核酸的提取与扩增,直接检测SARS-CoV-2的病毒颗粒表面的S蛋白,提高了检测效率。快速、超敏、便捷的检测方法的建立为即时检验的实施提供了坚实的基础。
本发明采用如下技术方案实现。
1.根据之前的文献报道合成CuDBC,并表征。
5-10mg 8OH-DBC配体和2-10mg Cu(OAc)
表征方法有:透射电镜图像,红外光谱,XRD粉末X射线衍射图谱,XPS光电子能谱。
2.合成APT@CuDBC纳米复合材料
将筛选得到的特异性识别S蛋白的APT(序列:
ATTACCGATGGCTTGTTTGTAATGTAGGGTTCCGTCGGAT)加入到CuDBC纳米材料中,
4℃振荡12h,加入己硫醇(HT)封闭1h,用PBST洗涤3次后备用。
3.探究比色免疫传感器的反应条件
(1)抗原孵育最优时长
在酶标板中加入的50μL,1μg/mL的S蛋白单克隆抗体(Ab1)溶液,4℃孵育12h,再使用BSA封闭30min,然后加入50μL,100ng/mL的S蛋白,分别孵育10min、20min、30min、40min、50min、60min、70min、80min、90min,清洗过后再加入APT@CuDBC孵育45min,最后加入200μL,pH=6,50mmol/L的2-(N-吗啉代)乙磺酸(MES)缓冲溶液50μL,10mM 4-氨基吡啶(4-AP)和50μL 10mM 2-(2,4-二氯苯氧基)丙酸(2,4-DP)显色,并使用紫外分光光度计进行测定510nm处的吸光度值。检测结果为抗原最佳孵育时长为30min。
(2)APT@CuDBC的最优孵育时长
在酶标板中加入的50μL,10 1g/mL的Ab1溶液,4℃孵育12h,再使用BSA封闭30min,然后加入50μL,100ng/mL的S蛋白,孵育30min,在酶标板中加入50μL,配制好的APT@CuDBC溶液,分别孵育15min、30min、45min、60min、75min、90min,最后加入后加入200μL,pH=6,50mmol/L的MES缓冲溶液50μL,10mM 4-AP和50μL 10mM,2,4-DP显色,并使用紫外分光光度计进行测定510nm处的吸光度值。检测结果为APT@CuDBC最佳孵育时长为45min。
(3)显色反应缓冲液的最优pH值,在酶标板中加入的50μL,1μg/mL的Ab1溶液,4℃孵育12h,再使用BSA封闭30min,然后加入50μL,100ng/mL的S蛋白,孵育30min,在酶标板中加入50μL,配制好的APT@CuDBC溶液,孵育45min,最后加入200μLpH不同的MES缓冲溶液,pH=3、4、5、6、7、8、9,50μL,10mM 4-AP和50μL 10mM,2,4-DP显色,并使用紫外分光光度计进行测定510nm处的吸光度值。检测结果为显色反应缓冲液最佳pH值为6。
(4)显色反应的最优反应温度,在酶标板中加入的50μL,1μg/mL的Ab1溶液,4℃孵育12h,再使用BSA封闭30min,然后加入50μL,100ng/mL的S蛋白,孵育30min,在酶标板中加入50μL,配制好的APT@CuDBC溶液,孵育45min,最后加入200μL,pH=6,MES缓冲溶液,50μL,10mM 4-AP和50μL 10mM,2,4-DP显色,显色温度为30℃,40℃、50℃、60℃、70℃、80℃、90℃,使用紫外分光光度计进行测定510nm处的吸光度值。检测结果为显色反应的最佳温度为60℃。
5.S蛋白的测定步骤
(1)在酶标板当中加入50μL,1μg/mL可特异性识别S蛋白的抗体(Ab1),4℃孵育12h;
(2)使用100μL,0.1mol/L,pH=7.2PBST清洗3次后,加入50μL,1mg/mL牛血清蛋白(BSA)封闭30min;
(3)封闭结束后,使用100μL,0.1mol/L,pH=7.2PBST清洗3次后,加入50μL不同浓度抗原孵育30min;
(4)使用100μL,0.1mol/L,pH=7.2PBST清洗3次,加入50μL,上述材料中已合成好的APT@CuDBC,孵育45min,洗净酶标板;
(5)加入200μL,pH=6的MES缓冲溶液,50μL,10mM 4-AP和50μL 10mM 2,4-DP,在60℃下进行显色15min,测定OD510 nm处的吸光度,绘制工作曲线。
除上述技术方案之外,本发明可以用来识别新型冠状病毒的分子还可以是其他生物分子,比如新型冠状病毒S蛋白多肽、多克隆抗体等。本发明中的金属有机框架材料CuDBC还可用其他酶活性较好的MOF材料替代。
本发明的有益效果为,1.由透射电镜和扫描电子显微镜的结果可以看出CuDBC呈棒状形态,长度在500nm至1μm之间,宽度在50nm至100nm之间,且棒与棒之间不重叠,分散性较好,表明了CuDBC材料已成功合成。
2.红外光谱显示CuDBC复合材料的表面吸收水(3443cm
3.光电子能谱(XPS)结果显示,由于Cu
4.X射线衍射(XRD)结果显示,CuDBC在8.04
5.随着S蛋白浓度增加,在510nm处检测到的吸光度信号增加,且在0.001-2000ng/mL的S蛋白浓度范围具有良好的线性关系。根据紫外分光光度计512nm处的吸收峰值变化,取每个浓度的吸收峰值,进行数据分析,以病毒浓度的对数为X轴,吸光度值为Y轴,构建标准曲线,得到的标准曲线方程为Y=0.0312log[C]+0.3045(R
7.在没有S蛋白加入的情况下,传感器对牛血清蛋白(Bovine Albumin,BSA)、溶菌酶(lysozyme)、大肠杆菌(E.coli)、金黄色葡萄球菌(S.aureus)、Na
本文成功制备了CuDBC纳米材料,并首次将其应用到生物传感器中。利用类似酶联免疫法的原理,通过“抗体-抗原-适配体”的夹心式识别,使用单克隆抗体与适配体作为识别元件,可特异性识别S蛋白,成功构建了比色免疫传感器。该传感器线性检测范围是0.001-2000ng/mL,且操作简便,特异性高、稳定好、成本较低,为新型冠状病毒检测提供了新的方法。
下面结合附图和具体实施方式本发明做进一步解释。
附图说明
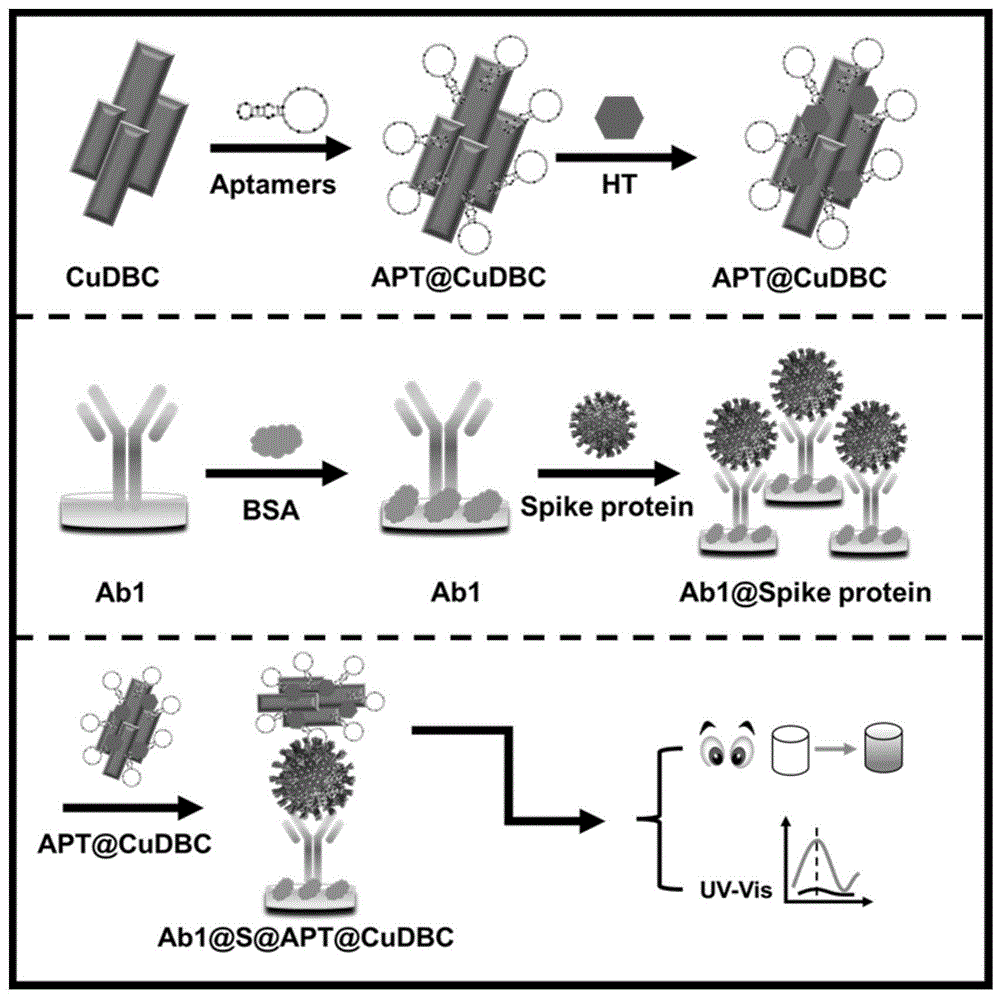
图1为本发明比色免疫传感器检测新型冠状病毒的原理图;
图2为本发明CuDBC纳米颗粒的TEM(A)和SEM(B)图;
图3为本发明CuDBC的FT-IR图谱(横坐标表示波数);
图4为本发明CuDBC的光电子能谱(横坐标表示结合能);
图5为本发明CuDBC的X射线衍射结果(横坐标表示衍射角度);
图6为本发明条件优化结果图:(A).Ab1最佳孵育时长结果;(B).APT@CuDBC最佳孵育时长结果;(C).显色反应缓冲液最适pH值结果;(D).最佳显色温度结果;
图7为本发明传感器的线性检测范围;(A)紫外吸收光强度与目标物浓度的关系;(B)紫外吸收光变化值与目标物浓度间的线性关系;
图8为本发明传感器的特异性检测结果图。
具体实施方式
实施例中所使用的化学试剂,溶剂均为分析纯;所使用的抗体均为商业化方法获得。
实施例1:
合成CuDBC
8.6mg 8OH-DBC配体和6mg Cu(OAc)
实施例2:
合成APT@CuDBC纳米复合材料
将100μL,1μmol/L筛选得到的特异性识别S蛋白的APT(序列:ATTACCGATGGCTTGTTTGTAATGTAGGGTTCCGTCGGAT)加入到1mL 1mg/mLCuDBC纳米材料中,4℃振荡12h,加入100μL50mmol/L己硫醇(HT)封闭1h,用PBST洗涤3次后备用。
实施例3:
图1为比色免疫传感器检测新型冠状病毒S蛋白的原理图,首先在酶标板当中加入50μL,1μg/mL可特异性识别S蛋白的抗体(Ab1),4℃孵育12h。使用PBST清洗3次后,加入50μL,1mg/mL牛血清蛋白(BSA)封闭30min。封闭结束后,使用PBST清洗3次后,加入50μL不同浓度抗原孵育30min。洗板3次后,加入50μL,上述材料中已合成好的APT@CuDBC纳米材料,孵育45min,洗净酶标板。
当目标抗原存在时,酶标板中已形成了抗体—抗原—适配体@纳米材料的夹心结构。结合纳米复合材料的酶活性,加入底物后,可使颜色由无色变为红色;同时,也可使用紫外分光光度计来读取吸光度数值,从而对新型冠状病毒进行检测。
本发明的突出创新在于:
1.首次将CuDBC纳米材料应用到生物传感器当中。
2.利用单克隆抗体与适配体能够特异性识别新型冠状病毒的特性,代替了金标准qPCR方法,无需核酸提取与扩增,直接识别新型冠状病毒颗粒,结合纳米材料较高的酶活性与稳定性,可通过肉眼判断和紫外分光光度仪判读检测结果,构建了夹心式新型冠状病毒比色免疫生物传感器。
以上所述的仅是本发明的部分具体实施例,方案中公知的具体内容或常识在此未作过多描述(包括但不仅限于简写、缩写、本领域惯用的单位)。应当指出,上述实施例不以任何方式限制本发明,对于本领域的技术人员来说,凡是采用等同替换或等效变换的方式获得的技术方案均落在本发明的保护范围内。本申请要求的保护范围应当以其权利要求的内容为准,说明书中的具体实施方式等记载可以用于解释权利要求的内容。
- 一种基于荧光金属有机框架材料的霉菌毒素比色传感方法
- 一种基于混合节点金属有机框架材料靶向诱导模拟酶失活的硫化氢比色传感器
