TSPO结合剂
文献发布时间:2023-06-19 10:08:35
相关申请
本案要求2018年6月22日(2018.06.22)提交的GB 1810312.7的权益和优先权,其全部内容通过引用结合在本申请中。
技术领域
本发明提供用于结合至TSPO的化合物、用于制备这些化合物的方法,用于将化合物结合至TSPO的方法,以及用于检测结合至TSPO的化合物的方法。
背景技术
正式地被称为外周二氮杂卓受体(peripheral diazepine receptor)(帕帕佐普洛斯(Papadopoulos)等)的18kDa转运蛋白(translocator protein,TSPO)在线粒体的外膜内表达,并且参与胆甾醇转运和甾族化合物合成(Lacapère)。TSPO在诸如脑中小神经胶质(microglia)(维尔姆斯(Wilms)等;以及科森扎-纳莎塔(Cosenza-Nashat)等)和外周内巨噬细胞(macrophages)(藤村(Fujimura)等;以及伯德(Bird)等)的炎症细胞中高度表达,因此TSPO已经作为整个身体病理炎症的标志。
在诸如痴呆和帕金森氏病的神经退行性疾病(杜邦(Dupont)等),以及心血管疾病、也就是动脉粥样硬化斑块(伯德,等)和心脏急性心肌埂塞后(杜邦,等)中,TSPO表达增加已经被证明。因此,在大范围的病理学中,一种用PET靶向TSPO的成功的成像方法具有显著的临床价值。另外,作为炎症的标志,近期,TSPO也已经被证实在神经保护(萨克莱(Thackeray)等)和心脏保护(莎乐(Schalle)等;以及帕拉迪斯(Paradis)等)中发挥作用,因此在疾病发生和进展的情况下,进一步扩大非侵入性TSPO成像以及针对疾病改善疗法的应用范围。
在炎症的正电子放射断层造影术(Positron Emission Tomography,PET)成像领域,TSPO是最广泛探索的目标之一。几十年前开发的典型TSPO PET放射性示踪物是
因此,正如最近发表的综述(阿拉姆(Alam)等)中总结的,在生成具有改善特性的新型TSPO放射性示踪物家族上已经付出了相当大的努力。尽管有这些发展,
因此,至今PK11195仍然是唯一的、在人类大脑中对rs6971多态性坚定地表现出不敏感的TSPO放射性示踪物(Owen et al.J.Nucl.Med.;以及Owen et al.J.Cereb.BloodFlow Metab.2010)。需要对rs6971多态性也表现出不敏感的TSPO的其他结合剂。
发明内容
通常,本发明提供用于结合转位蛋白(TSPO)的化合物,从而作为TSPO的示踪物、诸如放射性示踪物。因此,本发明的化合物可以用于在体内和体外检测TSPO的方法中。这样的方法可以用于炎症的识别,或者用于与TSPO水平改变相关的疾病的诊断,诸如神经性炎症、癌症以及心血管疾病。
本发明的化合物对rs6971遗传多态性不敏感,并且化合物也表现出对TSPO的亲和力,该亲和力是已知的TSPO结合剂PK11195的两倍左右。本发明的化合物在体内具有良好的动力学,和良好的剂量概况(dosimetric profile),并且因此适合用于临床。
本发明的化合物的体内表征还揭示了与TSPO表达一致的特异性摄取。单一浓度PK11195(1mg/kg)的阻断研究证实了靶向接合(target engagement),与基线扫描相比,阻断后测量的SUV值降低了64-81%。
本发明的化合物可以被认为是理想地适合作为用于TSPO的标记、诸如放射性标记,因为该化合物在人类大脑和心脏中对TSPO具有纳摩尔级的(nanomolar)亲和力,它们能够在体内渗入大脑,它们在体内的分布概况与TSPO蛋白表达一致,它们在血浆中的新陈代谢缓慢且组织中记录的新陈代谢物水平低。
本发明的第一方面中,提供了一种式(I)的化合物
以及其盐、溶剂合物和放射性标记形式。
在优选的实施方式中,式(I)的化合物为式(II)的化合物
以及其盐和溶剂合物。
与包括11C-PK11195的带有碳放射性标记的那些化合物、诸如本领域已知的化合物相比,带有氟放射性标记的TSPO结合剂、诸如式(II)的化合物,具有更长的半衰期。式(II)的化合物的剂量概况是这样的,即放射性标记化合物适合用于人类。
本发明的第二方面中,提供了一种制备式(I)的化合物的方法,所述方法包括用氟取代式(III)的化合物的溴的步骤:
本发明的第三方面中,提供了一种制备式(II)的化合物的方法,所述方法包含用18-氟取代式(IV)的化合物的氯的步骤:
通过用氯取代式(III)的化合物的溴,从式(III)的化合物获得或可获得式(IV)的化合物。
本发明还提供了一种组合物,所述组合物包括式(I)的化合物以及一种或多种药学上可接受的赋形剂。
在本发明的进一步的方面中,提供了一种检测式(I)的化合物的方法,所述方法包括将式(I)的化合物与TSPO接触从而形成式(I)的化合物与TSPO的复合物,且检测所述式(I)的化合物的步骤。
所述TSPO可以在体内或体外被提供。
本发明的所述化合物可以用于检测从受试者取出的器官样品,诸如心脏和大脑样品。相应地,本发明的所述方法可以用于检测例如在神经性病理学和心血管病理学中的TSPO并测定TSPO的水平。
在本发明的进一步的方面中,提供了用于检测受试者中式(I)的化合物的方法,所述方法包括向受试者施用式(I)的化合物,以及随后检测所述式(I)的化合物的步骤。
本文中,所述受试者可以是人类受试者。
所述受试者可以是已知或怀疑具有疾病的受试者,该疾病与TSPO水平改变、诸如TSPO水平升高相关,该疾病诸如神经性炎症、癌症和心血管疾病。
受试者可以具有与TSPO水平改变相关的疾病,并且所述受试者可以针对这种疾病正在经受治疗。本发明的所述方法可以用于检测TSPO水平中的变化,例如评估治疗的效果。
下面将进一步详细描述本发明这些和其他方面以及实施方式。
附图说明
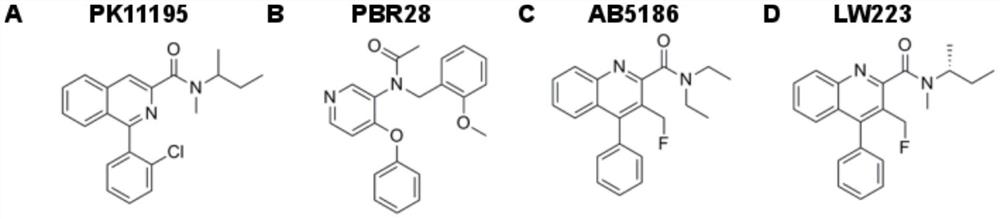
图1示出了已知的TSPO结合剂PK11195(A)、PBR28(B)和AB5186(C)、以及根据本发明实施方式的TSPO结合剂LW223(D)的结构。所述化合物以它们非标记的(非放射性标记的)形式示出。
图2示出来自高亲和力结合剂(HAB)、混合亲和力结合剂(MAB)和低亲和力结合剂(LAB)的人类大脑中TSPO配体的结合亲和力,其中(a)示出使用单位点拟合(one-sitefitting)绘制的平均PK11195结合亲和力曲线,HAB n=6,MBA n=8以及LAB n=4;(b)示出了除MAB使用双位点拟合(two-site fitting)之外,使用单位点拟合绘制的平均PBR28结合亲和力曲线,HAB n=4,MAB n=5和LAB n=4;(c)示出了除MAB使用双位点拟合之外,使用单位点拟合绘制的平均AB5186结合亲和力曲线,HAB n=6,MAB n=6和LAB n=5;(d)示出了使用单位点拟合绘制的平均LW223结合亲和力曲线,HAB n=5,MAB n=5和LAB n=4;以及(e)示出了针对各人类样品分别计算的PK11195亲和力值(K
图3示出了来自高亲和力结合剂(HAB)、混合亲和力结合剂(MAB)和低亲和力结合剂(LAB)的人类心脏中的TSPO配体的结合亲和力,其中(a)示出使用单位点拟合绘制的平均PK11195结合亲和力曲线,HAB n=4,MBA n=5以及LAB n=4;(b)示出了使用单位点拟合绘制的平均PBR28结合亲和力曲线,HAB n=4,MAB n=5和LAB n=4;(c)示出了除MAB使用双位点拟合之外,使用单位点拟合绘制的平均AB5186结合亲和力曲线,HAB n=4,MAB n=5和LAB n=4;(d)示出了使用单位点拟合绘制的平均LW223结合亲和力曲线,HAB n=5,MAB n=5和LAB n=4:以及(e)示出了针对各人类样品分别计算的PK11195亲和力值(K
图4示出了在体内
图5示出在体内结合至TSPO的
图6示出了结合至人类组织的
图7示出了离解常数(K
图8示出了在体内使用PK11195取代
图9示出了小鼠源器官的
图10示出了健康人类大脑组织中
图11示出了
具体实施方式
式(I)的化合物,包括式(II)的化合物,用作TSPO的结合剂。相应地,化合物可以用于识别例如在诸如人类的受试者中TSPO表达改变(诸如增加)以及可以用于识别那些患有或具有疾病的受试者,该疾病例如为神经性炎症、癌症或心血管疾病。
在下面进一步详细描述本发明的化合物及其合成和用途。
史蒂文森(Stevenson)等人先前描述过化合物11,该化合物11为在喹啉环上拥有碘甲基取代基的化合物,而不是由本案化合物需要的氟甲基基团。该化合物用于TSPO的SPECT成像中。史蒂文森等人没有描述用于作为放射性示踪物的化合物。此外,这项工作没有暗示这种化合物或任何衍生物是或者可能是对rs6971遗传多态性不敏感。
而且,史蒂文森等人报道的结合数据教导避免本发明化合物中存在的酰胺基团取代基的使用。因此,化合物11(酰胺态氮为甲基-和s-丁基-取代的)与相关化合物18(酰胺态氮为二乙基-取代的)之间的比较表明化合物18对TSPO具有最佳的亲和力(见史蒂文森等人的表1)
布莱尔(Blair)等人(Chem.Sci.)先前已经描述了示踪物-化合物4(对应于史蒂文森等人的化合物18)、5和6(AB5186)。布莱尔等人的工作表明了当卤素作为取代基置于苯基侧基(pendant phenyl group)上、而不是作为卤代甲基取代基存在于喹啉环时,碘代化合物与TSPO的结合得到改善。因此,布莱尔等人(Chem.Sci.)的图2中的数据示出了化合物5比化合物4具有更好的亲和力。
本案示出了,本发明的化合物比布莱尔等人(Chem.Sci.)描述的、包括化合物6的化合物具有更好的亲和力,化合物6为本申请中的参考化合物AB5186。
卡佩利(Cappelli)等人(J.Med.Lett.)描述了与史蒂文森等人和布莱尔等人(Chem.Sci.)描述的化合物相关的化合物及其用途。这个文件没有提到多态性结合的问题。
WO 02/26713侧重于用于治疗寄生虫感染的化合物。其公开的一些化合物与本案的化合物具有非常微小的相似之处。WO 02/26713没有提及TSPO或放射性示踪。
化合物
本发明提供了一种式(I)的化合物
以及其盐、溶剂合物和放射性标记形式(radioforms)。
优选地,所述式(I)的化合物为:
以及其盐、溶剂合物和放射性标记形式。
发明人发现,这种特定的立体形式-(R)-构型-对TSPO的亲和力比对其对映体的亲和力大约大五倍。
在优选的实施例中,所述化合物为式(II)的化合物
以及其盐和溶剂合物。
式(II)的化合物是放射性标记化合物,并且更具体地用氟放射性同位素
优选地,所述式(II)的化合物为:
以及其盐和溶剂合物。
相较于非标记的、非放射性标记的化合物,该放射性标记的化合物可以被称作标记化合物(hot compound)。
放射性形式、盐、溶剂合物和立体形(式)
式(I)的化合物或本文描述的任何其他化合物,包括原子被天然存在的或非天然存在的同位素取代的化合物。在一个实施方式中,所述同位素是稳定同位素。因此,此处描述的化合物包括,例如包含氘的化合物等。例如,H可以是任何同位素形式,包括
通常本发明的化合物包含诸如
在本发明优选的实施例中,可以将所述式(I)的化合物F原子提供为
式(I)的化合物或本文中描述的任何其他化合物的盐的实施例,包括所有药学上可接受的盐,诸如但不限于,诸如HCl盐和HBr盐的强无机酸的酸加成盐,以及诸如甲磺酸盐的强有机酸的加成盐。盐的更多的实施例包括硫酸盐和诸如乙酸盐本身、三氟乙酸盐或三氯乙酸盐的乙酸盐。
涉及式(I)的化合物或本文中描述的任何其他化合物,也涉及所述化合物的溶剂合物。溶剂合物的实施例包括水合物。
除非另有说明,否则涉及的特定化合物包括同分异构形式,包括其混合物(例如外消旋混合物)。这种同分异构形式的制备(例如,不对称合成)和分离(例如,分级结晶和色谱的方式)的方法要么是本领域已知的,要么可以通过已知方式采用本文中教导的方法或已知的方法容易地获得。
在本发明的一个方面涉及基本纯化形式的和/或基本不含污染物形式的化合物。
在一个实施方式中,基本纯化形式是至少50重量%,例如至少60重量%,例如至少70重量%,例如至少80重量%,例如至少90重量%,例如至少95重量%,例如至少97重量%,例如至少98重量%,例如至少99重量%。
除非另有说明,否则基本纯化形式是指任何立体异构或对映体形式的化合物。例如,在一个实施方式中,基本纯化形式是指立体异构体的混合物,即相对于其他化合物纯化的。在一个实施方式中,基本纯化形式是指一种立体异构体,例如光学纯的立体异构体。在一个实施方式中,基本纯化形式是指对映体的混合物。在一个实施方式中,所述基本纯化形式是指对映体的等摩尔混合物(即外消旋混合物,外消旋体)。在一个实施方式中,基本纯化形式是指一种对映体,例如光学纯的对映体。
在一个实施例中,污染物占是指不超过50重量%,例如不超过40重量%,例如不超过30重量%,例如不超过20重量%,例如不超过10重量%,例如不超过5重量%,例如不超过3重量%,例如不超过2重量%,例如不超过1重量%。
除非另有说明,否则污染物是指其他化合物,也就是说,不同于立体异构体和对映体。在一个实施方式中,污染物是指其他化合物以及其他立体异构体。在一个实施方式中,污染物是指其他化合物以及其他对映体。
在一个实施方式中,基本纯化形式是至少60%光学纯的(即,在摩尔基础上,化合物的60%是期望的立体异构体或对映体,而40%是不期望的立体异构体或对映体),例如至少70%光学纯的,例如至少80%光学纯的,例如至少90%光学纯的,例如至少95%光学纯的,例如至少97%光学纯的,例如至少98%光学纯的,例如至少99%光学纯的。
组合物
式(I)和(II)的化合物适用于结合至TSPO并且可以在体内结合。相应地,式(I)和(II)的化合物可以制备成用于施用至人类或动物体的组合物。
在式(I)的化合物被放射性标记的情况下,它们可以以至少0.1Mbq/mL、至少0.5Mbq/mL、至少1Mbq/mL、至少2MBq/mL或至少5MBq/mL的浓度提供至流体组合物中。
在式(I)的化合物被放射性标记的情况下,它们可以以至多10Mbq/mL、至多20Mbq/mL、至多50Mbq/mL、至多100Mbq/mL、至多200Mbq/mL、至多300Mbq/mL或至多200MBq/mL的浓度提供至流体组合物中。
所述化合物可以以选自上述给定值下限和上限的范围内的浓度来使用。例如,所述化合物可以以1-10MBq/mL的范围内的浓度来使用。
在本案的一些样例中,以2MBq/mL的浓度使用
通常,在盐溶液中使用所述式(I)和(II)的化合物,例如用于静脉内注射。
尽管可以单独施用所述式(I)的化合物,但还是希望将其作为药物剂型(例如,组合物、制剂、药剂)存在,所述药物剂型包括至少一种本文中描述的式(I)的化合物,以及本领域技术人员公知的一种或多种其他药学上可接受的成分,所述其他药学可接受的成分包括但不限于,药学上可接受的载体、稀释剂、赋形剂、辅助剂、填料、缓冲剂、防腐剂、抗-氧化剂、润滑剂、稳定剂、增溶剂、表面活性剂(例如,润湿剂)、掩蔽剂、着色剂、调味剂和甜味剂。
因此,本发明进一步提供了如上定义的组合物,以及制备组合物的方法,所述方法包括混合至少一种如本文中描述的式(I)的化合物以及一种或多种本领域技术人员已知的其他药学上可接受的成分,例如载体、稀释剂、赋形剂等。如果配制成离散的单元(如片剂等),每个单元包含预定量(剂量)的化合物。
如本文中使用的术语“药学上可接受的”,涉及化合物、成分、材料、组合物、剂型等,其在合理的医学判断范围内,适合用于与有问题(in question)的受试者(如人类)的组织接触,没有过度的毒性、刺激、过敏反应或其他问题或并发症,与合理的益处/风险比率相称。在与剂型中的其他成分相容的意义上,各载体、稀释剂、赋形剂等也需要是“可接受的”。
合适的载体、稀释剂、赋形剂等可以在标准药学教材(standard pharmaceuticaltexts)中找到,例如,《雷明顿氏药物科学(Remington's Pharmaceutical Sciences)》,第18版,马克出版公司(Mack Publishing Company),伊斯顿,宾夕法尼亚州,1990年;以及《药物赋形剂手册(Handbook of Pharmaceutical Excipients)》,第5版,2005年。
所述剂型可以通过药学领域公知的任何方法制备。这些方法包括将所述式(I)的化合物与构成一种或多种辅助成分的载体结合的步骤。通常,所述剂型通过将所述化合物与载体(例如,液体载体、分散的固体载体等)均匀且紧密地结合,并且如有必要,随后定型产品来制备。
可以制备所述剂型以提供用于快速释放;立即、延迟、定时或持续地释放;或其组合。
剂型可以适当地为液体、溶液(例如水性、非水性)、悬浮液(例如水性、非水性)、乳状液(例如水包油、油包水)、喷剂,雾剂或气溶胶的形式。
所述化合物可以溶解在、悬浮在或掺和于一种或多种其他药学上可接受的成分中。所述化合物可以存在于脂质体或其他微粒物中,所述脂质体或其他微粒物被设计成将所述化合物靶向至例如血液成分或一种或多种器官。
在所述载体为液体的情况下,适用于鼻内施用的剂型包括例如喷鼻剂、滴鼻剂,或者利用喷雾剂的气溶胶施用,包括所述化合物的水溶液或油溶液。作为替代的施用方法,干粉递送可以被用作雾化气溶胶的替代。
在载体为固体的情况下,适用于鼻内施用的剂型包括例如以粗粉存在的制剂,该粗粉末具有例如约20至约500微米范围内的粒度,其以这样的方式施用,即通过鼻腔通道从靠近鼻子的粉末容器中快速吸入鼻烟。
适用于肺施用的剂型(例如通过吸入或吹入疗法)包括使用合适的推进剂,诸如二氯二氟甲烷、三氯氟甲烷、二氯-四氟乙烷、二氧化碳或其他合适的气体,以来自加压包装的气溶胶喷雾剂形式存在的那些制剂。此外或可选地,用于肺施用的剂型可以被配制用于从雾化器或干粉吸入器施用。例如,所述剂型可以提供有载体或脂质体,提供合适的粒度以到达肺的适当部分,帮助递送适当的剂量以增强肺组织中的滞留。
适用于肠胃外施用的剂型(例如,通过静脉内或皮下注射或输注),包括将化合物溶解、悬浮或以其他方式提供(例如,在脂质体或其他微粒物中)于其中的水液体或无水液体、等压液体、无热原液体、无菌液体(例如溶液,悬浮液)。这样的液体可以另外包含其他药学上可接受的成分,诸如抗-氧化剂、缓冲剂、防腐剂、稳定剂、抑菌剂、悬浮剂、增稠剂和使所述制剂与指定受体的血液(或其他相关体液)等压的溶质。赋形剂的实施例包括,例如水、醇类、糖类、多元醇、甘油、植物油等。用于此类剂型的合适的等压载体的实施例包括氯化钠注射剂(Sodium Chloride Injection),林格氏溶液(Ringer's Solution)或乳酸盐林格氏注射剂(Lactated Ringer's Injection)。通常,液体中所述化合物的浓度为从约1ng/mL到约500μg/mL,例如约1ng/mL至约100μg/mL,例如从约10ng/mL到约10μg/mL,例如从约10ng/mL到约1μg/mL。所述剂型可以存在于单位剂量或多剂量密封的容器中,例如安瓿和小瓶,并且可以在冷冻干燥(冻干)条件下储存,仅需要在使用前立即添加例如注射用水的无菌液体载体。临时注射溶液和悬浮液可由无菌粉末、颗粒剂和片剂来制备。
制备方法
本发明还提供了用于制备式(I)化合物和式(II)化合物的方法。
在制备方法中,可以在合成的最后步骤中引入式(I)化合物和式(II)化合物中的氟。在所述式(I)的化合物包含氟作为放射性标记的情况下,例如在式(II)的化合物中,这尤其重要。制备本发明的化合物的方法不需要处理中间放射性标记的化合物,由于放射性随时间的流失,通常应避免处理中间放射性标记的化合物。在需要制备和纯化放射性标记的中间体化合物情况下会发生这样的情况。
所述式(I)的化合物可以由式(III)的化合物通过用氟取代所述式(III)的化合物中的溴来制备。所述式(III)的化合物为:
以及其盐、溶剂合物和放射性标记形式。
卤素取代反应,以及氟取代反应是本领域公知的。
所述式(III)的化合物可以与氟阴离子反应以得到所述式(I)的化合物。所述氟阴离子可以由氟盐提供,诸如与碱金属盐一起,例如氟化钾。所述取代反应可以在诸如18-冠醚-6催化剂的存在下进行。
所述式(II)的化合物可以由式(IV)的化合物、通过用19-氟取代所述式(IV)的化合物中的氯来制备。所述式(IV)的化合物为:
以及其盐、溶剂合物和放射性标记形式。
例如,式(IV)的化合物可以用诸如[
式(IV)的化合物可以从式(III)化合物、通过用氯取代式(IV)的化合物中的溴来制备。
例如,式(IV)的化合物可以用诸如LiCl的氯阴离子来处理。
本发明还提供了式(III)和式(IV)的化合物,及其盐、溶剂合物和放射性标记形式。
复合物
本发明的进一步的方面中,提供了一种式(I)的化合物与TSPO的复合物。本文中,式(I)的化合物是非共价结合至TSPO。
所述式(I)化合物与TSPO的复合物可以在体外或体内提供。所述TSPO可能存在于线粒体膜的外层上。
通常地,式(I)的化合物与TSPO以结合对来提供。因此,所述复合物中化合物和TSPO的化学计量为1:1。
当式(I)的化合物与TSPO在复合物中结合时,诸如在化合物被放射性标记的情况下,所述式(I)的化合物可以是可检测的。
在式(I)的化合物被放射性标记的情况下,诸如在式(II)的化合物中,所述化合物可以通过适当地、诸如正电子放射断层造影术的放射性标记方法来检测所述化合物。
当式(I)的化合物没有被放射性标记的情况下,可以通过包括例如NMR的其他方法来检测。
TSPO是转运蛋白。它可以被称为外周苯并二氮杂卓(peripheralbenzodiazepine)受体。
所述TSPO可以是哺乳动物的TSPO,诸如人类或啮齿动物的TSPO。
所述TSPO可以是一种包括NCBI参考序列:NP_000705.2的蛋白。
方法和用途
本发明的化合物用于结合至TSPO。所述化合物是可检测的,并且当与TSPO存在于复合物时是可检测的。
本发明的化合物可以与存在于体内或体外的TSPO接触,以形成诸如描述的复合物。随后,所述复合物可以通过检测本发明的化合物来检测。
在式(I)的化合物被放射性标记的情况下,例如化合物是式(II)的化合物的情况下,化合物可以通过正电子放射断层造影术(PET)来检测。
因此,通常,本案的方法包括使用包括PET(正电子放射断层造影术)的闪烁照相成像法对式(I)的化合物(诸如式(II)的化合物)进行成像。闪烁照相成像法可以包括使用照相机或扫描仪来检测单个平面中的放射性。PET成像系统可以包括环形的检测器阵列,该检测器阵列还可以检测多个维度的放射性。
有利地,本发明的所述化合物对TSPO内的突变是不敏感的,诸如rs6971遗传多态性。
所述方法可以包括将式(I)的化合物施用于诸如人类或动物的受试者的步骤。
本发明的方法可以包括在受试者的选自由大脑、心脏、肺、胆囊、肾上腺、肾脏和肠组成的组中的位点处检测的式(I)的化合物(诸如与TSPO存在于复合物)的步骤。
本发明还提供了一种对受试者中的TSPO表达进行成像的方法,所述方法包括将式(I)的化合物或包含所述化合物的组合物施用于受试者,并在受试者内产生一个或多个所述化合物分布的图像的步骤。
在一些实施方式中,诸如与神经性炎症有关的TSPO表达的开始速度和程度可以通过成像来确定。例如,这可以用于预测治疗神经性炎症的方法的结果。
此处,式(I)的化合物在受试者位点的结合表明该位点TSPO表达的量或程度。
下面更详细地描述了将式(I)化合物施用至受试者。
可以使用分子成像技术、诸如可以利用放射性标记,以产生成像剂在受试者内分布的一个或多个图像。
使用适当地分子成像技术,可以产生一个或多个图像,该图像示出了在施用成像剂后的一段时间内,全部或部分受试者中式(I)的化合物的分布。身体组织或区域中可检测标记的量或浓度表明该组织或区域中TSPO表达的量。相对于身体内其他组织或区域,身体组织或区域中式(I)化合物的浓度的增加表明该组织或区域中的细胞正经受TSPO表达增加。因此,本发明的成像剂可以用于TSPO表达,并且可以适用于检测与TSPO表达水平改变相关的疾病。
所述受试者可以具有疾病病症,所述疾病病症的特征为存在TSPO表达升高或降低(TSPO表达升高)的位点,并且一个或多个图像示出了本发明化合物在一个或多个位点的分布。
本发明还提供了一种用于确定对疾病病症的疗法有效的方法,所述疾病病症与TSPO表达升高或降低(诸如,TSPO表达升高)相关,该方法包括以下步骤:
在疗法之前和期间或之后,将式(I)的化合物或包含所述化合物的组合物施用于受试者;以及,
在受试者中TSPO表达升高或降低(诸如,TSPO表达升高)的一个或多个位点处,产生所述化合物分布的一个或多个图像。
在疗法期间或之后,可以产生所述式(I)的化合物在受试者中TSPO表达位点处分布的一个或多个图像。
相对于所述疗法之前,在所述疗法之后在升高的或降低的一个或多个位点处、本发明的化合物结合的变化(诸如降低或增加)表明所述疗法在提醒受试者TSPO表达中是有效的。
在疾病病症与TSPO表达升高相关的情况下,如果在一个或多个位点处所述化合物结合降低,则所述治疗可被认为是有效的。
在早期临床试验和随后的临床中,式(I)的化合物可以用于评估药物功效,其中它可以用于指导治疗。无效的治疗可以在早期阶段放弃,允许选择更有效的药物。
还提供了一种用于确定受试者的治疗方案功效的方法,所述方法包括:
使受试者经受治疗的初始方案;以及
确定受试者中式(I)化合物与TSPO结合的量或程度,
其中,响应于该方案结合的量或程度的变化表明所述方案在受试者中是有效的。
这种方法可以包含额外的步骤:
改变治疗的方案并使受试者经受改变的方案;
确定受试者中式(I)的化合物与TSPO结合的量或程度;
重复改变的方案和确定结合、直到观察到化合物结合的量或程度的变化的步骤,
其中,响应于所述方案、所述化合物结合的量或程度的变化表明所述方案在受试者中是有效的。
上述的方法中所述受试者可能具有神经性炎症,并且响应于所述方案、所述式(I)化合物结合的量或程度的降低表明所述方案在受试者中是有效的。
所述受试者可以具有特征为TSPO表达水平增加的疾病病症,并且响应于所述方案、受试者中一个或多个疾病位点与成像剂结合的量或程度的降低表明所述方案在受试者中是有效的。
剂量
通常,本发明的方法可以包括向受试者施用有效量的式(I)化合物,使得在靶向区域中有效标记TSPO。
本领域技术人员将理解,式(I)化合物和包含式(I)化合物的组合物的合适剂量可随患者而变化。确定最佳剂量通常包括平衡TSPO标记水平与任何风险或有害的副作用。
选定的剂量水平将取决于多种因素,包括但不限于施用途径、施用时间、化合物的排泄速率、治疗的持续时间、药物、化合物的使用,和/或受试者使用的材料,以及物种、性别、年龄、体重、病症、总体健康状况和患者的既往病史。尽管通常选择剂量以在作用位点处达到局部浓度,但是式(I)化合物的量和施用途径最终由医师、兽医或临床医生的判断,使得达到所需效果而不造成实质性有害的或有毒的副作用。
在标记和检测所需的全部时间内,施用可以连续地或间歇地(例如,以适当的间隔分次的剂量)以单剂量作用。确定最有效的施用方式和剂量的方法是本领域技术人员公知的,并且将随剂型、靶细胞和/或器官、以及所治疗的受试者而变化。单次或多次施用可以由主治医师、兽医或临床医生选择的剂量水平和方式来进行。
通常,式(I)化合物的合适剂量为每天每千克受试者体重约10μg至约250mg(更通常的为约100μg至约25mg)的范围内。在式(I)的化合物是盐或溶剂合物等的情况下,施用量是基于母体化合物计算的,并且因此实际使用的重量是成比例增加的。
在式(I)的化合物是放射性标记的情况下,它们可以以如下列出的量使用,例如以剂型使用。
所述化合物可以以至少0.1MBq、至少0.5MBq、至少1MBq、至少5MBq、至少10MBq或至少20MBq的量使用。
所述化合物可以以至多50MBq、至多100MBq、至多200MBq、至多200MBq或至多500MBq的量使用。
所述化合物可以以选自上述值的下限和上限范围内的量使用。例如,所述化合物可以以20至100MBq的量使用。
受试者所经历的生物剂量可能是低的,诸如每剂量20mSv,诸如每次扫描。优选地,所述生物剂量为每剂量15mSv或更少,每剂量10mSv或更少,诸如每剂量7mSv或更少。
试剂盒
本发明还提供了一种试剂盒,其包含(a)例如通常在合适的容器和/或合适的包装中提供的式(I)的化合物或包括由式(I)中任一种所定义的化合物的组合物;以及(b)使用说明,例如如何施用所述该化合物或组合物的书面说明。
施用途径
式(I)的化合物或包括式(I)化合物的组合物可以通过任何方便的施用途径向受试者施用,无论是全身/外周还是局部(即在所需作用的位点)。
施用途径包括,但不限于,肺(例如通过口或鼻、使用例如喷雾剂、例如通过吸入或吹入);胃肠外,例如通过注射或输注,包括皮下、皮肤内、肌肉内、静脉内、动脉内、心脏内、鞘内、脊柱内、囊内、囊下、眶内、腹膜内、气管内、表皮下、关节内,蛛网膜下腔以及胸骨内;例如通过皮下地或肌内注射植入贮库(depot)或储存器(reservoir)。
受试者
可以向受试者施用式(I)的化合物,用于包括TSPO表达水平和TSPO表达分布的TSPO的检测。
所述受试者可以是脊索动物、脊椎动物、哺乳动物、胎盘哺乳动物、有袋类动物(例如袋鼠,袋熊)、啮齿动物(例如豚鼠、仓鼠、大鼠、小鼠)、鼠科动物(例如小鼠)、兔形目动物(例如,兔)、鸟类动物(例如,鸟),犬科动物(例如,狗),猫科动物(例如,猫),马科动物(例如,马),猪类动物(例如,猪),绵羊属动物(例如绵羊),牛科动物(例如牛),灵长目动物,类人猿类动物(例如猴子或猿),猴类动物(例如小猿,狒狒),猿类动物(例如大猩猩,黑猩猩,红毛猩猩,长臂猿)或人类。此外,受试者可以是其发育的任何形(式),例如,胎儿。所述受试者可以是脊椎动物,诸如水生脊椎动物,例如鱼(例如斑马鱼)。
还设想了可以在非人类动物上实施本发明。非人类哺乳动物可以是啮齿动物。啮齿动物包括大鼠、小鼠、豚鼠、毛丝鼠以及其他用于实验室研究的、类似尺寸的小型啮齿动物。
在一个实施方式中,所述受试者是人类,诸如成年人类
在一个实施方式中,所述受试者是啮齿动物,诸如小鼠。
其他预设
在本文中,上述实施方式的每种合适的组合明确地被公开,犹如每种组合是单独和明确地列举。
鉴于目前公开的,本发明的各种进一步的方面和实施方式对于本技术的技术人员将是显而易见的。
本文中使用的“和/或”被视为是两个指定特征或组件中的每个、或的两个指定特征或组件中的一个的具体公开。例如,“A和/或B”将被认为是(i)A、(ii)B和(iii)A和B中的每个的具体公开,正如每个在本文中单独列出一样。
除非上下文另有指示,否则上述特征的描述和定义不限于本发明的任何特定方面或实施方式,并且同样适用于所描述的所有方面和实施方式。
现在将通过实施方式并参考上文描述的附图来说明本发明的某些方面和实施方式。
实验和结果
一般实验
所有试剂和起始物料从商业资源获得的并且直接使用。所有午睡溶剂(drysolvent)使用PureSolv 500MD溶剂纯化系统进行纯化。除非另有说明,否则所有反应在氩气下进行。盐水被定义为氯化钠水溶液的饱和溶液。
快速柱色谱法(Flash column chromatography)使用Fisher Matrix二氧化硅60进行。预先涂有硅胶60(UV254)的马歇雷-纳高(Macherey-Nagel)铝背板用于薄层色谱法,并使用UV光使其可见。
用布鲁克(Bruker)DPX 400光谱仪或布鲁克500分光仪记录
用JASCO FTIR 410分光仪记录红外光谱。
使用电子碰撞,化学电离或快速原子轰击技术记录质谱。使用双聚焦磁分析质谱仪(dual-focusing magnetic analyser mass spectrometer)记录HRMS光谱。
使用盖伦坎普(Gallenkamp)熔点仪测定熔点。
用相应的外消旋混合物校准手性HPLC方法。
如先前报道的方法(史蒂文森等人)制备3-甲基-4-苯基喹啉-2-羧酸。
化合物的制备
式(I)的化合物以下面所示的方案制备。所述化合物被称为LW233。
方案1-LW233的制备
(R)-(N-仲丁基)-3-甲基-4-苯基喹啉-2-羧酰胺
向3-甲基-4-苯基喹啉-2-羧酸(2.54g,9.65mmol)的无水N,N-二甲基甲酰胺(250mL)中添加O-(苯并三唑-1-基)-N,N,N’,N’-四甲基脲阳离子六氟磷酸盐(O-(benzotriazol-1-yl)-N,N,N′,N′-tetramethyluronium hexafluorophosphate)(5.49g,14.5mmol)和N,N’-二异丙基乙胺(3.40mL,19.3mmol)。在添加(R)-(-)-仲丁胺(1.10mL,10.6mmol)之前,反应混合物在室温搅拌0.5h并且随后加热至40℃保持4h。反应混合物冷却至室温,用乙酸乙酯(300mL)稀释并且用水(3×200mL)和盐水(200mL)洗涤。将有机层干燥(MgSO
Mp 152–154℃(lit.mp 157-158℃-参见卡佩利(Cappelli)等人(J.Med.Chem.));IR(KBr)3287(NH)、2968(CH)、1641(CO)、1539、1448、1157、761cm
(R)-(N-仲丁基)-N-甲基-3-甲基-4-苯基喹啉-2-羧酰胺
向(R)-(N-仲丁基)-3-甲基-4-苯基喹啉-2-羧酰胺(2.81g,8.82mmol)的四氢呋喃(176mL)溶液中添加氢化钠(60%分散在矿物油中,0.710g,17.6mmol)。在添加碘甲烷(2.75mL,44.1mmol)之前,混合物在室温搅拌0.5h。将得到的溶液在室温搅拌3h并且随后通过添加水淬火。水相用二乙醚(3×10mL)萃取。合并的有机相用10%硫代硫酸钠水溶液(10mL)、盐水(10mL)洗涤、干燥(Na
NMR谱示出了1:1的旋转异构体混合物。记录两种旋转异构体的信号。Mp 114–117℃(lit.mp 117-118℃-参见卡佩利等人(J.Med.Chem.);IR(KBr)2969(CH)、1637(CO)、1466、1072、731cm
(R)-3-溴甲基-(N-仲丁基)-N-甲基-4-苯基喹啉-2-羧酰胺
向搅拌、脱气的(R)-(N-仲丁基)-N-甲基-3-甲基-4-苯基喹啉-2-羧酰胺(2.70g,8.12mmol)氯仿(300mL)溶液中添加N-溴代琥珀酰亚胺(N-bromosuccinimide)(2.17g,12.2mmol)和过氧化二苯(甲)酰(dibenzoyl peroxide)(0.20g,0.812mmol),并将该溶液加热回流6h。随后添加另一部分的N-溴代琥珀酰亚胺(1.00g,5.61mmol),并该溶液进一步地加热回流16h。反应混合物冷却至室温、过滤并且真空除去溶剂。随后粗残留物用乙酸乙酯(100mL)稀释并且用水(3×100mL)洗涤。将有机层干燥(MgSO
NMR谱示出了2:1的旋转异构体混合物。仅记录主要的旋转异构体的信号。Mp 160–164℃;IR(KBr)2970(CH)、1631(CO)、1484、1397、1046、766cm
(R)-(N-仲丁基)-3-氯甲基-N-甲基-4-苯基喹啉-2-羧酰胺
向(R)-3-溴甲基-(N-仲丁基)-N-甲基-4-苯基喹啉-2-羧酰胺(0.500g,1.22mmol)的无水四氢呋喃(10mL)溶液中添加氯化锂(0.160g,3.66mmol),并且反应混合物在室温搅拌16h。反应使用水(30mL)来淬火且萃取至乙酸乙酯(3×30mL)中。将有机层合并且用盐水(90mL)洗涤、干燥(MgSO
NMR谱示出了1.5:1的旋转异构体混合物。仅记录主要的旋转异构体的信号。Mp140-142℃;IR(KBr)2970(CH)、1620(CO)、1481、1404、1219、748cm
LW223-(R)-(N-仲丁基)-3-氟甲基-N-甲基-4-苯基喹啉-2-羧酰胺
向18-冠醚-6(18-crown-6)(0.032g,0.12mmol)的乙腈(2.5mL)溶液中添加氟化钾(0.036g,0.61mmol)并且得到的悬浮液在室温搅拌0.5h。随后,逐滴添加(R)-3-溴甲基-(N-仲丁基)-N-甲基-4-苯基喹啉-2-羧酰胺(0.050g,0.12mmol)的乙腈:二氯甲烷(2:1,9.0mL)溶液,且将反应混合物加热回流72h。反应完成后,反应混合物冷却至环境温度并且添加水(20mL)。溶液用二氯甲烷(3×20mL)萃取、干燥(MgSO
NMR谱示出了3:1的旋转异构体混合物。仅记录主要的旋转异构体的信号。Mp 146–148℃;IR(纯的)2972(CH)、1628(CO)、1559、1485、1398、1049、970cm
用手性AD-H柱(chiralcel AD-H column)(己烷:
式(II)的化合物以下面所示的方案制备。所述化合物被称为
方案2-
在碳酸钾和Kryptofix 222存在下,使用商业的合成器GE
将最终产物配制在含有10%乙醇的生理盐水的生理溶液中。经过55分钟的总合成时间后,得到具有35%平均非衰变校正产率(从
生物学测试
与人类组织的体外竞争和饱和结合试验
所有使用人类组织的研究均依据苏格兰东部研究伦理服务局(the East ofScotland Research Ethics Service)(爱丁堡脑库(Edinburgh Brain Bank),11/ES/0022)进行。获得了51个大脑(78%男性,年龄53.9±9.5)和29个心脏(83%女性,年龄48.2±13.2)的样品,并且对rs6971遗传多态性进行筛选并分为如先前所述的(Owen etal.J.Cereb.Blood Flow Metab.2012)高亲和力结合剂(HAB)、混合亲和力结合剂(MAB)或低亲和力结合剂(LAB)。为了排除TSPO结合中性别依赖的差异(费尔韦瑟(Fairweather)等人),本研究中仅使用男性样品。在离心(32000g,10min,4℃)前,样品组织在10x w/v缓冲液(50mM Tris-Base,pH 7.4,4℃)中均质。随后,将组织团粒悬浮于10x w/v缓冲液中,并且在将其重悬于缓冲液(2mL)中前再次离心。随后使用Bio-Rad蛋白质试验(Bio-Rad,美国)评估样品的蛋白质浓度,将其等分并保存在-80℃直至使用。
进行如先前报道的(布莱尔等人.(Med.Chem.Commun.))竞争结合试验。简要地说,在缓冲溶液中制备250μg蛋白/mL的每个样品,随后将200μL该溶液以及10μL我们试验的配体PK11195(西格玛-奥德里奇,美国)、PBR28(ABX,德国)、AB5186或14种不同浓度的LW223(范围为0.001-3,000nM)一起添加至100μL的1nM
使用GraphPad Prism版本6(格拉夫派得软件(GraphPad Software),美国)拟合所有结合亲和力曲线。使用最小二乘算法(least squares algorithm)比较单位点拟合和双位点拟合,并且使用F-检验比较模型选择。如果p<0.05,则否定无效假设(认为单点拟合更合适)。各组(HAB、MAB或LAB)最小抑制归一化的平均SB%用于确定单位点拟合合适还是双位点拟合合适,并随后用于计算LAB:HAB比率。通过基于平均组拟合,拟合单个组织样品以计算亲和力值(K
评述
竞争结合试验用于计算已建立的TSPO配体PK11195和PBR28以及我们的配体AB5186和LW223(如图1所示)的亲和力(K
在使用人类大脑的竞争结合试验中,PK11195不受遗传多态性的影响,LAB:HAB亲和力比率为1(图2(a)),不同于PBR28的比率为49(图2(b))。配体AB5186受遗传多态性的影响,其比率为9(图2(b)),与不受影响的LW223不同,其比率为1。在PK111195和LW223结合研究中,单独计算的所有大脑样品的亲和力值表明HAB和LAB之间没有显着差异(分别为图2(e)和(h)H)。LW223的平均亲和力为0.6nM,其是PK11195的2倍。HAB和LAB中单独计算的PBR28和AB5186的亲和力值的比较显示各组之间存在显着差异(图2(f)和(g))。PBR28和AB5186中的MAB组适合双位点拟合,而所有其他实验更适合单位点拟合。
与在大脑一样,PK11195也不受心脏遗传多态性的影响,LAB:HAB比率为1(图3(a))。PBR28和AB5186在心脏和大脑中受影响的程度相似,比率分别为48和7(分别为图3(b)和(c))。LW223不受心脏多态性的影响,其比率为1(图3(d))。在PK111195和LW223结合研究中,单独计算的所有心脏样品的亲和力值均证明HAB和LAB之间没有显着差异(分别为图3(e)和(h))。在心脏中,LW223的平均亲和力与PK11195在1.7nM处相同。此外,AB5186实验中只有MAB组适合双位点拟合。
以前,已有的体内成像证据表明
动物与外科手术
所有实验均依据当地爱丁堡大学动物伦理委员会进行,并根据1986年《动物(科学程序)法》(Animals(Scientific Procedures))由内政部批准。28只成年雄性斯普拉格-杜勒(Sprague-Dawley)大鼠(357.1±8.1g和10.2±0.4周)和2只C57bl/6(25.3±3.7g和10.1±0.0周)用于本研究,其中2只C57bl/6(26.0±5.3g和13.5±5.7周)用于附加的研究。将动物圈养在标准的12h光照:12小时黑暗条件下,随时供应食物和水。实验当天,用1.5-2.5%异氟烷(50/50氧气/一氧化二氮,1L/min)来诱导维持麻醉。对于成像实验,如前所述的(沃诺克(Warnock)等人),在股静脉或尾静脉中建立了静脉内(i.v.)管线以用于注射放射性示踪物,并对股动脉插管以允许自动采集血样。
在另一组实验中(放射性新陈代谢(radiometabolite)研究),将股动脉插管用于血液采样,并经由尾静脉静脉内注射施用放射性示踪物。股静脉和动脉的手术插管操作如下:将填充肝素化盐水(20IU/mL)的聚乙烯导管(PE50)借助立体显微镜插入左股动脉或静脉中,并用绷带(6-0丝线)牢固地固定。用手术胶水将导管固定在适当的位置。通过加热的扫描床或加热垫维持体温,并且通过直肠温度计监测体温。在实验期间持续检测包括心率以及呼吸速率的生命体征。
PET研究
研究设计:
用
使用β-探针自动血液采样器的动脉输入函数
如先前所述的(Warnock等人),商业上可获得的β-探针系统(Twilite2,思维思(Swisstrace),瑞士)用于测量血液放射性。这种系统允许以1秒的时间分辨率进行全血动脉输入函数测量,并且不会因手术诱导的动静脉分流而造成失血。利用在单独研究(放射性新陈代谢实验)中获得的数据,由自动血液采样器测量的全血动脉输入函数对血浆与全血比率(plasma-to-whole blood ratio)和体内新陈代谢进行了校正。
图像采集和重建
使用临床前PET/CT小动物扫描仪(nanoPET/CT,Mediso,匈牙利)获取所有PET数据。获得了用于衰减校正的CT扫描(半圆形全轨迹,最大视场,480个投影,50kVp,300ms和1:4分箱(binning))。放射性示踪物施用后,立即使用3维1:5模式获得了120分钟的放射扫描,并重新按照如下分箱:18×10s;2×30s;1×60s;2×2min;10×5min;6×10min。PET图像使用Mediso的迭代Tera-Tomo三维重建算法和如下设置进行重建:4次迭代、6个子集、全探测器模型、低正则化、启用窄带滤波器、立体像素大小为0.4mm以及400-600keV能量窗。将PET数据进行随机、散射和衰减校正。
图像处理和数据分析
重建扫描被导入至PMOD 3.8软件(PMOD科技(PMOD Technologies),瑞士)。感兴趣积(Volumes of interest,VOI)为在感兴趣的器官周围手动绘制的。生成时间活性曲线(Time-activity curves,TAC),并且标准化摄取值(standardized uptake values,SUVs)以VOI浓度除以注射剂量再除以动物体重计算得出。使用房室分析(compartmentalanalysis)(1-组织(1T)和2-组织(2T)模型)和图形分析(Logan图和Ichise多变量分析)进行动力学建模,以估算不同组织中的分布体积(V
DVR的测试-再测试再现性以平均测量值的绝对值除以标准差计算:ABS(平均测试-再测试)/SD(测试/再测试)来计算。
剂量学
将重建的全身PET扫描导入PMOD 3.8软件(PMOD科技,瑞士),并且在表现出比背景(即源器官)更高的放射浓度的器官周围绘制VOIs。下列器官被定义为源器官:大脑、心脏、肺、胆囊、肝脏、肠、肾上腺、肾脏和膀胱。在动物体周围绘制全身VOI,并将其用于量化全身剩余活性,即全身活性减去源器官活性。在每个时间点,源器官的测量活性表示为注射剂量的百分比(%ID)。
停留时间τ,定义为在靶向器官中的累积活性(ā)与注射活性(A
评述
在小鼠和大鼠中,静脉内推注之后,
在注射后120分钟,大鼠动脉血中
在注射
全身有效时间-活性曲线示出,注射剂量的最高峰值%出现在大肠中,其次是肝脏、肺、肾脏、心脏、大脑、胆囊、膀胱和肾上腺(见图9)。使用归一化的tau值以及雄性和雌性成人人类体模(phantom)的剂量学估算示出关键器官(critical organ)是肾上腺。男性和女性体模的全身有效剂量估算分别为15.3μSv/MBq和18.4μSv/MBq(表1)。
在对进一步的老鼠进行了额外的研究之后,发现关键器官是下肠壁。雄性和雌性体模的全身有效剂量估算分别为20.5μSv/MBq和23.7μSv/MBq(表2)。
表1-选定靶向器官中估算的吸收剂量
表2-选定靶向器官中估算的吸收剂量
放射性新陈代谢物和动脉血处理及其分析
放射性示踪物施用后2、5、10、20、30、60和120分钟采集动脉血样(69.8±9.2MBq,n=17只大鼠)。所有血样均为1mL,并且从不同动物中手动收集以生成群体曲线,从而遵守大鼠终末动脉血液的总血容量限制。血液采集后,所有样品保存在冰上直至分析。使用400-1400keV窗口(珀金埃尔默Wizzard2(Perkin Elmer Wizzard2),美国)的井型γ-计数器评估全血和血浆中的放射性。血浆样品(400μL)通过乙腈变性处理,并且在Luna C18(2)柱(Luna C18(2),10×250mm,10μm,菲罗门,英国)、通过HPLC(Ultimate2000,赛默飞世尔(ThermoFisher),英国)进行分析,流动相为乙腈/水:70/30、流速为4mL/min,以估算母体分数。使用超滤单元(
将1-2级石蜡包埋的人类深部脑卒中组织和患病的冠状动脉组织切片进行脱蜡、再水化并在缓冲溶液(50mM Tris-Base,pH 7.4)中培养30分钟,然后,在存在或不存在PK11195(卒中组织中为30μM,冠状组织中为10μM)或LW223(10μM,非特异性结合组)的情况下、用2MBq/mL的
评述
放射自显影术用于成像
一般性统计分析
Graphpad Prism版本6(格拉夫派得软件公司,美国)用于所有拟合、统计分析和图形生成。在竞争结合试验和饱和试验中,使用alpha为0.2的Grubbs检验去除实验三组中的异常值。如相关图例所示,本研究使用未配对和配对的t-检验(t-tests)对两组进行比较,p<0.05被认为是统计学显著的。除非在图或表的图例中另有说明,否则所有误差线均表示标准误差平均值(SEM)。
评述
最近,首次发表了详细介绍了具有和不具有Thr
作为第一个对rs6971多态性不敏感的氟化TSPO配体,
这项研究的局限性与大多数开发新型TSPO放射性示踪物的研究所面临的局限性相似。首先,本研究中LAB的患病率约为14%,虽然高于其他研究中报道的患病率(藤田(Fujita)等人),但限制了可用于测试的样品。然而,这项研究发现大脑中PK11195和PBR28的LAB:HAB比率值与先前报道的相似(Owen et al.J.Cereb.Blood Flow Metab.2012;Owen等人;Owen et al.J.Cereb.Blood Flow Metab.),PBR28和AB5186在LAB和HAB之间达到统计学上的显着差异。在体外结合研究结果没有反映出体内结合研究结果的领域中,也出现了一些争议。TSPO放射性示踪物
由于炎症,诸如巨噬细胞的吞噬细胞和小胶质细胞在一系列病理中的作用,成功的TSPO成像方法的开发具有巨大的潜力。在这项研究中,我们证明了
总而言之,
附加实验和结果
在大鼠心肌埂塞模型中
大鼠经历永久性左冠状动脉前降支结扎以诱发心肌埂塞,并且在7天后使用
参考文献
本说明书中提及的所有文献通过引用以其整体合并在本文中。
Alam et al.Med.Mol.Imaging(2010).51,283–296(2017).
Bielohuby et al.Am.J.Physiol.Metab.293,E139–E146(2007).
Bird et al.Atherosclerosis 210,388–391(2010).
Blair et al.Med.Chem.Commun.4,1461-1466(2013).
Blair et al.Chem.Sci.6,4772-4777(2015).
Calsolaro et al.Alzheimer’s Dement.11,P792(2015).
Cappelli et al.J.Med.Chem.40,2910–2921(1997).
Cappelli et al.J.Med.Lett.14,4055-4066(2006)
Charbonneau et al.Circulation 73,476–483(1986).
Chauveau et al.Eur.J.Nucl.Med.Mol.Imaging 35,2304–2319(2008).
Cosenza-Nashat et al.Neuropathol.Appl.Neurobiol.35,306–328(2009).
Dupont et al.Int.J.Mol.Sci.18,785(2017).
Endres et al.J.Nucl.Chem.50,1276-82(2009).
Fairweather et al.J.Cardiovasc.Transl.Res.7,192–202(2014).
Fujimura et al.Atherosclerosis 201,108–111(2008).
Fujita et al.EJNMMI Res.7(2017),doi:10.1186/s13550-017-0334-8.
Gaemperli et al.Eur.Heart J.33,1902–1910(2012).
Hindorf et al.J.Nucl.Med.45,1960–5(2004).
Hui et al.Cancer 73,951-957(1994).
Ichise et al.J.Cereb.Blood Flow Metab.22,1271–1281(2002).
Ikawa et al.J.Nucl.Med.(2016),doi:10.2967/jnumed.116.178996.
Innis et al.J.Cereb.Blood Flow Metab.27,1533–1539(2007).
Khanuja et al.Genet.Commun.92,7729–7733(1995).
Kobayashi et al.J.Cereb.Blood Flow Metab.38,393–403(2018).
Kreisl et al.Neuroimage 49,2924–2932(2010).
Lacapère Steroids 68,569–585(2003).
Li et al.Clin.Exp.Pharmacol.Physiol.42,1068–1074(2015).
Li et al.Science 347,555–558(2015).
Lin et al.Genomics 18,643–50(1993).
Logan et al.J.Cereb.Blood Flow Metab.16,834–840(1996).
Logan Nucl.Med.Biol.27,661–670(2000).
Luus et al.J.Label.Compd.Radiopharm.53,501–510(2010).
Owen et al.J.Cereb.Blood Flow Metab.30,1608–18(2010).
Owen et al.J.Cereb.Blood Flow Metab.32,1–5(2012).
Owen et al.J.Nucl.Med.52,24–32(2011).
Papadopoulos et al.Trends Pharmacol.Sci.27,402–409(2006).
Paradis et al.Cardiovasc.Res.98,420–427(2013).
Schalle et al.J.Pharmacol.Exp.Ther.333,696–706(2010).
Stabin et al.J.Nucl.Med.47,655–9(2006).
Stevenson et al.Bioorg.Med.Chem.Lett.20,954–957(2010).
Thackeray et al.J.Am.Coll.Cardiol.71,263–275(2018).
Warnock et al.EJNMMI Res.1,1–11(2011).
Wilms et al.Neurobiol.Dis.14,417–424(2003).
WO 02/26713
Zanotti-Fregonara et al.ACS Chem.Neurosci.(2014),doi:10.1021/cn500138n.
- TSPO结合剂
- 一种TSPO转位蛋白PET探针在神经炎症中的显影方法
