一种编码A27L保护性抗体的mRNA及其应用
文献发布时间:2024-01-17 01:27:33
技术领域
本发明涉及一种编码A27L保护性抗体的mRNA及其应用,具体地说,涉及一种编码抗痘苗病毒A27L蛋白特异性抗体的mRNA分子及其在制备抗正痘病毒感染的药物中的应用;属于生物技术领域。
背景技术
正痘病毒属(Orthopoxvirus)归类于痘病毒科(Poxviridae)脊索动物痘病毒亚科(Chordopoxvirinae),成员包括可感染人和哺乳动物的多种痘病毒。其中,目前已知的对人类致病的正痘病毒有4种:天花病毒、痘苗病毒、牛痘病毒和猴痘病毒,并且这4种病毒的基因组同源性大于90%,存在交叉保护作用。特别是自2022年5月以来,英国、葡萄牙等多个非猴痘流行国家相继出现猴痘确诊病例,随着病例数不断增加、分布范围日益扩散,加之人际传播、社区传播的确认,2022年7月23日,世界卫生组织宣布猴痘疫情为“国际关注的突发公共卫生事件”,正痘病毒感染开始引起全球公共卫生领域的密切关注。当前,我国尚无获批特异性抗正痘病毒药物,主要是对症支持和并发症的治疗。研发安全高效的特异性药物以有效应对潜在的正痘病毒感染威胁十分必要。
中和抗体药物靶向性强、特异性高,可直接与病毒表面蛋白结合,阻断病毒感染,在人群暴露于病毒前后均能发挥保护效果,是传染病防治的有效手段。然而,传统蛋白抗体药物开发往往依赖于细胞培养,生产周期长、工艺复杂、成本高昂。与蛋白质相比,核酸的理化特点相对简单,易于制备纯化并且成本低。将编码特定抗体的信使核糖核酸(mRNA)分子通过递送系统导入生物体内,以机体细胞作为生物反应器来表达相应的抗体进而发挥其生物学功能的策略,不仅能够有效减少由抗体体外表达翻译异常修饰引起的异质性及抗体的错误折叠,并且可以有效地避免抗体复杂的体外生产及纯化过程,易于实现快速及大规模生产。
mRNA疫苗是通过将编码保护性抗原的mRNA分子递送至体内,进而在机体内表达出相应抗原以刺激机体产生特异性体液免疫反应产生抗体,并且往往需要至少2次免疫接种以获得理想的抗体水平,因此多用于疾病的预防。不同于mRNA疫苗,mRNA抗体是通过将编码保护性抗体的mRNA分子递送至机体内直接产生抗体,在暴露前和暴露后均可使用,兼具疾病预防和治疗的效果。
正痘病毒在复制过程中存在2种不同形式的感染性病毒颗粒:细胞外包膜病毒(Extracellular enveloped virion,EEV)和细胞内成熟病毒(Intracellular maturevirion,IMV)。这些表面结构蛋白主要负责病毒粘附、进入、包装和复制等,也是激活宿主体液免疫反应的主要蛋白。以痘苗病毒为例,其IMV表面蛋白A27L能够与细胞表面的硫酸乙酰肝素结合,在病毒粘附过程中发挥重要作用,并能诱导保护性中和抗体产生。研究同时也发现,痘苗病毒A27L与猴痘病毒A29L、天花病毒A30L、牛痘病毒A28L高度同源,彼此之间存在交叉保护。
在现有技术中,针对A27L的具有交叉中和活性的抗体已有报道。美国陆军传染病医学研究院的研究人员基于编码抗A33R蛋白的人-黑猩猩嵌合抗体c6C的基因序列、抗B5R蛋白的人-黑猩猩嵌合抗体c8A的基因序列、抗痘苗病毒L1R蛋白的人-鼠嵌合抗体c7D11的基因序列,分别构建了mRNA抗体,通过肌肉注射兔后可在体内产生抗体,但是血清中和抗体水平低,不太可能提供抗痘病毒感染的攻毒保护,未实现预期的技术效果。这一研究结果表明,利用mRNA技术基于现有抗体序列开发mRNA抗体,存在技术效果的不可预期性。当前,尚无能够在机体内产生保护性中和抗体的编码抗A27L蛋白抗体的mRNA分子的相关报道。
发明内容
为克服现有技术存在的缺陷,本发明的目的之一在于提供一种编码A27L保护性抗体的mRNA,所述mRNA为一种具有抗正痘病毒感染活性的编码抗A27L蛋白抗体的mRNA,将所述mRNA递送至体内后,能够在生物体内表达针对A27L蛋白的保护性单克隆抗体并分泌至血液循环中,起到保护机体抵御正痘病毒感染的作用。
本发明的目的之二在于提供一种编码A27L保护性抗体的mRNA的应用,所述应用为在制备抗正痘病毒感染的药物中的应用。
为实现本发明的目的,提供以下技术方案。
一种编码A27L保护性抗体的mRNA,所述mRNA由构建物A和构建物B组成:
构建物A为编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的轻链mRNA构建物(简称为:mRNA-mab301-LC),按照正义链,即5'→3'方向,依次包括如下元件:
5’帽结构、5’非编码区(5’UTR)、人源抗体卡帕轻链信号肽、抗体mab301轻链、3’非编码区(3’UTR)和多聚腺苷酸序列(poly A);
构建物B为编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的重链mRNA构建物(简称为:mRNA-mab301-HC),按照正义链,即5'→3'方向,依次包括如下元件:
5’帽结构、5’非编码区(5’UTR)、人源抗体卡帕轻链信号肽、抗体mab301重链、3’非编码区(3’UTR)和多聚腺苷酸序列(poly A)。
其中,所述5’UTR的核苷酸序列为:
CUUGUUCUUUUUGCAGAAGCUCAGAAUAAACGCUCAACUUUGGC;
在序列表中如SEQ ID NO:3所示。
所述人源抗体卡帕轻链信号肽的氨基酸序列为:
MELGLSWIFLLAILKGVQC;
在序列表中如SEQ ID NO:4所示。
所述人源抗体卡帕轻链信号肽的核苷酸序列为:
AUGGAGCUGGGACUGAGCUGGAUUUUUCUGCUGGCCAUUCUGAAGGGGGUGCAGUGC;
在序列表中如SEQ ID NO:5所示。
所述抗体mab301轻链的氨基酸序列为:
SYELTQSPSVSVSPGQTARITC
其中,CDR1、CDR2、CDR3用下划线标出;在序列表中如SEQ ID NO:6所示。
所述抗体mab301轻链的核苷酸序列为:
UCCUACGAGCUGACACAGAGCCCCAGCGUGUCCGUGAGCCCCGGCCAGACUGCCAGGAUCACAUGC
其中,CDR1、CDR2、CDR3用下划线标出;在序列表中如SEQ ID NO:7所示。
所述抗体mab301重链的氨基酸序列为:
EVQLLESGGGLVQPGGSLRLSCAASGFSFS
其中,CDR1、CDR2、CDR3用下划线标出;在序列表中如SEQ ID NO:8所示。
所述抗体mab301重链的核苷酸序列为:
GAAGUGCAGCUGCUGGAGUCCGGCGGCGGCCUGGUGCAGCCCGGCGGCAGCCUGCGGCUGAGCUGCGCCGCUAGCGGGUUCAGCUUCUCC
其中,CDR1、CDR2、CDR3用下划线标出;在序列表中如SEQ ID NO:9所示。
本发明的CDR分析依据网站http://www.abysis.org/abysis/sequence_input/key_annotation/key_annotation.cgi完成。
3’UTR的核苷酸序列为:
UAGGCUGGAGCCUCGGUGGCCAUGCUUCUUGCCCCUUGGGCCUCCCCCCAGCCCCUCCUCCCCUUCCUGCACCCGUACCCCCGUGGUCUUUGAAUAAAGUCUGAGUGGGCGGCACUAGU;
在序列表中如SEQ ID NO:10所示。
根据不同mRNA的需求,可在mRNA的5’端灵活添加不同的5’帽结构,如m
在本发明的一些优选的实施方案中,所述5'帽结构为m
“m
所述多聚腺苷酸序列(poly A)可以包含50个~400个腺苷酸,优选包含100个~160个腺苷酸。
所述mRNA中部分或全部的尿嘧啶和/或胞嘧啶进行了能够提高所述mRNA在生物体内稳定性的化学改性。
所述化学改性包括利用以下物质置换所述mRNA中的至少50%、至少60%、至少70%、至少80%、至少90%或100%的尿嘧啶。
其中,置换尿嘧啶的物质选自假尿苷、N1-甲基假尿苷、N1-乙基假尿苷、2-硫尿苷、4’-硫尿苷、5-甲基胞嘧啶、5-甲基尿苷、2-硫基-1-甲基-1-去氮杂-假尿苷、2-硫基T-甲基-假尿苷、2-硫基-5-氮杂-尿苷、2-硫基-二氢假尿苷、2-硫基-二氢尿苷、2-硫基-假尿苷、4-甲氧基-2-硫基-假尿苷、4-甲氧基-假尿苷、4-硫基-1-甲基-假尿苷、4-硫基-假尿苷、5-氮杂-尿苷、二氢假尿苷、5-甲氧基尿苷和2'-O-甲基尿苷中的至少一种,优选假尿苷、N1-甲基假尿苷或N1-乙基假尿苷,进一步优选N1-甲基假尿苷;和/或,
所述化学改性包括利用5-甲基胞嘧啶置换所述mRNA中的至少50%、至少60%、至少70%、至少80%、至少90%或100%的胞嘧啶。
优选构建物A的核苷酸序列为:
CUUGUUCUUUUUGCAGAAGCUCAGAAUAAACGCUCAACUUUGGCGCCGCCACCAUGGAGCUGGGACUGAGCUGGAUUUUUCUGCUGGCCAUUCUGAAGGGGGUGCAGUGCUCCUACGAGCUGACACAGAGCCCCAGCGUGUCCGUGAGCCCCGGCCAGACUGCCAGGAUCACAUGCAGCGGCGACGCCCUGCCCGAGCAGUACGCCUACUGGUACCAGCAGAAGCCCGGCCAGGCCCCCGUGCUCGUGAUCUACAAGGACAGCGAGCGGCCCUCCGGCAUUCCCGAGCGGUUCAGCGGCAGCGGCAGCGGUACAACAGUGACCCUGACCAUCACAGGGGUGCAGGCCGAGGAUGAGGCCGAUUACUACUGCCAGAGCGCCGAUAACAGCGGGACAUACGAGGUGUUCGGGACCGGGACCAAGGUGACUGUGCUGGGGCAGCCCAAGGCCGCCCCCAGCGUGACACUGUUCCCCCCCUCCAGCGAGGAGCUGCAGGCCAACAAGGCCACCUUAGUGUGUCUGAUCUCAGACUUUUACCCUGGCGCCGUCACAGUGGCCUGGAAGGCCGACAGCAGCCCCGUCAAAGCUGGCGUGGAAACCACAACCCCCUCCAAACAGUCCAACAACAAAUACGCCGCCAGCUCCUACCUGAGCCUGACACCCGAGCAGUGGAAGUCCCACCGGAGCUACAGCUGCCAGGUGACACACGAGGGGAGCACCGUGGAAAAGACAGUGGCCCCCACCGAGUGCAGCUAAGAAUUCUAGGCUGGAGCCUCGGUGGCCAUGCUUCUUGCCCCUUGGGCCUCCCCCCAGCCCCUCCUCCCCUUCCUGCACCCGUACCCCCGUGGUCUUUGAAUAAAGUCUGAGUGGGCGGCACUAGUAn;
其中,An表示多聚腺苷酸序列(poly A),n表示腺苷酸的数量;构建物A的核苷酸序列在序列表中如SEQ ID NO:1所示。
构建物A的核苷酸序列还可以选自与SEQ ID NO:1具有至少70%、至少80%或至少90%同源性的核苷酸序列。
优选构建物B的核苷酸序列为:
CUUGUUCUUUUUGCAGAAGCUCAGAAUAAACGCUCAACUUUGGCGCCGCCACCAUGGAGCUGGGACUGAGCUGGAUUUUUCUGCUGGCCAUUCUGAAGGGGGUGCAGUGCGAAGUGCAGCUGCUGGAGUCCGGCGGCGGCCUGGUGCAGCCCGGCGGCAGCCUGCGGCUGAGCUGCGCCGCUAGCGGGU
UCAGCUUCUCCAGCUACGCCAUGAGCUGGGUGCGGCAGGCCCCCGGCAA
GGGCCUGGAGUGGGUGAGCGGGAUCGGGAACUCCGGGGAUCGGACCUU
CUACGCCGAUAGCGCCAAGGGGAGGUUCACCAUCUUCAGAGACAACAG
CAACAACAGGCUGUACCUGCAGAUGAACUCCCUGCGGGCCGCCGACACC
GCCGUCUACUACUGCGCUAAGUGGGGCCGGUUUGAGUCCGGGGCCUUC
UGGGGGCAGGGCGUGCUGGUGACCGUGAGCUCCGCCAGCACCAAGGGC
CCAAGCGUGUUCCCACUGGCCCCUAGCAGCAAGAGCACUAGCGGGGGC
ACCGCCGCCCUGGGGUGCCUGGUGAAGGAUUACUUCCCCGAGCCCGUG
ACAGUGAGCUGGAACUCCGGGGCCCUCACAUCCGGCGUGCACACAUUCC
CCGCCGUGCUGCAGUCCAGCGGGCUCUACAGCCUCAGCAGCGUGGUGAC
AGUGCCCUCCUCCAGCCUCGGGACCCAGACAUACAUCUGCAACGUGAAC
CACAAGCCCAGCAACACAAAGGUGGAUAAGCGCGUGGAGCCCAAGAGC
UGCGACAAGACACACACAUGCCCCCCCUGCCCCGCCCCUGAGGCCGCCG
GCGGGCCCAGCGUGUUUCUGUUCCCCCCUAAGCCCAAGGAUACACUGU
ACAUUACAAGGGAGCCCGAGGUCACUUGCGUGGUGGUGGAUGUGAGCC
ACGAGGACCCUGAGGUGAAGUUCAACUGGUACGUCGAUGGGGUGGAGG
UGCACAACGCCAAGACCAAGCCCAGGGAGGAGCAGUACAACAGCACCU
ACAGGGUGGUGUCCGUGCUGACAGUGCUGCACCAGGACUGGCUGAACG
GGAAGGAGUACAAGUGCAAGGUGAGCAACAAGGCCCUCCCAGCCCCCA
UUGAAAAGACCAUCAGCAAGGCCAAGGGCCAGCCCAGGGAGCCCCAGG
UGUACACACUCCCCCCCAGCCGGGAGGAGAUGACAAAGAACCAGGUGA
GCCUGACCUGCCUGGUGAAGGGGUUCUACCCCUCCGACAUUGCCGUGG
AGUGGGAGUCCAACGGGCAGCCCGAGAACAACUACAAGACCACCCCCCC
CGUGCUGGACAGCGACGGGAGCUUCUUCCUGUACAGCAAGCUGACUGU
CGAUAAGAGCAGGUGGCAGCAGGGGAACGUGUUCAGCUGCUCCGUGAU
GCACGAGGCCCUGCACAACCACUACACCCAGAAGUCCCUGAGCCUGAGC
CCCGGCAAGUAAGAAUUCUAGGCUGGAGCCUCGGUGGCCAUGCUUCUU
GCCCCUUGGGCCUCCCCCCAGCCCCUCCUCCCCUUCCUGCACCCGUACCC
CCGUGGUCUUUGAAUAAAGUCUGAGUGGGCGGCACUAGU
An;
其中,An表示多聚腺苷酸序列(poly A),n表示腺苷酸的数量;构建物B的核苷酸序列在序列表中如SEQ ID NO:2所示。
构建物B的核苷酸序列还可以选自与SEQ ID NO:2具有至少70%、至少80%或至少90%同源性的核苷酸序列。
一种本发明所述的编码A27L保护性抗体的mRNA的应用,所述应用为所述mRNA在制备抗正痘病毒感染的药物中的应用。
所述正痘病毒是指正痘病毒属病毒,优选为痘苗病毒、猴痘病毒、牛痘病毒和天花病毒中的至少一种。
所述抗正痘病毒感染的药物是指预防感染正痘病毒的药物,和/或感染正痘病毒后进行治疗的药物,所述药物可以以药物组合物或是试剂盒的形式出现。
一种药物组合物,包含本发明所述的一种编码A27L保护性抗体的mRNA和递送载体,所述药物组合物作为抗正痘病毒感染的药物。
优选所述递送载体为纳米颗粒。
进一步地,优选所述递送载体为脂质纳米颗粒,如纳米脂球(LNP)。
更进一步地,优选所述脂质纳米颗粒具有50nm~200nm的平均直径,且具有小于0.4的多分散性系数值。
一种试剂盒,包含本发明所述的一种编码A27L保护性抗体的mRNA和/或本发明所述的药物组合物,作为抗正痘病毒感染的药物。
有益效果
(1)本发明提供了一种编码A27L保护性抗体的mRNA,所述mRNA通过具有独创性的分子设计,通过合并频繁的密码子和/或具有更高tRNA丰度的密码子;富集鸟嘌呤-胞嘧啶含量提高体外的稳态mRNA水平和体内的蛋白表达量;重点关注5’UTR和3’UTR的选择、信号肽的选择等mRNA表达关键元件的设计,实现了在生物体内正确合成编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301。
(2)本发明提供了一种编码A27L保护性抗体的mRNA的应用,所述的mRNA接种BALB/c小鼠后,可在小鼠体内产生具有中和活性的抗体,并且可以保护小鼠抵御正痘病毒感染,具备在制备抗正痘病毒感染的药物中的应用。
(3)本发明提供了一种编码A27L保护性抗体的mRNA及其应用,本发明提供的mRNA抗体与传统依赖哺乳动物细胞体外培养表达的蛋白抗体相比,具有颠覆性的优势。mRNA抗体以机体自身细胞作为抗体生产的生物工厂,不仅能够产生自然状态下的抗体翻译后修饰,有效减少由抗体体外表达翻译异常修饰引起的异质性及抗体的错误折叠,并且能够有效地避免抗体复杂的体外生产及纯化过程。此外,mRNA技术作为通用性技术平台,mRNA抗体的制备工艺较传统蛋白更为简单、易实现快速及大规模标准化生产,并且便于储存和运输。
(4)本发明提供了一种药物组合物,通过将本发明所述的mRNA和药学上可接受的载体结合,并选择脂质纳米颗粒进行包装递送,获得用于抗正痘病毒感染的信使核糖核酸(mRNA)抗体。
(5)本发明提供了一种试剂盒,包含本发明所述的一种编码A27L保护性抗体的mRNA和/或本发明所述的药物组合物,作为抗正痘病毒感染的药物制品,应用前景广阔。
附图说明
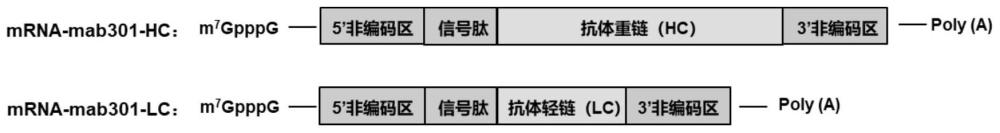
图1为实施例1中编码A27L保护性抗体的mRNA分子的构建策略示意图。
图2为实施例1中编码A27L保护性抗体的mRNA分子的琼脂糖凝胶电泳鉴定结果。
图3为实施例2中编码A27L保护性抗体的mRNA体外表达情况鉴定结果。
图4为实施例3中mRNA制剂mRNA-mab301-LNP的粒径检测结果。
图5为实施例4中经mRNA制剂mRNA-mab301-LNP注射的小鼠血清中和抗体效价。
具体实施方式
下面结合附图和具体实施例来详述本发明,但不作为对本发明专利的限定。
实施例1合成编码正痘病毒抗体的mRNA分子
(1)mRNA的分子设计
针对抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的轻链和重链氨基酸序列,设计了一种编码A27L保护性抗体的mRNA,所述mRNA由构建物A和构建物B组成,如图1所示:
构建物A为编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的轻链mRNA构建物(简称为:mRNA-mab301-LC),按照正义链,即5'→3'方向,依次包括如下元件:
5’帽结构、5’非编码区(5’UTR)、人源抗体卡帕轻链信号肽、抗体mab301轻链、3’非编码区(3’UTR)和多聚腺苷酸序列(poly A);
构建物B为编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的重链mRNA构建物(简称为:mRNA-mab301-HC),按照正义链,即5'→3'方向,依次包括如下元件:
5’帽结构、5’非编码区(5’UTR)、人源抗体卡帕轻链信号肽、抗体mab301重链、3’非编码区(3’UTR)和多聚腺苷酸序列(poly A)。
其中,所述5’UTR的核苷酸序列如SEQ ID NO:3所示。
所述人源抗体卡帕轻链信号肽的氨基酸序列如SEQ ID NO:4所示,核苷酸序列如SEQ ID NO:5所示。
所述抗体mab301轻链的氨基酸序列如SEQ ID NO:6所示,核苷酸序列如SEQ IDNO:7所示。
所述抗体mab301重链的氨基酸序列如SEQ ID NO:8所示,核苷酸序列如SEQ IDNO:9所示。
3’UTR的核苷酸序列如SEQ ID NO:10所示。
所述5’帽结构为m
(2)mRNA的合成:根据mab301的轻链和重链核苷酸序列,以及mRNA表达载体ABOP-028(Zhang NN,et.al.A Thermostable mRNA Vaccine against COVID-19)序列,设计引物,引物名称及序列如表1所示。
表1
其中,AB028-F作为上游引物,与下游引物301LC-R构成AB028-F/301LC-R引物对,用于构建DNA转录模板质粒pAB028-mab301-LC(轻链质粒);AB028-F作为上游引物,与下游引物301HC-R构成AB028-F/301HC-R引物对,用于构建DNA转录模板质粒pAB028-mab301-HC(重链质粒)。
将上述构建的轻链和重链DNA转录模板质粒分别使用BsaⅠ限制性内切酶(购自NEB公司)进行线性化,得到线性化质粒。分别以线性化质粒为模板,以天然三磷酸核苷(ATP、CTP、UTP和GTP,购自上海兆维公司)为底物,利用T7 RNA聚合酶(购自近岸公司)进行体外转录(IVT)反应;加入DNase I(购自诺唯赞公司)消化模板DNA;加入7.5M氯化锂溶液(购自Invitrogen公司)纯化mRNA;利用牛痘病毒加帽酶(10U/μL,购自近岸公司)对获得的mRNA进行5’端加帽,利用帽结构2’-O-甲基转移酶(50U/μL,购自近岸公司)完成帽结构甲基化;最后加入7.5M氯化锂溶液(购自Invitrogen公司)纯化加帽的mRNA,获得编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的轻链mRNA分子(mRNA-mab301-LC),核苷酸序列如SEQID NO:1所示,以及编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的重链mRNA分子(mRNA-mab301-HC),核苷酸序列如SEQ ID NO:2所示。
对mRNA-mab301-LC和mRNA-mab301-HC和进行1%(W/V)琼脂糖凝胶电泳鉴定,结果如图2所示,可见轻链mRNA分子和重链mRNA分子条带单一且大小符合预期,表明成功纯化获得的编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的轻链mRNA分子和重链mRNA分子。
实施例2mRNA的体外表达情况鉴定
转染前1天分别将BHK-21细胞(ATCC,#CCL-10)传至6孔板,细胞密度为1×10
实验组使用Lipofectamine MessengerMAX脂质体转染试剂(购自Thermo公司)转染,将mRNA-mab301-LC和mRNA-mab301-HC按照摩尔比1:1共转染BHK-21细胞,6小时后,将转染上清更换为Opti-MEM培养基(购自Thermo公司)。
对照组除未加入mRNA-mab301-LC和mRNA-mab301-HC外,其余步骤同实验组。
分别收集实验组转染后24小时的细胞培养上清和对照组的细胞培养上清,分别5000g离心去除细胞碎片。
将16μL实验组去除细胞碎片后的细胞培养上清与5×还原蛋白上样缓冲液(购自生工生物公司)充分混合,置于沸水浴中煮样10min,得到实验组蛋白样品。
将16μL对照组去除细胞碎片后的细胞培养上清与5×还原蛋白上样缓冲液(购自生工生物公司)充分混合,置于沸水浴中煮样10min,得到对照组蛋白样品。
将实验组蛋白样品(mRNA-mab301)和对照组蛋白样品(mock)通过8%~20%聚丙烯酰胺凝胶电泳进行Western Blot鉴定,使用的抗重链的二抗为HRP标记的山羊抗人IgG(购自中杉金桥,用含有2%脱脂奶粉的PBS进行1:5000(V/V)稀释),抗轻链的二抗为HRP标记的山羊抗人IgG(购自abcam公司,用含有2%脱脂奶粉的PBS进行1:10000(V/V)稀释),实验结果如图3所示,抗体mRNA转染BHK-21细胞上清中,可检测到抗体重链(约50KDa)和抗体轻链(约25KDa)成功表达。
实施例3mRNA分子的纳米脂球包封
将实施例1制得的mRNA-mab301-LC和mRNA-mab301-HC以摩尔比1:1进行混合,获得编码mab301抗体的mRNA原液。利用NanoAssemblr Ignite
实施例4mRNA分子的体内中和活性鉴定
分别设置实验组和对照组如下:
实验组(mRNA-mab301-LNP):将1mg/kg实施例3制得的mRNA-mab301-LNP通过尾静脉注射6~8周龄的BALB/c小鼠,小鼠数量为6只,24h后通过眼眶后静脉丛采血的方式采集小鼠血样,分离血清,并将血清于56℃灭活30min后用于空斑减少中和试验(PlaqueReduction Neutralization Test,PRNT)。将BSC-1细胞(ATCC,#CCL-26)传至24孔板中,次日待细胞密度达到90%进行实验;用含有体积分数为1%的BSA的HBSS(HBSS-1%BSA)将血清以2倍梯度进行稀释,分别稀释至如下梯度:1:10、1:20、1:40、1:80、1:160、1:320;用HBSS-1%BSA将痘苗病毒WR株(Taxonomy ID:696871)IMV病毒稀释至50PFU/90μL,再加入10μL豚鼠补体(购自索莱宝公司)得到病毒稀释液;将100μL病毒稀释液与上述各稀释梯度血清100μL分别等体积混合后置于37℃孵育1h,弃去24孔板中的细胞培养液,加入200μL上述血清-病毒混合液,于37℃、5%CO
对照组(Placebo):将不含有mRNA的空纳米脂球(LNP)通过尾静脉注射6~8周龄的BALB/c小鼠,其余同实验组。
实验组和对照组的实验结果如图5所示,图5中,左侧为对照组结果,右侧为实验组结果,表明将编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的mRNA分子递送至生物体内后能够产生具有中和活性的抗体。
由于正痘病毒属痘病毒之间的同源性,且已有研究证实同属痘病毒的抗原性相近,病毒感染后诱导机体产生的抗体可提供交叉免疫保护,即具有抵抗其他正痘病毒感染的作用。从实施例4结果,本领域技术人员可以推定本发明的编码抗痘苗病毒IMV表面蛋白A27L的单克隆抗体mab301的mRNA分子在机体内能够产生对其他正痘病毒属的痘病毒,如猴痘病毒、天花病毒、牛痘病毒具有交叉中和活性的保护性抗体,且根据保护性抗体水平推断能够有效保护机体抵抗正痘病毒,如猴痘病毒、天花病毒、牛痘病毒的感染。
- 一种用于血凝方法检测PCV2病毒的双功能纳米抗体、编码基因及其应用
- 一种艰难梭菌谷氨酸脱氢酶的纳米抗体、编码序列及其筛选方法和应用
- 一种长链非编码RNA lncRNA-6585及其抗体与应用
- 微针注射mRNA编码双特异性抗体药物的试剂、方法和应用
- mRNA编码的纳米抗体及其应用
