一种检测犬冠状病毒和犬细小病毒的核酸组合物、试剂盒及应用
文献发布时间:2023-06-19 11:59:12
技术领域
本发明涉及病原体检测技术领域,具体而言,涉及一种检测犬冠状病毒和犬细小病毒的核酸组合物、试剂盒及应用。
背景技术
病毒性肠炎是引起6月龄以下犬的传染性腹泻的最常见原因之一。犬冠状病毒(Canine coronavirus,CCoV或CCV)和犬细小病毒(Canine Parvovirus,CPV)已被确认为是引起犬病毒性肠炎的主要病原体。其中,犬细小病毒传染性强、发病率高,且对环境及常见消毒剂具有较强的抵抗力。而犬冠状病毒为单链RNA病毒,具有囊膜,对热、去污剂等较为敏感。犬感染CCV或CPV后,可表现出不同程度的胃肠道症状,初期以呕吐为主,随着病情的发展可出现糊状、半糊状、水样腹泻,CPV还可引起番茄汁样腥臭粪便,后迅速出现脱水。病犬和康复犬均可带毒,病原主要经消化道传播,且常以混合感染的形式出现,当犬冠状病毒和犬细小病毒混合感染犬时,患犬可出现严重的出血性肠炎,导致患犬的死亡率显著升高。而快速、准确地确定引起犬消化道疾病的病原体种类,对于患犬的临床鉴别诊断及治疗有着重要的意义。
目前临床中最常用诊断方法为胶体金检测或普通PCR检测。例如专利CN201711054378.X提供了一种犬冠状病毒抗体快速定量检测卡及使用方法,胶体金法存在检测灵敏度低的问题;普通PCR的灵敏度虽然较高,但检测的病原体单一。
鉴于此,特提出本发明。
发明内容
本发明的目的在于提供一种检测犬冠状病毒和犬细小病毒的核酸组合物、试剂盒及应用以解决上述技术问题。
本发明是这样实现的:
本发明提供了一种检测犬冠状病毒和犬细小病毒的核酸组合物,其包括用于检测犬冠状病毒的第一核酸组合物和用于检测犬细小病毒的第二核酸组合物,第一核酸组合物包括引物对1和探针1,引物对1的核苷酸序列具有与SEQ ID NO.1-2所示的序列至少80%的一致性,探针1的核苷酸序列具有与SEQ ID NO.3所示的序列至少80%的一致性,第二核酸组合物包括引物对2和探针2,引物对2的核苷酸序列具有与SEQ ID NO.4-5所示的序列至少80%的一致性,探针2的核苷酸序列具有与SEQ ID NO.6所示的序列至少80%的一致性。
在本发明应用较佳的实施方式中,上述引物对1的核苷酸序列如SEQ ID NO.1-2所示,探针1的核苷酸序列如SEQ ID NO.3所示,引物对2的核苷酸序列如SEQ ID NO.4-5所示,探针2的核苷酸序列如SEQ ID NO.6所示。
在本发明应用较佳的实施方式中,上述探针1和探针2的5’端均标记有荧光报告基团,3’端均标记有荧光淬灭基团。
在本发明应用较佳的实施方式中,上述荧光报告基团为HEX、FAM、TET、CF532、JOE、TAMRA、ROX、CY3、CY5、Texas Red、NED、Alexa Flour或VIC,淬灭基团为MGB、TAMRA、BHQ1、BHQ2、BHQ3或QSY。
本发明提供了一种检测试剂盒,其包括上述的核酸组合物。
本发明提供了一种上述核酸组合物在制备检测试剂盒中的应用。
本发明提供了一种试剂,其包括上述的核酸组合物。
在本发明应用较佳的实施方式中,上述试剂为冻干试剂或液体试剂。
上述核酸组合物或上述试剂在鉴定或辅助鉴定犬消化道病毒中的应用;应用为非疾病诊断或治疗为目的的应用;犬消化道病毒为犬冠状病毒和犬细小病毒中的至少一种。
本发明还提供了一种含有上述核酸组合物的鉴定或辅助鉴定犬消化道病毒的芯片。
本发明具有以下有益效果:
本发明提供了一种可以同时检测犬冠状病毒和犬细小病毒的核酸组合物,该组合物可以用于犬消化道病毒实时荧光定量PCR的检测,经发明人验证该核酸组合物检测病原体的特异性好,且灵敏度高,对于两种病原体的最低检测限均达到5×10
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
图1为检测CCV的引物和探针的筛选结果图;
图2是检测CPV的引物和探针的筛选结果图;
图3是试剂盒特异性测试中CCV检测通道结果;
图4是试剂盒特异性测试中CPV检测通道结果;
图5是试剂盒检测限测试中CCV在最低检测限时的荧光定量PCR扩增曲线图;
图6是试剂盒检测限测试中CPV在最低检测限时的荧光定量PCR扩增曲线图;
图7为待测样本荧光定量PCR扩增结果图;
图8为犬冠状病毒的PCR扩增产物测序后的BLAST对比结果图;
图9为犬细小病毒的PCR扩增产物测序后的BLAST对比结果图。
具体实施方式
现将详细地提供本发明实施方式的参考,其一个或多个实例描述于下文。提供每一实例作为解释而非限制本发明。实际上,对本领域技术人员而言,显而易见的是,可以对本发明进行多种修改和变化而不背离本发明的范围或精神。例如,作为一个实施方式的部分而说明或描述的特征可以用于另一实施方式中,来产生更进一步的实施方式。
本发明提供了一种检测犬冠状病毒和犬细小病毒的核酸组合物,其包括用于检测犬冠状病毒的第一核酸组合物和用于检测犬细小病毒的第二核酸组合物,第一核酸组合物包括引物对1和探针1,引物对1的核苷酸序列具有与SEQ ID NO.1-2所示的序列至少80%的一致性,探针1的核苷酸序列具有与SEQ ID NO.3所示的序列至少80%的一致性,第二核酸组合物包括引物对2和探针2,引物对2的核苷酸序列具有与SEQ ID NO.4-5所示的序列至少80%的一致性,探针2的核苷酸序列具有与SEQ ID NO.6所示的序列至少80%的一致性。
上述第一核酸组合物是基于犬冠状病毒的全基因组序列设计的,犬冠状病毒的全基因组序列参照NCBI序列号KY063616.1。第二核酸组合物是基于犬细小病毒的全基因组序列设计的,犬细小病毒的全基因组序列参照NCBI序列号MW653256.1。
在一种实施方式中,引物对1的核苷酸序列具有与SEQ ID NO.1-2所示的序列85%、88%、90%、95%、99%或100%的一致性;探针1的核苷酸序列具有与SEQ ID NO.3所示的序列85%、88%、90%、95%、99%或100%的一致性,引物对2的核苷酸序列具有与SEQID NO.4-5所示的序列85%、88%、90%、95%、99%或100%的一致性,探针2的核苷酸序列具有与SEQ ID NO.6所示的序列85%、88%、90%、95%、99%或100%的一致性。
在本发明应用较佳的实施方式中,上述引物对1的核苷酸序列如SEQ ID NO.1-2所示,探针1的核苷酸序列如SEQ ID NO.3所示,引物对2的核苷酸序列如SEQ ID NO.4-5所示,探针2的核苷酸序列如SEQ ID NO.6所示。
序列如下:
在本发明应用较佳的实施方式中,上述探针1和探针2的5’端均标记有荧光报告基团,3’端均标记有荧光淬灭基团。
在本发明应用较佳的实施方式中,上述荧光报告基团为HEX、FAM、TET、CF532、JOE、TAMRA、ROX、CY3、CY5、Texas Red、NED、Alexa Flour或VIC,淬灭基团为MGB、TAMRA、BHQ1、BHQ2、BHQ3或QSY。
此外,在其他实施方式中,上述荧光报告基团以及猝灭基团可以根据需要进行自适应调整,并不限于上述限定的几种类型,只要能满足荧光的激发和猝灭均可行,在一种可选的实施方式中,在检测CCV和CPV的探针标记不同最大激发波长的荧光报告基因。
本发明提供了一种检测试剂盒,其包括上述的核酸组合物。
在一种实施方式中,上述检测试剂盒还包括检测缓冲液,酶,水和dNTP。上述缓冲液用于荧光定量PCR检测用,可选自市售的常规荧光定量PCR时的缓冲液。
本发明提供了一种上述核酸组合物在制备检测试剂盒中的应用。可选的,在试剂盒中设置引物对的上下游引物单独分装,在一种可选的实施方式中,上述试剂盒中带有用于稀释引物的水(超纯水)。
本发明提供了一种试剂,其包括上述的核酸组合物。
在本发明应用较佳的实施方式中,上述试剂为冻干试剂或液体试剂。可选的,将上述引物对1中的上下游引物单独冻干制粉,分装于试剂保存管中作为单独的产品或者成套的产品;同样的方法将引物对2中的上下游引物单独冻干制粉,分装于试剂保存管中作为单独的产品或者成套的产品。
可选的,将上述核酸组合物制备为液体试剂,将相应的引物对或探针溶于水中。
上述核酸组合物或上述试剂在鉴定或辅助鉴定犬消化道病毒中的应用;应用为非疾病诊断或治疗为目的的应用;犬消化道病毒为犬冠状病毒和犬细小病毒中的至少一种。
本发明还提供了一种含有上述核酸组合物的鉴定或辅助鉴定犬消化道病毒的芯片。例如在芯片的固相载体上锚固上述的核酸组合物以实现犬冠状病毒和犬细小病毒的检测。固相载体可以选择市售的任意一种载体。在一种实施方式中,也可选自将上述核酸组合物通过核酸偶联物偶联至相应的微珠上。
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
本实施例提供了一种检测犬冠状病毒(CCV)和犬细小病毒(CPV)的核酸组合物,其包括用于检测犬冠状病毒的第一核酸组合物和用于检测犬细小病毒的第二核酸组合物。其中,第一核酸组合物包括引物对1和探针1,第二核酸组合物包括引物对2和探针2。上述引物对1的核苷酸序列如SEQ ID NO.1-2所示,探针1的核苷酸序列如SEQ ID NO.3所示,引物对2的核苷酸序列如SEQ ID NO.4-5所示,探针2的核苷酸序列如SEQ ID NO.6所示。
序列如下:
上述核酸组合是通过查询两种病原的相关资料文献,并对相关基因进行分析筛选获得的。犬冠状病毒的全基因组序列参照NCBI序列号KY063616.1。犬细小病毒的全基因组序列参照NCBI序列号MW653256.1。使用引物探针设计软件选择合适的序列,即尽量避免引物间形成二聚体和发卡结构,且其引物退火温度在60℃左右。
实施例2
本实施例提供了一种检测试剂盒,其包括实施例1提供的核酸组合物。本实施例提供的试剂盒采用25μL的反应体系,包括12.5μL的PCR反应液(包括逆转录酶、Taq DNA聚合酶、dNTP、MgCl
犬冠状病毒的引物探针组:0.15μL的CCV-F,0.2μL的CCV-R,0.2μL的CCV-P;
犬细小病毒的引物探针组:0.15μL的CPV-F,0.15μL的CPV-R,0.2μL的CPV-P,3.7μL的DEPC处理水、5μL的模板。其中PCR反应液购自珠海宝锐生物。
实施例3
本实施例提供了一种检测试剂,其包括实施例1提供的核酸组合物。
实施例4
本实施例提供了一种检测犬冠状病毒(CCV)和犬细小病毒(CPV)的核酸组合物,其包括用于检测犬冠状病毒的第一核酸组合物和用于检测犬细小病毒的第二核酸组合物。其中,第一核酸组合物包括引物对1和探针1,第二核酸组合物包括引物对2和探针2。
对比例1
提供了一种检测犬冠状病毒(CCV)和犬细小病毒(CPV)的核酸组合物,其包括表1所示的用于检测犬冠状病毒的CCV-F1与CCV-R1引物对,以及CCV-P1探针;用于检测犬细小病毒的CPV-F1与CPV-R1引物对,以及CPV-P1探针。
需要说明的是,本对比例中的核酸组合物的序列筛选方法同实施例1。
表1序列表。
实验例1
本实验例对上述实施例1和对比例1中的核酸组合物进行筛选测试。
委托赛默飞世尔科技公司进行合成实施例1和对比例1中的引物探针,并按照说明书进行稀释。
分别对犬冠状病毒、犬细小病毒的临床样本进行核酸提取,提取后的病毒核酸先使用市售世纪元亨的PCR单项检测试剂进行扩增,以确认样本中是否确实含有犬冠状病毒或犬细小病毒(采用下述的PCR反应条件进行扩增,扩增结果参照图7所示,由图7可知待测样本中分别含有犬冠状病毒和犬细小病毒)。
分别使用不同引物或探针组合配制PCR试剂,采用25μL的反应体系,包括12.5μL的PCR反应液(包括逆转录酶、Taq DNA聚合酶、dNTP、MgCl
犬冠状病毒的引物探针组:0.15μL的CCV-F/CCV-F1,0.2μL的CCV-R/CCV-R1,0.2μL的CCV-P/CCV-P1;
犬细小病毒的引物探针组:0.15μL的CPV-F/CPV-F1,0.15μL的CPV-R/CPV-R1,0.2μL的CPV-P/CPV-P1,6.45μL的DEPC处理水、5μL的模板。其中PCR反应液购自珠海宝锐生物。
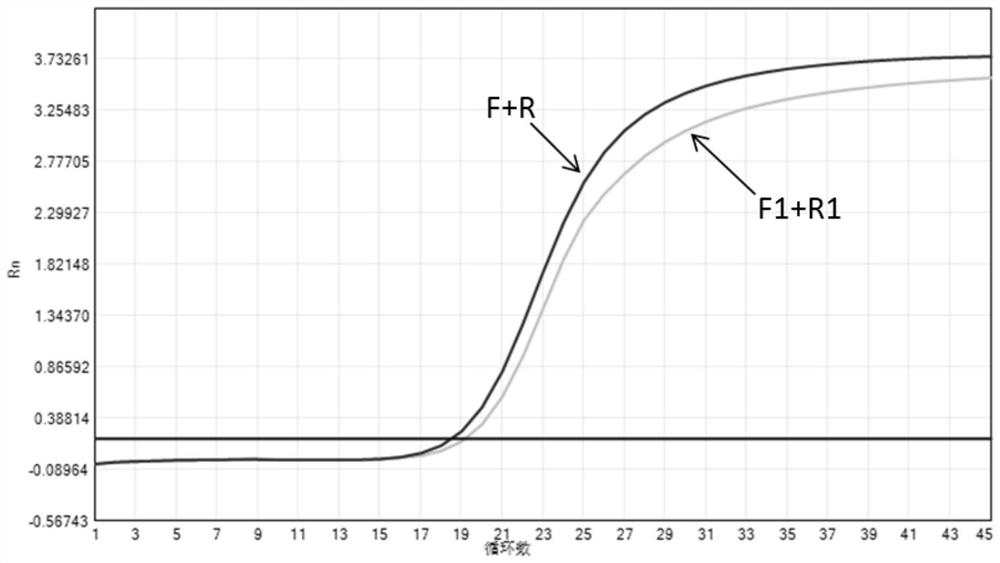
并加入对应的阳性病毒核酸,进行扩增,PCR反应条件为:(1)50℃逆转录10min;(2)95℃预变性3min;(3)95℃变性5s;(4)60℃退火/延伸20s,采集荧光。其中(3)-(4)共进行40个循环。荧光定量扩增结果如图1和图2所示。本实验例中,CCV荧光报告基团为FAM,淬灭基团为BHQ1;CPV荧光报告基团为HEX,淬灭基团为BHQ1。
对各引物或探针组合的扩增结果进行筛选,优选的引物组应满足Ct值较小且荧光值更高。按照图1和图2的对比结果,选出每种病原体检测结果中最佳的一对引物,即实施例1提供的核酸组合物其Ct值较小且荧光值更高。
为确认各引物或探针的特异性,将PCR的扩增产物进行测序,测序委托西安擎科生物科技有限公司进行。测序结果在NCBI中进行BLAST对比,对比结果显示扩增产物确实为CCV(图8)或CPV(图9)的片段,符合预期。
实验例2
本实验例对实施例2提供的检测试剂盒进行特异性、灵敏度以及重复性实验。
具体地,首先对引物探针的反应浓度进行筛选测试,筛选范围在0.1-1μM范围内。按照各引物探针的不同浓度配制相应的PCR反应液,对实验例1中已确认为阳性的各病毒核酸临床样本进行扩增。通过扩增结果筛选出引物探针反应浓度,最终确定的各病原体引物探针反应浓度如下表所示:
试剂盒采用25μL的反应体系,包括12.5μL的PCR反应液(包括逆转录酶、Taq DNA聚合酶、dNTP、MgCl
犬冠状病毒的引物探针组:0.15μL的CCV-F/CCV-F1,0.2μL的CCV-R/CCV-R1,0.2μL的CCV-P/CCV-P1;
犬细小病毒的引物探针组:0.15μL的CPV-F/CPV-F1,0.15μL的CPV-R/CPV-R1,0.2μL的CPV-P/CPV-P1,6.45μL的DEPC处理水、5μL的模板。其中PCR反应液购自珠海宝锐生物。
PCR反应条件为:(1)50℃逆转录5-30min;(2)95℃预变性2-5min;(3)95℃变性5-15s;(4)60℃退火/延伸20-40s,采集荧光。其中(3)-(4)共进行40个循环。发明人对反应条件进行优选,在不影响性能的条件下尽量缩减时间,最终确定的反应条件为:50℃10min,95℃3min,95℃5s,60℃20s,共40个循环,其中60℃设置采集荧光信号。
试剂盒特异性测试:
按照上述犬消化道病毒核酸检测试剂盒的组分及比例进行配制,然后分别加入目标病毒和其它干扰病原体进行测试,包括犬冠状病毒、犬细小病毒、犬瘟热病毒、犬腺病毒2型、犬副流感病毒。其它干扰病原体来自西农宠物医院。按照优化后的PCR反应条件进行扩增反应。
图3为CCV检测通道扩增图,图3中有扩增曲线的为CCV病毒,其余病原体均未扩增;图4为CPV检测通道扩增图,其中有扩增曲线的病原体为CPV病毒,其余病原均未扩增。
试剂盒重复性测试:
本实验对CCV及CPV临床样本进行扩增,每种样本重复扩增10次,得出下表2数据,结果显示,上述试剂盒检测CCV和CPV的变异系数(CV,%)均小于2%。
表2重复性测试数据。
试剂盒灵敏度测试:
将各病原体的质粒分别稀释至5×10
图5是CCV在最低检测限(5×10
采集的荧光信号结果生成荧光曲线,曲线明显呈S型且Ct值≤36即可判定对应荧光检测通道的病原体为阳性。
本发明提供的试剂盒的优点在于:可一次性检测关于犬消化道感染的两种病毒,特异性好,灵敏度高,检测时间短,且检测过程无需开盖,无污染。有利于快速准确地检测临床犬消化道疾病。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
SEQUENCE LISTING
<110> 上海基灵生物科技有限公司
<120> 一种检测犬冠状病毒和犬细小病毒的核酸组合物、试剂盒及应用
<160> 6
<170> PatentIn version 3.5
<210> 1
<211> 18
<212> DNA
<213> 人工序列
<400> 1
aattctcgtg gtcggatc 18
<210> 2
<211> 19
<212> DNA
<213> 人工序列
<400> 2
atctgctggt ccttgtttg 19
<210> 3
<211> 24
<212> DNA
<213> 人工序列
<400> 3
ttcattcttc aaccccatta ccga 24
<210> 4
<211> 20
<212> DNA
<213> 人工序列
<400> 4
ctattgaaat tctgtgcctc 20
<210> 5
<211> 20
<212> DNA
<213> 人工序列
<400> 5
aaatggtggt aagcccaaac 20
<210> 6
<211> 22
<212> DNA
<213> 人工序列
<400> 6
caggtgatga atttgctaca cc 22
- 一种检测犬冠状病毒和犬细小病毒的核酸组合物、试剂盒及应用
- 一种检测α-地中海贫血的核酸组合物、其基因芯片、其试剂盒及其应用
