一种图像激发超微注射方法、系统及设备
文献发布时间:2023-06-19 18:37:28
技术领域
本发明涉及超微注射技术领域,尤其涉及一种图像激发超微注射方法、系统及设备。
背景技术
在基于液滴的微流控系统中,向液滴添加试剂是一项重要的技术。Pico-injection超微注射是一种强大而实用的微流控技术,可以高通量完成两项微流体的融合。但现阶段应用这项技术时通常是不区分液滴内容物、对所有经过的液滴都进行注射的,这使得它在面对具有不同内容物的液滴时,仍有改良空间。
现有的微流控系统在单细胞测序分析应用中,由于现有的单细胞测序技术需要保证单测序微珠和单个细胞的配对,所以细胞浓度都会设置成很低来避免出现液滴包裹多个细胞的情况,这样也导致生成的液滴绝大多数的液滴是空包,只有小部分液滴是单包,生成单包液滴效率低;并且在单细胞测序分析中还需要对液滴进行分选、对细胞染色,一定程度上对细胞存在伤害。
发明内容
本发明的目的是提供一种图像激发超微注射方法、系统及设备,旨在解决现有微流控系统在单细胞测序分析应用中仍存在改进空间的问题。
第一方面,本发明实施例提供一种图像激发超微注射方法,包括:
通过制备生成液滴,其中液滴包括没有包裹细胞的空包液滴、包裹单个细胞的单包液滴以及包裹多个细胞的多包液滴;
将所述液滴注入微流控芯片并使所述液滴在所述微流控芯片的通道中逐个通过;
对逐个经过图像捕获区域的所述液滴进行图像识别处理,输出当前所述液滴为目标液滴的置信度;
当当前所述液滴为目标液滴时触发激发注射操作,并在所述目标液滴经过注射区域时向所述目标液滴注射反应试剂。
第二方面,本发明实施例提供一种图像激发超微注射系统,包括:
制备单元,用于通过制备生成液滴,其中液滴包括没有包裹细胞的空包液滴、包裹单个细胞的单包液滴以及包裹多个细胞的多包液滴;
注入单元,用于将所述液滴注入微流控芯片并使所述液滴在所述微流控芯片的通道中逐个通过;
图像识别单元,用于对逐个经过图像捕获区域的所述液滴进行图像识别处理,输出当前所述液滴为目标液滴的置信度;
注射单元,用于当当前所述液滴为目标液滴时触发激发注射操作,并在所述目标液滴经过注射区域时向所述目标液滴注射反应试剂。
第三方面,本发明实施例提供了一种图像激发超微注射设备,包括:第一注射泵、第二注射泵、第三注射泵、液滴生成芯片和微流控芯片;所述图像激发超微注射设备还包括如权利要求8所述的图像激发超微注射系统;
所述液滴生成芯片用于制备液滴;所述第一注射泵用于将液滴注入所述微流控芯片;所述第二注射泵用于将间隔液注入所述微流控芯片;所述第三注射泵用于将反应试剂注入目标液滴。
本发明实施例公开了一种图像激发超微注射方法、系统及设备。该方法包括:通过制备生成液滴,其中液滴包括没有包裹细胞的空包液滴、包裹单个细胞的单包液滴以及包裹多个细胞的多包液滴;将液滴注入微流控芯片并使液滴在微流控芯片的通道中逐个通过;对逐个经过图像捕获区域的液滴进行图像识别处理,输出当前液滴为目标液滴的置信度;当当前液滴为目标液滴时触发激发注射操作,并在目标液滴经过注射区域时向目标液滴注射反应试剂。本发明实施例将图像处理与超微注射集成,不需要对液滴进行物理标记,避免了实验过程中液滴内容物、细胞污染的风险;通过图像激发的超微注射系统,只有目标液滴经过时才会被注入反应试剂,减少了反应试剂的使用量。
附图说明
为了更清楚地说明本发明实施例技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为本发明实施例提供的目标液滴时触发激发注射方法的流程示意图;
图2为本发明实施例提供的目标液滴时触发激发注射方法的子流程示意图;
图3为本发明实施例提供的目标液滴时触发激发注射方法的又一子流程示意图;
图4为本发明实施例提供的目标液滴时触发激发注射方法的又一子流程示意图;
图5为本发明实施例提供的目标液滴时触发激发注射方法的又一子流程示意图;
图6为本发明实施例提供的目标液滴时触发激发注射系统的示意性框图;
图7为本发明实施例提供的图像识别处理的示意性框图;
图8为本发明实施例提供的置信度的结果示意图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
应当理解,当在本说明书和所附权利要求书中使用时,术语“包括”和“包含”指示所描述特征、整体、步骤、操作、元素和/或组件的存在,但并不排除一个或多个其它特征、整体、步骤、操作、元素、组件和/或其集合的存在或添加。
还应当理解,在此本发明说明书中所使用的术语仅仅是出于描述特定实施例的目的而并不意在限制本发明。如在本发明说明书和所附权利要求书中所使用的那样,除非上下文清楚地指明其它情况,否则单数形式的“一”、“一个”及“该”意在包括复数形式。
还应当进一步理解,在本发明说明书和所附权利要求书中使用的术语“和/或”是指相关联列出的项中的一个或多个的任何组合以及所有可能组合,并且包括这些组合。
请参阅图1,图1为本发明实施例提供的图像激发超微注射方法的流程示意图;
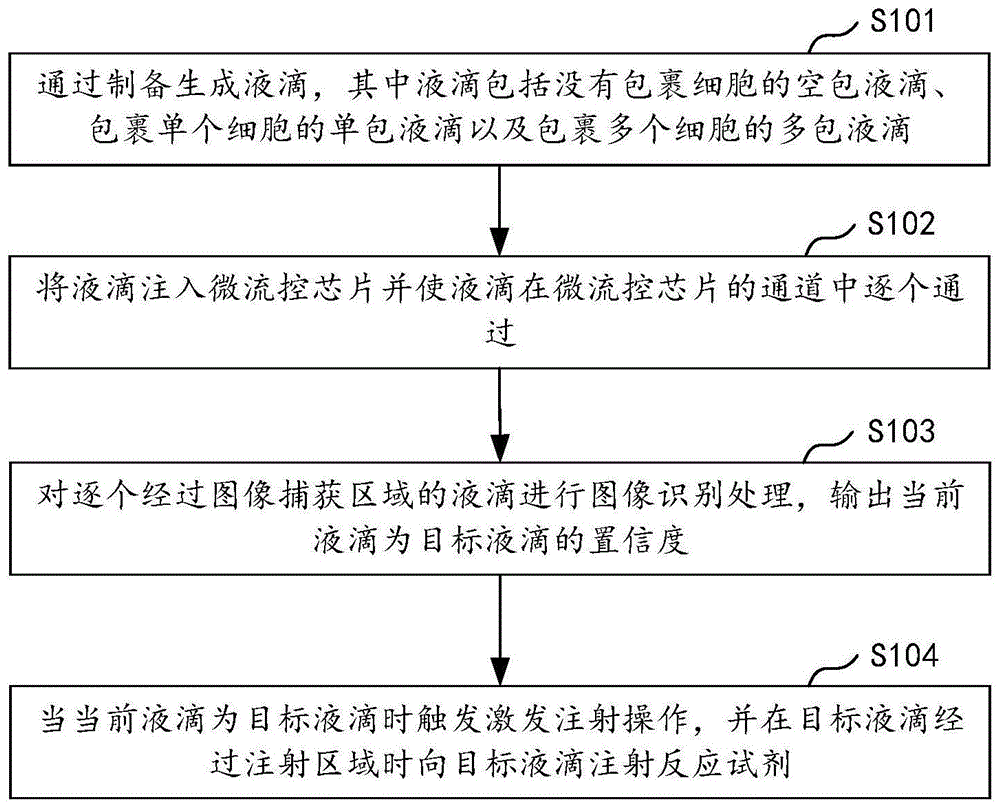
如图1所示,该方法包括步骤S101~S104。
S101、通过制备生成液滴,其中液滴包括没有包裹细胞的空包液滴、包裹单个细胞的单包液滴以及包裹多个细胞的多包液滴;
其中,将预设浓度的细胞重悬于细胞培养液中,将细胞培养液与氟化油注入液滴生成芯片中进行流聚焦后生成液滴。
S102、将液滴注入微流控芯片并使液滴在微流控芯片的通道中逐个通过;
其中,将液滴注入微流控芯片中,微流控芯片中狭窄的通道会让液滴逐一通过。
S103、对逐个经过图像捕获区域的液滴进行图像识别处理,输出当前液滴为目标液滴的置信度;
其中,由PC端对液滴的图像进行识别处理并给出当前液滴为目标液滴的置信度,并当置信度超过设定阈值是可判定当前液滴为目标液滴。
S104、当当前液滴为目标液滴时触发激发注射操作,并在目标液滴经过注射区域时向目标液滴注射反应试剂。
其中,通过识别出目标液滴后,可以仅对目标液滴注射反应试剂,减少了反应试剂使用量。
本实施例可以应用于特定数量细胞测序分析中,将包裹特定数量细胞的液滴作为目标液滴,通过在图像捕获区域逐个获取经过的液滴的图像,通过图像识别处理计算每一液滴的液滴类型,并在识别到存在特定数量细胞的液滴时激发注射系统,以实现对特定数量的液滴进行注入反应试剂,以便于后续进行特定数量细胞的培养。
本实施例主要应用于单细胞测序分析中,本方案中可以设置较高的细胞浓度来提高液滴包裹单细胞的概率,减少了获取足够数量单细胞液滴所需的时间;将包裹单个细胞的液滴作为目标液滴,通过图像识别处理的方式不需要对液滴进行物理标记即可筛选出单包液滴,避免了实验过程中液滴内容物、细胞污染的风险;并通过图像激发注射的方式只对经过的单包液滴注入反应试剂,减少了反应试剂的用量。
在一实施例中,如图2所示,步骤S102包括:
S201、将液滴注入微流控芯片中;
S202、将间隔油注入微流控芯片中并与液滴交汇,通过间隔油使液滴在微流控芯片的通道中逐个间隔通过。
本实施例中,通过第一注射泵将液滴从液滴入口注入微流控芯片中,液滴在微流控芯片的通道中从液滴入口向收集口移动,在移动的过程中通过第二注射泵从其他入口注入间隔油,间隔油进入微流控芯片的通道中后与液滴交汇,间隔油可以增加液滴与液滴间隔,可以提高液滴的识别和超微注射的准确性。
在一实施例中,如图3所示,步骤S103包括:
S301、获取逐个经过图像捕获区域的当前液滴的图像;
S302、对图像进行二值化处理得到二值化图像;
S303、对二值化图像中的液滴位置进行填充并计算填充位置中的连通域的面积;
S304、将单个面积大于或等于预设面积的连通域判定液滴的视野滴,将面积小于预设面积的连通域判定为噪声。
本实施例为液滴识别的过程,该过程通过图像识别处理判断图像中的液滴。具体的:首先,通过在显微镜上设置高速相机以对经过微流控芯片中的图像捕获区域的液滴进行摄像并获取图像;然后,对图像进行背景减法操作以示出运动目标(即待识别的液滴)的位置和形状;然后,对图像进行二值化处理得到二值化图像,二值化图像中可以更清晰的展示出运动目标的位置和形状;最后,对二值化图像中的液滴位置进行填充和关闭,即可计算出液滴位置中的连通域,并将面积大于或等于预设面积(优选为200个像素面积)的连通域视为视野滴,其余小于预设面积的连通域认为是噪声。
在一实施例中,如图4所示,步骤S103还包括:
S401、对当前液滴的二值化图像进行边缘提取,得到轮廓图;
S402、计算轮廓图内的连通域的面积;
S403、将面积处在预设像素点范围内的连通域判定为细胞;
S404、多次对比轮廓图内的细胞数量和目标液滴中设定的细胞数量,输出当前液滴为目标液滴的置信度。
本实施例为目标液滴的识别过程,该过程通过图像识别处理判断液滴是否为需要的目标液滴;具体的:对液滴的二值化图像进行边缘提取后得到轮廓图,轮廓图可以方便连通域的识别,在轮廓图内,不同数量的细胞会形成不同数量的连通域;比如空包液滴的轮廓图内因为不存在细胞,因此只存在一整个空包液滴为作为一个连通域;比如单包液滴因为存在一个细胞,因此会存在对应一个细胞位置的一个连通域和对应单包液滴中非细胞位置的其他连通域;比如多包液滴的轮廓图内因为存在多个细胞,因此会存在一一对应多个细胞位置的多个连通域和对应多包液滴中非细胞位置的其他连通域;基于此,本实施例根据细胞的实际大小设定一个预设像素点范围(优选为大于5个像素点小于50个像素点的面积范围),将处在预设像素点范围内的连通域判定为细胞;如此,通过计算轮廓图内的所有连通域的大小,并一一与预设像素点范围进行对比即可知晓轮廓图内的细胞数量,从而识别出该液滴是否为目标液滴。
本实施例以单细胞液滴为目标液滴为例进行介绍,即通过图像识别处理得到液滴的轮廓图内仅有一个连通域的面积处在预设像素点范围内时,判断该液滴为目标液滴。而在判断的过程中,因为细胞会在液滴内运动,存在多个细胞时可能因为细胞在三维空间中的重叠导致在二维图像上细胞数量的误判,因此本实施例引入置信度,每一液滴在经过微流控芯片时,经过多次的图像识别处理后,最后将判定为目标液滴的次数与总识别次数的比值作为该液滴为目标液滴的置信度,置信度超过预设阈值时判定为目标液滴。
为方便理解,本实施例以如图7所示的单包液滴a、双胞液滴b和空包液滴c的识别为例,单包液滴a作为目标液滴;单包液滴a、双胞液滴b和空包液滴c的图像依次进行二值化处理、边缘提取和图像转化,最终得到单包液滴a、双胞液滴b和空包液滴c的轮廓图,并分别对单包液滴a、双胞液滴b和空包液滴c的轮廓图分别进行多次识别处理,并按上述置信度的计算方式进行计算后分别输出单包液滴a的置信度为100%,双胞液滴b的置信度为6.25%(即存在两个细胞在三维空间中视野重叠的情况),空包液滴c的置信度为0%(参考图8)。可以理解的,本实施例的预设阈值可根据实验数据进行设定,本实施例不做具体限定。
在一实施例中,如图5所示,步骤S104还包括:
S501、当当前液滴为目标液滴时生成注射信号;
S502、根据注射信号产生上升沿;
S503、根据上升沿产生正弦波信号;
S504、将正弦波信号进行信号放大后输入微流控芯片的电极;
S505、通过微流控芯片的电极对从注射区域经过的目标液滴进行介电泳作用,同时向注射区域内的目标液滴中注入反应试剂。
本实施例为激发注射信号并完成反应试剂注入的目标液滴的过程。
本实施例由PC端对液滴的图像实时进行图像识别处理并确认出目标液滴,当PC端识别到目标液滴时通过串口对单片机发送注射信号,当单片机收到由PC端传输的注射信号后立刻触发第三注射泵开启并产生一个上升沿,通过上升沿触发信号发生器以一定的频率和幅度产生正弦波信号,正弦波信号经高压放大器放大后输入到微流控芯片的电极,微流控芯片的电极对注射区域形成介电泳的作用,当前经过注射区域的目标液滴的油水界面变得不稳定,此时第三注射泵朝向目标液滴注射的反应试剂可以进入目标液滴中,从而完成注射,被注射的目标液滴在远离电极后油水界面重新达到稳定的状态,因此最后在收集口收集的液滴即使堆积在一起也不会发生液滴融合的情况。
可以理解的,在完成对目标液滴的注射后,在微流控芯片的收集口用离心管收集液滴,若将包裹了一个细胞的单细胞液滴作为目标液滴,取少量液滴通过显微镜观察可看到:只有单细胞液滴会被注入反应试剂,空包和多包液滴都不会被注入反应试剂。
可以理解的,在一些其他应用场景中,本发明采用的图像识别处理还可以对非均一大小的液滴进行识别,以获取不同大小的液滴面积,并通过设定多个面积阈值,可以划分出如小液滴、中液滴和大液滴等液滴类型,具体划分数量可以根据实际情况进行设定,本实施例不做具体限定。对应的,针对不同液滴类型,本实施例还设定了第三注射泵的不同注射指令,不同注射指令下可注射出不同量的反应试剂,以对应不同大小的液滴类型,如此,可以根据识别到的液滴类型触发不同的注射指令,从而实现往不同大小的液滴中添加不同比例的反应试剂。
可以理解的,在一些其他应用场景中,如在对于特定数量细胞的培养的应用中,可以采用本发明技术先对特定数量细胞的液滴进行筛选,而后向特定数量细胞的液滴中注射水凝胶,固化后重新收集以实现特定数量细胞的培养。
需补充的是,为适用于不同的应用场景中,本方案采用的算法可根据实际情况进行适应性调整,如图像计算过程中设涉及的阈值大小、注射过程中涉及的压力大小、试剂用量大小等等均为在本方案的适用范围内。
本发明实施例还提供一种图像激发超微注射系统,该图像激发超微注射系统用于执行前述图像激发超微注射方法的任一实施例。具体地,请参阅图6,图6是本发明实施例提供的图像激发超微注射系统的示意性框图。
如图6所示,图像激发超微注射系统600,包括:制备单元601、注入单元602、图像识别单元603以及注射单元604。
制备单元601,用于通过制备生成液滴,其中液滴包括没有包裹细胞的空包液滴、包裹单个细胞的单包液滴以及包裹多个细胞的多包液滴;
注入单元602,用于将液滴注入微流控芯片并使液滴在微流控芯片的通道中逐个通过;
图像识别单元603,用于对逐个经过图像捕获区域的液滴进行图像识别处理,输出当前液滴为目标液滴的置信度;
注射单元604,用于当当前液滴为目标液滴时触发激发注射操作,并在目标液滴经过注射区域时向目标液滴注射反应试剂。
该系统可以应用于特定数量细胞测序分析中,将包裹特定数量细胞的液滴作为目标液滴,通过在图像捕获区域逐个获取经过的液滴的图像,通过图像识别处理计算每一液滴的液滴类型,并在识别到存在特定数量细胞的液滴时激发注射系统,以实现对特定数量的液滴进行注入反应试剂,以便于后续进行特定数量细胞的培养。
本发明实施例还提供一种图像激发超微注射设备,其特征在于,包括:第一注射泵、第二注射泵、第三注射泵、液滴生成芯片和微流控芯片;图像激发超微注射设备还包括如上所述的图像激发超微注射系统;
液滴生成芯片用于制备液滴;第一注射泵用于将液滴注入微流控芯片;第二注射泵用于将间隔液注入微流控芯片;第三注射泵用于将反应试剂注入目标液滴。
在一实施例中,图像激发超微注射设备还包括PC端、单片机、信号发生器和高压放大器;PC端用于发送注射信号至单片机;单片机用于根据注射信号触发第三注射泵开启并产生上升沿,并将上升沿发送至信号发生器;信号发生器用于根据上升沿产生正弦波信号并经高压放大器放大后输入微流控芯片的电极;微流控芯片的电极用于对注射区域处的目标液滴进行介电泳作用,同时经由第三注射泵在注射区域处注射反应试剂至目标液滴中。
所属领域的技术人员可以清楚地了解到,为了描述的方便和简洁,上述描述的系统和设备的具体工作过程,可以参考前述方法实施例中的对应过程,在此不再赘述。
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到各种等效的修改或替换,这些修改或替换都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以权利要求的保护范围为准。
- 一种拍摄方法、图像的显示方法、系统及设备
- 一种基于四维陈氏超混沌系统与K-means聚类的图像加密方法
- 一种图像获取方法及装置、自主定位导航系统、计算设备
- 一种基于深度学习的图像分割方法、系统及电子设备
- 一种文本图像超分辨率方法和系统、电子设备、存储介质
- 一种图像超分方法、系统及存储介质和终端设备
