一种基于炎症反应分型的过敏原筛查试剂盒及其应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于生物技术领域,具体涉及一种基于炎症反应分型的过敏原筛查试剂盒及其应用。
背景技术
过敏性疾病诊断最主要是筛查出患者对哪种过敏原过敏,目前过敏原体外筛查方法包括血清学和细胞学检测。临床上常用的过敏原筛查试剂盒以检测血清中的总IgE(tIgE)和过敏原特异性IgE(sIgE)为诊断指标,过敏原特异性sIgE检测在过敏性疾病的体外诊断中起着关键作用。sIgE水平越高,其与过敏性疾病的相关性就越强。单独监测tIgE水平不能用于诊断过敏性疾病,需要与sIgE水平联合分析。细胞学检测最常见的应用是嗜碱性粒细胞激发试验(BAT)。监测嗜碱性粒细胞脱颗粒有两种方法:一种是通过流式细胞术检测嗜碱性粒细胞膜标记物如CD63/CD203c的表达,另一种是基于酶联免疫吸附法测定组胺等炎症介质。这两种方法的检测原理是:特异性过敏原通过上调嗜碱性粒细胞的激活标志物的表达或释放组胺等介质使患者发生过敏反应。
基于血清学检测的过敏原筛查试剂盒通常以sIgE的浓度分级作为诊断依据,但sIgE结果的分级并不一定与疾病的严重程度相关。sIgE阳性并不总是与临床症状相一致,有明显过敏临床症状的也不一定能够检测到sIgE阳性,特别是食物过敏、小分子物质过敏等。因为过敏原还存在有非IgE依赖的途径引起炎症介质的释放使患者发生过敏反应。因此,血清sIgE的诊断有效性较低,难以与临床表现相一致。
目前细胞学检测应用的是嗜碱性粒细胞活化试验(BAT),通过流式细胞术检测嗜碱性粒细胞膜活化标记物如CD63/CD203c的表达,但嗜碱性粒细胞极其罕见,约占血液中白细胞总数的0.2%。因此,通过流式细胞术检测嗜碱性粒细胞表面活化标志物的难度非常大。另外,也有检测全血中嗜碱性粒细胞释放组胺水平来衡量发生过敏反应的严重程度,但是组胺是一种含氮的有机化合物,稳定性差且检测方法复杂。
发明内容
针对现有技术存在的问题,本发明目的在于提供一种基于炎症反应分型的过敏原筛查试剂盒及其应用。本发明过敏原筛查试剂盒通过体外测试即可真实地反映患者接触过敏原后发生的炎症反应,达到与体内试验相当的检测效果。
基于上述目的,本发明采用的技术方案如下:
第一方面,本发明提供一种基于炎症反应分型的过敏原筛查试剂盒,所述试剂盒包括过敏原刺激物、细胞因子标准品、细胞因子的包被抗体和细胞因子的检测抗体;所述过敏原刺激物包括过敏原提取物和/或过敏原组分蛋白。
本发明试剂盒的检测原理如下:
过敏原刺激物刺激待检血细胞后,由抗原递呈细胞摄取、加工形成抗原肽与MHCII类分子的复合物。若机体在致敏的状态下,该复合物能够与表达有过敏原特异性T细胞抗原受体(TCR)的T细胞结合,从而使T细胞活化。取决于过敏原的性质和局部环境中的激素和细胞因子的不同,活化的T细胞通常可分化成Th2细胞和/或Th17细胞并对应分泌不同类型的细胞因子,如Th2细胞主要分泌IL-4、IL-5和IL-13,Th17细胞主要分泌IL17。这些炎症性细胞因子具有多种功能参与了过敏反应的发生。本发明的试剂盒通过检测不同类型的细胞因子可以分析出受过敏原刺激后患者发生的炎症类型。本发明试剂盒通过体外测试即可真实地反映患者接触过敏原后发生的炎症反应,达到与体内试验相当的检测效果。
优选地,过敏原包括屋尘螨、粉尘螨、疥螨、蟑螂、蜜蜂、猫、马、蛔虫、桦树、柳杉、杉木、梯牧草、欧蓍草、黑麦草、女贞、大麦、苹果、花生、蟹、虾、扁豆、鲭鱼、牡蛎和糠秕马拉色菌。
优选地,所述细胞因子包括IL-4、IL-5、IL-13和IL-17A。
优选地,所述试剂盒中过敏原刺激物的终浓度为5~100μg/ml。
优选地,所述试剂盒还包括PBS缓冲液、清洗液、非特异性封闭液、链霉亲和素偶联辣根过氧化物酶溶液、底物溶液和终止液。
优选地,所述清洗液为含0.05%吐温20的PBS缓冲液;所述非特异性封闭液为含3%BSA的清洗液;所述底物溶液为3,3,5,5-四甲基联苯胺溶液;所述终止液为2M的硫酸溶液。
优选地,所述试剂盒的检测对象为血液样本。
第二方面,本发明提供上述基于炎症反应分型的过敏原筛查试剂盒的使用方法,包括如下步骤:
(1)将过敏原刺激物加入细胞培养板,每孔加入待测血液样本混匀,经孵育、离心,吸取细胞培养上清液;
(2)将步骤(1)所得细胞培养上清液、细胞因子标准品加入含有待检细胞因子的包被抗体的孔板中,经孵育、清洗液清洗后,向孔板中加入细胞因子的检测抗体,孵育、清洗;
(3)接着向孔板中加入链霉亲和素偶联辣根过氧化物酶溶液,经孵育、清洗后,再加入底物溶液,经孵育后,加入终止液,终止反应;
(4)将孔板置于酶标仪上读取450nm、570nm处的OD值,依据标准曲线计算细胞因子的浓度,基于细胞因子的浓度对过敏等级以及炎症反应分型进行判定。
第三方面,本发明提供上述基于炎症反应分型的过敏原筛查试剂盒在过敏原筛查中的应用,基于试剂盒检测到的待检样本的细胞因子的浓度对是否过敏及过敏等级进行判定;
判定标准如下:细胞因子浓度<8pg/mL,则判定为阴性,指示待检样本对所检过敏原不过敏;细胞因子浓度≥8pg/mL,则判定为阳性,指示待检样本对所检过敏原过敏;
过敏等级如下:
1级:8pg/mL~12pg/mL;
2级:13pg/mL~17pg/mL;
3级:18pg/mL~22pg/mL;
4级:23pg/mL~32pg/mL;
5级:33pg/mL~52pg/mL;
6级:≥53pg/mL;
第四方面,本发明提供上述基于炎症反应分型的过敏原筛查试剂盒在过敏原引起的炎症反应分型中的应用,基于试剂盒检测到的待检样本的细胞因子的类型及浓度对炎症反应分型进行判定,判定标准如下:
细胞因子中IL-4、IL-5、IL-13中任一项的浓度大于等于8pg/mL,则炎症反应分型为Th2型;细胞因子中IL-17A的浓度大于等于8pg/mL,则炎症反应分型为Th17型。
与现有技术相比,本发明的有益效果如下:
本发明通过检测新的生物标记物,能够真实反映患者接触过敏原后发生的炎症反应,包含了IgE依赖和非IgE依赖途径导致的炎症反应,远优于过去单纯的血清IgE检测,可达到皮肤点刺试验(SPT)、食物激发试验等体内试验相当的效果,同时又避免了体内试验时发生严重过敏反应的风险。不仅如此,本方法还能诊断出接触过敏原后患者发生的炎症反应类型(Th2型还是Th17型),能够指导临床用药,特别指导用激素是否有效,是否要采用其他生物制剂,是医学理论与实践的双重创新。
附图说明
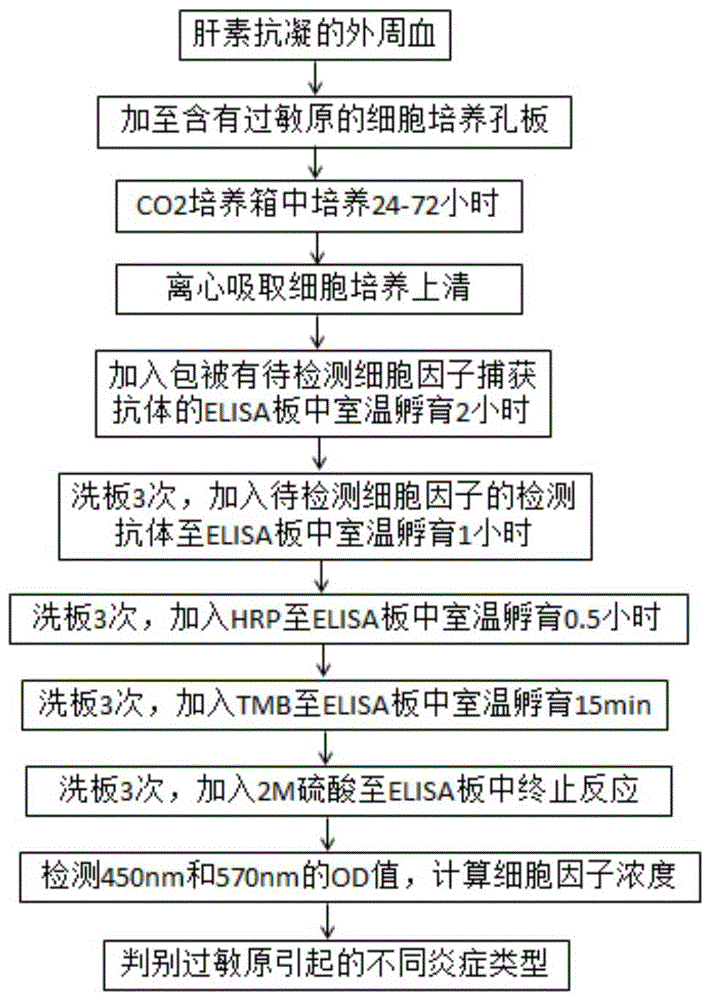
图1为本发明试剂盒的使用方法流程图。
具体实施方式
为更好地说明本发明的目的、技术方案和优点,下面将结合具体实施例对本发明作进一步说明。本领域技术人员应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
实施例中所用的试验方法如无特殊说明,均为常规方法;所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1
本实施例提供本发明试剂盒的组成以及使用方法和判定标准,具体如下:
一、试剂盒的组成
本发明试剂盒包括:过敏原刺激物、炎症性细胞因子的标准品、细胞因子的包被抗体和细胞因子的检测抗体、PBS缓冲液、清洗液、非特异性封闭液、HRP溶液、TMB底物、终止液。
其中,过敏原的物种来源有:屋尘螨、粉尘螨、疥螨、蟑螂、蜜蜂、猫、马、蛔虫、桦树、柳杉、杉木、梯牧草、欧蓍草、黑麦草、女贞、大麦、苹果、花生、蟹、虾、扁豆、鲭鱼、牡蛎、糠秕马拉色菌,该刺激物组合包含这些物种来源的过敏原提取物和/或过敏原组分蛋白。过敏原刺激物于试剂盒中的终浓度为5~100μg/mL。
炎症性细胞因子包括:IL-4、IL-5、IL-13、IL-17A,试剂盒可检测的炎症性细胞因子的浓度范围是0-500pg/mL。
PBS缓冲液为pH7.4的磷酸盐缓冲液,其组成如下:NaCl 8.0g、KH
清洗液为含0.05%吐温20的PBS缓冲液。
非特异性封闭液为含3%BSA溶液的清洗液。
HRP溶液为链霉亲和素偶联辣根过氧化酶溶液。
TMB底物为3,3,5,5-四甲基联苯胺溶液。
终止液为2M硫酸溶液。
二、试剂盒的使用方法
本发明试剂盒的使用方法如图1所示,包括如下步骤:
1、检测样品为肝素抗凝管保存的外周血;
2、将过敏原刺激物(不同的过敏原提取物或过敏原组分蛋白在反应体系中的终浓度在5~100μg/mL之间,过敏原刺激物溶液体积为总反应体积的10%)加入细胞培养板中,以等体积的PBS作为阴性对照,然后在每孔加入一定体积(总反应体积的90%)的全血,混匀。37℃,5%CO
3、4℃2500rpm离心5min,吸取细胞培养上清液;
4、按照ELISA操作流程进行细胞因子浓度的检测,步骤如下:
1)在96孔ELISA板中加入待检测细胞因子的包被抗体,4℃孵育过夜,用清洗液洗板3次,加入非特异性封闭液,室温孵育1小时,用清洗液洗板1次,晾干4℃保存,此板为含有待检测细胞因子包被抗体的96孔板;
2)将50~100μL细胞培养上清液、细胞因子标准品(浓度范围在0~500pg/mL之间)加入步骤1)的96孔板中,室温孵育2小时;
3)用清洗液洗板3次,加入细胞因子检测抗体到孔板中,室温孵育1小时;
4)用清洗液洗板3次,加入HRP溶液到孔板中,室温孵育0.5小时;
5)用清洗液洗板5次,加入TMB底物到孔板中,室温孵育15~30min;。
6)加入终止液终止反应;
7)在酶标仪上读取450nm及570nm的OD值;
8)计算OD 450nm减去OD 570nm的数值,根据标准曲线的数值计算细胞因子的浓度进行结果判断。
5、结果判定标准:以过敏原刺激全血后上清液(检测孔)细胞因子浓度减去PBS刺激全血后上清液(阴性对照孔)细胞因子浓度的数值作为判定值,即以检测孔与阴性对照孔的细胞因子浓度的差值作为判定值,当判定值≥8pg/mL时,判定为阳性,即患者对该过敏原过敏。
A.根据判定值进行的分级标准如下:
0级:<8pg/mL,即判定为阴性,表示待测对象对该过敏原不过敏;
则依据过敏程度进行分级:
1级:8pg/mL~12pg/mL
2级:13pg/mL~17pg/mL
3级:18pg/mL~22pg/mL
4级:23pg/mL~32pg/mL
5级:33pg/mL~52pg/mL
6级:≥53pg/mL。
B.炎症分型的标准:
Th2型:IL-4、IL-5、IL-13中任一个炎症性细胞因子的检测浓度≥8pg/mL;
Th17型:IL-17A的检测浓度≥8pg/mL。
实施例2
本实施例以粉尘螨作为过敏原,利用实施例1所述试剂盒进行粉尘螨过敏原的筛查及炎症反应分型,具体方法如下:
1、将3种尘螨过敏原刺激物20μL分别加入到96孔细胞培养板中,同时加入20μLPBS缓冲液作为阴性对照。该刺激物包括:粉尘螨提取物HDM、粉尘螨过敏原组分蛋白Der f1和Der f 2,蛋白浓度均为200μg/mL。
2、加入肝素抗凝血至上述细胞培养板,180μL/孔,混匀。37℃,5%CO
3、将细胞培养板离心,4℃2500rpm,5min,吸取细胞培养上清液。
4、按照ELISA操作流程分别进行IL13、IL17A细胞因子浓度的检测。
1)将细胞培养上清液、IL13和IL17A细胞因子标准品(浓度依次为0pg/mL、7.8125pg/mL、15.625pg/mL、31.25pg/mL、62.5pg/mL、125pg/mL、250pg/mL、500pg/mL)分别加入到已包被有IL13、IL17A抗体的96孔板中,50μL/孔,室温孵育2小时。
2)用清洗液洗板3次,分别加入50μL的IL13、IL17A检测抗体(1:250)到孔板中,室温孵育1小时。
3)用清洗液洗板3次,加入HRP溶液(1:100)到孔板中,50μL/孔,室温孵育0.5小时。
4)用清洗液洗板5次,加入TMB底物到孔板中,50μL/孔,室温避光孵育15min。
5)加入终止液25μL/孔。
6)在酶标仪上读取450nm及570nm的OD值,即OD
7)计算OD
8)细胞因子浓度的计算结果如表1所示。
表1
9)按照本试剂盒分级标准计算所得等级与现有常用过敏原筛查方法等级的比较
依据表1中各待检样本细胞因子的检测结果,参照实施例1中记载的过敏等级判定标准以及炎症反应分型标准,对表1中的结果进行等级分类及反应分型,表2中的数据即对应的过敏等级。
表2本发明试剂盒检测结果等级与sIgE、SPT检测结果等级的比较
结果分析:从表1的细胞因子浓度值根据本发明的分级标准可得到表2的等级,本发明的优势在于:
第一,Unicap公司的血清sIgE检测等级分为0-6级,皮肤点刺试验SPT的等级分为0-4级,本发明检测结果的等级分为0-6级,从待检样本1~4的结果比较可以看出,本发明的检测结果等级与sIgE、SPT的等级相当。
从待检样本1上看,本发明的检测等级更接近体内试验的SPT等级,说明本发明的检测结果比血清sIgE更能反映体内真实的炎症水平,同时本发明作为体外检测能够避免体内试验引起严重过敏反应的风险。
第二,本发明检测出的IL13和IL17A细胞因子浓度可以作为判断Th2和Th17炎症分型的依据,从待检样本1的结果可以看出该受试者在粉尘螨过敏原的刺激下,可以同时引起Th2和Th17型的炎症。
而待检样本2和待检样本3的受试者只引起Th2型的炎症。目前常用的过敏原筛查方法sIgE和SPT都无法区分炎症分型。
第三,本发明能够同时使用过敏原总提取物和过敏原组分蛋白进行检测,从待检样本1~3的检测结果可以看出受试者在对过敏原总提取物(HDM)过敏的基础上,具体对哪种过敏原组分蛋白(Der f 1还是Der f 2)过敏,并且能够显示不同的过敏原组分蛋白在不同受试者上引起的是Th2还是Th17型的炎症反应。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
