唾液素salivaricin在制备IL-21受体抑制剂中的应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于IL-21受体抑制剂技术领域,具体涉及唾液素salivaricin在制备IL-21受体抑制剂中的应用。
背景技术
唾液素(salivaricin)是一种细菌素,即细菌分泌的抗菌肽。唾液链球菌K12可分泌salivaricinA2和B,编码二者的基因位于一个190kp的大质粒上,经细菌核糖体合成后,通过翻译后修饰形成最终含有22-25个氨基酸的多肽结构。唾液素属于羊毛硫氨酸抗生素,具有抑菌作用,可通过结合病原菌的脂质体II而干扰细菌细胞壁的合成,抗菌谱较窄,可靶向杀死特定细菌,是解决抗生素滥用危机最理想和最有希望的工具。
salivaricin A2和B可抑制致病性链球菌的增值,如化脓链球菌(Streptococcuspyogenes),停乳链球菌(Streptococcus dysgalactiae),变形链球菌(Streptococcus mutans)等。除了抗菌作用,细菌素的免疫调节活性也逐渐受到关注。有研究显示乳链菌肽Nisin(经典细菌素之一)对人体外周血淋巴细胞具有调控作用,可抑制其分泌促炎因子。唾液链球菌K12也具有免疫调节活性,可通过阻断NF-κB信号通路而抑制炎性介质的表达,进而缓解支气管上皮、喉上皮以及肠上皮细胞的炎症反应。而且,研究者认为唾液链球菌K12发挥免疫调节作用很可能依赖于其分泌的细菌素salivaricinA2和B。然而,唾液素salivaricin是否具有免疫调节作用尚未见报道,值得深入研究。
此外,IL-21及其受体在自身免疫病的发病机制中发挥关键作用,靶向IL-21或其受体的小分子抑制剂(如TNFR2-IL21R融合蛋白)已被证明可有效治疗自身免疫病如类风湿关节炎。然而,目前现有的IL-21受体抑制剂虽然可有效抑制自身免疫反应,但也使得感染风险大大增加,因此需要开发新型的IL-21受体抑制剂。
发明内容
本发明的目的在于提供唾液素salivaricin在制备IL-21受体抑制剂中的应用,所述唾液素salivaricin可直接与IL-21受体(IL-21R)结合,并抑制细胞因子IL-21与其受体(IL-21R)的结合。
本发明提供了唾液素salivaricin在制备IL-21受体抑制剂中的应用。
优选的,所述唾液素salivaricin包括salivaricinA2和/或salivaricinB。
优选的,所述salivaricinA2的氨基酸序列如SEQ ID NO.1所示;
所述salivaricin B的氨基酸序列如SEQ ID NO.2所示。
本发明还提供了唾液素salivaricin在制备IL-21/IL-21R信号通路阻断剂中的应用。
本发明还提供了唾液素salivaricin在制备诱导IL-21受体构象发生改变的试剂中的应用。
有益效果:本发明提供了唾液素salivaricin在制备IL-21受体抑制剂中的应用,实施例中本发明运用体外实验体系,使用表面等离子体共振(Surface PlasmonResonance)技术发现唾液素salivaricin可直接与IL-21受体(IL-21R)结合,并抑制细胞因子IL-21与其受体(IL-21R)的结合。同时,还基于圆二色技术发现salivaricin可诱导IL-21受体构象发生改变。由于受体构象对其结合力有决定作用,IL-21受体构象改变可能抑制了IL-21与受体的结合。本发明还运用T细胞体外分化体系,发现唾液素salivaricin可通过阻断IL-21/IL-21R信号通路,抑制异常活化的效应性T细胞。本发明所述唾液素salivaricin可为IL-21受体抑制剂提供原料,还可以从上游途径调节免疫稳态,并应用于治疗免疫炎性疾病。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
图1为唾液素salivaricin的化学合成与纯化及鉴定结果图;
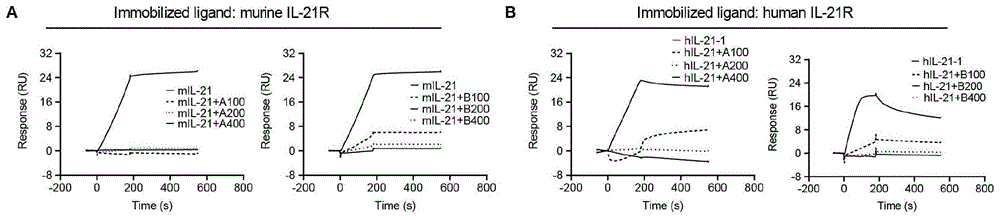
图2为唾液素salivaricin与IL-21受体直接结合的结果图;
图3为唾液素salivaricin阻断IL-21与受体的结合结果图;
图4为唾液素salivaricin诱导IL-21受体构象改变结果图;
图5为唾液素salivaricin特异性抑制Tfh细胞分化和IL-21合成结果图。
具体实施方式
本发明提供了唾液素salivaricin在制备IL-21受体抑制剂中的应用。
本发明所述唾液素salivaricin优选包括salivaricinA2和/或salivaricinB,且所述salivaricin A2的氨基酸序列优选如SEQ ID NO.1所示:KRGTGWFATITDDCPNSVFVCC;所述salivaricin B的氨基酸序列优选如SEQ ID NO.2所示:GGGVIQTISHECRMNSWQFLFTCCS。
本发明对所述唾液素salivaricin的来源并没有特殊限定,优选包括提取自唾液链球菌或直接人工合成,所述提取方法优选参考中国专利CN109675017A。本发明对人工合成的方法并没有特殊限定,经纯化后纯度>98%,且符合科学研究的要求即可。
本发明实施例中,运用体外实验体系,使用表面等离子体共振(Surface PlasmonResonance)技术发现唾液素salivaricinA2或salivaricin B均可直接与IL-21受体结合,并抑制细胞因子IL-21与其受体的结合,继而阻断IL-21受体信号通路,因此可将唾液素salivaricinA2或salivaricin B作为IL-21受体及其下游信号通路抑制剂。
本发明还提供了唾液素salivaricin在制备诱导IL-21受体构象发生改变的试剂中的应用。
本发明实施例中,还利用圆二色谱技术对IL-21受体的二级结构进行检测,发现salivaricinA2或salivaricinB均可诱导IL-21受体构象发生改变。
本发明还提供了唾液素salivaricin在制备IL-21受体及其下游信号通路抑制剂中的应用。
为了进一步说明本发明,下面结合附图和实施例对本发明提供的唾液素salivaricin在制备IL-21受体抑制剂中的应用进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
实施例1唾液素salivaricin的化学合成与纯化及鉴定
(1)唾液素salivaricin的化学合成:salivaricin A2(KRGTGWFATITDDCPNSVFVCC)和B(GGGVIQTISHECRMNSWQFLFTCCS)均为普通直线多肽,采用固相多肽合成的方法来生产:
①树脂溶涨:将树脂放入反应管中,加DMF(15mL/g),30min。
②脱保护:去掉DMF,加20%哌啶DMF溶液(15mL/g),5min,去掉再加20%哌啶DMF溶液(15mL/g),15min。
③检测:抽掉哌啶溶液,取十几粒树脂,用乙醇洗三次,加入茚三酮、KCN和苯酚溶液各一滴,105℃~110℃加热5min。
④洗:以此使用DMF(10mL/g)洗两次,甲醇(10mL/g)洗两次,DMF(10mL/g)洗两次。
⑤缩合:保护氨基酸三倍过量,HBTU三倍过量,均用尽量少DMF溶解,加入反应管,立刻加入NMM十倍过量,反应30min。
⑥洗:依次使用DMF(10mL/g)洗一次,甲醇(10mL/g)洗两次,DMF(10mL/g)洗两次。
⑦重复上述操作步骤⑥一次。最后一次洗涤:DMF(10mL/g)两次,甲醇(10mL/g)两次,DMF(10mL/g)两次,DCM(10mL/g)两次。
⑧裂解:配制裂解液(10/g)TFA94.5%;水2.5%;EDT 2.5%;TIS 1%120min。
⑨吹干洗涤:将裂解液用氮气尽量吹干,用乙醚洗六次,然后常温挥干。
⑩切割及后处理:使用切割液(TFA/TIS/EDT/H
(2)唾液素salivaricin的纯化:先用水溶解,如果水溶性不好加入乙腈,不能太多,必要时可以加乙二胺,醋酸等。一般用反相C8柱,流动相为含0.1%TFA水和乙腈,梯度为20%~80%。
(3)唾液素salivaricin的鉴定:使用高效液相色谱仪(HPLC)对多肽的纯度和分子量进行鉴定,具体方法如下:
配置HPLC流动相:A:0.1%TFA+100%ACN(乙腈),B:0.1%TFA+100%Water。HPLC的波长选择是220nm,梯度设置,A项是30%,B项是70%。梯度设置好之后,让机器运行进行机械的平衡,跑梯度跑平衡;用毛细管取少量的样品,溶解在0.5mL的离心管中,选用合适的溶解试剂(一般直接用水溶解),可用超声波超声震荡至澄清;吸取10μL或者20μL的样品进行测试,跑样大概25~30分钟。
使用化学合成的方法获取salivaricinA2和B,使用高效液相色谱仪(HPLC)对纯化的salivaricin进行分子量和纯度鉴定,结果如图1所示,salivaricinA2的分子量为2420.77(图1中A),salivaricinB的分子量为2805.23(图1中B),二者的纯度均>98%。此外,毒素含量检测结果显示,salivaricinA2和B的内毒素的含量均<5EU/mg(图1),符合科学研究的要求。
实施例2唾液素salivaricin与IL-21受体直接结合
实施方法:
使用表面等离子体共振(Surface Plasmon Resonance,SPR)的方法检测唾液素与IL-21受体的结合力,使用仪器为Biacore 8K(GE Healthcare)。具体操作步骤如下:使用pH4.5的醋酸缓冲液溶解将人或小鼠的IL-21受体(IL-21R,Sino Biological,20nM),并将其固定在CM5芯片上,条件为25℃,缓冲液为PBS-P(GE Healthcare)。将salivaricinA2或B配置成含5%DMSO的溶液,浓度为6.25、12.5、25、50、100、200、400、600和800Μm(图2中线条自下而上浓度依次增加),阴性对照肽为二者的反向合成多肽(NA,SEQ ID NO.3:CCVFVSNPCDDTITAFWGTGRK和NB,SEQ ID NO.4:SCCTFLFQWSNMRCEHSITQIVGGG),配置浓度为12.5、25、50、100、200和400μM。将上述配置好的溶液依次加入机器通道,机器自动运行检测不同浓度溶液与受体的结合强度。亲和力使用解离常数(Dissociation Constants,KD)来表示,分析软件为Biacore 8K Evaluation Software。
使用SPR的方法检测salivaricin与IL-21受体(IL-21R)的结合力,结果如图2所示,唾液素salivaricn可特异性结合IL-21受体。具体的:salivaricinA2和B与小鼠IL-21R的结合力分别为12.6μM和10.1μM,而阴性对照肽NA和NB与小鼠IL-21R无结合(图2中A)。SalivaricinA2和B与人IL-21R的结合力分别为212μM和167μM,而阴性对照肽NA和NB与人IL-21R也无结合(图2中B)。
实施例3唾液素salivaricin阻断细胞因子IL-21与其受体的结合
使用SPR的方法检测唾液素salivaricin对IL-21与其受体结合力的影响,仪器型号为Biacore 8K(GE Healthcare),使用竞争性实验模式。IL-21受体固定方法同上,缓冲液为PBS-P(GE Healthcare),将不同浓度的salivaricin(100、200和400μM)加入缓冲液中,检测基于不同浓度salivaricin存在的条件下,IL-21(Sino Biological,1nM)与IL-21R(SinoBiological,20nM)的结合力。
使用SPR的竞争性实验模式检测唾液素salivaricin对细胞因子IL-21与受体(IL-21R)结合力的影响,结果如图3所示,唾液素salivaricin阻断IL-21与IL-21受体结合的效应具有浓度依赖性,salivaricin的浓度越大,抑制效果越明显。并且,salivaricin可完全阻断小鼠IL-21与其受体的结合。具体的:
salivaricin可降低小鼠IL-21与其受体(murine IL-21R)的亲和力,当缓冲液中无salivaricin时,小鼠IL-21与IL-21R的最高反应性为26.34U,而当缓冲液中含有salivaricinA2(100-400μM)时,小鼠IL-21与IL-21R的反应性降为0(图3中A);当缓冲液中含有100μM salivaricin B时,小鼠IL-21与受体的最高反应性降为6U,而200或400μMsalivaricinB则可使小鼠IL-21与其受体的反应性降为0(图3中A)。类似地,salivaricin也可降低人IL-21与其受体(human IL-21R)的亲和力,当缓冲液中无salivaricin时,人IL-21与IL-21R的最高反应性为21.58U,而当缓冲液中含有100μM salivaricinA2时,小鼠IL-21与IL-21R的最高反应性降为6.88U,而200或400μM salivaricinA2则使人IL-21与IL-21R的反应性降为接近0(图3中B);当缓冲液中含有salivaricin B时,人IL-21与IL-21R的反应性降为3.71~0U(图3中B)。
实施例4唾液素salivaricin诱导IL-21受体构象改变
使用圆二色谱(Circulardichroism spectroscopy)仪(ChirascanV100,Jasco,Easton,MD,USA)检测不同缓冲体系下IL-21受体的二级结构,工作温度为室温(25℃)。将salivaricinA2或B配置成浓度为10mg/mL的溶液,IL-21(Sino Biological)和IL-21R(SinoBiological)的浓度为1mg/mL。缓冲液为纯水,终体积为100μL。将检测样本加入1.0mm直径的石英小皿(Hellma UK)中,采集波长为180~260nm,频宽(bandwidth)为1nm,检测样本有:IL-21R(0.1mg/ml),IL-21R(0.1mg/ml)+IL-21(0.1mg/ml),IL-21R(0.1mg/ml)+salivaricinA2(10mg/ml)或B(10mg/ml),IL-21R(0.1mg/ml)+IL-21(0.1mg/ml)+salivaricinA2(10mg/ml)或B(10mg/ml)。圆二色谱的分析软件为CDNN v2.1。
使用圆二色谱仪检测不同条件下IL-21受体(IL-21R)的二级结构如Helix、Antiparallel、Parallel、Beta-Turn和Rndm.Coil的比例。IL-21与IL-21R结合后,IL-21R的各种二级结构的比例均无变化(图4中A),表明受体的构象无明显改变;而salivaricinA2或B与IL-21R结合后,受体的二级结构比例发生了改变,主要表现为Helix减少,从12.34%减少为1.48%(salivaricin A2)或0.071%(salivaricin B)(图4中B和C)。并且,当salivaricinA2或B与IL-21共孵育时,IL-21R的二级结构也有明显改变,也是主要表现为Helix减少,从13.67%减少为0.15%(salivaricinA2)或5.66%(salivaricinB)(图4中B和C)。
实施例5唾液素salivaricin特异性抑制Tfh细胞分化和IL-21合成
实施方法:
(1)T细胞体外分化:分离小鼠淋巴结细胞,流式分选
T细胞亚群分化条件如下:
Tfh-like(20ng/mL IL-6+20ng/mL IL-21+10μg/mL anti-IFNγ+10μg/mL anti-IL-4);
Th17(20ng/mL IL-6+50ng/mL IL-23+2ng/mL TGF-β+10μg/mL anti-IFNγ+10μg/mL anti-IL-4);
Th1(1ng/mL IL-12+10ng/mL IL-210ug/mL+anti-IL-4);
Treg(0.1ng/mL TGF-β+5ng/mL IL-2)。
(2)荧光定量PCR检测基因表达:使用RNA提取试剂盒(RNAprep Pure Micro Kit,TIANGEN Biotech Co.,Ltd)提取细胞总RNA。使用寡核苷酸(Oligonucleotide,Invitrogen),拟转录酶(Revertaid reverse transcriptase,Invitrogen)和核糖核酸酶抑制剂(RiboLock RNase Inhibitor,Invitrogen)反转录出cDNA。基因表达使用AceQ qPCRSYBR Green MasterMix(Vazyme Biotech)进行检测。内参基因为Actb。引物序列如表1所示:
表1引物序列
(3)ELISA检测细胞因子表达:收集细胞培养上清,遵照ELISA试剂盒(MultiScience,Shanghai,China)说明书进行操作,即配置标准品,样本稀释,一抗孵育,洗板,二抗孵育,洗板,显色,读取数值,结果分析。
(4)流式细胞术检测淋巴细胞亚群比例:制备单细胞悬液,加流式抗体(BioLegend,San Diego,CA,USA)进行染色,洗涤重悬后上流式机(BD FACSAria
在Tfh-like细胞分化的条件下,与Tfh细胞分化相关的特异性标记的mRNA表达量降低,表明salivaricin可抑制Tfh细胞的分化:唾液素salivaricinA2处理组Bcl6,cxcr5和il21三个基因mRNA的表达分别减少了25~58%,26~59%和15~76%,而salivaricin B处理组三个基因mRNA的表达分别减少了40~59%,35~41%和28~71%(图5中A-C)。此外,Tfh-like细胞中IL-21的表达在salivaricin A2处理组减少了67~98%,而salivaricin B处理组IL-21的表达减少了46~87%(图5中D),表明salivaricin可抑制Tfh细胞分泌IL-21的功能。然而,在Th17细胞分化的条件下,salivaricin对Th17细胞的比例无明显影响(图5中E)。同样,在Th1和Treg细胞分化的条件下,salivaricin对Th1和Treg的比例无明显影响(图5中F和图5中G)。
尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例,而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其他实施例,这些实施例都属于本发明保护范围。
