一种基于偏振热声矩阵的微波热声成像装置及方法
文献发布时间:2024-04-18 19:59:31
技术领域
本发明属于微波热声成像的技术领域,具体涉及一种基于偏振热声矩阵的微波热声成像装置及方法。
背景技术
微波热声成像是一种以生物组织电特性差异为原理基础的多物理场耦合成像方法,其采用脉冲微波作为激发源,通过热弹性效应产生的超声波呈递深层生物组织的结构与功能信息,融合了微波成像高对比度和超声成像高分辨率的优点。生物组织中的极性分子、离子吸收微波能量后通过热弹性效应产生超声波,被激发的超声波携带着生物组织病理、生理信息向外传播,通过采集生物组织周围各个方向的超声信号可以重建出组织内部形态结构与功能图像。由于微波的低散射特性,通过微波到超声能量传递形式的变换,微波热声成像技术可实现生物组织无损、数厘米深度、百微米分辨率的成像。但是,现有的微波热声成像技术无法获取生物组织的空间结构信息,无法对生物组织各向异性度、空间排列取向和手性状态进行定量描述,降低对生物组织的成像准确性。
发明内容
本发明的主要目的在于克服现有技术的缺点与不足,提供一种基于偏振热声矩阵的微波热声成像装置及方法,通过对生物组织样品照射不同状态的偏振微波得到样品激发的超声波,在对超声波进行分析得到微波热声矩阵,进一步得到各向异性微波吸收矩阵,实现对生物组织各向异性度、空间排列取向和手性状态进行定量描述,从而提高生物组织的微波热声成像准确性。
为了达到上述目的,本发明一方面采用一种基于偏振热声矩阵的微波热声成像装置,包括微波激励源、天线辐射组件、超声换能器、超声波信号处理组件及计算机;
所述微波激励源用于生成微波激励信号;
所述天线辐射组件与微波激励源连接,用于根据微波激励信号向生物组织样品照射线偏振微波和圆偏振微波生成超声波;
所述超声换能器用于接收生物组织样品在天线辐射组件中产生的超声波,并生成与超声波对应的超声波信号;
所述超声波信号处理组件与超声换能器连接,用于对超声波信号进行处理,从而生成数字信号;
所述计算机与超声波信号处理组件连接,用于根据数字信号对生物组织样品进行超声图像实时重建,从而完成对生物组织样品的各向异性度、空间排列取向和手性状态的定量表征;
所述计算机还与微波激励源连接,用于控制微波激励源信号的生成。
作为优选的技术方案,所述微波激励源为脉冲式微波激励源;
所述微波激励源生成频率为0.5~10GHz,重复频率为10~100Hz,脉冲宽度为50~550ns,峰值功率为70kW的脉冲微波激励信号。
作为优选的技术方案,所述天线辐射组件包括偶极子天线和圆偏振天线;
所述偶极子天线根据微波激励信号发射线偏振微波;所述线偏振微波具有多种不同的极化方向;
所述圆偏振天线根据微波激励信号发射圆偏振微波;
所述偶极子天线和圆偏振天线分别在不同时段向生物组织样品照射对应的偏振微波。
作为优选的技术方案,所述装置还包括步进电机,与偶极子天线连接,用于驱动偶极子天线,改变偶极子天线的极化方向,从而使偶极子天线在四个不同的极化方向上发射线偏振微波;
所述计算机与步进电机连接,通过步进电机控制偶极子天线的旋转方向和旋转角度。
作为优选的技术方案,所述偶极子天线根据微波激励信号在-45
所述圆偏振天线根据微波激励信号发射左圆偏振微波或右圆偏振微波。
作为优选的技术方案,所述超声换能器为阵列式超声换能器,并且位于垂直于天线辐射组件极化面的平面上;
所述超声换能器和生物组织样品共同浸没在超声耦合液中;
所述阵列式超声换能器为128个阵元且呈半环形的聚焦阵列超声换能器,中心频率为3.5MHz,阵元间距为1.45mm,阵元弧长为15mm,阵元宽度为1.35mm;
所述超声耦合液为矿物油或变压器油。
作为优选的技术方案,所述超声波信号处理组件包括放大器和数字采样器;
所述放大器与超声换能器连接,用于对超声波信号进行放大处理;
所述数字采样器与放大器连接用于对经过放大处理的超声波信号进行采样处理,从而生成与超声波信号对应的数字信号;
所述放大器包括128路通道,最大增益为80dB;
所述数字采样器的采样频率为40MHz。
另一方面,本发明还提供一种使用上述微波热声成像装置的生物组织偏振测量方法,包括下述步骤:
将生物组织样品放入微波热声成像装置中,通过计算机控制微波激励源生成微波激励信号;
根据微波激励信号,控制天线辐射组件向生物组织样品照射四个不同极化方向的线偏振微波和两种不同类型的圆偏振微波,生成生物组织样品的超声波;所述超声波包括在每个极化方向的线偏振微波超声波和每种类型的圆偏振微波超声波;
通过超声换能器接收生物组织样品的超声波,并生成与其对应的超声波信号;
使用超声波信号处理组件对超声波信号进行处理,生成对应的数字信号;
计算机对数字信号进行分析,得到生物组织样品在线偏振微波和圆偏振微波照射下对应的偏振热声矩阵;
基于偏振热声矩阵,确定生物组织样品的各向异性微波吸收矩阵,并进一步确定生物组织样品的各向异性度、空间排列取向和手性状态。
作为优选的技术方案,所述四个不同极化方向的线偏振微波分别为-45
所述两种不同类型的圆偏振微波分别为左圆偏振微波和右圆偏振微波;
通过测量四个不同极化方向的线偏振微波的热声信号幅值和两种不同类型的圆偏振微波的热声信号幅值,得到偏振热声矩阵S
S
其中,TA
使用斯托克矢量S
S
其中,S
基于偏振热声矩阵和斯托克矢量构建关系方程式:
S
其中,M
求解关系方程式得到生物组织样品的各向异性微波吸收矩阵M
,
其中,M
作为优选的技术方案,所述各向异性微波吸收矩阵M
,
其中,TA
从各向异性微波吸收矩阵M
,
其中,各向异性度DOA的取值范围为0~1;当各向异性度DOA=1时,微波吸收是完全各向异性;当各向异性度DOA=0时,微波吸收是完全各向同性;
当各向异性度DOA≠0时,利用各向异性微波吸收矩阵M
,
其中,当空间排列取向OCAC=0时,表明目标生物组织或细胞的空间排列取向与电矢量方向一致;
对于生物组织样品的手性状态,若各向异性微波吸收矩阵M
本发明与现有技术相比,具有如下优点和有益效果:
1、本申请提供的微波热声矩阵成像装置与方法通过向样品照射不同状态的线偏振微波和圆偏振微波,并采集样品在不同偏振微波照射下对应激发形成的超声波;对超声波信息分析,得到样品在在不同偏振微波照射激发下对应的微波热声矩阵,并构建微波热声矩阵与所有偏振微波的极化状态的斯托克矢量之间的关系方程;通过解算关系方程得到样品的各向异性微波吸收矩阵,再根据样品的各向异性微波吸收矩阵,确定样品的各向异性度、空间排列取向和手性状态,这样通过微波热声矩阵成像技术,对样品的组织偏振测量提供直接高效的策略,对生物组织各向异性度、空间排列取向和手性状态进行定量描述,从而提高生物组织的微波热声成像准确性。
2、本发明提供的微波热声成像装置其采用微波作为能量激发、超声波作为信息载体,可以做到非侵入、高深度、高分辨成像,有利于精准诊断深部病变。
3、本申请提供的微波热声成像装置不同于一般微波热声成像技术,可以精准定量分析目标生物组织各向异性度、空间排布取向和手性状态,极大地提升了对微波激发优势的利用。
4、本发明提供的微波热声成像装置具备快速检测的能力,且装置结构简单、使用方便,可以广泛应用于生物体内部结构检测,便于产业化。
附图说明
为了更清楚地说明本申请实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本申请的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
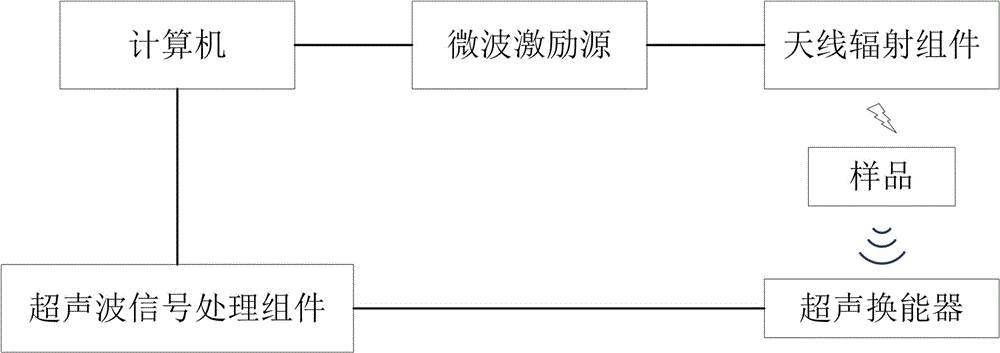
图1为本发明实施例中一种基于偏振热声矩阵的微波热声成像装置的结构示意图。
图2为本发明实施例中天线辐射组件的结构示意图。
图3为本发明实施例中微波热声成像装置包含步进电机的结构示意图。
图4为本发明实施例中超声波信号处理组件的结构示意图。
图5为本发明实施例中微波热声成像装置的成像过程图。
图6为本发明实施例中微波热声成像装置的成像结果图。
具体实施方式
为了使本技术领域的人员更好地理解本申请的目的、特征和优点,下面将结合本申请实施例中的附图,对本申请实施例中的技术方案进行清楚、完整地描述。显然,所描述的实施例仅仅是本申请一部分实施例,而不是全部的实施例。基于本申请中的实施例,本领域技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本申请保护的范围。
在本申请中提及“实施例”意味着,结合实施例描述的特定特征、结构或特性可以包含在本申请的至少一个实施例中。在说明书中的各个位置出现该短语并不一定均是指相同的实施例,也不是与其它实施例互斥的独立的或备选的实施例。本领域技术人员显式地和隐式地理解的是,本申请所描述的实施例可以与其它实施例相结合。
为了便于说明,本申请实施例的结构示意图中,仅仅示出了与本发明实施例相关的部分,本领域技术人员可以理解,图示结构并不构成对装置的限定,可以包括比图示更多或更少的部件,或者组合某些部件,或者不同的部件布置。
如图1所示,本实施例提供一种基于偏振热声矩阵的微波热声成像装置,包括微波激励源、天线辐射组件、超声换能器、超声波信号处理组件、步进电机及计算机;
其中,微波激励源用于生成微波激励信号;
天线辐射组件与微波激励源连接,用于根据微波激励信号向生物组织样品照射线偏振微波和圆偏振微波生成超声波;
超声换能器用于接收生物组织样品在天线辐射组件中产生的超声波,并生成与超声波对应的超声波信号;
超声波信号处理组件与超声换能器连接,用于对超声波信号进行处理,从而生成数字信号;
计算机与超声波信号处理组件连接,用于根据数字信号对生物组织样品进行超声图像实时重建,从而完成对生物组织样品的各向异性度、空间排列取向和手性状态的定量表征;
计算机还与微波激励源连接,用于控制微波激励源信号的生成。
在另一实施例中,微波激励源为脉冲式微波激励源;该微波激励源生成频率为0.5~10GHz,重复频率为10~100Hz,脉冲宽度为50~550ns,峰值功率为70kW的脉冲微波激励信号。通过该脉冲式微波激励源为天线辐射组件提供微波激励信号,能够激励天线辐射组件向外发射不同类型的微波。其中,该脉冲式微波激励源可与计算机连接,这样可以通过计算机控制调整脉冲式微波激励源的重复频率和脉冲宽度,使得生成的脉冲微波激励信号的重复频率能够在10-100Hz范围内和脉冲宽度能够在50-550ns范围内调整变化,从而改善脉冲式微波激励源的脉冲微波激励信号的发射性能。
在另一实施例中,如图2所示,天线辐射组件包括偶极子天线和圆偏振天线;其中,偶极子天线根据微波激励信号发射线偏振微波;线偏振微波具有多种不同的极化方向;圆偏振天线根据微波激励信号发射圆偏振微波。实际操作中,偶极子天线和圆偏振天线分别在不同时段向生物组织样品照射对应的偏振微波,这样该天线辐射组件能够向生物组织样品照射不同类型的偏振微波,使得生物组织样品的内部组织受到不同类型的微波激励,从而产生不同的超声波。
在另一实施例中,如图3所示,本发明微波热声成像装置还包括步进电机,与偶极子天线连接,用于驱动偶极子天线,改变偶极子天线的极化方向,从而使偶极子天线在四个不同的极化方向上发射线偏振微波;同时,计算机与步进电机连接,通过步进电机控制偶极子天线的旋转方向和旋转角度,这样能够改变该偶极子天线的极化方向,每当步进电机将该偶极子天线驱动旋转到一个特定的极化方向时,该偶极子天线会在该极化方向上向生物组织样品照射线偏振微波,使生物组织样品能够接收到对应极化方向的线偏振微波。
进一步的,偶极子天线根据微波激励信号在-45
在另一实施例中,超声换能器为阵列式超声换能器,并且位于垂直于天线辐射组件极化面的平面上;并且超声换能器和生物组织样品共同浸没在超声耦合液中。可以理解的是,该超声换能器可为但不限于是包括128个阵元并且呈半环形的聚焦阵列,其中心频率为3.5MHz,阵元间距为1.45mm,阵元弧长为15mm,阵元宽度为1.35mm,这样能够保证该超声换能器准确全面地接收来自该生物组织样品的超声波。此外将该超声换能器设成位于垂直于该天线辐射组件的极化面的平面上,能够提高该超声换能器对超声波的接收效率。将该超声换能器和该生物组织样品共同浸没在超声耦合液中,能够保证该样品发出的超声波无损耗地传输到该超声换能器,其中该超声耦合液可为但不限于是矿物油或变压器油。
在另一实施例中,如图4所示,超声波信号处理组件包括放大器和数字采样器;其中,放大器与超声换能器连接,用于对超声波信号进行放大处理;数字采样器与放大器连接用于对经过放大处理的超声波信号进行采样处理,从而生成与超声波信号对应的数字信号。该放大器对该超声波信号进行放大增益处理,其包括128路通道,最大增益可为80dB;该数字采样器的采样频率为40MHz,这样能够提高对该超声波信号的处理可靠性。
本发明还一实施例中提供一种使用上述微波热声成像装置的生物组织偏振测量方法,包括下述步骤:
将生物组织样品放入微波热声成像装置中,通过计算机控制微波激励源生成微波激励信号;
根据微波激励信号,控制天线辐射组件向生物组织样品照射四个不同极化方向的线偏振微波和两种不同类型的圆偏振微波,生成生物组织样品的超声波;其中,超声波包括在每个极化方向的线偏振微波超声波和每种类型的圆偏振微波超声波;
通过超声换能器接收生物组织样品的超声波,并生成与其对应的超声波信号;
使用超声波信号处理组件对超声波信号进行处理,生成对应的数字信号;
计算机对数字信号进行分析,得到生物组织样品在线偏振微波和圆偏振微波照射下对应的偏振热声矩阵;
基于偏振热声矩阵,确定生物组织样品的各向异性微波吸收矩阵,并进一步确定生物组织样品的各向异性度、空间排列取向和手性状态。
进一步的,四个不同极化方向的线偏振微波分别为-45
通过测量四个不同极化方向的线偏振微波的热声信号幅值和两种不同类型的圆偏振微波的热声信号幅值,得到偏振热声矩阵S
S
其中,TA
具体而言,本申请首次提出采用穆勒矩阵进行偏振态信息的处理,对于不同偏振态信息的处理,其过程如下:
对于时谐场,根据热声效应理论,热声信号的强度P
P
在上述公式(1)中,P
对于微波与目标相互作用,目标的微波吸收系数依赖于其电导率σ的分布。对于各向同性介质,电导率σ是一个标量;对于各项异性介质,电导率σ是一个张量。在热声成像中,各向异性目标的电导率σ是一个非线性和各向异性的张量,其张量矩阵是一个正定矩阵,并可如下表示:
(3),
在上述公式(3)中,r表示微波场电矢量。
当各向异性目标的电导率二维分布确定时,比如,若已知各向异性目标的电导率分布主要沿各向异性目标长轴方向,若微波场电矢量强度不变的情况下,但微波场电矢量方向发生改变,在各向异性目标的长轴方向上的电场分量E
|E
在上述公式(4)中,θ表示微波场电矢量与长轴方向的夹角。
同时,单位时间内单位质量的物质吸收的电磁能量SAR可表示为关于r和θ的函数,即:
SAR(r,θ) = σ
因此,各向异性目标的热声信号的强度P
P
由上述公式(6)可知,对应各向异性目标的热声信号的强度,会受电导率分布和微波场电矢量方向与长轴方向的夹角的影响。为了完备各向异性目标的电矢量吸收特征,引入六个偏振态分别为-45
在偏振微波热声矩阵成像理论中,使用斯托克矢量S
S
其中,S
通过将六个不同极化状态的激励微波场依次照射以激发生物组织样品各向异性目标,得到相应的热声信号振幅,并基于偏振热声矩阵和斯托克矢量构建关系方程式:
S
其中,M
求解关系方程式得到生物组织样品的各向异性微波吸收矩阵M
(9),
其中,M
进一步的,从生物组织样品的各向异性微波吸收矩阵M
(10),
其中,TA
由于生物组织样品各向异性目标中的细胞排列的有序度的变化反映不同细胞之间的相互作用、结构和功能的特性,因此从各向异性微波吸收矩阵M
(11),
其中,各向异性度DOA的取值范围为0~1;当各向异性度DOA=1时,微波吸收是完全各向异性,表明生物组织样品的目标生物组织或细胞排列是完全有序的,在这种情况下,热声信号振幅会随微波场电矢量与各向异性目标长轴方向的夹角变化;当各向异性度DOA=0时,微波吸收是完全各向同性,表明生物组织样品的目标生物组织或细胞排列是完全无序,这种情况下,热声信号振幅不会随微波场电矢量与各向异性目标长轴方向的夹角变化;
当各向异性度DOA≠0时,利用各向异性微波吸收矩阵M
(12),
其中,空间排列取向OCAC只在DOA≠0的情况下讨论,即若生物组织样品的目标生物组织或细胞空间排列为各向同性,排列是杂乱的,无讨论意义。因此当各向异性度DOA≠0时,表明生物组织样品的各向异性目标不是各项同性,此时若空间排列取向OCAC=0时,则表明目标生物组织或细胞的空间排列取向与电矢量方向一致;
对于生物组织样品的手性状态,若各向异性微波吸收矩阵M
请参阅图5和6所示,分别本申请一实施例提供的微波热声矩阵成像装置的成像过程示意图和成像结果示意图。图5为该微波热声矩阵成像装置的成像过程示意图,其反映微波照射到生物组织样品上对应的偏振微波热声信号的生成情况,其中α
总体而言,本发明通过向生物组织样品照射不同状态的线偏振微波和圆偏振微波,并采集生物组织样品在不同偏振微波照射下对应激发形成的超声波;对超声波信息分析,得到生物组织样品在不同偏振微波照射激发下对应的微波热声矩阵,并构建微波热声矩阵与所有偏振微波极化状态的斯托克矢量之间的关系方程;通过解算关系方程得到各向异性微波吸收矩阵,再基于各向异性微波吸收矩阵确定生物组织样品的各向异性度、空间排列取向和手性状态,为生物组织偏振测量提供直接高效的策略,对生物组织各向异性度、空间排列取向和手性状态进行定量描述,从而提高生物组织的微波热声成像准确性。
需要说明的是,对于前述的各方法实施例,为了简便描述,将其都表述为一系列的动作组合,但是本领域技术人员应该知悉,本发明并不受所描述的动作顺序的限制,因为依据本发明,某些步骤可以采用其它顺序或者同时进行。
以上实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 一种形貌可控的钴铝双氢氧化物/还原氧化石墨烯复合材料及其制备方法
- 一种添加石墨烯微弧氧化环氧锶黄复合涂层及制备方法
- 氧化石墨烯/六方氮化硼三维复合泡沫和双网络结构环氧复合材料及其制备方法和应用
- 氧化石墨烯/六方氮化硼三维复合泡沫和双网络结构环氧复合材料及其制备方法和应用
