一种美阿沙坦钾的有关物质及其制备方法
文献发布时间:2023-06-19 19:28:50
1、技术领域
本发明属于药物化学技术领域,具体涉及一种美阿沙坦钾的关键有关物质结构及其制备方法。
2、背景技术
美阿沙坦钾是由日本武田药品工业株式会社开发的血管紧张素II受体拮抗剂(ARBs),是阿齐沙坦的酯类前药。美阿沙坦钾/氯噻酮的复方片剂于2011年12月20日在美国获批上市。在中国,美阿沙坦钾片于2021年1月19日获得NMPA批准上市。
杂质研究作为原料药工艺开发的一项重要研究内容,直接关系到药物的质量控制以及安全性,通过鉴定药物产品中的杂质结构,可以明确该杂质的毒性及准确确定产品中杂质的量,也可确定该杂质的产生的来源,从而制定有效的控制策略,将其在API中残留量控制在符合药用的限度(0.1%或更低)以下,进而有助于加强对产品质量和安全性的控制。
API的杂质主要来自API本身的降解和制造过程。工艺杂质包括未反应的原材料,中间体,反应副产物,原材料或中间体中所含的杂质的衍生物,反应过程使用的溶剂、试剂、催化剂残留或其参与反应的杂质,API降解产物等。Improved Process forAzilsartanMedoxomil ANew Angiotensin Receptor Blocker.Org.Process Res.Dev.2013,17,1,77-86公开了美阿沙坦钾的杂质13、14的结构及制备方法。
本发明人在美阿沙坦钾的系列研究中发现,有一关键未知杂质在原料和市售制剂中均有检出,现有技术未见该有关物质的具体报道,本发明人还发现该有关物质对美阿沙坦钾的质量有较大影响,需要识别和制备出进而用于美阿沙坦钾的纯度、杂质和定量分析,以有效控制产品质量,对进一步提高美阿沙坦钾质量控制的水平和安全性有重要意义。
3、发明内容
本发明公开了一种美阿沙坦钾的有关物质化合物A的结构,并提供其制备方法和分析方法,以满足药物质量控制的需要。
本发明公开了美阿沙坦钾关键有关物质化合物A的结构:
化合物A是阿齐沙坦酯的同分异构体杂质,物理化学性质接近,工艺过程中的清除率相对较低,极易残留在成品中,是引起药物质量风险的关键因素之一。现有文献报道有关美阿沙坦钾烷基重排的杂质种类较多,通常认为分子间的烷基迁移为主要产生因素。从计算化学数据和试验现象分析,化合物A的产生原因应为乙基的分子内迁移,计算化学数据表明美阿沙坦钾能量较低的构象中,氮负离子与乙氧基的距离仅为
美阿沙坦钾的有关物质化合物A尚无文献报道,其获得方式可以通过调整反应液pH值及采用高极性溶剂提高其生成量,然后对反应母液的浓缩进行分离纯化。但化合物A在生产制备工艺中产生量大约0.5~2%,且与美阿沙坦钾性质十分相近,难以分离。专利发明人对该有关物质在生产工艺中的控制策略和获得方法进行了深入研究,提供简单高效的制备方法,在降低溶剂消耗和环保压力的同时,提高对照品质量和制备效率。
本发明进一步提供了一种化合物A的制备方法,包括如下步骤:
(1)阿齐沙坦酯在溶剂中与乙基化试剂反应,制得化合物C;
(2)化合物C在酸性条件下脱乙基反应,经纯化制得化合物A。
其中,步骤(1)中,溶剂选自水、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、二甲基亚砜、四氢呋喃、2-甲基四氢呋喃、丁酮、丙酮、N-甲基吡咯烷酮、环丁砜、三氯甲烷中的一种或多种,优选为水、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、二甲基亚砜中的一种或多种;乙基化试剂选自溴乙烷、氯乙烷、硫酸二乙酯、碳酸二乙酯、苯磺酸乙酯、甲磺酸乙酯、三氟甲磺酸乙酯中的一种或多种;所述反应的反应温度为10-90℃,优选20-60℃。
步骤(2)中,所述酸性条件为利用选自盐酸、硫酸、磷酸、甲磺酸、三氟甲磺酸的一种或多种的酸性试剂调节溶液pH≤4,优选pH≤2;所述纯化操作选自结晶纯化、萃取洗涤纯化、硅胶色谱柱纯化及制备液相仪器纯化中的一种或多种。
目前由于化合物A未在美阿沙坦钾的研究资料以及其他文献中报道,发明人对该有关物质也进行了分析方法的研究,并对己有分析方法进行了改进,以提高对包括化合物A在内的美阿沙坦钾有关物质的检测灵敏度和精确性,降低药物产品的质量风险和药物质量控制的检测成本。
本发明进一步提供了一种美阿沙坦钾及其关键杂质化合物A的高效液相色谱测定方法,色谱条件包括:
色谱柱:用十八烷基硅烷键合硅胶为填充剂的色谱柱,优选YMC-Pack Pro C18,4.6mm×150mm,5μm或效能相当的色谱柱;
流动相:流动相A:50mmol/L磷酸二氢铵缓冲液(用磷酸调节pH值至3.0)-乙腈(95:5);流动相B:乙腈-50mmol/L磷酸二氢铵缓冲液(用磷酸调节pH值至3.0)(70:30);
流速:1.0ml/min;
柱温:25℃;
检测波长:240nm;
进样体积:10μl;
洗脱程序:流动相A和流动相B按以下梯度运行:
本发明的有益技术效果为:
(1)本发明公开了美阿沙坦钾的关键有关物质化合物A,确证了其结构,并提供了满足杂质对照品质量要求的简单高效制备方法。
(2)原料和制剂人员可以根据公开的杂质结构明确其产生来源及产生的影响因素,并在生产工艺中制定合理的控制策略,确保产品质量及安全有效。
(3)可以较好的满足美阿沙坦钾质量研究与控制对关键有关物质的数量与质量的需求,实现质量分析人员对产品中该杂质残留量准确定量研究,从而确定合理的内控标准及货架期标准,确保产品安全有效。
(4)优化了分析方法,提高了包括化合物A在内的有关物质的检测准确度,极大降低药物的质量风险。
4、附图说明
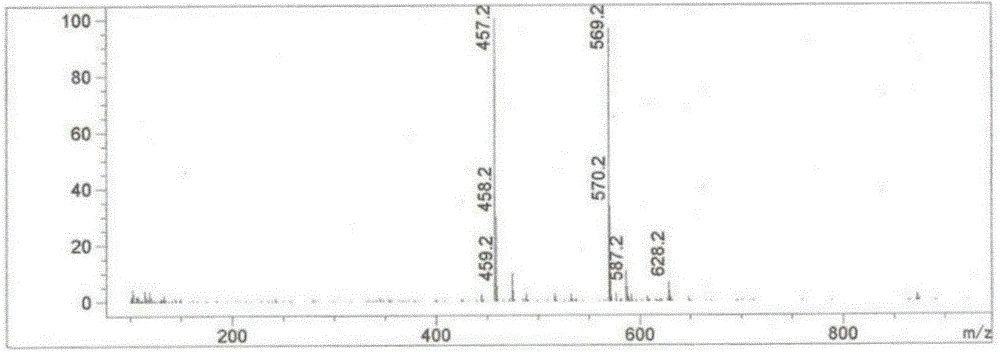
图1为实施例1制备所得的化合物A的质谱图。
图2为实施例1制备所得的化合物A的高效液相纯度图谱。
图3为实施例1制备所得的化合物A的核磁共振氢谱图。
图4为实施例3美阿沙坦钾高效液相色谱图谱。
图5为实施例3美阿沙坦钾加速试验高效液相色谱图谱。
5、具体实施方式
下面详细描述本发明的具体实施例,需要说明的是下面描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。
实施例1化合物A的制备
取阿齐沙坦酯3.0克,投入24.0克DMF中搅拌溶解。加入碳酸钾1.9克和溴乙烷2.1克,加热至35℃反应2小时。反应液加水稀释,并用二氯甲烷萃取三次。合并有机相,无水硫酸钠干燥后,35℃真空回收溶剂至干。向剩余物中加入乙醇10.0克及4M盐酸2毫升,加热至55℃保温搅拌1小时。降温,抽滤,滤饼55℃鼓风干燥,得棕黄色固体0.8克,收率26.7%,HPLC纯度94.7%。
MS:m/z,569[M+H]
1
实施例2化合物A的线性验证实验
杂质贮备液的制备:取化合物A对照品适量,精密称定,分别加溶剂溶解并定量稀释制成每1ml中约含各杂质0.1mg的溶液。
美阿沙坦钾贮备液的制备:取美阿沙坦钾对照品适量,精密称定,加溶剂溶解并定量稀释制成每1ml中约含0.1mg的溶液。
线性贮备液的制备:精密量取化合物A贮备液与美阿沙坦钾贮备液各5ml,置同一50ml量瓶中,用溶剂稀释至刻度,摇匀。
线性试验:精密量取线性贮备液1.0ml、3.0ml、5.0ml、7.5ml、9.0ml,分别置5个不同的50ml量瓶中,用溶剂稀释至刻度,摇匀,作为线性1~线性5溶液。
定量限溶液:线性试验中线性溶液1即为定量限溶液。
精密量取线性溶液、定量限溶液各10μl,分别注入液相色谱仪,记录色谱图,以峰面积对浓度作曲线,用最小二乘法计算回归方程及相关系数。美阿沙坦、化合物A在相应浓度范围内线性良好。
美阿沙坦钾有关物质线性试验结果:
实施例3美阿沙坦钾液相分析方法
按高效液相色谱法(中国药典2020年版通则0512)测定。
溶剂:乙腈-水-冰醋酸(V/V/V)(80:20:1)。
供试品溶液:(1)取美阿沙坦钾约50mg,置50ml量瓶中,加溶剂使溶解并稀释刻度,摇匀。(5℃水浴放置)。
(2)取美阿沙坦钾(加速6个月)约25mg,置25ml量瓶中,加溶剂使溶解并稀释刻度,摇匀。(5℃水浴放置)。
色谱条件:用十八烷基硅烷键合硅胶为填充剂(YMC-Pack Pro C18,4.6mm×150mm,5μm或效能相当的色谱柱);以50mmol/L磷酸二氢铵缓冲液(用磷酸调节pH值至3.0)-乙腈(95:5)为流动相A,以乙腈-50mmol/L磷酸二氢铵缓冲液(用磷酸调节pH值至3.0)(70:30)为流动相B,按下表梯度洗脱;流速为每分钟1.0ml;柱温为25℃;进样温度为5℃;检测波长为240nm;进样体积10μl。
梯度运行表
测定法:精密量取供试品溶液,注入液相色谱仪,记录色谱图。见附图4。
结果:化合物A相对保留时间为0.92。
/>
