一种用于同步修复软硬组织缺损的仿生复合支架及其基于3D打印的成型方法
文献发布时间:2023-06-19 11:27:38
技术领域
本发明属于复合支架技术领域,具体为一种用于同步修复软硬组织缺损的仿生复合支架及其基于3D打印的成型方法。
背景技术
唇腭裂是常见的先天性畸形,每1000个新生儿中约有1.7个唇腭裂患者。唇腭裂不仅影响患者的形象,而且对语言学习、牙齿健康、面容发育以及心理健康等多个方面具有负面影响。导致唇腭裂的原因有很多,例如基因缺陷、染色体变异以及环境影响等,目前尚不能完全通过产检排除。一般地,唇腭裂分为单纯唇裂、单纯腭裂、单侧唇裂合并腭裂以及双侧唇裂合并腭裂四类,其中单纯腭裂、单侧唇裂合并腭裂以及双侧唇裂合并腭裂同时具有软组织与骨组织的缺损,给修复带来困难。
目前,唇腭裂修复方式称为腭成形术。第一位能够完全修复腭裂的学者是VonLangenbeck,其术式被称为Von Langenbeck腭成形术,该术式通过松动双侧黏骨膜瓣来闭合硬腭。这项技术适合于修复单纯腭裂,现在经常与其他术式一起使用。Veau-Wardill-Kilner腭成形术由于可以增加腭的长度而被广泛使用,该术式向后翻转黏骨膜瓣,可以改善腭咽功能。Furlow双反Z形腭成形术松动鼻、口粘膜并向后移动,可以延长软腭,对上颌生长发育和语言学习更有利。以上腭成形术虽然在一定程度上修复了腭裂,却不能修复腭部的骨缺损,且手术创面大、出血量大,术后并发症多,感染可能性高。此外,骨面瘢痕的产生对发音造成影响。
采用与唇腭裂患者缺损相一致的载有成骨细胞与成纤维细胞的复合支架将为骨缺损处提供支撑,并引导骨生长,软组织支架部分可以覆盖创面,促进软组织修复。因此,制备用于同步修复软硬组织缺损的仿生复合支架具有重要意义。
发明内容
本发明为了解决现有的同步修复软硬组织缺损技术的不足,提供一种用于同步修复软硬组织缺损的仿生复合支架及其基于3D打印的成型方法。本发明涉及到了两种支架和多种中间模具,即载有成纤维细胞的第一支架、载有骨髓间充质干细胞的第二支架以及成型时使用的树脂模具、壳聚糖模具与PDMS(聚二甲基硅氧烷)模具。树脂模具、壳聚糖模具采用DLP(数字光处理)打印而成,PDMS模具由树脂模具、壳聚糖模具作为模具浇筑热固化而成。
复合支架首先采用TCP(磷酸三钙)光敏树脂混合浆料经DLP光固化成型、脱脂烧结形成陶瓷骨架,然后借助PDMS模具在TCP支架上分层浇筑分别载有成纤维细胞与骨髓间充质干细胞的GelMA(甲基丙烯酸化水凝胶)水凝胶并光固化形成。本发明提出的仿生复合支架具有生物相容性,可用于同步修复软硬组织缺损。
为了实现上述目的,本发明采用如下技术方案:
本发明的其中一个目的在于提供一种用于同步修复软硬组织缺损的仿生复合支架,由载有成纤维细胞的第一支架、以及载有骨髓间充质干细胞的第二支架构成,所述的骨髓间充质干细胞填充在第二支架的内部孔隙中;
所述的第二支架上设有起定位作用的凸出边缘,第一支架位于第二支架的上下表面,第一支架与第二支架通过燕尾槽连接。
作为本发明的优选,所述的第一支架采用载有成纤维细胞的水凝胶支架;所述的第二支架采用陶瓷骨架,所述的陶瓷骨架内部填充载有骨髓间充质干细胞的水凝胶。
作为本发明的优选,所述的陶瓷骨架上下表面孔隙尺寸为50-120微米,陶瓷骨架的内部孔隙尺寸为300-600微米。
作为本发明的优选,所述的燕尾槽设置在陶瓷骨架的上下表面,燕尾槽的下底宽度为200-400微米,上底宽度为50-150微米。
本发明的另一个目的在于提供一种上述的用于同步修复软硬组织缺损的仿生复合支架的基于3D打印的成型方法,包括如下步骤:
步骤1:根据已有的硬组织模型,制备陶瓷骨架,所述陶瓷骨架的上表面或者下表面留有起定位作用的凸出边缘;
步骤2:根据已有的软硬组织模型为原型,通过DLP打印得到树脂模具、第一壳聚糖模具和第二壳聚糖模具,所述的树脂模具与软硬组织模型的外轮廓一致,且与陶瓷骨架相对应的位置预设有形状、大小一致的凸出边缘;
所述的第一壳聚糖模具和第二壳聚糖模具均由垂直部和水平部连接构成,呈L型结构;
步骤3:将壳聚糖模具粘结在树脂模具的两侧,所述的树脂模具中对应于陶瓷骨架凸出边缘的一面朝上;第一壳聚糖模具的水平部与树脂模具的侧壁中下位置抵接,第一壳聚糖模具的垂直部平行于树脂模具的厚度方向;第二壳聚糖模具的水平部与树脂模具的侧壁底部抵接,与树脂模具下表面平齐,第二壳聚糖模具的垂直部平行于树脂模具的厚度方向;
步骤4:将PDMS与固化剂按比例混合,形成PDMS预聚物,浇筑在培养皿中进行真空脱泡;脱泡后,将粘结在一起的树脂模具与壳聚糖模具置于培养皿中,由于浮力作用,树脂模具的底部与培养皿的底部之间留有间隙;置于55℃条件下固化过夜,然后将模具从培养皿中取出,通过酸溶液溶解去除壳聚糖模具,形成第一浇筑通道和第二浇筑通道,之后将树脂模具取出,留下具有浇筑管道的PDMS模具;
步骤5:将步骤1制备得到的陶瓷骨架置于PDMS模具中,通过第一浇筑通道浇筑载有骨髓间充质干细胞的水凝胶,通过第二浇筑通道浇筑载有成纤维细胞的水凝胶,并且在陶瓷骨架上表面浇筑载有成纤维细胞的水凝胶,使陶瓷骨架上表面与PDMS模具平齐;采用蓝光交联固化成型;
步骤6:切开PDMS模具,取出制备好的复合支架。
与现有技术相比,本发明的优势在于:
(1)本发明在第一支架和第二支架的连接处设置了燕尾槽微锁结结构,提高了第一支架与第二支架之间的结合强度,支架之间不会相互脱开或错动。
(2)本发明的第二支架设计有起定位作用的凸出边缘,保证了成型精度,并且在后续的支架应用中也起到了定位作用,适用于多种应用场合。
(3)本发明采用3D打印与模型浇筑相结合的方法,将具有不同性质、需要不同后处理的两种材料结合成复合支架,在保证强度的同时还兼具有生物相容性,可用于同步修复软硬组织缺损;
(4)传统的DLP打印技术由于光散射作用,实际打印线条的直径略大,容易导致支架实际孔隙率低于设计孔隙率的问题,本发明采用模型补偿的方式,预先提高孔隙率,解决了DLP打印中孔隙率偏低的问题。
附图说明
图1为本实施例中的仿生复合支架模型结构示意图;
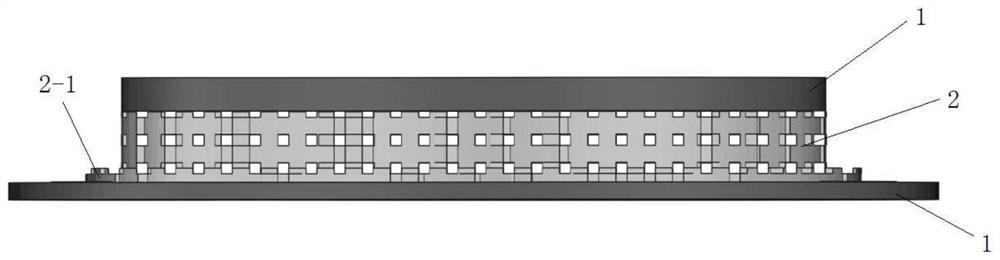
图2为本实施例中制备得到的仿生复合支架结构示意图;
图3为本实施例中的仿生复合支架内部结构示意图
图4为本实施例中的树脂模具结构示意图;
图5为本实施例中的壳聚糖模具结构示意图;
图6为本实施例中的PDMS模具结构示意图;
图7为本实施例中的成型过程示意图;
图中:1第一支架,2第二支架,2-1凸出边缘,2-2燕尾槽,3陶瓷骨架,4水凝胶,5PDMS模具,6-1第一浇筑通道,6-2第二浇筑通道。
具体实施方式
这里将详细地对示例性实施例进行说明,其示例表示在附图中。下面的描述及附图时,除非另有表示,不同附图中的相同数字表示相同或相似的要素。以下示例性实施例中所描述的实施方式并不代表与本申请相一致的所有的实施方式。相反,它们仅是与如所附中权利要求书中所详述的,本申请的一些方面相一致的装置的例子。
需要说明,本申请实施例中所有方向性指示(诸如上、下、左、右、前、后……)仅用于解释在某一特定姿态(如附图所示)下各部件之间的相对位置关系、运动情况等,如果该特定姿态发生改变时,则该方向性指示也相应地随之改变。
另外,在本申请中涉及“第一”、“第二”等的描述仅用于描述目的,而不能理解为指示或暗示其相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括至少一个该特征。另外,各个实施例之间的技术方案可以相互结合,但是必须是以本领域普通技术人员能够实现为基础,当技术方案的结合出现相互矛盾或无法实现时应当认为这种技术方案的结合不存在,也不在本申请要求的保护范围之内。
本发明涉及到了两种支架和多种中间模具,即载有成纤维细胞的第一支架1、载有骨髓间充质干细胞的第二支架2以及成型时使用的树脂模具、壳聚糖模具与PDMS(聚二甲基硅氧烷)模具。树脂模具、壳聚糖模具采用DLP(数字光处理)打印而成,PDMS模具由树脂模具、壳聚糖模具作为模具浇筑热固化而成。
具体的,本发明提出的一种用于同步修复软硬组织缺损的仿生复合支架由载有成纤维细胞的第一支架、以及载有骨髓间充质干细胞的第二支架构成,所述的骨髓间充质干细胞填充在第二支架的内部孔隙中;
如图1-3所示,所述的第二支架上设有起定位作用的凸出边缘2-1,第一支架位于第二支架的上下表面,第一支架与第二支架通过燕尾槽2-2连接。
在本发明的一项具体实施中,所述的第一支架采用载有成纤维细胞的水凝胶支架,所述的成纤维细胞用于促进组织修复,起到仿生作用;所述的第二支架采用陶瓷骨架3,所述的陶瓷骨架内部填充载有骨髓间充质干细胞的水凝胶4。所述的陶瓷骨架上下表面孔隙尺寸为50-120微米,陶瓷骨架的内部孔隙尺寸为300-600微米。所述的燕尾槽设置在陶瓷骨架的上下表面,燕尾槽的下底宽度为200-400微米,上底宽度为50-150微米。
在本实施例中,所述的陶瓷骨架上下表面孔隙尺寸为100微米,陶瓷骨架的内部孔隙尺寸为500微米。所述的燕尾槽设置在陶瓷骨架的上下表面,燕尾槽的下底宽度为300微米,上底宽度为100微米。
本发明还提出了一种用于制备上述复合支架的基于3D打印的成型方法,首先采用TCP(磷酸三钙)光敏树脂混合浆料经DLP光固化成型、脱脂烧结形成陶瓷骨架,然后借助PDMS模具在TCP支架上分层浇筑分别载有成纤维细胞与骨髓间充质干细胞的GelMA(甲基丙烯酸化水凝胶)水凝胶并光固化形成。本发明提出的仿生复合支架具有生物相容性,可用于同步修复软硬组织缺损。
本发明采用的PDMS模具是以树脂模具、壳聚糖模具为基础,浇筑热固化成型得到的。
下面对具体的成型过程进行介绍,主要步骤如下:
步骤1:根据已有的硬组织模型,制备陶瓷骨架,所述陶瓷骨架的上表面或者下表面留有起定位作用的凸出边缘;
步骤2:根据已有的软硬组织模型为原型,通过DLP打印得到树脂模具、第一壳聚糖模具和第二壳聚糖模具;所述的硬组织模型、软硬组织模型是根据实际需求,由常规技术手段获得的。
所述的树脂模具与软硬组织模型的外轮廓一致,且与陶瓷骨架相对应的位置预设有形状、大小一致的凸出边缘;本实施例中,树脂模具作为本发明的核心辅助制造模具,其表面光滑,为实心结构,如图4所示。
所述的第一壳聚糖模具和第二壳聚糖模具均由垂直部和水平部连接构成,呈L型结构,如图5所示。
步骤3:将壳聚糖模具粘结在树脂模具的两侧,所述的树脂模具中对应于陶瓷骨架凸出边缘的一面朝上;第一壳聚糖模具的水平部与树脂模具的侧壁中下位置抵接,第一壳聚糖模具的垂直部平行于树脂模具的厚度方向;第二壳聚糖模具的水平部与树脂模具的侧壁底部抵接,与树脂模具下表面平齐,第二壳聚糖模具的垂直部平行于树脂模具的厚度方向;
步骤4:将PDMS与固化剂按比例混合,形成PDMS预聚物,浇筑在培养皿中进行真空脱泡;在本实施例中,优选为PDMS与固化剂按照10:1的质量比混合。
脱泡后,将粘结在一起的树脂模具与壳聚糖模具置于培养皿中,可采用树脂作为粘结剂,本实施例中,采用高度为150mm培养皿;由于浮力作用,树脂模具的底部与培养皿的底部之间留有间隙,本实施例中形成的间隙约1mm,也就是说,会在树脂模具与培养皿底部仍存在一层约1mm厚的PDMS;置于55℃条件下固化过夜,然后将模具从培养皿中取出,通过酸溶液溶解去除壳聚糖模具,形成第一浇筑通道6-1和第二浇筑通道6-2,之后将树脂模具取出,留下具有浇筑管道的PDMS模具5,如图6所示;
步骤5:如图7所示,将步骤1制备得到的陶瓷骨架置于PDMS模具中,通过第一浇筑通道浇筑载有骨髓间充质干细胞的水凝胶,通过第二浇筑通道浇筑载有成纤维细胞的水凝胶,并且在陶瓷骨架上表面浇筑载有成纤维细胞的水凝胶,使陶瓷骨架上表面与PDMS模具平齐;采用蓝光交联固化成型;在本实施例中,所述的水凝胶中预添加0.5%w/v LAP(苯基-2,4,6-三甲基苯甲酰基膦酸锂)作为光交联剂,蓝光交联固化的时间为30s。
步骤6:切开PDMS模具,取出制备好的复合支架。
上述中的水凝胶优选GelMA水凝胶。
在本实施例中,陶瓷骨架制备方法为:
1.1)将TCP粉末、树脂、分散剂按比例混合,得到TCP树脂混合浆料;本实施例中,TCP粉末、树脂、分散剂的质量比为66:29:5,树脂型号为SP700,分散剂型号为BYK111。
1.2)根据已有的硬组织模型,利用DLP将TCP树脂混合浆料光固化成型,由于使用DLP光固化成型时,固化时间因模型切片层厚而异,本实施例中,支架使用20微米层厚切片,优选为曝光功率为30mw/cm
在光固化成型过程中,由于光散射作用,DLP打印产生实际打印线条直径略大于设计直径,易导致支架实际孔隙率低于设计孔隙率,在本发明的预实验中,采用56%的设计孔隙率,最终可获得50%孔隙率支架。本发明采用模型补偿的方式,预先提高孔隙率,解决了DLP打印中孔隙率偏低的问题,设置DLP打印的孔隙率高于实际孔隙率的5%-15%;本实施例中,设置DLP打印的孔隙率高于实际孔隙率的10%。
在一项具体实施中,若打印得到的孔隙率与实际孔隙率之间的误差低于阈值,则进入下一步骤;否则,降低设置的DLP打印的孔隙率,重复进行光固化成型过程。本实施例中,阈值设置2%。
1.3)脱脂烧结:首先在室温下以0.5-1.2℃/min的速率升温至400-500℃,在400-500℃下保温20-40min,随后从400-500℃以1.5-2.5℃/min的速率升温至1100-1300℃,在1100-1300℃下保温100-150min,取出陶瓷骨架空冷。本实施例中,优选为首先在室温下以1℃/min的速率升温至480℃,在480℃下保温30min,随后从480℃以2℃/min的速率升温至1240℃,在1240℃下保温2h,取出陶瓷骨架空冷。
为了顺利实现图7的基于3D打印的成型方法,所述第一壳聚糖模具的垂直部长度为50%-95%的树脂模具厚度,第二壳聚糖模具的垂直部长度与树脂模具厚度一致。
在本发明的一项具体应用中,可以将上述制备得到的仿生复合支架结合辅助连接设备应用于唇腭裂患者的腭裂临床修复,在临床修复过程中涉及到的手术及治疗方法不在本发明的保护范围内,为了使本领域技术人员对本发明的研究意义有更清晰的认知,下面对腭裂临床修复过程进行一下简要说明。
应用于腭裂临床修复的仿生复合支架需要结合患者的实际缺损组织模型进行个性化定制,实际缺损组织模型可采用本领域常规的技术手段即可获得,例如对腭裂处进行CT扫描等。制备得到的仿生复合支架与唇腭裂患者的软硬组织缺损形态相符,可以减少手术创口面积与出血量,减少术后面部发育畸形的可能性,此外还需结合临床上的其他常规技术手段将仿生复合支架缝合在缺损部位,通过其他辅助连接设备固定,降低松动可能。复合支架中的陶瓷骨架可以提供合适的支撑作用与骨引导再生作用,水凝胶仿生的软组织支架覆盖创面,可以有效促进创面愈合,减少外部感染,起到保护作用。
上述只是对本发明的其中一个应用场景的介绍,说明其具备临床意义,但实现上述目的还需结合所应用领域的一些常规技术手段和设备。
附图和实施例中展示的复合支架的结构或者基于3D打印的成型方法的过程只是若干优选实施方式中的一种,应当指出,本发明不限于上述结构和基于3D打印的成型方法。对于本领域的普通技术人员来说,依然可以对前述的技术方案进行修改,或者对其中部分技术特征进行等同替换。而这些修改或替换,在不脱离本发明技术方案本质的前提下,均应认为是本发明的保护范围。
- 一种用于同步修复软硬组织缺损的仿生复合支架及其基于3D打印的成型方法
- 一种用于同步修复软硬组织缺损的仿生复合支架及其基于3D打印的成型方法
