一种骨组织工程支架材料及其制备方法
文献发布时间:2023-06-19 11:54:11
技术领域
本发明属于高新材料技术领域,具体涉及一种骨组织工程支架材料及其制备方法。
背景技术
由创伤、感染、肿瘤等引起的大段骨缺损是骨科临床的常见病症。就数量而言,骨缺损手术已经成为仅次于输血的人体组织移植,临床需求量巨大。传统的骨缺损修复方法包括:自体骨移植、异体同种骨移植、异种骨移植,但这些方法存在较大弊端,大大限制了其临床应用。目前采用组织工程方法构建复合种子细胞、支架材料和生长因子的生物活性人工骨被认为是未来进行骨缺损修复和骨再造最有效的方法之一。
支架材料作为骨组织再生的框架,是骨组织工程研究的中心环节之一,其直接影响种子细胞的生存、迁移、增值、代谢。一种理想的支架材料应具备:①良好的生物相容性、无毒、不致畸,能安全用于人体;②良好的可塑形性与一定的机械强度;③合适的孔径(200~400μm)、高孔隙率(最好达85%以上)的三维多孔结构;④可降解性和降解速率的可控性;⑤无抗原作用;⑥良好的材料/细胞界面,能促进细胞的粘附和增殖;⑦来源不受限制,易消毒、运输方便。目前骨组织工程支架材料主要有天然支架材料、人工合成支架材料和复合支架材料。
天然支架材料主要有天然高分子材料(壳聚糖、甲壳素、透明质酸、胶原等)和天然无机材料(天然珊瑚、人或动物的脱蛋白骨等)。天然支架材料一般无毒、抗原性弱,亲水性、生物相容性及细胞亲和性好且其降解产物氨基酸可被完全吸收,但其缺点是强度较差,降解时间不能精确计算,力学和加工性能不好,质量重复性差。
人工合成支架材料即用物理化学的方法合成的细胞外基质替代物,主要合成的有无机支架材料(羟基磷灰石、磷酸三钙等)和有机高分子支架材料(聚乳酸、聚羟基乙酸等)。无机支架材料具有有良好的生物相容性和骨传导性,并且生物陶瓷类轻度溶解所形成的高钙离子层及微碱性环境,可有效促进骨细胞的粘附、增值和分化。但是存在脆性大,降解性较差,抗折及抗冲击性能不能满足人工骨的要求。有机高分子支架材料易塑形,细胞相容性好,具有可控的降解性和吸收率,降解产物可通过生理代谢途径代谢掉;缺点是亲水性不足,细胞吸附力弱,降解产物会使局部微环境呈酸性,对组织产生不利影响,机械强度不足等。
单纯的天然材料和人工合成材料在应用时各有优缺点,复合支架材料是将二者结合而制备成的支架材料,在性能上取优补短,更符合骨组织工程要求,也可更好的应用于临床骨修复。复合材料集合了多种材料的优点,不但可保证材料有足够的强度,而且能更有效地结合种子细胞及生长因子,同时具有合适的降解速率可匹配骨组织重新构建,并能增加支架材料的骨传递性和骨诱导性。近年来,骨组织工程支架材料的研究热点主要集中于复合材料的研究。复合材料主要有生物陶瓷材料与天然高分子材料的复合,生物陶瓷材料与人工合成材料的复合,生物陶瓷材料的复合等。虽然复合支架材料在各类骨修复中已经取得良好的效果,目前尚无一种骨组织工程支架材料可以解决骨修复中的所有问题,在各类不同骨修复中仍然存在较多的问题,如支架材料降解速率与成骨速率匹配问题。聚乳酸-聚己内酯(PLGA)是一种FDA批准可用于临床的一种有机高分子材料,故以PLGA为有机主体的复合支架材料大量制备,并应用于各类骨修复,但在降解性能与成骨性能匹配方面尚有待进一步改善。PLGA本身降解可调,但降解周期也在半年-几年不等,当与其他材料复合后,其复合支架材料的降解不仅要考虑PLGA自身属性,而且要考虑其他材料对PLGA降解的影响,才能更准确地评价复合支架材料的降解速率,进而需综合调控支架材料的各方面性能才能实现与成骨速率的匹配。因此,目前仍然需要发展新的骨组织工程支架材料及其制备技术,尤其针对各类骨缺损修复中存在的关键细节问题,制备出更符合各类临床骨修复用的支架材料。
介孔生物活性玻璃(Mesoporous bioactive glasses,MGB)是指孔径介于2-50nm的一类多孔生物活性玻璃材料。与传统的无介孔生物活性玻璃相比,MGB具有更高的比表面积、孔体积,表现出更优的成骨性能,并且MBG为无机材料,与聚合物复合后可明显改善聚合物的疏水性能,提高其生物相容性,此外降解后产物主要以离子形式存在,可被人体代谢,对人体并无严重毒害效应,因此MBG已被广泛用作制备复合支架材料的无机成分。
发明内容
本发明主要目的在于提供一种骨组织工程支架材料及其制备方法,本发明所述支架材料具有符合组织工程支架材料的孔径和孔隙率,具有良好的成型性,骨诱导和传导性;并且其降解周期可进行调控,本发明所述骨组织工程支架材料克服了现有支架材料存在如降解周期不可调控,骨诱导性和传导性较差以及制备成本高等不足,并具有良好的促成骨效应,可适用于各类不同骨缺损修复。此外,本发明所述骨组织工程支架材料的制备方法简单,成本低廉,适于放大生产。
为实现上述目的,本发明采用以下技术方案:
本发明提供一种骨组织工程支架材料,所述材料以聚乙交酯-聚己内酯两嵌段为聚合物主体材料,以介孔生物活性玻璃粉为无机生物活性成分;介孔生物活性玻璃粉均匀分散于支架材料内部。
优选地,所述骨组织工程支架材料的孔径为300-450μm,孔隙率为75-80%。
优选地,所述介孔生物活性玻璃粉占所述骨组织工程支架材料重量的10-40%。
进一步优选地,所述介孔生物活性玻璃粉为硅钙磷介孔生物活性玻璃粉或钒掺杂硅钙磷介孔生物活性玻璃粉。
优选地,所述硅钙磷介孔生物活性玻璃粉中SiO
优选地,所述硅钙磷介孔生物活性玻璃粉的制备方法,包括以下步骤:
(1)通风室温条件下0.5-1.0mol/L的盐酸,量取一定量盐酸加入到无水乙醇中,得混合溶液;
(2)首先将模板剂聚环氧乙烷-聚环氧丙烷-聚环氧乙烷三嵌段共聚物(P123)溶解于步骤(1)中的混合溶液中,常温下搅拌直到P123完全溶解,然后加入Ca(NO
(3)全部加完后,在室温条件下连续搅拌24-48h,得到溶胶溶液,再将得到的溶胶溶液转移到培养皿进行诱导蒸发,室温下连续诱导48-120h,将得到干凝胶置于高温煅烧箱式炉,以升温速率1-3℃/min,升温至250-300℃时,保温2-3h,再继续升温至600-700℃,升温速率为1-2℃/min,然后保温6-8h,整个煅烧过程处于空气气氛中,煅烧结束后关闭箱式炉,室温下自然降温至室温,取出样品,最后将得到的除去模板剂的白色粉末研磨,过<325目筛网,即得到可用于制备骨组织工程支架材料的硅钙磷介孔生物活性玻璃粉末。
进一步优选地,所用模板剂P123分子量MW=5800Da,Ca(NO
优选地,所述钒掺杂硅钙磷介孔生物活性玻璃粉的制备方法,具体包括以下步骤:
1)浓盐酸配制:通风室温条件下配置1.6-2.0mol/L的浓盐酸;
2)模板剂的分散:称量模板剂加入上述盐酸中,于30-40℃以搅拌速率1000-3000r/min搅拌0.5h-2h,直至模板剂均匀分散于盐酸溶液中;
3)钙、磷、硅和钒源的引入:在持续搅拌的条件下,首先加入钒源,待其完全溶解后,加入钙源,待其完全溶解后,再加入磷源,最后再加入硅源,硅源、钙源、磷源和钒源之间的摩尔比为80-150:0.5-1:1-5:5-15;
4)水热过程:待加完钒、钙、磷、硅源后,将3)得到的混合体系于35-38℃持续搅拌12-24h,得到溶胶溶液,然后将溶胶溶液在玻璃棒引流下转移到反应釜中,控制温度于90-120℃,水热反应24-72h;
5)收集介孔粉末:反应结束后,自然降温至室温,将4)得到的混合体系4000-7000r/min离心5-10min,倒掉上清液,依次用蒸馏水和无水乙醇各清洗2-5次,然后将粉末转移到方形瓷舟中,置于电热鼓风烘干箱中,温度设置40-60℃,干燥12-24h,得到介孔生物活性玻璃粉末;
6)模板剂去除:将5)得到的介孔生物活性玻璃粉末置于高温箱式炉,升温速率为1-3℃/min,升温至250-300℃时,保温2-3h,再继续升温至600-700℃,升温速率为1-2℃/min,然后保温6-8h,整个煅烧过程处于空气气氛中,煅烧结束后关闭箱式炉,室温下自然降温至室温,取出样品,既得到除去模板剂的白色掺钒的硅钙磷介孔生物活性玻璃粉末。
本发明还提供以上任一项所述骨组织工程支架材料的制备方法,其包括以下步骤:
将聚乙交酯-聚己内酯溶解于六氟异丙醇后,加入介孔生物活性玻璃粉,均匀分散于溶液中,加入致孔剂;经造粒、压模、沥虑,即得。
优选地,聚乙交酯-聚己内酯与六氟异丙醇的固液比为10-15%w/v;聚乙交酯-聚己内酯与致孔剂的质量比为1:6-7。
优选地,为使介孔生物活性玻璃粉均匀分散于溶液中的方法:将加入介孔生物活性玻璃粉加入到溶液中后,2000-4000r/min持续搅拌12h-24h,再超声分散30-60min。
优选地,所述致孔剂为氯化钠,氯化钠颗粒粒径为300-450μm。
优选地,所述造粒,包括以下步骤:将加入致孔剂后的溶液滴加到无水乙醇中进行造粒,其中滴加速率为20-30滴/min,滴加同时伴随搅拌,搅拌速率500-1000r/min;
优选地,所述压模包括以下步骤:造粒后,以1000-2000r/min搅拌速率持续搅拌30-50min后,倒掉无水乙醇,再加入新的无水乙醇,再继续以相同搅拌速率持续搅拌1-5h后,收集沉淀物,将其装入模具中,以8-12MPa压力压制3-5min,即可得到试样;
优选地,所述沥滤包括以下步骤:将压膜后的试样,室温通风条件下干燥12-24h,然后将试样放入水中4000-6000r/min搅拌浸泡72-120h,间隔6-12h换水一次,并随时观察支架的沥滤状况,来调整搅拌速率,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。
与现有技术相比,本发明具有以下优势:
聚乙内酯(PGA)是一种降解速率较快的聚合物,其降解速率比聚乳酸(PLLA)更快;聚己内酯(PCL)是一种降解速率相对较慢的聚合物,因此本发明以PGA和PCL为原料合成的PGA-PCL两嵌段聚合物,具有更可调控的降解周期,并且降解周期范围更广。本发明结合具有优异促成骨性能的MBG以及降解速率可控的PGA-PCL,制备出MBG/PGA-PCL复合支架材料,可实现更优的骨修复效果。
本发明所述支架材料具有符合组织工程支架材料的孔径和孔隙率,具有良好的成型性,骨诱导和传导性;并且其降解周期可进行调控,通过调控介孔生物活性玻璃与聚已醇酸-聚己内酯比例来调控复合支架材料的力学性能、亲疏水性、降解速率以及骨再生修复能力;本发明所述骨组织工程支架材料克服了现有支架材料存在如降解周期不可调控,骨诱导性和传导性较差以及制备成本高等不足,并具有良好的促成骨效应,可适用于各类不同骨缺损修复。本发明所述基于介孔生物活性玻璃/聚乙交酯-聚己内酯复合支架材料的综合物化性能以及促成骨效应,该材料在骨组织工程领域中作为骨修复材料,具有广泛的应用前景。
本发明所述骨组织工程支架材料的制备方法简单,成本低廉,适于放大生产。
附图说明
构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
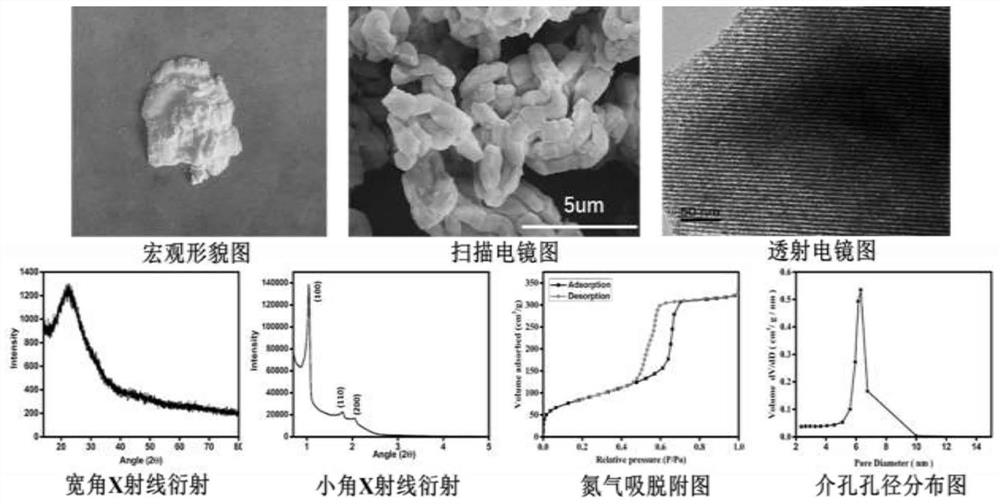
图1为实例1制备的介孔生物活性玻璃的宏观形貌图及其介孔结构性能表征图;
图2为实例2制备MBG/PGA-PCL复合支架材料宏观形貌图;
图3为实例3制备的MBG/PGA-PCL复合支架材料孔隙率变化图;
图4为实例4制备的MBG/PGA-PCL复合支架材料MicroCT三维重建图及扫描电镜图;
图5为实例5制备的MBG/PGA-PCL复合支架材料上硅、钙、磷元素在支架材料上分布图以及EDS能谱图;
图6为实例4-6制备的MBG/PGA-PCL复合支架材料体内降解图;
图7为实例5,7制备的MBG/PGA-PCL复合支架材料体内修复小鼠颅骨缺损图。
具体实施方式
应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作和/或它们的组合。
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
实施例1
一种骨组织工程支架材料的制备方法,包括以下步骤:
⑴介孔生物活性玻璃粉体制备:称取60g无水乙醇加入到烧杯中,再量取1ml0.5mol/L盐酸加入到无水乙醇中,再称取4.0g P123加入到无水乙醇中,常温下搅拌直到P123完全溶解;然后称取1.4g Ca(NO
⑵MBG/PGA-PCL复合支架材料制备:量取10ml六氟异丙醇于小玻璃瓶中,再称量1gPGA-PCL溶解于六氟异丙醇中,室温下以搅拌速率3000r/min持续搅拌2h,直至PGA-PCL完全溶解;称取0.12g MBG粉体边搅拌边缓慢加入到PGA-PCL溶液中,室温下以搅拌速率4000r/min持续搅拌24h后,再超声分散30min,使MBG粉体均匀分散于溶液中得到均匀分散的悬浮液;然后称取6g NaCl颗粒加入到悬浮液中,以1000r/min搅拌速率,连续搅拌10min;然后首先量取250ml无水乙醇加入到烧杯中,在通风橱中将含NaCl颗粒悬浮液通过吸管缓慢滴入无水乙醇溶剂中,其中滴加速率为30滴/min,滴加同时伴随搅拌,搅拌速率500r/min;滴加完悬浮液后,再1000r/min搅拌速率持续搅拌30min后,倒掉无水乙醇,再加入250ml新无水乙醇,再继续以相同搅拌速率持续搅拌3h后,收集烧杯底部沉淀物,将其装入直径12mm的不锈钢圆柱型模具中,在室温下以10MPa压力压制5min,即可得到高度30mm的圆柱型试样;将获得的试样,在室温通风条件下干燥20h,然后将试样装入自制的镂空塑料杯中,放入去离子水中不停地搅拌浸泡96h,搅拌速率为5000r/min,中间间隔6h,换一次去离子水,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。
图1为制备的介孔生物活性玻璃的宏观形貌图及其介孔结构性能表征图。
实施例2
一种骨组织工程支架材料的制备方法,包括以下步骤:
⑴介孔生物活性玻璃粉体制备:称取60g无水乙醇加入到烧杯中,再量取1ml0.5mol/L盐酸加入到无水乙醇中,再称取4.0g P123加入到无水乙醇中,常温下搅拌直到P123完全溶解;然后称取1.4g Ca(NO
⑵MBG/PGA-PCL复合支架材料制备:量取10ml六氟异丙醇于小玻璃瓶中,再称量1gPGA-PCL溶解于六氟异丙醇中,室温下以搅拌速率3000r/min持续搅拌2h,直至PGA-PCL完全溶解;称取0.34g MBG粉体边搅拌边缓慢加入到PGA-PCL溶液中,室温下以搅拌速率4000r/min持续搅拌24h后,再超声分散30min,使MBG粉体均匀分散于溶液中得到均匀分散的悬浮液;然后称取6g NaCl颗粒加入到悬浮液中,以1000r/min搅拌速率,连续搅拌10min;然后首先量取250ml无水乙醇加入到烧杯中,在通风橱中将含NaCl颗粒悬浮液通过吸管缓慢滴入无水乙醇溶剂中,其中滴加速率为30滴/min,滴加同时伴随搅拌,搅拌速率500r/min;滴加完悬浮液后,再1000r/min搅拌速率持续搅拌30min后,倒掉无水乙醇,再加入250ml新无水乙醇,再继续以相同搅拌速率持续搅拌3h后,收集烧杯底部沉淀物,将其装入直径12mm的不锈钢圆柱型模具中,在室温下以10MPa压力压制5min,即可得到高度30mm的圆柱型试样;将获得的试样,在室温通风条件下干燥20h,然后将试样装入自制的镂空塑料杯中,放入去离子水中不停地搅拌浸泡96h,搅拌速率为5000r/min,中间间隔6h,换一次去离子水,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。图2为制备MBG/PGA-PCL复合支架材料所用模具图以及支架材料的宏观形貌图;
实施例3
一种骨组织工程支架材料的制备方法,包括以下步骤:
⑴介孔生物活性玻璃粉体制备:称取60g无水乙醇加入到烧杯中,再量取1ml0.5mol/L盐酸加入到无水乙醇中,再称取4.0g P123加入到无水乙醇中,常温下搅拌直到P123完全溶解;然后称取1.4g Ca(NO
⑵MBG/PGA-PCL复合支架材料制备:量取10ml六氟异丙醇于小玻璃瓶中,再称量1gPGA-PCL溶解于六氟异丙醇中,室温下以搅拌速率3000r/min持续搅拌2h,直至PGA-PCL完全溶解;称取0.12g MBG粉体边搅拌边缓慢加入到PGA-PCL溶液中,室温下以搅拌速率4000r/min持续搅拌24h后,再超声分散30min,使MBG粉体均匀分散于溶液中得到均匀分散的悬浮液;然后称取5g/6g/7g/8g/9g NaCl颗粒加入到悬浮液中,以1000r/min搅拌速率,连续搅拌10min;然后首先量取250ml无水乙醇加入到烧杯中,在通风橱中将含NaCl颗粒悬浮液通过吸管缓慢滴入无水乙醇溶剂中,其中滴加速率为30滴/min,滴加同时伴随搅拌,搅拌速率500r/min;滴加完悬浮液后,再1000r/min搅拌速率持续搅拌30min后,倒掉无水乙醇,再加入250ml新无水乙醇,再继续以相同搅拌速率持续搅拌3h后,收集烧杯底部沉淀物,将其装入直径12mm的不锈钢圆柱型模具中,在室温下以10MPa压力压制5min,即可得到高度30mm的圆柱型试样;将获得的试样,在室温通风条件下干燥20h,然后将试样装入自制的镂空塑料杯中,放入去离子水中不停地搅拌浸泡96h,搅拌速率为5000r/min,中间间隔6h,换一次去离子水,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。图3为制备的MBG/PGA-PCL复合支架材料孔隙率变化图;
实施例4
一种骨组织工程支架材料的制备方法,包括以下步骤:
⑴介孔生物活性玻璃粉体制备:称取60g无水乙醇加入到烧杯中,再量取1ml0.5mol/L盐酸加入到无水乙醇中,再称取4.0g P123加入到无水乙醇中,常温下搅拌直到P123完全溶解;然后称取1.4g Ca(NO
⑵MBG/PGA-PCL复合支架材料制备:量取10ml六氟异丙醇于小玻璃瓶中,再称量1gPGA-PCL溶解于六氟异丙醇中,室温下以搅拌速率3000r/min持续搅拌3h,直至PGA-PCL完全溶解;称取0.12g MBG粉体边搅拌边缓慢加入到PGA-PCL溶液中,室温下以搅拌速率4000r/min持续搅拌20h后,再超声分散40min,使MBG粉体均匀分散于溶液中得到均匀分散的悬浮液;然后称取6g NaCl颗粒加入到悬浮液中,以1200r/min搅拌速率,连续搅拌12min;然后首先量取250ml无水乙醇加入到烧杯中,在通风橱中将含NaCl颗粒悬浮液通过吸管缓慢滴入无水乙醇溶剂中,其中滴加速率为30滴/min,滴加同时伴随搅拌,搅拌速率700r/min;滴加完悬浮液后,再1200r/min搅拌速率持续搅拌50min后,倒掉无水乙醇,再加入250ml新无水乙醇,再继续以相同搅拌速率持续搅拌4h后,收集烧杯底部沉淀物,将其装入直径12mm的不锈钢圆柱型模具中,在室温下以10MPa压力压制5min,即可得到高度30mm的圆柱型试样;将获得的试样,在室温通风条件下干燥24h,然后将试样装入自制的镂空塑料杯中,放入去离子水中不停地搅拌浸泡120h,搅拌速率为5000r/min,中间间隔8h,换一次去离子水,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。图4为制备的MBG/PGA-PCL复合支架材料MicroCT三维重建图及扫描电镜图。
实施例5
一种骨组织工程支架材料的制备方法,包括以下步骤:
⑴介孔生物活性玻璃粉体制备:称取60g无水乙醇加入到烧杯中,再量取1ml0.5mol/L盐酸加入到无水乙醇中,再称取4.0g P123加入到无水乙醇中,常温下搅拌直到P123完全溶解;然后称取1.4g Ca(NO
⑵MBG/PGA-PCL复合支架材料制备:量取10ml六氟异丙醇于小玻璃瓶中,再称量1gPGA-PCL溶解于六氟异丙醇中,室温下以搅拌速率3000r/min持续搅拌3h,直至PGA-PCL完全溶解;称取0.34g MBG粉体边搅拌边缓慢加入到PGA-PCL溶液中,室温下以搅拌速率4000r/min持续搅拌20h后,再超声分散40min,使MBG粉体均匀分散于溶液中得到均匀分散的悬浮液;然后称取6g NaCl颗粒加入到悬浮液中,以1200r/min搅拌速率,连续搅拌12min;然后首先量取250ml无水乙醇加入到烧杯中,在通风橱中将含NaCl颗粒悬浮液通过吸管缓慢滴入无水乙醇溶剂中,其中滴加速率为30滴/min,滴加同时伴随搅拌,搅拌速率700r/min;滴加完悬浮液后,再1200r/min搅拌速率持续搅拌50min后,倒掉无水乙醇,再加入250ml新无水乙醇,再继续以相同搅拌速率持续搅拌4h后,收集烧杯底部沉淀物,将其装入直径12mm的不锈钢圆柱型模具中,在室温下以10MPa压力压制5min,即可得到高度30mm的圆柱型试样;将获得的试样,在室温通风条件下干燥24h,然后将试样装入自制的镂空塑料杯中,放入去离子水中不停地搅拌浸泡120h,搅拌速率为5000r/min,中间间隔8h,换一次去离子水,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。图5为制备的MBG/PGA-PCL复合支架材料上硅、钙、磷元素在支架材料上分布图以及EDS能谱图。
实施例6
一种骨组织工程支架材料的制备方法,包括以下步骤:
⑴介孔生物活性玻璃粉体制备:称取60g无水乙醇加入到烧杯中,再量取1ml0.5mol/L盐酸加入到无水乙醇中,再称取4.0g P123加入到无水乙醇中,常温下搅拌直到P123完全溶解;然后称取1.4g Ca(NO
⑵MBG/PGA-PCL复合支架材料制备:量取10ml六氟异丙醇于小玻璃瓶中,再称量1gPGA-PCL溶解于六氟异丙醇中,室温下以搅拌速率3000r/min持续搅拌3h,直至PGA-PCL完全溶解;称取0.67g MBG粉体边搅拌边缓慢加入到PGA-PCL溶液中,室温下以搅拌速率4000r/min持续搅拌20h后,再超声分散40min,使MBG粉体均匀分散于溶液中得到均匀分散的悬浮液;然后称取6g NaCl颗粒加入到悬浮液中,以1200r/min搅拌速率,连续搅拌12min;然后首先量取250ml无水乙醇加入到烧杯中,在通风橱中将含NaCl颗粒悬浮液通过吸管缓慢滴入无水乙醇溶剂中,其中滴加速率为30滴/min,滴加同时伴随搅拌,搅拌速率700r/min;滴加完悬浮液后,再1200r/min搅拌速率持续搅拌50min后,倒掉无水乙醇,再加入250ml新无水乙醇,再继续以相同搅拌速率持续搅拌4h后,收集烧杯底部沉淀物,将其装入直径12mm的不锈钢圆柱型模具中,在室温下以10MPa压力压制5min,即可得到高度30mm的圆柱型试样;将获得的试样,在室温通风条件下干燥24h,然后将试样装入自制的镂空塑料杯中,放入去离子水中不停地搅拌浸泡120h,搅拌速率为5000r/min,中间间隔8h,换一次去离子水,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。
实施例7
一种骨组织工程支架材料的制备方法,包括以下步骤:
⑴介孔生物活性玻璃粉体制备:称取60g无水乙醇加入到烧杯中,再量取1ml0.5mol/L盐酸加入到无水乙醇中,再称取4.0g P123加入到无水乙醇中,常温下搅拌直到P123完全溶解;然后称取1.4g Ca(NO
⑵MBG/PGA-PCL复合支架材料制备:量取10ml六氟异丙醇于小玻璃瓶中,再称量1gPGA-PCL溶解于六氟异丙醇中,室温下以搅拌速率2000r/min持续搅拌3h,直至PGA-PCL完全溶解;称取0.67g MBG粉体边搅拌边缓慢加入到PGA-PCL溶液中,室温下以搅拌速率3000r/min持续搅拌20h后,再超声分散40min,使MBG粉体均匀分散于溶液中得到均匀分散的悬浮液;然后称取6g NaCl颗粒加入到悬浮液中,以1200r/min搅拌速率,连续搅拌15min;然后首先量取250ml无水乙醇加入到烧杯中,在通风橱中将含NaCl颗粒悬浮液通过吸管缓慢滴入无水乙醇溶剂中,其中滴加速率为30滴/min,滴加同时伴随搅拌,搅拌速率800r/min;滴加完悬浮液后,再1200r/min搅拌速率持续搅拌50min后,倒掉无水乙醇,再加入250ml新无水乙醇,再继续以相同搅拌速率持续搅拌4h后,收集烧杯底部沉淀物,将其装入直径12mm的不锈钢圆柱型模具中,在室温下以10MPa压力压制5min,即可得到高度30mm的圆柱型试样;将获得的试样,在室温通风条件下干燥24h,然后将试样装入自制的镂空塑料杯中,放入去离子水中不停地搅拌浸泡120h,搅拌速率为5000r/min,中间间隔8h,换一次去离子水,最后将沥滤后的支架材料置于室温通风条件下晾干,即可得到最终的骨组织工程支架材料。
实施例8
一种骨组织工程支架材料的制备方法,包括以下步骤:
(1)介孔生物活性玻璃粉体制备:用质量分数37%的浓盐酸于容量瓶中配置1.60mol/L盐酸,再用量筒量取50ml 1.60mol/L盐酸于100ml烧杯中,然后用分析天平称取1.0g P123(MW=5800)溶解于50ml,1.67mol/L盐酸中,水浴37℃条件下持续搅拌1h,直到P123完全溶解,溶液呈透明状态,然后用分析天平称取0.068g Na3VO4·12H2O,持续搅拌条件下缓慢加入溶液中,待其完全溶解后,再称取1.98g Ca(NO3)2·4H2O,持续搅拌条件下缓慢加入溶液中,待其完全溶解后,再逐滴加入0.309ml的TEP,滴加的速率为12滴/min,加完后持续搅拌15min,最后再滴加入3.049ml TEOS,滴加的速率为10滴/min,全部加完后将混合溶液37℃水浴条件下持续搅拌12h,然后将混合溶液在玻璃棒引流下转移到聚四氟乙烯反应釜内胆中,于恒温100℃条件下,水热反应48h,反应结束后,待温度自然冷却至室温时,将得到的混合体系液体转移到50ml离心管中,于4000r/min离心5min,倒掉上清液,依次用蒸馏水和无水乙醇各清洗3次,然后将粉末转移到方形瓷舟中,置于电热鼓风烘干箱中,恒温60℃条件下干燥12h,最后将得到的粉末置于高温箱式煅烧炉中,在空气气氛中以升温速率为1℃/min,升温至250℃时,保温2h,再继续以1℃/min升温速率升温至600℃,然后保温6h,煅烧结束后关闭箱式炉,自然降温至室温,取出样品,既得到除去模板剂的白色介孔生物活性玻璃粉末。
其它步骤均与实施例7所述方法相同。
实例4-6制备的MBG/PGA-PCL复合支架材料体内降解情况如图6所示;实施例5、7制备的MBG/PGA-PCL复合支架材料体内修复小鼠颅骨缺损能力如图7所示。
以上描述仅为结合实际合成技术以及原理的本发明部分实例,本发明不仅仅局限于以上实例,只要在本发明技术方案所涉及的参数范围内,均可制备出MBG/PGA-PCL复合的骨组织工程支架材料,本发明所涉及的技术参数范围包括制备MBG粉末的物料配比;搅拌速率及时间;液体滴加速率;煅烧温度、时间以及制备复合支架材料的PGA-PCL与六氟异丙醇的固液比;MBG掺入比例;PGA-PCL与致孔剂比例;搅拌速率及时间;液体滴加速率;压模压力及时间;沥滤时间等。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 一种用于骨组织工程的光固化复合材料及基于其的骨组织工程支架
- 一种骨组织工程用的多孔羟基磷灰石/壳聚糖复合材料支架及其制备方法
