芳基环丙基类化合物制备方法和用途
文献发布时间:2024-04-18 19:52:40
本发明涉及医药技术领域,具体而言,涉及芳基环丙基类化合物或其对映异构体,非对映异构体,氘代化合物及其药学上可接受的盐。该类化合物制备方法及其在听力损失方面预防/治疗作用。
背景技术
耳聋是人类高发病率的感官或功能缺陷性疾病。耳毒性药物是临床上造成听力损失或障碍的重要原因,同时也是临床上儿童听力损失或障碍的重要原因。由于内耳毛细胞损伤后缺乏再生能力,并且毛细胞的损伤会导致与其相连的螺旋神经节神经元退化,因此,毛细胞及螺旋神经节神经元损伤保护及其机制的研究在耳聋防治中尤为重要。
目前耳毒性药物所致毛细胞及螺旋神经节神经元的损伤保护研究主要集中在以下几个方面:1)减轻氧化应激反应损伤,如抗氧化剂和自由基清除剂等; 2)抑制凋亡信号转导通路,如JNK信号通路、X连锁凋亡抑制蛋白(X-linked inhibitor of apoptosisproteins, XIAP)等;3)表观遗传学调控,如非编码微小RNA(miRNA)调控、DNA甲基化及组蛋白调控等。国内在耳毒性药物损伤听觉保护研究方面已经
取得了一定成果。龚树生等研究表明,TrkB受体激动剂可以保护螺旋神经节神经元抵抗庆大霉素损伤。李华伟等研究表明,过表达XIAP能够使耳蜗毛细胞抵抗新霉素造成的耳毒性损伤。
近年来,表观遗传学调控是分子生物学领域研究的热点,这种调控反映了环境-基因-表型的相互作用,对于维持细胞稳定性具有重要意义。研究发现,表观遗传调控在生物早期发育、胚胎干细胞分化、神经系统发育及肿瘤发生发展过程中起着重要作用。
特异性抑制组蛋白甲基化转移酶G9a/GLP能够维持线粒体稳定性,抑制Caspase-3等经典细胞凋亡通路,从而实现抑制毛细胞凋亡和毛细胞保护的作用。赖氨酸特异性去甲基化酶1 (lysine-specific demethylase1,LSD1)是最早发现的组蛋白去甲基化酶,它通过与
CoREST形成复合物,特异性的作用于组蛋白H3K4 产生去甲基作用。LSD1通过调节H3K4二甲基化水平在器官发育及细胞存活等生命过程中发挥重要作用.
LSD1抑制剂通过提高耳蜗毛细胞中的组蛋白H3K4me2表达水平和/或降低耳蜗毛细胞凋亡标志物Cleaved Caspase-3表达水平,从而抑制细胞凋亡通路,实现抑制耳蜗毛细胞凋亡和耳蜗毛细胞保护的作用。
目前市场上还没有被FDA批准可用于预防或治疗听力损失的药物,在研的小分子化合物包括SENS-401, kenpaullone等。芳基环丙基胺类化合物作为LSD1抑制剂,属于表观遗传药物,与其它在研药物作用机制不同,它通过提高耳蜗毛细胞中的组蛋白H3K4me2表达水平和/或降低耳蜗毛细胞凋亡标志物Cleaved Caspase-3表达水平,从而抑制细胞凋亡通路,实现抑制耳蜗毛细胞凋亡和耳蜗毛细胞保护的作用。
发明内容
本发明的目的在于提供一类具有听力丧失预防/治疗作用的芳基环丙基类化合物,即由通式(I)表示的芳基环丙基类化合物或其对映异构体,非对映异构体,氘代化合物及其药学上可接受的盐。
本发明的另一目的在于提供一种制备上述通式(I)表示的芳基环丙基类或其对映异构体,非对映异构体,氘代化合物或其药学上可接受的盐的方法。
其中:
R
R
术语“烃基”是指烷基、烯基或炔基,例如“C
术语“氘代烃基”是指烷基、烯基或炔基中一个或多个氢原子被氘原子取代,其中“C
术语“C
所述卤原子指氟、氯、溴或碘。
对于具有结构通式(I)的芳基环丙基类化合物的药学上可以接受的盐,包括可药用酸加成盐,通过用无机酸或有机酸处理结构通式(I)化合物的游离碱,可以得到其药学上可接受的盐。所述的无机酸为盐酸、氢溴酸、磷酸或硫酸;所述的有机酸为抗坏血酸、烟酸、柠檬酸、酒石酸、乳酸、马来酸、丙二酸、富马酸、乙醇酸、琥珀酸,丙酸、乙酸,三氟乙酸,甲磺酸,苯磺酸,对甲基苯磺酸等。
本发明的化合物可以以未溶剂化的和与药学上可接受的溶剂(例如水,乙醇等)溶剂化的形式存在。通常,对于本发明的目的,认为溶剂化的形式等同于未溶剂化的形式。
本发明的具有通式(I)的化合物可通过下列合成途径合成,该途径包括类似于化学领域中所熟知者,特别是根据本文说明部分的方法。起始物质一般可由商业来源,如Aldrich化学公司(美国威斯康辛州密尔瓦基)取得,或通过本领域技术人员所熟知的方法即可制备
除非另有说明,在下述反应路线中,所述的化合物的各符号具有相同的含义。为了说明之用,下列所示的反应路线提供用于合成本发明的化合物以及关键中间产物的可能途径。有关个别反应步骤的更详细的说明,请见后述的实施例部分。本领域技术人员将了解可使用其他合成途径合成本发明的化合物。虽然在反应路线中显示及于后述部分论及特定的起始物质与试剂,但其可轻易地以其他起始物质与试剂替代,从而提供多种衍生物和/或适用其他反应条件。此外,鉴于本公开内容,可使用本领域技术人员所熟知的常规化学反应,而进一步修饰通过本文的方法所制备的众多化合物。
本发明提供一种制备上述通式(I)表示的芳基环丙基类或其对映异构体,非对映异构体,氘代化合物或其药学上可接受的盐的方法,该方法按如下反应路线进行:
具体实施方式
通过下列实施例说明本发明的技术方案。然而,应了解本发明保护的范围不限于这些实施例中的特定细节,因为鉴于本发明的公开内容,其他变化对本领域普通技术人员是已知和显而易见的。
提供以下实验例以进一步阐明本发明。
实验样品分析所用仪器及试剂
核磁共振谱由Varian公司的Mercury-400型核磁共振仪测定。LC-MS由ThermoFinnigan LCQDECA×P型质谱仪测定。柱层析分离所用硅胶为青岛海洋化工厂产品(200-300目)。TLC硅胶板为烟台化工生产的HSF-254薄层层析预制板,采用紫外灯,碘缸显色。紫外灯为上海顾村电光仪器厂ZF-1型三用紫外分析仪。合成中所用原料为市售产品;或者通过本领域已知的方法制备;或者根据本文所述方法制备。
实施例
除非另有说明,否则在本说明书实施例的化合物中,立体化合物构型由相对应化合物指示的化学名定义,不过,所绘制的结构可以代表多个具体的构型。然而,本发明涉及本文所述和所定义的化合物的所有立体异构体。因此,本发明包括实施例中所述根据其化学名所定义的化合物,且除此之外,还包括具有相应绘制结构中所示绝对构型的化合物。
使用如下缩写:
Boc: 叔丁基氧基羰基,DMF: N,N-二甲基甲酰胺,EtBr: 溴乙烷, t-BuOH: 叔丁醇,PE: 石油醚,EA: 乙酸乙酯,THF: 四氢呋喃,TEPA:三乙基磷酸酯,TEA: 三乙胺,DMSO:二甲亚砜,Me
实施例1:(反式)-2-(4-乙氧-3-氟苯基)-N-苯基环丙基-1-酰胺
步骤1:
取250ml三口瓶,控温0-5℃,依次加入DMF,对位羟基醛和碳酸钾,再缓慢滴加EtBr,滴加完毕,维持温度20-25℃搅拌反应16-18h,TLC检测原料基本反应完全(PE/EA=10:1,Rf=0.4)。将反应液倾倒入冰水中,搅拌5-10min。抽滤,滤饼用冰水淋洗,20-25℃真空干燥,得白色固体物16.3g,摩尔收率99%。所得粗品无需纯化,直接投入下一步反应。
步骤2:
取250ml三口瓶,控温-5-0℃,依次加入THF,t-BuOK;降温至-15℃ - -10℃滴加TEPA,滴加完毕,维持温度-15℃ - -10℃搅拌反应30min;再滴加对位乙氧基醛/THF溶液,滴加完毕,维持温度-15℃ - -10℃搅拌反应30min,TLC检测原料基本反应完全(PE/EA=10:1,Rf=0.45)。将反应液倾倒入冰水中,用乙酸乙酯萃取两次,合并有机相,用饱和食盐水洗涤,无水硫酸钠干燥,35℃减压浓缩溶剂,得油状物粗品。柱层析纯化(PE/EA=10 : 1),得6.1g白色固体物,摩尔收率93%。
1H NMR(400MHz, CDCl
步骤3:
取50ml三口瓶,控温20-25℃,依次加入DMSO,Me
1H NMR(400MHz, CDCl
步骤4:
取50ml三口瓶,控温20-25℃,依次加入甲醇,苯基环丙基甲酸酯,搅拌溶清;控温20-25℃,滴加氢氧化钠水溶液,滴加完毕,维持温度40-45℃搅拌反应约3h,TLC检测原料苯基环丙基甲酸酯基本反应完全(PE/EA=5 : 1,Rf=0.1)。35℃减压浓缩溶剂至干,得白色固体残余物;向残余物中加入水,用2N 盐酸调PH=3-4,用乙酸乙酯萃取两次,用饱和食盐水洗涤,无水硫酸钠干燥,35℃减压浓缩溶剂,得白色固体粗品,摩尔收率103.0%。所得粗品无需纯化,直接投入下一步反应。
步骤5:
取50ml三口瓶,控温0-5℃,依次加入DMF,HATU,DIPEA和苯基环丙基甲酸, 搅拌0.5 h后,再加入苯胺,反应温度自然升20-25℃,反应16-18h,TLC检测原料基本反应完全,将反应混合物倒入水中,用乙酸乙酯萃取两次,用饱和食盐水洗涤,无水硫酸钠干燥,35℃减压浓缩溶剂得白色固体粗品。柱层析纯化(PE/EA=5 : 1),得0.55g白色固体物,摩尔收率54.5%。
MS(ESI) : m/z=300.1 [M+H].
1H NMR(400MHz, CDCl
对于其它目标化合物,除改变起始原料溴化物和醛以外,按照与实施例1中描述的相同的方法制备。
生物活性测试实施例
1)斑马鱼侧线系统模型的建立
本发明所采用的实验动物为Brn3c:mGFP转基因斑马鱼,养殖方案按照《ZebrafishBook》(http://www.zfin.org)常规进行。建立斑马鱼侧线系统模型如下,其中Brn3c:mGFP转基因斑马鱼的侧线神经系统毛细胞表达绿色荧光蛋白(图1)。
图1:斑马鱼侧线系统模型的建立。图示为5 dpf Brn3c:GFP 转基因斑马鱼侧线器及神经丘的整体观。其中箭头代表初级侧线系统神经丘L1-L5和尾部神经丘T1-T3,星号代表次级侧线系统神经丘。
2)药效试验
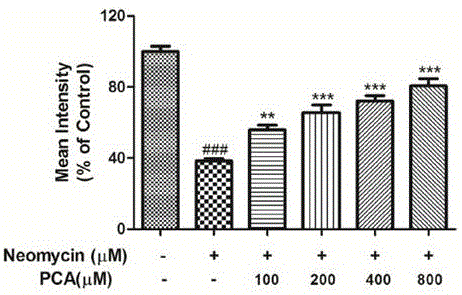
本实验以小分子化合物PCA为代表进行药物筛选。化合物PCA溶于DMSO,该溶液溶于斑马鱼饲养用水,配置浓度分别为100μM,200μM,400μM,800μM。2小时后加入含10μM新霉素Neomycin的斑马鱼饲养用水,1小时后再洗去新霉素,MS-222麻醉5分钟,4%PFA固定2小时,荧光显微镜观察测线器毛细胞存活情况,对存活毛细胞进行计数,结果显示不同浓度PCA处理组毛细胞的数量均高于对照组,证实化合物对毛细胞凋亡保护作用的有效性和特异性。
上述例子仅作为说明的目的,本发明的范围并不受此限制。对本领域的技术人员来说进行修改是显而易见的,本发明以所附权利要求保护的范围为准。
