一种改性镍铁复合氧载体及其制备方法和应用
文献发布时间:2023-06-19 11:17:41
技术领域
本发明属于化学链燃烧氧载体技术领域,具体涉及一种改性镍铁复合氧载体及其制备方法和应用。
背景技术
氢能是一种理想的二次能源载体,在空气中燃烧主要产物为水,不造成任何环境污染,已然成为世界上能源发展的重要方向。但是目前国内外制氢主要来源于化石燃料的重整工艺,其制备需要经历气体净化、合成气重整、变换和变压吸附等过程。这种方式不仅工艺复杂,而且能耗高,制氢效率低;同时合成气自身的价值被忽视,如燃烧供热、发电,或通过费托合成制备乙醇等高值燃料等。化学链技术是一种能源高效转化利用的新方式,通过不同反应器之间的耦合串联,可实现高纯氢和高纯合成气的制备。生物油作为一种能量密度高,易储存的生物质能源形式,近些年来得到了广泛的关注。但生物油直接加氢制生物柴油,用于化学链制氢或合成气则面临氢气纯度低,氧载体失活,团聚烧结等现象。
本申请的发明人在先前提交的专利申请CN202011629463.6,一种镍铁复合氧载体及其制备方法和应用,提出了一种镍体复合氧载体的制备和应用,实现了高纯氢与合成气的共制备,其中合成气的纯度接近80%,且H
因此,还需要对镍铁复合氧载体的进一步改性优化。
发明内容
针对现有技术的以上缺陷或改进需求,本发明提供了一种改性镍铁复合氧载体,通过氧化铈、氧化铝、氧化锆等改性剂的掺杂,改善氧载体的结构稳定性,进一步提高制备的合成气及氢气品质,同时解决镍铁复合氧载体循环性能差的材料缺陷。
为实现上述目的,按照本发明的一个方面,提供了一种改性镍铁复合氧载体的制备方法,将氧化镍,三氧化二铁和改性剂加水混合均匀后干燥得到前驱体,将前驱体在900-1000℃煅烧6-9h,即可获得改性镍铁复合氧载体,所述改性剂为氧化铈、氧化铝、氧化锆中的一种或多种的混合。
作为优选,所述改性剂为氧化铈。
作为优选,所述氧化镍、三氧化二铁和改性剂的质量之比为(15-25):(50-60):(15-25),优选的,所述氧化镍与所述三氧化二铁的质量比为1:4。
作为优选,恒温干燥的温度为100-120℃,干燥时间为6-9h。
作为优选,所述氧化镍,所述三氧化二铁和所述改性剂是通过球磨混合均匀。
按照本发明的另一方面,提供了一种改性镍铁复合氧载体,根据前面所述的制备方法制备而成。
按照本发明的另一方面,提供了改性镍铁复合氧载体的应用,所述应用为基于化学链技术耦合制氢与合成气的应用。
作为优选,包括以下步骤:
(1)将改性镍铁复合氧载体与生物油混合后反应,获得还原态的改性镍铁复合氧载体和合成气;
(2)将还原态的改性镍铁复合氧载体与水蒸气反应,获得氢气,还原态的改性镍铁复合氧载体得到部分氧化;
(3)部分氧化后的改性镍铁复合氧载体通过空气彻底氧化,完成再生。
作为优选,所述步骤(1)中还加入了水蒸气,所述水蒸汽的液体体积与生物油的液体体积之比值为1.2-2。
作为优选,所述步骤(1),步骤(2)和步骤(3)的反应温度为900℃,所述生物油为有机固废热解而成,所述合成气为CO和H2的混合气体。
本发明的有益效果有:
(1)本发明在专利申请CN202011629463.6的基础上加入改性剂,改善氧载体的结构稳定性。其中CeO
(2)本发明改性镍铁复合氧载体活性更高,目标产物选择性跟更强,制氢能力更突出,制备的合成气纯度达到81%,合成气产率进一步提升至2.01Nm
(3)本发明的改性镍铁复合氧载体在共制备氢与合成气中的应用,与现有的化学链技术及先前专利相比,不仅克服了生物油在化学链技术中应用缺陷,促进生物油更加高值化利用,同时长期循环使用中展现了优异的稳定性,更加符合工业的实际应用。
附图说明
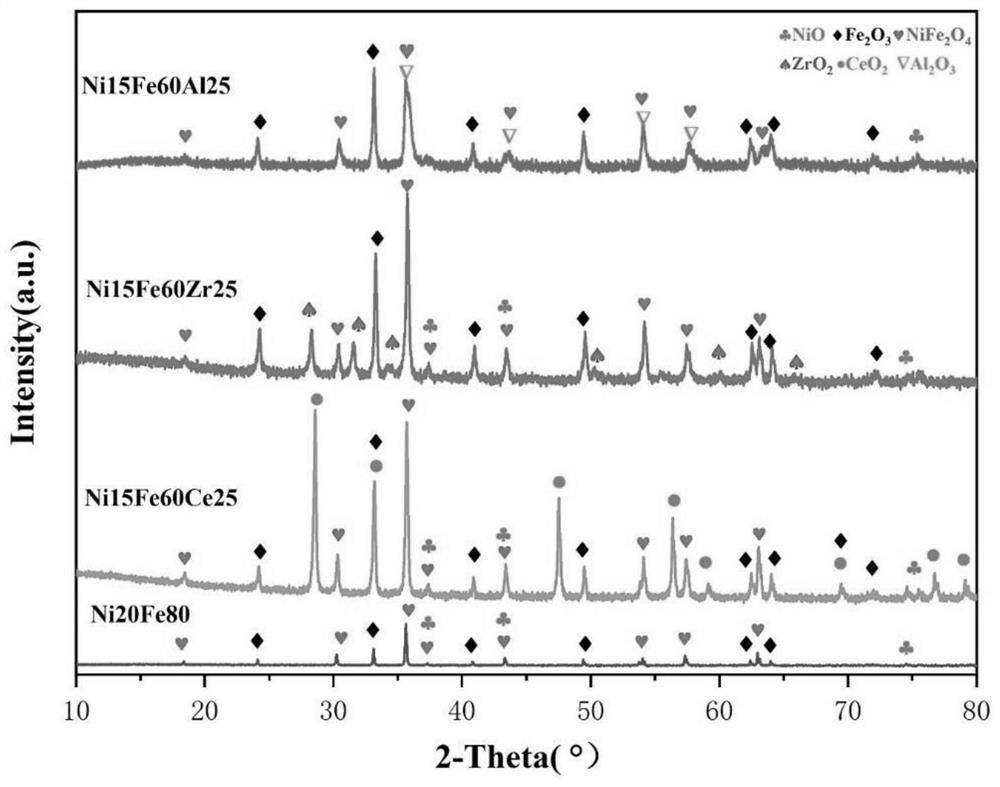
图1是本发明实施例1-3和对比实施例1制备的复合氧载体XRD图。
图2是本发明对比实施例1制备的复合氧载体SEM图。
图3是本发明实施例1制备的复合氧载体SEM图。
图4是本发明实施例2制备的复合氧载体SEM图。
图5是本发明实施例3制备的复合氧载体SEM图。
图6是应用实施例1.1-1.4合成气产率测试图。
图7是应用实施例1.1-1.4氢气纯度测试图。
图8是应用实施例1.1-1.4生物油还原阶段物相结构XRD测试图。
图9是应用实施例2.1-2.4合成气产率测试图。
图10是应用实施例2.1-2.4氢气纯度测试图。
图11是应用实施例2.1-2.4经过5次循环后的复合氧载体XRD图。
图12是应用实施例2.4经过5次循环后的复合氧载体SEM图。
图13是应用实施例2.1经过5次循环后的复合氧载体SEM图。
图14是应用实施例2.2经过5次循环后的复合氧载体SEM图。
图15是应用实施例2.3经过5次循环后的复合氧载体SEM图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
实施例
实施例1
一种CeO
(1)称取15g的氧化镍(NiO)粉末,60g的氧化铁(Fe
(2)将球磨罐中的溶液倒入烧杯,在105℃的恒温干燥箱内,干燥6h,蒸发多余的溶剂水得到前驱体,将前驱体放入马弗炉内,900℃下煅烧6小时,得到镍铁复合氧载体,记为Ni15Fe60Ce25复合氧载体。
实施例2
一种ZrO
(1)称取15g的氧化镍(NiO)粉末,60g的氧化铁(Fe
(2)将球磨罐中的溶液倒入烧杯,在105℃的恒温干燥箱内,干燥6h,蒸发多余的溶剂水,得到前驱体,将前驱体放入马弗炉内,900℃下煅烧6小时,得到镍铁复合氧载体,记为Ni15Fe60Zr25复合氧载体。
实施例3
一种Al
(1)称取15g的氧化镍(NiO)粉末,60g的氧化铁(Fe
(2)将球磨罐中的溶液倒入烧杯,在105℃的恒温干燥箱内,干燥6h,蒸发多余的溶剂水,得到前驱体,将前驱体放入马弗炉内,900℃下煅烧6小时,得到镍铁复合氧载体,记为Ni15Fe60Al25复合氧载体。
对比实施例1
(1)称取20g的氧化镍(NiO)粉末,80g的氧化铁(Fe
(2)将球磨罐中的溶液倒入烧杯,在105℃的恒温干燥箱内,干燥6h,蒸发多余的溶剂水得到前驱体,将前驱体放入马弗炉内,900℃下煅烧6小时,得到镍铁复合氧载体,记为Ni20Fe80复合氧载体。
测试实施例
1.XRD测试测试。将实施例1-3和对比实施例1制备的氧载体进行XRD测试,测试结果如图1所示。三种金属改性后的氧载体与Ni20Fe80一样,都存在Fe
2.SEM测试。将实施例1-4和对比实施例1制备的氧载体进行,测试结果如图2-5所示。三种改性剂掺杂后的氧载体明显分散性更好,具有更丰富的孔隙结构。
应用实施例
1.第一组应用实施例。将氧载体在固定床管式反应器中,先后通入生物油制备合成气,然后通过水蒸汽制备氢气,具体如下所述。
应用实施例1.1Ni15Fe60Ce25复合氧载体
(1)称取10g载氧体放入固定床管式反应器,在空气氛围下升温至900℃,然后再用氮气吹托10min,排净管内空气后,利用注射泵共通入为2.8ml、流速为0.14ml/min的生物油和3.36ml、流速为0.168ml/min的水蒸气;同时利用在线色谱分析尾气组分含量及产率;
(2)待色谱中各气体组分浓度降至0.5%以下,通入10ml,流速为0.165ml/min的去离子水,利用在线色谱分析氢气浓度及产量。
其中,载气流速(空气,氮气)均为500ml/min;色谱对尾气组分记录时间间隔单位为秒,其中尾气各组分含量以500ml/min氮气为基准计算。
应用实施例1.2Ni15Fe60Zr25复合氧载体。
应用实施例1.3Ni15Fe60Al25复合氧载体。
应用实施例1.4Ni20Fe80复合氧载体。
2.第二组应用实施例。本应用实施例与第一组实施例不同之处在于,将复合氧载体进行了5次循环测试,具体如下所述。
应用实施例2.1Ni15Fe60Ce25复合氧载体
(1)称取10g载氧体放入固定床管式反应器,在空气氛围下升温至900℃,然后再用氮气吹托10min,排净管内空气后,利用注射泵共通入为2.8ml、流速为0.14ml/min的生物油和3.36ml、流速为0.168ml/min的水蒸气;同时利用在线色谱分析尾气组分含量及产率;
(2)待色谱中各气体组分浓度降至0.5%以下,通入10ml,流速为0.165ml/min的去离子水,利用在线色谱分析氢气浓度及产量。
(3)再通入空气,待色谱中氧气组分达到21%左右,即说明氧载体得到完全氧化再生;然后继续重复(1)(2)(3),达到5次为止。
其中,载气流速(空气,氮气)均为500ml/min;色谱对尾气组分记录时间间隔单位为秒,其中尾气各组分含量以500ml/min氮气为基准计算。
应用实施例2.2Ni15Fe60Zr25复合氧载体。
应用实施例2.3Ni15Fe60Al25复合氧载体。
应用实施例2.4Ni20Fe80复合氧载体。
将应用实施例1.1-1.4进行合成气产率测试,测试结果如图6所示。从图6中可以看到Ni15Fe60Ce25氧载体相较于Ni20Fe80,合成气产率从1.77Nm
将应用实施例1.1-1.4进行氢气纯度测试,测试结果如图7所示。从图7中可知Ni15Fe60Ce25改性氧载体氢气的纯度及产率相较于Ni20Fe80氧载体进一步得到提升。这是因为Fe
将应用实施例1.1-1.4生物油还原阶段物相结构进行XRD测试,测试结果如图8所示。还原态的Ni15Fe60Ce25氧载体出现了钙钛矿型结构CeFeO
Ni15Fe60Zr25氧载体经过生物油还原后出现了大量Fe
针对Ni15Fe60Al25氧载体,在还原阶段的确发现了惰性尖晶石FeAl
将应用实施例2.1-2.4进行5次循环的合成气产率测试,测试结果如图9所示。从图9可知,Ni15Fe60Ce25氧载体在5次循环中合成气的产率在,合成气纯度维持在81%左右;Ni15Fe60Zr25氧载体的合成气产率在,合成气纯度随循环次数增加略有提升。但是Ni15Fe60Ce25与Ni15Fe60Zr25两种改性后的氧载体在多次循环中相比Ni20Fe80有更高的合成气纯度及产率。而Ni15Fe60Al25氧载体合成气的产率及纯度随循环次数增加而不断上涨,根据研究可以推测这可能是由于在多次循环过程中惰性尖晶石FeAl
将应用实施例2.1-2.4进行氢气纯度测试,测试结果如图10所示。由图10可知,Ni15Fe60Ce25在5次循环制氢过程中,不仅氢气产率最高并且氢气纯度一直维持在96%左右,制备氢与合成气的性能得到进一步的提升,同时表现出了优异的循环稳定性。而这则表明了CeO
Ni15Fe60Zr25同样在5次循环过程中表现出了优异的循环稳定性,这是因为ZrO2具有更强的结构稳定性,能够在多次循环保证氧载体孔隙结构不发生明显变化,从而保证晶格氧的释放速率稳定。但是Ni15Fe60Zr25氢气产率及纯度则相对较低,这是因为ZrO
同样的,Ni15Fe60Al25氧载体制氢能力明显降低是因为两种惰性尖晶石结构FeAl
将应用实施例2.1-2.4 5次循环后的复合氧载体进行XRD测试,测试结果如图11所示。Ni20Fe80氧载体中的NiFe2O4结构出现了明显的相分离,而Ni15Fe60Ce25,Ni15Fe60ZrO2,Ni15Fe60Al25三种改性氧载体中NiFe2O4的结晶度仍很高,说明改性金属的添加保证了氧载体结构的稳定。但是Ni15Fe60Al25依旧有FeAl2O4的物相结构,这对于产氢来讲是不利的。因此,结合上述讨论分析可得Ni15Fe60Ce25是最佳的改性氧载体。
将应用实施例2.1-2.4 5次循环后的复合氧载体进行SEM测试,测试结果如图12-15所示。Ni20Fe80氧载体出现了明显的孔隙结构坍塌,表面团聚现象明显,而Ni15Fe60Ce25,Ni15Fe60ZrO2,Ni15Fe60Al25三种改性氧载体的结构依旧稳定,这说明了三种改性金属的添加对氧载体的循环稳定性起到了积极的作用。其中Ni15Fe60Ce25氧载体的孔隙结构更为明显,这对于晶格氧的释放是有利的,同时也证明了上述相关测试结果。
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 一种改性镍铁复合氧载体及其制备方法和应用
- 一种LaFeO3-(Cu-Al@Al2O3-CoO)高温复合相变蓄热氧载体的制备方法与应用
