用于改变流体中的颗粒的浓度的系统和方法
文献发布时间:2023-06-19 12:02:28
技术领域
本发明涉及通过改变流体中的颗粒的浓度来进行流体分级和富集的领域。特别地,本发明涉及使用与声波发生器相关联的系统来改变流体中的给定颗粒组的浓度。
背景技术
在本领域中,对于分离颗粒悬浮液、特别是细胞悬浮液如全血、骨髓或脑脊液,或矿物悬浮液如矿浆或泥浆中的成分,基于过滤或离心方法的系统是公知的。
在典型的血液分级过程中,全血被收集在第一管中,然后离心以将全血分离成其成分。通过将空管连接至第一管并操作阀,血液成分被传送至其他管。所述血液成分可以是红细胞、血小板、血浆等。
然而,全血的过滤或离心产生了几个问题。离心的高旋转速度允许全血分层,从而分离其成分,但也会引起对细胞的强烈的剪切。血细胞也可能因过滤而受损,因为它们被迫通过膜孔。过滤和离心过程也是昂贵的,需要对设备进行彻底的清洁,对于分离全血成分不是100%有效的,耗时并且需要对样品进行繁重的操作。
全血成分的声泳分离克服了这些缺点中的许多。实际上,因为它不需要任何旋转或机械力,并且施加的声学力较低,因此防止了血液成分的损坏。
在全血成分的典型声泳分离中,全血被引入通道中,并且在所述通道内产生超声场。这使得能够在通道中产生声压节点。全血成分迁移到声压节点以允许选择性分离。
文献WO2017/191289公开了使用多血袋系统对全血成分进行的这种声泳分离。所述系统包括串联布置的若干血液收集袋和用于传送流体的传送装置。全血被引入系统中,并在传送设备中经受连续的声泳分离,从而导致其成分的分离。然而,因为不可能执行分离的循环并且成分的一部分能够逃出声泳分离,因此这种系统不允许全血成分的100%有效分离。
类似的问题出现在除血液分级之外的领域中,例如水去污或需要改变流体中颗粒浓度的其他领域。
考虑到上述现有技术,本发明的一个目的是提供一种简单、廉价的系统,该系统允许以最佳效率改变流体中的一个或多个颗粒组的浓度,特别是对流体分级、使流体富一种或若干成分、使流体贫一种或若干成分。
本发明的另一目的是提供一种用于改变流体中的一个或若干颗粒组的浓度的简单且快速的方法。
发明内容
为此,本发明涉及一种用于改变流体中包含的至少一个给定颗粒组的浓度的系统,该系统包括:
-第一容器和第二容器;
-第一传送设备和第二传送设备,其中,第一容器流体地连接至第一传送设备的入口,并且第二容器流体地连接至第二传送设备的入口,第一传送设备和第二传送设备中的每一个包括:
腔室,其配置成与用于在腔室内产生声波的至少一个声波发生器相关联;
至少两个出口,所述至少两个出口包括用于富所述给定颗粒组的流体的第一出口和用于贫所述给定颗粒组的流体的第二出口;
第一出口流体地连接至第一容器,并且第二出口流体地连接至第二容器;以及
-用于使第一和第二容器中的每一个中的流体的体积保持恒定的装置。
在本发明中,表述“改变流体中包含的至少一个给定颗粒组的浓度”包括增加所述浓度或降低所述浓度,特别是为了分级、使流体富至少一个给定颗粒组或使流体贫至少一个给定颗粒组。
本发明的系统能够用于将流体分级为多个给定颗粒组。
根据所产生的声波的波长和通道的几何形状,所述给定颗粒组中的颗粒选择性地被引导至每个传送设备的第一出口。例如,在腔室具有包括第一中心出口和两个第二周边出口的三个出口的情况下,所述颗粒被引导至第一中心出口。
在一个实施例中,本发明的系统包括流量控制装置,用于在系统内施加受控的流量,特别是施加从容器的出口到传送设备的入口以及从传送设备的出口到容器的入口的受控的流量。
根据一个实施例,所述流量控制装置包括控制单元、用于执行表示第一容器和/或第二容器中的流体的体积的测量结果的测量装置以及用于在系统内施加流体流动的流动装置。
根据一个实施例,控制单元被配置成通过根据表示第一容器和/或第二容器中的流体的体积的测量结果来调节在系统中循环的流体的流速以使第一容器和第二容器中的每一个中的流体的体积保持恒定。在该实施例中,系统中流体的流动优选地始终被控制。
在一个实施例中,测量装置被配置成测量第一容器和/或第二容器中的流体的体积,以及/或者第一容器和/或第二容器的重量,以及/或者第一容器和/或第二容器中的流体流速。例如,测量装置可以是称重秤、流量计或用于测量重量、体积、流量或本领域已知的代表体积的任何其他值的任何其他装置。
在一个实施例中,表示第一容器和/或第二容器中的流体的体积的测量结果是第一容器和/或第二容器中的流体的体积的测量结果,以及/或者第一容器和/或第二容器的重量的测量结果,以及/或者第一容器和/或第二容器中的流体流速的测量结果。特别地,流体流速有利地在第一容器的入口处和/或第二容器的入口处测量。
在一个实施例中,第一容器和/或第二容器被实时称重以确保它们的重量保持恒定并且流速被电子调节。
在一个实施例中,流动装置被配置成调节第一和第二容器以及第一和第二传送设备的入口处的流速。在该实施例中,所述流动装置与测量装置协同工作,以确保第一和第二容器中的每一个中的流体的体积是恒定的。通常,流动装置施加的流速通过测量装置来控制,该测量装置测量容器中的流体的体积、和/或容器的重量、和/或容器中的流体流速。
在一个实施例中,流动装置位于第一和第二容器以及第一和第二传送设备的出口处。
在一个实施例中,流动装置包括泵,例如蠕动泵、齿轮泵、离心泵、隔膜泵、旋转叶片泵、活塞泵、压力泵、重力以及它们的衍生物。在一个实施例中,流动装置包括阀。在该实施例中,所述流动装置调节第一和第二容器以及腔室的入口处的流速,以防止完全排空第一和/或第二容器。
在一个实施例中,在第一和第二传送设备中的每一个的入口处的流体流速为0.1mL/min至50mL/min。
在一个实施例中,在第一和第二容器中的每一个的入口处的流体流速为0.1mL/min至50mL/min。
在一个实施例中,本发明的系统包括至少三个出口,所述至少三个出口包括用于富所述给定颗粒组的流体的第一中心出口和用于贫所述给定颗粒组的流体的两个第二周边出口。在该实施例中,当在腔室中施加声场时,给定颗粒组迁移到在腔室的中心产生的声压节点并且在第一中心出口处被输送,而流体的其他成分在腔室的侧面上的第二周边出口处被输送。
在一个实施例中,本发明的系统是闭环系统。在该实施例中,流体在系统中循环若干次,直到第二容器中的给定颗粒组的浓度达到预定水平。
在一个实施例中,所述预定水平等于或低于所述颗粒的纯度要求。所述要求可以是监管要求或客户要求。
在一个实施例中,本发明的系统是闭环分离器。它能够用于使给定颗粒组从流体中分离和/或使所述流体富集所述颗粒组。
在一个实施例中,本发明的系统是无菌的。
在一个实施例中,本发明的系统是封闭系统。
在一个实施例中,该系统是一次性的。在该实施例中,一次性确保良好的卫生、规章遵从性并节省时间。在该实施例中,系统在每次使用之后被更换。
根据一个实施例,系统及其所有部件是可消毒的。在该实施例中,能够使用清洁浴、消毒擦或本领域技术人员已知的任何其他方式对系统进行消毒。
在一个实施例中,系统是便携式系统。在该实施例中,系统的尺寸和所述系统的每个部件之间的连接允许所述系统容易被运输。
在一个实施例中,流体是液体。
在一个实施例中,流体是选自包括以下项的组中的生物流体:人类和/或非人类细胞悬浮液、细胞簇悬浮液、血液、全血、手术血、富血小板血浆、血沉棕黄层、尿液、血清、淋巴液、流体化粪便、脂肪组织、骨髓、脑脊液、精子、脐带血、乳液、唾液、组织、蛋清、贝类混合物或者它们的混合物。
在一个实施例中,流体能够是但不限于:缓冲介质、水、油、泥浆、空气或它们的混合物。
在一个实施例中,第一容器和/或第二容器中包含的流体是选自包括以下项的组的生物流体:人类和/或非人类细胞悬浮液、血液、全血、手术血、富血小板血浆、血沉棕黄层、尿液、血清、淋巴液、流体化粪便、脂肪组织、骨髓、脑脊液、精子、脐带血、乳液、唾液、组织、蛋清、贝类混合物或者它们的混合物。
在一个实施例中,包含在第一容器和/或第二容器中的流体能够是但不限于:缓冲介质、水、油、泥浆、空气或它们的混合物。
根据一个实施例,缓冲介质是用于保存和/或用于抗凝的添加剂溶液。根据一个示例性实施例,用于保存的添加剂溶液例如是SAG-甘露糖醇(SAGM)、PAS III M或SSP+。
根据一个示例性实施例,用于抗凝的添加剂溶液例如是柠檬酸盐-磷酸盐-葡萄糖溶液(CPD)。
在一个实施例中,颗粒选自包括以下项的组:生物细胞、分散介质中的分散细胞、单分散或多分散细胞、血细胞、血小板、红细胞、白细胞、癌细胞、干细胞、祖细胞、细菌、蛋白质、脂质体、细胞器、细胞簇、病毒、囊泡、微粒、纳米颗粒、微泡、微珠、微生物、寄生虫、藻类、沙子、沉积物、灰尘、抗体、粉末、配子、寄生虫卵、浮游生物、组织、脂肪、花粉、孢子、金属颗粒或者它们的混合物。
在多分散细胞的情况下,细胞之间的尺寸差异可以使得细胞能够根据它们朝向沿着腔室的厚度产生的声压节点的迁移速度的差异而被分离。
根据一个实施例,生物流体是全血,并且本发明的系统允许在不进行离心的情况下对血液制品进行分级以及使血液制品富例如红细胞(RBC)、白细胞(WBC)、血小板、诸如贫血小板血浆(PPP)或富血小板血浆(PRP)的血浆。
在一个实施例中,颗粒的平均尺寸为1nm至1mm。小蛋白质的平均尺寸通常为约1nm,而细胞簇的平均尺寸能够高达1mm。
在一个实施例中,声波的波长大于待分离的颗粒的平均尺寸,优选地大于或等于该平均尺寸的十倍。
在一个实施例中,至少在沿着产生声波的纵向轴线的位置处,腔室的厚度大于或等于待分离的颗粒的平均尺寸的十倍。
在一个实施例中,流体包括待从流体分离的多于一个颗粒组,例如2、3、4、5、6、7、8、9、10个颗粒组。在该实施例中,不同波长的声波被用于从流体分离每个颗粒组。
在一个实施例中,流体富多于一个颗粒组,例如2、3、4、5、6、7、8、9、10个颗粒组。
在一个实施例中,流体贫多于一个颗粒组,例如2、3、4、5、6、7、8、9、10个颗粒组。
在一个实施例中,第一容器中的流体能够富至少一个颗粒组,而第二容器富至少另一个颗粒组。
在一个实施例中,系统的部件之间的连接是无菌的。
在一个实施例中,第一和第二容器各自被配置成包含流体,包含在第一容器中的流体富至少一个给定颗粒组,并且包含在第二容器中的流体贫所述颗粒组。
在一个实施例中,第一和第二容器中的每一个是流体被传送、储存或收集到其中的腔室、生物反应器、瓶、袋、囊、小瓶、储存器、模块或瓶。
在一个实施例中,第一容器和第二容器具有相同的体积。
在一个实施例中,第一容器和第二容器具有不同的体积。
在一个实施例中,第一容器的体积与第二容器的体积之间的比率为0.1至10。
控制第一和第二容器中的流体的体积或所述体积之间的比率允许根据流体的体积和给定颗粒组的浓度对收集在第一容器中的最终流体进行控制。
在一个实施例中,第一容器具有至少一个入口和至少一个出口。
在一个实施例中,第一容器具有一个入口,该入口配置成将流体添加到所述容器中,并且流体地连接至腔室的第一出口。
在一个实施例中,第二容器具有至少一个入口和至少一个出口。
在一个实施例中,第二容器具有一个入口,该入口配置成将流体添加到所述容器中,并且流体地连接至腔室的第二出口。
在一个实施例中,第一容器具有两个入口:第一入口,其配置成将流体添加到所述容器中,以及第二入口,其流体地连接至腔室的第一出口。
在一个实施例中,第二容器具有两个入口:第一入口,其配置成将流体添加到所述容器中,以及第二入口,其流体地连接至腔室的第二出口。
在一个实施例中,第一和第二容器是一次性的。在该实施例中,一次性确保良好的卫生、监管要求并节省时间。在该实施例中,第一和第二容器在每次使用后被更换。
在一个实施例中,第一和/或第二容器具有由隔膜封闭的第二入口,从而允许使用针对其内容物进行注射或取样。
在一个实施例中,第一和/或第二容器具有第二入口,该第二入口允许它们流体地连接至另一容器,以便在分离过程之前将其内容物分配到第一和/或第二容器中。
在一个实施例中,第一和/或第二容器流体地连接至至少一个静脉穿刺针。在本实施例中,所述静脉穿刺针能够与受试者的静脉连接。静脉穿刺针可以用于将血液从所述受试者传送至第一和/或第二容器,并且在在传送设备中通过至少一次之后将富集的血液传送回所述受试者。
在一个实施例中,第一和第二容器和/或腔室包含生物相容的、抗微生物的和/或低过敏性的材料。生物相容材料是有利的,因为它允许与生物流体接触。抗微生物和/或低过敏性材料是有利的,因为它防止与流体接触时的不期望的微生物的生长和/或过敏。
在一个实施例中,所述材料的示例包括但不限于:聚合物,例如有机聚合物或无机聚合物;金属,例如不锈钢;凝胶,例如水凝胶;玻璃,例如熔融石英,耐热玻璃;晶体,例如硅;陶瓷,例如碳化硅;或它们的混合物。
在一个实施例中,聚合物的示例包括但不限于:聚氨酯、硅酮、聚乙烯、聚(甲基丙烯酸甲酯)(PMMA)、聚甲基戊烯、聚苯乙烯、聚碳酸酯、聚二甲基硅氧烷或它们的混合物。
在一个实施例中,第一和第二传送设备不是串联布置的。在该实施例中,容器中包含的流体在第一和第二传送设备中不被声波连续处理。
在一个实施例中,第一和第二传送设备被平行布置。在该实施例中,在被收集在第一或第二容器中之前,利用第一和第二传送设备中的声波同时地处理容器中包含的流体,从而确保所述容器的每一个中的流体的体积始终保持恒定。
在一个实施例中,第一和第二传送设备是一次性的。在该实施例中,一次性确保良好的卫生、监管要求并节省时间。在该实施例中,第一和第二容器在每次使用后被更换。
在一个实施例中,第一或第二传送设备的每一个包括与腔室流体连通的至少一个入口,所述入口流体连接至第一或第二容器中的一个。
在一个实施例中,每个传送设备的腔室沿纵向轴线延伸,具有横截面,该横截面具有沿第一横向轴线测量的宽度和沿垂直于第一横向轴线的第二横向轴线测量的厚度,该宽度大于或等于该厚度,腔室具有沿第二横向轴线的第一壁和第二壁。
在一个实施例中,腔室具有圆柱形形状或平行六面体形状。
在一个实施例中,腔室是通道。
在一个实施例中,腔室的宽度/厚度比大于1。
腔室的厚度等于沿第二横向轴线测量的第一壁和第二壁分开的距离。
在一个实施例中,腔室的厚度为10μm至1mm。
在一个实施例中,腔室是微通道,即腔室在其整个长度上具有等于或小于1mm的厚度。
在一个实施例中,声波具有波长λ,并且腔室的厚度基本上等于λ/4的倍数。
在一个实施例中,腔室的厚度沿着腔室的纵向轴线是恒定的或可变的。
在一个实施例中,腔室的宽度大于0.1mm。
在一个实施例中,腔室的宽度沿着腔室的纵向轴线是恒定的或可变的。
在一个实施例中,腔室在其长度的至少一部分上、特别是在其整个长度上具有矩形、正方形、卵形或圆形的横截面。
在一个实施例中,腔室沿纵向轴线的长度大于1cm。
在一个实施例中,第一或第二传送设备中的每一个包括至少一个反射器,所述至少一个反射器沿着纵向轴线与所述至少一个声波发生器相对地定位。
在一个实施例中,反射器是由金属、优选地为钛或不锈钢制成的层。
在一个实施例中,反射器是自由空气或泡沫状材料例如软木的层。
在一个实施例中,反射器是在传送设备的腔室外部的自由空气的层。
在一个实施例中,由于一方面反射器与另一方面流体和壁的材料之间的阻抗差异,声波在腔室的第一壁与第二壁之间来回发生多次反射。
在一个实施例中,反射器的声反射系数为0.5至1,优选地为0.75至1,更优选地为0.9至1。根据一个实施例,第二壁(即,反射器层)由声反射系数表现为0.5至1、优选地为0.75至1、更优选地为0.9至1的材料制成。
在一个实施例中,反射器包括具有与流体的声阻抗不同的声阻抗的材料。
在一个实施例中,反射器包括具有比流体的声阻抗差的声阻抗的材料。
在一个实施例中,反射器包括具有比流体的声阻抗优的声阻抗的材料。
在一个实施例中,腔室的第一和/或第二壁、优选地为第一壁和第二壁两者包括具有与流体的声阻抗相似的声阻抗的材料。
在一个实施例中,面向与声波发生器耦合的第一壁的第二壁包括具有比流体的声阻抗大至少十倍的声阻抗的材料。在腔室的壁中使用具有高声阻抗的材料是有利的,因为其通过促进显著压力极值的形成而改善了颗粒的声聚焦。
在一个实施例中,腔室的第一和/或第二壁、优选地为第一壁和第二壁两者包括选自以下项的组的材料:矿物玻璃、有机玻璃、石英、热塑性材料例如PMMA或聚碳酸酯、金属或它们的混合物。
在一个实施例中,腔室的第一和/或第二壁可以是板、圆柱体或球体的部分的形式。
在一个实施例中,腔室的第一和/或第二壁是不透明的,即腔室的第一和/或第二壁不是光学透明的,即它们对于200nm至50μm的波长不透明。
在一个实施例中,腔室的第一和/或第二壁是光学透明的,即它们对于200nm至50μm的波长是透明的。如果期望获取腔室内存在的诸如细胞的颗粒的图像,则该实施例是特别有利的。
在一个实施例中,第一传送设备和/或第二传送设备包括与腔室流体连通的单个入口。
在一个实施例中,第一传送设备和/或第二传送设备包括沿腔室的长度布置的多个声波发生器。所述声波发生器位于腔室的同一侧。替选地,所述声波发生器彼此相对地定位。
当流体以高速流动时或者当要产生大颗粒层时,使用多个声波发生器是有利的。在第一种情况下,发电机下的飞行时间随着流体速度的增加而减少。这可能需要使用较多数量的换能器以实现聚焦。在第二种情况下,例如在没有流动的情况下,可以使用多个声波发生器来形成大颗粒层。
当使用多个声波发生器时,它们中的至少一个可以沿着腔室的宽度产生声波。
在一个实施例中,声波发生器是压电换能器、宽带声波发生器或电磁振动器。
在一个实施例中,声波发生器在腔室的外部。
在一个实施例中,第一传送设备和/或第二传送设备还包括耦合到声波发生器的发射器层。
在一个实施例中,声波发生器与腔室的第一壁耦合。
在一个实施例中,例如,声波发生器通过干声耦合与腔室的第一壁耦合。在所述实施例中,第一壁是发射器,而第二壁是反射器层。
根据一个实施例,至少一个声波发生器利用耦合层耦合至第一壁(即,发射器层)。
根据一个实施例,所述耦合层由热塑性弹性体、热塑性聚氨酯或硅树脂制成。
根据一个实施例,所述耦合层由油或包含油的混合物制成。
根据一个实施例,第一壁(即,发射器层)的声导系数为0.5至1,优选地为0.75至1,更优选地为0.9至1。根据一个实施例,第一壁(即,发射器层)由声导系数表现为0.5至1、优选地为0.75至1、更优选地为0.9至1的材料制成。
在一个实施例中,声波发生器例如通过粘结或本领域已知的任何其他方式集成在腔室的第一壁内。
在一个实施例中,声波发生器可以例如固定至腔室的第一壁。这种固定可以通过本领域技术人员已知的任何方式进行,特别是通过胶合进行。
在一个实施例中,反射器可以例如固定至腔室的第二壁。这种固定可以通过本领域技术人员已知的任何方式进行,特别是通过胶合进行。
在一个实施例中,反射器可以例如暂时放置在腔室的第二壁上。
在一个实施例中,声波发生器可以被提供正弦电压。在一个变型中,声波发生器可以被提供有三角波或方波电压。
在一个实施例中,声波发生器可以通过数字或模拟控制来操作。
在一个实施例中,在声波发生器与腔室的第一壁之间可以存在声匹配材料层。可以通过使用本领域技术人员已知的任何适于该目的的材料来提供声匹配。
在一个实施例中,声波发生器产生体声波、表面声波驻波、多维声波或声学驻波。
在一个实施例中,声波发生器在腔室的厚度上而不是在腔室的宽度上产生声力场。该实施例是特别有利的,因为它允许形成颗粒层。
在一个实施例中,声波发生器在腔室的厚度和宽度上产生声力场。该实施例是特别有利的,因为可以使颗粒组根据它们的尺寸在腔室的任何区域中移动,并且因此可以分选和分级诸如生物流体的颗粒悬浮液。
在一个实施例中,声波相对于腔室的纵向轴线的入射角为85°至95°,例如89°至91°。
在一个实施例中,声波相对于腔室的纵向轴线的入射角基本上为90°。
在一个实施例中,声波的波长λ为5μm至2cm。
在一个实施例中,声波发生器在频率f下操作,该频率f能够不同于腔室沿第二横向轴线的共振频率f
表述“f
在一个实施例中,声波发生器在等于或小于100MHz的频率下操作,特别是在0.05至100MHz的频率下操作。该实施例是特别有利的,因为其允许在不损伤活细胞的情况下处理它们。
在一个实施例中,声波发生器优选地以不同于f
在一个实施例中,至少一层颗粒例如细胞通过声聚焦形成。
在一个实施例中,通过所产生的声波在流体内形成至少一个声压极值。
颗粒层优选地聚焦在由所产生的声波在流体内形成的声压极值(声波节或波腹)处。例如,形成多个不同颗粒层,这些层中的每一个都存在于不同的声压极值处。
在该实施例中,细胞层可以在腔室中的声压极值处形成,从而允许第一容器中的流体富所述细胞。
所形成的颗粒层可以具有沿腔室的纵向轴线伸长的形状,并且当在垂直于聚焦平面的方向上观察时,可为例如椭圆形或矩形形状。在一个变型中,当沿垂直于其聚焦平面的方向观察时,所形成的颗粒层可以具有圆形或正方形形状。
在一个实施例中,系统的不同部件之间的流体连接包括本领域技术人员已知的任何装置,例如柔性歧管或管以及夹具或阀。它们在附图中的表示不代表它们的尺寸和位置。
在一个实施例中,本发明的系统还包括第三容器和第三传送设备。
在一个实施例中,本发明的系统包括多个容器和多个传送设备。在该实施例中,每个容器可以连接至一个传送设备,即容器的数量等于传送设备的数量,或者每个容器可以连接至多于一个传送设备,通常是两个传送设备。该实施例是特别有利的,因为它允许分离流体中的多于一个颗粒组。
在一个实施例中,本发明的系统还可以包括被设计成允许通过非侵入性装置进行测量的若干设备,所述非侵入性装置包括但不限于声学、光学或电磁装置。
本发明还涉及一种用于借助于系统来改变流体中包含的至少一个给定颗粒组的浓度的方法,所述系统包括:
-第一容器和第二容器;
-第一传送设备和第二传送设备,每个传送设备包括:
腔室,其配置成与用于在腔室内产生声波的至少一个声波发生器相关联;
入口和至少两个出口,所述至少两个出口包括用于富所述给定颗粒组的流体的第一出口和用于贫所述给定颗粒组的流体的第二出口;
该方法包括以下初步步骤:
(a)将一定体积的流体引入第一容器中并将一定体积的流体引入第二容器中;
(b)通过在第一和第二传送设备中的每一个的腔室内部产生声波来施加声场;
随后的步骤是:
(c)同时地将包含在第一容器中的流体传送至第一传送设备的腔室中以及将包含在第二容器中的流体传送至第二传送设备的腔室中;
(d)同时地将从第一和第二传送设备的第一出口收集的富所述给定颗粒组的流体传送至第一容器中以及将从第一和第二传送设备的第二出口收集的贫所述给定颗粒组的流体传送至第二容器中;
其中,在步骤(c)和(d)期间,第一和第二容器中的相应的流体体积保持恒定。
在一个实施例中,该方法包括以下步骤:
(a’)提供如上所述的本发明的系统;
(a)将一定体积的流体引入第一容器中并将一定体积的流体引入第二容器中;
(b)通过在第一和第二传送设备中的每一个的腔室内部产生声波来施加声场;
随后的步骤是:
(c)同时地将包含在第一容器中的流体传送至第一传送设备的腔室中并且将包含在第二容器中的流体传送至第二传送设备的腔室中;
(d)同时地将从第一和第二传送设备的第一出口收集的富所述给定颗粒组的流体传送至第一容器中并且将从第一和第二传送设备的第二出口收集的贫所述给定颗粒组的流体传送至第二容器中;
其中,在步骤(c)和(d)期间,第一和第二容器中的相应的流体体积保持恒定。
本发明的方法是一种用于分离流体中的至少一个给定颗粒组的简单且快速的方法。
本发明的方法还使得能够通过对经处理的颗粒的选择性声聚焦来进行无过滤器过滤。
在一个实施例中,该方法由如上所述的本发明的系统实现。
在一个实施例中,本发明的系统与用于在每个传送设备的腔室内产生声波的至少一个声波发生器相关联。
在一个实施例中,步骤(c)和步骤(d)是同时的。
在一个实施例中,流体从第一和第二容器中之一通过第一和第二传送设备之一并且到达第一和第二容器之一来连续地循环。
在一个实施例中,本发明的方法包括测量第一容器和/或第二容器中的流体的体积,以及/或者第一容器和/或第二容器的重量,以及/或者第一容器和/或第二容器中的流体流速。
在一个实施例中,提供流量控制装置以用于施加受控的流量,特别是施加从容器的出口到传送设备的入口以及从传送设备的出口到容器的入口的受控的流量。
根据一个实施例,所述流量控制装置包括控制单元、测量装置和流动装置。
根据一个实施例,控制单元配置成通过根据表示第一容器和/或第二容器中的流体的体积的测量结果来调节在系统中循环的流体的流速以使第一容器和第二容器中的每一个中的流体的体积保持恒定。在该实施例中,系统中流体的流动优选地始终被控制。
在一个实施例中,测量装置被配置成测量第一容器和/或第二容器中的流体的体积,以及/或者第一容器和/或第二容器的重量,以及/或者第一容器和/或第二容器中的流体流速。例如,测量装置可以是称重秤、流量计或用于测量重量、体积、流量或本领域已知的代表体积的任何其他值的任何其他装置。
在一个实施例中,表示第一容器和/或第二容器中的流体的体积的测量结果是第一容器和/或第二容器中的流体的体积的测量结果,以及/或者第一容器和/或第二容器的重量的测量结果,以及/或者第一容器和/或第二容器中的流体流速的测量结果。
在一个实施例中,第一容器和/或第二容器被实时称重以确保它们的重量保持恒定并且流速被电子调节。
在一个实施例中,流动装置被配置成调节第一和第二容器以及第一和第二传送设备的入口处的流速。在该实施例中,所述流动装置与测量装置协同工作,以确保第一和第二容器中的每一个中的流体的体积是恒定的。通常,由流动装置施加的流速通过测量容器的体积或重量的测量装置来控制。
在一个实施例中,流动装置位于第一和第二容器以及第一和第二传送设备的出口处。
在一个实施例中,流动装置包括泵,例如蠕动泵、齿轮泵、离心泵、隔膜泵、旋转叶片泵、活塞泵、压力泵、重力以及它们的衍生物。在一个实施例中,流动装置包括阀。在该实施例中,所述流动装置调节第一和第二容器以及腔室的入口处的流速,以防止完全排空第一和/或第二容器。
在一个实施例中,在第一和第二传送设备中的每一个的入口处的流体流速为0.1mL/min至50mL/min。
在一个实施例中,在第一和第二容器中的每一个的入口处的流体流速为0.1mL/min至50mL/min。
在一个实施例中,该方法包括根据表示第一容器和/或第二容器中的流体的体积的测量结果来调节第一和第二容器以及第一和第二传送设备的入口处的相应流速。
在一个实施例中,重复步骤(c)和(d),直到第二容器中的流体中的给定颗粒组的浓度达到预定水平。在该实施例中,包含在容器中的流体在传送设备中重复循环,直到第二容器中的给定颗粒组浓度达到预定水平,即,使第一容器中的流体富至少一个颗粒组,同时第二容器中的流体贫所述颗粒组。在该实施例中,该方法是闭环方法或连续环方法。
在一个实施例中,所述预定水平等于或低于初始水平。
在一个实施例中,重复步骤(c)和(d),直到第二容器中流体中的给定颗粒组的浓度低于或等于可忽略的水平。
在一个实施例中,所述可忽略的水平低于或等于所需的纯度水平。在血浆的情况下,EU要求为每升50×10
在一个实施例中,该方法还包括从受试者流体取样的步骤。
在一个实施例中,能够例如通过血液取样、献血、尿液取样、粪便取样、器官捐赠、腰椎穿刺、脐带血捐赠、骨髓采集、挤奶、牛奶捐赠、贝类混合、活组织检查或本领域已知的任何程序来从受试者处采样流体。
在一个实施例中,流体能够例如通过水取样、泥浆取样或本领域已知的任何程序来从环境中取样。
在一个实施例中,富血细胞的流体被收集在第一容器中,而贫血细胞的血浆被收集在第二容器中。
在一个实施例中,富血小板的流体被收集在第一容器中,而血浆被收集在第二容器中。
在一个实施例中,富血细胞的流体被收集在第一容器中,而贫血细胞的血液被收集在第二容器中。
在一个实施例中,富血小板的流体被收集在第一容器中,而贫血小板但包含红细胞和白细胞的流体被收集在第二容器中。
在一个实施例中,富胰岛的流体被收集在第一容器中,而贫胰岛的流体被收集在第二容器中。
在一个实施例中,富干细胞的流体被收集在第一容器中,而贫干细胞的流体被收集在第二容器中。
在一个实施例中,富巨核细胞的流体被收集在第一容器中,而贫巨核细胞的流体被收集在第二个容器中。
在一个实施例中,富脂质体的流体被收集在第二容器中,而贫脂质体的流体被收集在第一容器中。
在一个实施例中,富微生物的流体被收集在第一容器中,而贫微生物的流体被收集在第二容器中。
在一个实施例中,富循环细胞的流体被收集在第一容器中,而贫循环细胞的流体被收集在第二容器中。
在一个实施例中,富寄生物的流体被收集在第一容器中,而贫寄生物的流体被收集在第二容器中。
在一个实施例中,富乳脂的流体被收集在第二容器中,而贫乳脂的流体被收集在第一容器中。
在一个实施例中,富颗粒的流体被收集在第一容器中,而贫颗粒的流体被收集在第二容器中。
在一个实施例中,富微泡的流体被收集在第二容器中,而贫微泡的流体被收集在第一容器中。
在一个实施例中,该方法还包括使富至少一个给定颗粒组的流体返回或重新分配给受试者的最终步骤。在一个实施例中,该方法还包括使富至少一个给定颗粒组的流体重新分配给提供初始流体样品的受试者的步骤。
在一个实施例中,本发明的方法可以使得至少一个颗粒(例如细胞)层能够通过声聚焦形成。特别地,本发明的方法可以包括使存在于通过声聚焦形成的层中的至少两种化学物质或两种类型的细胞发生反应的步骤。
在一个实施例中,本发明的方法还可以包括步骤(c)与(d)之间的若干步骤,以允许通过包括但不限于声学、光学或电磁装置的非侵入性装置进行测量,并且因此控制声发生器和/或流动装置,从而允许完美地控制第一和第二容器中的最终产品。
本发明还涉及本发明的系统或本发明的方法的用途。
在一个实施例中,本发明的系统或本发明的方法用于流体富集或流体分级。
在一个实施例中,本发明的系统或本发明的方法用于颗粒操作例如细胞操作、颗粒分离例如细胞分离、颗粒洗涤例如细胞洗涤、颗粒计数例如细胞计数、颗粒分选例如细胞分选、颗粒浓缩、颗粒消除、颗粒隔离。所述颗粒可以是细胞、微生物、细胞器、细菌、病毒、寄生虫、沙子、沉积物、浮游生物、藻类、细胞簇、组织、蛋白质、微泡、脂肪、花粉、孢子、金属颗粒、寄生虫卵或它们的混合物。
在一个实施例中,本发明的系统或本发明的方法用于细胞治疗,例如细胞洗涤和细胞分选。
在一个实施例中,本发明的系统或本发明的方法用于流式细胞术。
在一个实施例中,本发明的系统或本发明的方法在以下方法中使用:分选物种的方法;诊断或分析的方法;纯化、富集或贫化物种的方法;合成物种的方法;改变物种的物理或化学特性的方法;医药产品研究的方法;或混合方法或测量扩散系数的方法。
在一个实施例中,本发明的系统或本发明的方法用于再生医学。在该实施例中,能够将富集的流体施用于受试者以确保组织或流体的再生。
在一个实施例中,本发明的系统或本发明的方法用于对例如采矿或钻井设施中的水、油或石油进行去污。
定义
在本发明中,下列术语具有下列含义:
-“血液”是指悬浮在血浆和/或添加剂溶液中的血细胞的组合。
-“血细胞”是指红细胞、白细胞和血小板。
-“血沉棕黄层”是指含有在对全血离心后获得的白细胞和血小板中的大部分的悬浮液(血浆层与红细胞层之间的薄层)。
-“细胞簇”是指细胞团块或细胞组。
-“细胞处理”是指用于诊断或生产目的的应用于细胞悬浮液的任何处理。
-“细胞悬浮液”是指悬浮在培养基、优选为液体培养基中的细胞混合物或单一类型的细胞。
-“恒定体积”是指偏差小于10%、优选为小于1%的体积。
-“贫化流体”或贫含流体是指与其初始浓度相比,损失了给定颗粒组的至少50%的流体。
-“富集流体”是指与其初始浓度相比已经获得给定颗粒组的至少50%的流体。
-“流体连接”是指装置的几个部分使用管道以流体能够安全地从一个部分传送至另一部分的方式被连接。
-“腔室的纵向轴线”是指接合腔室的横截面的中心点的集合的线。腔室的纵向轴线可以是直的或弯曲的,并且可以包含在一个平面中,该平面可以是腔室的一些或所有横截面的对称平面。
-“颗粒”是指包含在流体中的任何物体、成分或细胞。
-“血浆”是指红细胞、白细胞和血小板已经移除的血液的液体成分。
-“血小板”是指参与导致血凝块形成的初级止血的细胞机制的无核细胞。术语血小板或凝血细胞能够互换使用。
附图说明
当结合附图阅读时,将更好地理解以下详细描述。为了说明的目的,在优选实施例中示出了该系统。然而,应当理解,本申请不限于所示的精确布置、结构、特征、实施例和方面。附图不是按比例绘制的,并且不旨在将权利要求的范围限制到所描述的实施例。因此,应当理解,在所附权利要求中提到的特征后面跟随有附图标记的情况下,包括这样的标记仅仅是为了增强权利要求的可理解性,并且决不限制权利要求的范围。
本发明的特征和优点将从系统的实施例的以下描述中变得明显,该描述仅通过示例的方式并且参照附图给出,在附图中:
图1是对腔室内的颗粒施加声场的示意图。
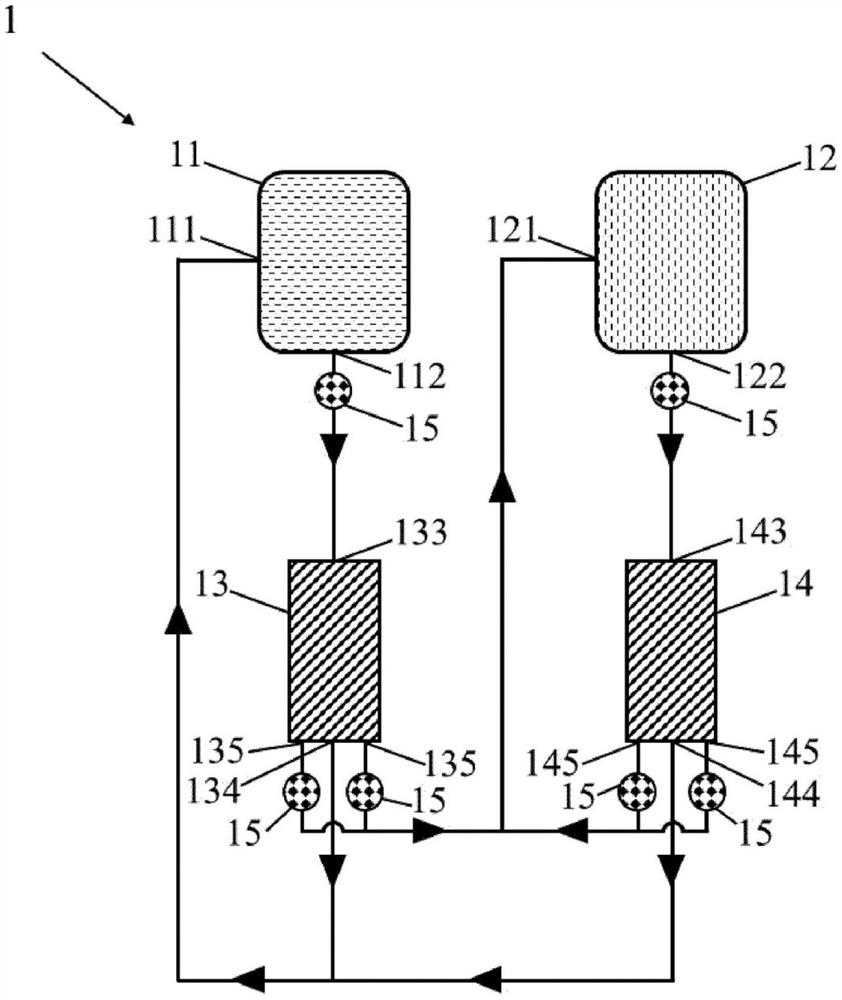
图2是根据本发明的第一实施例的系统的示意图。
图3是图2的系统的传送设备的示意图。
图4是根据本发明的第二实施例的系统的示意图。
图5是示出根据本发明的一个实施例的方法的步骤的流程图。
虽然已经描述和示出了各种实施例,但是详细描述不应被解释为限制于此。在不偏离由权利要求限定的本公开内容的真实精神和范围的情况下,本领域技术人员能够对实施例进行各种修改。
具体实施方式
如图1所示,在声波发生器16与反射器4之间的腔室内的粒子2上施加声场引起所述粒子2的运动,从而允许在所述声场的节点处使所述粒子2聚集。
在该示例中,在反射器4与壁5之间的腔室中产生超声波,该壁与和发射器层耦合的声波发生器16相关联。这使得能够在腔室的中心产生声压节点(取决于声波发生器16操作的选定频率),并因此产生声辐射力(ARF)。ARF以高达百倍于重力当量的力将颗粒2推向压力节点。悬浮在流体中的粒子2然后将迁移到声压节点,并且然后能够保持被俘获在该位置。
在腔室中能够产生多个声节点,所述声节点能够位于腔室的中心,或者偏离腔室的中心。
这是特别有利的,因为其允许在没有任何可能损坏颗粒2——尤其是如果所述颗粒2是易碎的,例如细胞——的机械力、过滤或离心步骤的情况下分离流体内的颗粒2。
在图2和图3所示的第一实施例中,根据本发明的系统1包括:
-第一容器11,其包括入口111和出口112;
-第二容器12,其包括入口121和出口122;
-第一传送设备13和第二传送设备14,其中,第一容器11流体地连接至第一传送设备13的入口133,并且第二容器12流体地连接至第二传送设备14的入口143,第一传送设备13和第二传送设备14中的每一个均包括:
□·腔室131、141;
□·三个出口134、135、144、145,这三个出口包括用于富所述给定颗粒组的流体的第一中心出口134、144和用于贫所述给定颗粒组的流体的两个第二周边出口135、145;
-泵15,其被配置成调节入口111、121、133、143处的流速。
图3示出了包括在图2所示的系统中的传送设备13、14的腔室131或141的示意性的较大比例视图。
在该实施例中,第一容器11和第二容器12均配置成包括流体,第一容器11中所包括的流体富至少一组颗粒,并且第二容器12中所包括的流体贫所述颗粒组。
在该实施例中,操作系统1包括以下步骤:一定体积的流体被引入第一容器11中,并且一定体积的流体被引入第二容器12中;通过在第一和第二传送设备13、14中的每一个的腔室131、141内部产生声波来向所述流体施加声场;然后,包含在第一容器11中的流体被传送至第一传送设备141的腔室131中,并且同时包含在第二容器12中的流体被传送至第二传送设备14的腔室141中,由此给定颗粒组迁移到腔室13、14中的通过在所述腔室131、141中产生声场而形成的声压节点,并且在中心出口134、144处传送,而流体的其他成分在腔室131、141的侧面的周边出口135、145处输送;从第一和第二传送设备13、14的中心出口134、144收集的富所述给定颗粒组的流体被传送到第一容器11中,并且从第一和第二传送设备13、14的周边出口135、145收集的贫所述给定颗粒组的流体被同时传送到第二容器中。在操作期间,通过根据表示第一容器11和/或第二容器12中的流体的体积的测量结果来调节通过泵15获得的在系统1中循环的流体的流速以使第一和第二容器中的各自的流体体积保持恒定。
该实施例特别有利,因为在不使用任何机械力的情况下使给定颗粒组与流体的其他成分分离,因此防止对所述给定颗粒组的任何损坏。
该实施例特别有利,因为容器和腔室的入口111、121、133、143处的流速被调节以确保所述容器11、12中的每一个中的流体的体积始终保持恒定,从而防止所述容器11、12之一的不合时宜的排空。通过使这些体积保持恒定,完美地控制了最终产品的体积和颗粒浓度。
如图3所示,在该实施例中,每个传送设备13、14包括:
·腔室131、141,其被配置成与用于产生声波的声波发生器16相关联;
·反射器,其位于所述至少一个声波发生器16对面,在该示例中,该反射器是围绕腔室131、141的空气3;以及
·三个出口134、135、144、145,所述三个出口包括用于富所述给定颗粒组的流体的第一中心出口134、144和用于贫所述给定颗粒组的流体的两个第二周边出口135、145。
在该实施例中,每个传送设备13、14的腔室131、141沿着纵向轴线(x)延伸,具有横截面,该横截面具有沿着第一横向轴线(y)测量的宽度和沿着垂直于第一横向轴线的第二横向轴线(z)测量的厚度,该宽度大于或等于该厚度,腔室131、141具有沿着第二横向轴线(z)的第一和第二壁132、136、142、146。腔室131、141具有350至450μm的厚度、0.7至2.1cm的宽度以及1至6cm的长度,并且壁132、136、142、146由PMMA制成。
在该实施例中,流体在腔室131、141的入口133、143处被引入。在腔室131、141的入口133、143处的流速范围为0.4至0.6mL/min。与所述腔室131、141相关联的声波发生器16在腔室131、141中产生频率范围为1.8至2MHz的声波,该声波被反射器反射,该反射器是位于腔室131、141外部的空气3。这在腔室131、141中产生至少一个压力节点,允许给定颗粒组朝向中心出口134、144选择性地迁移,同时流体的其他成分在周边出口135、145处排出。声波发生器16能够与发射器层(图3中未示出)耦合。
该实施例是特别有利的,因为通过声波发生器16在腔室131内产生声场。如图1中所解释的,这种简单的布置允许在没有任何可能损坏颗粒——尤其是如果所述颗粒是易碎的,例如细胞——的机械力、过滤或离心步骤的情况下分离流体内的颗粒。
在图4所示的第二实施例中,与第一实施例的元件相似的元件具有相同的附图标记。第二实施例与第一实施例的系统1的不同之处在于,每个传送设备13、14仅包括两个出口。更准确地说,根据本发明的第二实施例的系统1包括:
-第一容器11,其包括入口111和出口112;
-第二容器12,其包括入口121和出口122;
-第一传送设备13和第二传送设备14,其中,第一容器11流体地连接至第一传送设备13的入口133,并且第二容器12流体地连接至第二传送设备14的入口143,第一传送设备13和第二传送设备14中的每一个均包括:
□·腔室131、141;
□·两个出口134、135、144、145,这两个出口包括用于富所述给定颗粒组的流体的第一出口134、144和用于贫所述给定颗粒组的流体的第二出口135、145;
-泵15,其被配置成调节第一和第二容器以及腔室的入口111、121、133、143处的流速。
在该实施例中,第一容器11和第二容器12各自被配置成包括流体,第一容器11中所包括的流体富至少一个颗粒组,并且第二容器12中所包括的流体贫所述颗粒组。
在该实施例中,第一和第二容器11、12中的相应的流体体积始终保持恒定。
该实施例是特别有利的,因为容器和腔室的入口111、121、133、143处的流速被调节以确保所述容器11、12中的每一个中的流体的体积始终保持恒定,从而防止所述容器11、12之一的不合时宜的排空。
如图5所示,本发明的方法包括以下步骤:
-提供本发明的系统1;
-通过借助于每个声波发生器16在第一和第二传送设备13、14的各自的腔室131、141内产生声波来施加声场;
-同时地将包含在第一容器11中的流体传送至第一传送设备13以及将包含在第二容器12中的流体传送至第二传送设备14;
-同时地将从第一出口收集的富至少一个颗粒组的流体传送至第一容器11以及将从第二出口收集的贫所述颗粒组的流体传送至第二容器12。
此外,调节第一和第二容器11、12以及腔室131、141的入口111、121、133、143处的流速,使得第一和第二容器11、12中的相应的流体体积在该方法的步骤期间保持恒定。
如上所述,本发明的方法是一种用于在不需要任何稀释的情况下从流体中分离至少一个颗粒组的简单且快速的方法。此外,在所述方法期间不需要过滤、离心或任何需要机械力的步骤。这防止了对待分离的颗粒组的损坏。
实施例
通过以下示例进一步说明本发明。特别地,使用图2和图3的系统来实现以下示例。
材料和方法
在本发明的第一和第二容器中注入等量的富血小板血浆,因此第一和第二容器中的每一个都容纳系统中的血小板总量的50%。血小板浓度可以从高浓度变化到稀释的样品。血小板的平均直径为2μm。
流动装置引导流体通过传送设备。启动流量控制装置,以使得每个容器在整个过程中保持恒定体积的流体,并相应地控制流速。传送设备入口的流量保持在0.4至0.6mL/min内。传送设备腔室具有350至450μm的厚度、0.7至2.1cm的宽度和1至6cm的长度。
借助于声波发生器在传送设备中感应出声力场。声波的频率设定在1.8至2MHz,具有正弦波形。
结果
第一容器富集血小板,而第二容器贫化血小板,直到在第二容器中达到预定的血小板水平。在2.5小时的处理之后,第一容器容纳60%至80%的血小板,而第二容器容纳20%至40%的血小板。
材料和方法
在本发明的第一和第二容器中注入等量的稀释的全血,因此第一和第二容器中的每一个都容纳系统中的血细胞总量的50%。血细胞的浓度可以从高浓度变化到稀释的样品。红细胞的平均直径为6μm,而血小板的平均直径为2μm。
流动装置引导流体通过传送设备。启动流量控制装置,以使得每个容器在整个过程中保持恒定体积的流体,并相应地控制流速。传送设备入口的流量保持在0.6至1mL/min内。传送设备腔室具有350至450μm的厚度、0.7至2.1cm的宽度和1至6cm的长度。
借助于声波发生器在传送设备中感应出声力场。声波的频率设定在1.8至2MHz,具有正弦波形。这种声学力场引起红细胞朝向中心出口迁移,而血小板倾向于停留在侧向出口中。
结果
第一容器富集红细胞,而第二容器中贫化红细胞,直到在第二容器中达到预定的红细胞水平。在2.5小时的处理后,第一容器容纳95%至99%的红细胞,而第二容器容纳1%至5%的红细胞。
附图标记说明
1—系统
11—第一容器
111—入口
112—出口
12—第二容器
121—入口
122—出口
13—第一传送设备
131—腔室
132—腔室的第一壁
133—入口
134—第一出口
135—第二出口
136—腔室的第二壁
14—第二传送设备
141—腔室
142—腔室的第一壁
143—入口
144—第一出口
145—第二出口
146—腔室的第二壁
15—流动装置
16—声波发生器
2—颗粒
3—空气
4—反射器
5—壁
x—纵向轴线
y—第一横向轴线
z—第二横向轴线。
- 用于改变流体中的颗粒的浓度的系统和方法
- 用于磁流变流体中磁性颗粒浓度的测量和控制的方法和设备
