一种区分CAR-T治疗之后CRS重轻症的临床标志物及其应用
文献发布时间:2024-04-18 19:58:26
技术领域
本发明涉及生物医药技术领域,尤其涉及一种区分CAR-T治疗之后CRS重轻症的临床标志物及其应用。
背景技术
嵌合抗原受体T细胞疗法(Chimeric Antigen Receptor T-Cell Immunotherapy,CAR-T)是一种治疗肿瘤的精准靶向疗法,通过基因工程技术,将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),专门识别体内肿瘤细胞,并通过免疫作用释放大量的多种效应因子,它们能高效地杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。
在CAR-T细胞回输到体内后识别抗原阳性的靶细胞导致T细胞大量活化、增殖,会导致免疫细胞产生大量的炎症因子,从而出现细胞因子释放综合征(cytokine releasesyndrome,CRS)。其临床特征表现为发热、低血压和多器官功能障碍等。在CAR-T治疗之后部分患者会出现不同程度细胞因子释放综合症(CRS),严重时会危及生命。目前区分细胞因子释放综合症(CRS)等级的标准有CTCAE标准、MD Anderson癌症中心/Lee分级和基于CRP的分级等,这些标准根据临床现象以及药物治疗等来判断患者细胞因子释放综合症(CRS)严重程度。尽管如此,我们也需要更多的线索来区分重轻症患者从而进行更有效地治疗。
CD163是在巨噬细胞上表达的膜受体分子,其作为血红蛋白-触珠蛋白复合物的胞吞受体发挥功能。通过这种在生理学上非常重要的功能,CD163每天摄取约1g的血红蛋白,因此,该蛋白质可能是巨噬细胞上表达最高的受体。因此,通过CD163的表达来判-断细胞因子释放综合症(CRS)的严重程度的研究具有广泛的前景。
发明内容
本发明的目的在于克服现有技术的不足,通过CD163的表达来判-断细胞因子释放综合症(CRS)的严重程度从而可以进行有效治疗并且开发新的治疗方法。
为了实现本发明的目的,本发明通过以下技术手段实现解决上述技术问题:
CD163作为标志物在制备区分嵌合抗原受体T细胞疗法(CAR-T)治疗之后细胞因子释放综合症(CRS)重轻症的方法中使用的试剂盒的用途。
本发明首次公开了CD163作为标志物用来区分CAT-T治疗之后的细胞因子释放综合症(CRS)严重程度,通过血清IL6表达和CAR-T细胞扩增数确认CD163表达和细胞因子释放综合症(CRS)严重程度的相关性。
优选地,所述CD163作为标志物的方法为测量血清中CD163的表达水平。
优选地,测量所述CD163的表达水平的方法包括质谱检测法和平行反应监测法。平行反应监测(PRM)是一种基于高分辨、高精度质谱的离子监视技术,能够对目标蛋白质、目标肽段进行选择性检测,从而实现对目标蛋白质/肽段的定量。
优选地,所述CD163的表达水平的质谱检测法包括以下步骤:收取CAR-T治疗前后患者的血清样本,将血清样本经过胰酶消化为肽段后在质谱仪中[Q Exactive HF-X混合四极-Orbitrap或Orbitrap Exploris 480(Thermo Fisher)]进行检测;
在数据依赖采集(data-dependent acquisition,DDA)模式下采集数据,每一个检测循环中优先采集信号相对较强的肽段离子进行碎裂,得到二级谱图,解析二级谱图进行肽段定性分析,对蛋白质进行鉴定;数据依赖采集模式(DDA)是基于鸟枪法的原理,在每一个检测循环中优先采集信号相对较强的肽段离子进行碎裂,得到二级谱图,DDA数据依赖型扫描模式通常可以鉴定出数千种蛋白质;
在质谱仪中DDA模式下,质谱原始数据由Proteome Discoverer(Version2.4.0.305,Thermo Fisher Scientific)软件进行搜库从而分析蛋白表达,进而表征血清中CD163的表达。
优选地,所述CD163的表达水平的平行反应监测法(Parallel ReactionMonitoring,PRM)包括以下步骤:收取CAR-T治疗前后患者的血清样本,将血清样本经过胰酶消化为肽段后进行平行反应监测;
利用四级杆质量分析器的选择检测能力,在一级质谱中选择性地检测目标肽段的母离子信息;
在碰撞池中对母离子进行碎裂,在二级质谱中检测所选择的母离子窗口内的所有碎片的信息,对目标蛋白质/肽段进行准确地特异性分析。
具体的,使用nanooflow DIONEX UltiMate 3000RSLCnano系统(ThermoScientific,San Jose,USA)和Q Exactive HF-X混合四极-orbitrap(Thermo FisherScientific,San Jose,USA)对多肽进行LC-MS/MS(液相色谱-串联质谱法)分析,液相色谱串联质谱(LC-MS/MS)中,液相色谱负责分离待测物与干扰物,质谱负责检测;样品进样后首先在流动相的携带下进入色谱柱,经过色谱柱分离后进入质谱进行检测,在三重四级杆中一级质谱扫描特定范围离子或允许特定离子进入碰撞室,在碰撞室内分子离子碰撞裂解,形成子离子进入二级质谱,二级质谱扫描特定范围离子或允许特定离子进入检测器,平行反应监测(PRM)检测结果导入Skyline(MacCoss Lab,University of Washington),这是一款用于定量数据处理和蛋白质组学分析的开源软件,进行数据分析,在该软件中选择目标蛋白的肽段来表征该蛋白的表达,使用肽段EAEFGQGTGPIWLNEVK用来量化CD163进而确认CD163表达。
细胞因子释放综合症(CRS)分级依据美国移植和细胞治疗学会(AmericanSociety for Transplantation and Cellular Therapy,ASTCT,原美国血液和骨髓移植学会)分级标准,进而将CRS 1-2级分为轻症,CRS 3-5级定为重症。
与现有技术相比,本发明的有益效果在于:
1、本发明首次公开了CD163作为标志物用来区分CAT-T治疗之后的细胞因子释放综合症(CRS)严重程度,通过血清IL6表达和CAR-T细胞扩增数确认CD163表达和细胞因子释放综合症(CRS)严重程度的相关性。
2、本发明通过质谱检测和平行反应监测(PRM)验证了CAR-T治疗之后CD163表达和细胞因子释放综合症(CRS)变化趋势一致并且在细胞因子释放综合症(CRS)重症患者中表达高于轻症,在炎症最重时的第七天,CD163表达到达峰值并且重轻症差异最明显,这些结果提示CD163在区分细胞因子释放综合症(CRS)时是重要的临床指标。
附图说明
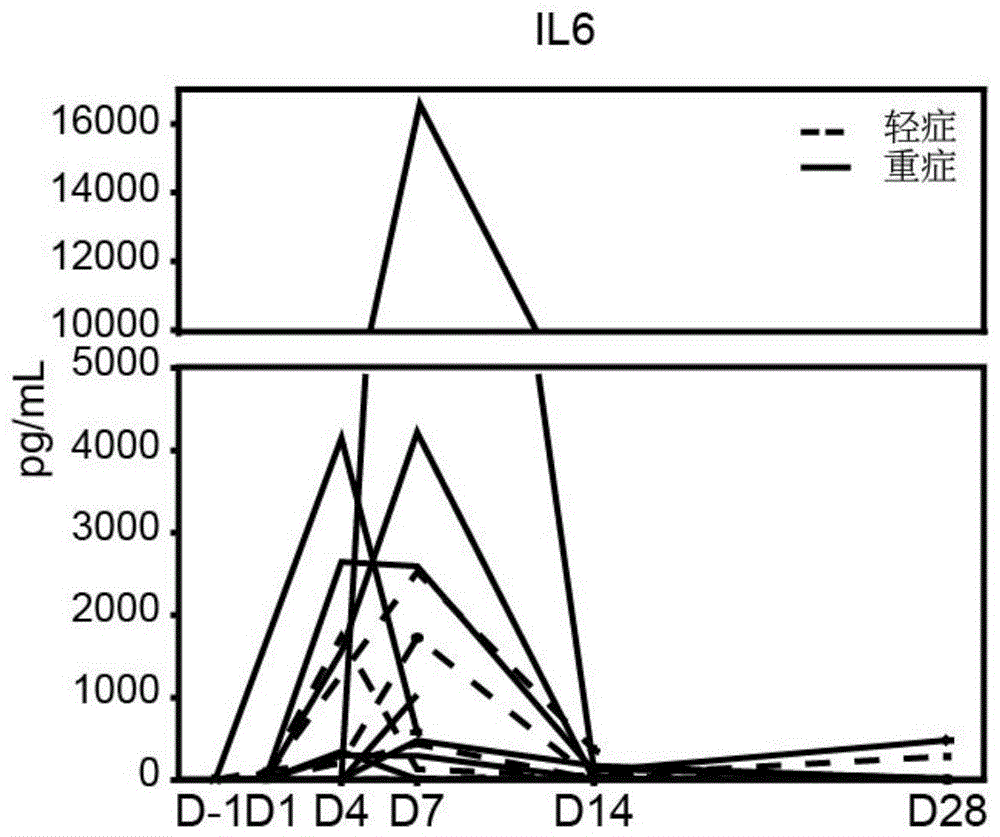
图1为本发明实施例的患者CAR-T治疗前后6个时间点血清IL6表达情况图;
图2为本发明实施例的患者CAR-T治疗前后6个时间点CAR-T细胞扩增数结果图;
图3为本发明实施例的质谱检测患者CAR-T治疗之后血清中CD163的表达情况图;
图4为本发明实施例的PRM验证患者血清中CD163的表达情况图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明附图说明和实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
下述实施例中所用的试验材料和试剂等,如无特殊说明,均可从商业途径获得。
实施例中未注明具体技术或条件者。均可以按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。
实施例1
本实施例公开CD163作为标志物用来区分CAT-T治疗之后的细胞因子释放综合症(CRS)严重程度。
1、样本收集
本实施例收集了8名接受CD19 CAR-T治疗的B-ALL患者治疗前后6个时间点(D-1,D1,D4,D7,D14,D28)45个血清样本。本实施例使用美国移植和细胞治疗学会(ASTCT,前美国血液和骨髓移植学会)的分类标准将患者分为轻症(细胞因子释放综合症(CRS)1-2级)或重症(细胞因子释放综合症(CRS)3-5级)。这8名患者包括2名轻症和6名重症。收集另外3名重症和3名轻症患者的32个血清样本进行平行反应监测(PRM)验证。本研究由医学伦理委员会批准,所有受试者在入组前均被告知并提供书面知情同意书。
用血清分离管抽取样本;血液在室温下凝固约30分钟后,以1000g离心10分钟。使用前提取血清并保存在-80℃,所有样品在进行分析前都没有解冻两次以上。
样本处理前可先测试上述患者CAR-T治疗前后6个时间点血清IL6表达情况和CAR-T细胞扩增数结果图,结果分别如图1和图2所示,可以看出,上述8名CD19 CAR-T治疗的B-ALL患者在治疗后的第7天IL6表达量和CAR-T细胞扩增数均达到最高。
2、样本前处理
待血清恢复室温后,将4μL血清与400μL PBS(磷酸盐缓冲盐溶液)混合,首先使用高选择性14种高丰度蛋白去除树脂试剂盒(High Select
使用3k MWCO过滤装置(Thermo Fisher Scientific
然后添加200ul裂解缓冲液[三乙基碳酸氢铵缓冲液(Triethylammoniumbicarbonate buffer,TEAB)];接下来,分别用25ul 100mM三(2-羧乙基)膦[tris(2-carboxyethyl)phosphine,TCEP,高效的二硫键还原剂,打开二硫键]和12.5ul800mM碘乙酰胺(Iodoacetamide,IAA,半胱氨酸和组氨酸的烷基化试剂,可以保证蛋白质样品完全变性并保持还原状态)在31.5℃下进行二硫键还原和烷基化反应,还原的过程是将蛋白的二硫键打开,然后烷基化可以修饰巯基,防止游离的巯基再生成二硫键,使得蛋白分子呈链状,增加蛋白质的溶解性,以及暴露出尽可能多的酶切位点,接着双步胰酶(中国北京华立石科技有限公司)消化蛋白质为多肽。
加入终浓度为1%三氟乙酸(Trifluoroacetic acid,TFA,一种强酸,在酸性条件下胰酶失活)(Thermo Fisher)终止消化反应。用连续质量标签(TMTpro)16plex(ThermoFisher)试剂1200rpm室温孵育60min标记多肽,TMTpro 16plex标记试剂是新一代串联质谱标签,可同时标记16个样品(TMTpro 126,TMTpro 127N,TMTpro 127C,TMTpro 128N,TMTpro128C,TMTpro 129N,TMTpro 129C,TMTpro 130N,TMTpro 130C,TMTpro 131N,TMTpro 131C,TMTpro 132N,TMTpro 132C,TMTpro 133N,TMTpro 133C,TMTpro 134N,TMTpro 134C),一组标签试剂里的所有标签,均带有相同的质量(例如:同质),化学结构则由一个氨基反应基团,平衡基团和同位素报告基团组成。
在MS/MS片段化后,氨基反应基团与氨基酸N端或赖氨酸发生反应,在一级质谱中,不同来源的相同肽段被标记后出现相同的质荷比,在同一个保留时间流出。在二级质谱中,平衡基团,被不同标签标记的相同肽段出现不同的报告基团,不同报告基团的峰面积能反映出某肽段在当前样本的含量,通过比较不同报告基团的峰面积就能找到某个肽段在不同样本中的表达差异。
在高效液相色谱仪(Dinex Ultimate 3000UHPLC)(Thermo Fisher)中以500μL/min的流速,用96min高PH反相液相色谱(reverse-phase liquid chromatography,RPLC)梯度将TMT标记的多肽分离为96个馏分。最后将96个馏分等距合并(例:1号,25号,49号,72号合成一管)成24个后在真空中干燥。
3、质谱检测CD163的表达
在质谱分析之前,干肽在2%乙腈(Acetonitrile,ACN)/0.1%甲酸溶剂中重新溶解,然后用质谱仪[Q Exactive HF-X混合四极-Orbitrap或Orbitrap Exploris 480(Thermo Fisher)]进行检测;
在数据依赖采集(data-dependent acquisition,DDA)模式下采集数据:每一个检测循环中优先采集信号相对较强的肽段离子进行碎裂,得到二级谱图,解析二级谱图进行肽段定性分析,对蛋白质进行鉴定;数据依赖采集模式(DDA)是基于鸟枪法的原理,在每一个检测循环中优先采集信号相对较强的肽段离子进行碎裂,得到二级谱图,DDA数据依赖型扫描模式通常可以鉴定出数千种蛋白质。液相(LC)梯度为60分钟,流速为300nL/min。
在质谱仪中DDA模式下,质谱原始数据由Proteome Discoverer(Version2.4.0.305,Thermo Fisher Scientific)软件进行搜库从而分析蛋白表达,进而表征血清中CD163的表达。
本实施例的质谱原始数据由Proteome Discoverer(Version 2.4.0.305,ThermoFisher Scientific)用2020年5月7日从UniProt网站下载的FASTA文件(20377个蛋白质)分析。前体离子质量公差设置为10ppm,生产质量公差设置为0.02Da。蛋白质组学数据质量控制(QC)方法是每个批次使用相同的30个样品的混合物,用TMT pro-126标记,以校准来自不同批次的数据并评估其定量准确性。
4、PRM进一步验证CD163的表达
另外收集的32个血清样本如前文所述方法处理为多肽,在平行反应监测(PRM)模式下,采用nanooflow DIONEX UltiMate 3000RSLCnano系统(Thermo Scientific,SanJose,USA)和Q Exactive HF-X混合四极-orbitrap(Thermo Fisher Scientific,SanJose,USA)对多肽进行LC-MS/MS(液相色谱-串联质谱法)分析,液相色谱串联质谱(LC-MS/MS)中,液相色谱负责分离待测物与干扰物,质谱负责检测;
样品进样后首先在流动相的携带下进入色谱柱,经过色谱柱分离后进入质谱进行检测,质谱根据被测物的质荷比(m/z)进行检测,被测物在离子源转换成气相离子进入质谱,在三重四级杆中一级质谱扫描特定范围离子或允许特定离子进入碰撞室,在碰撞室内分子离子碰撞裂解,形成子离子进入二级质谱,二级质谱扫描特定范围离子或允许特定离子进入检测器,平行反应监测(PRM)检测结果导入Skyline(MacCoss Lab,University ofWashington),这是一款用于定量数据处理和蛋白质组学分析的开源软件,进行数据分析,在该软件中选择目标蛋白的肽段来表征该蛋白的表达(使用公共内部保留时间预测保留时间,隔离时间窗口设置为10分钟,手动检查所有集成的峰值,以确保正确的峰值检测和集成),我们使用肽段EAEFGQGTGPIWLNEVK用来量化CD163进而确认CD163表达,结果如图4所示。
如图3、图4所示的结果可以看出,本实施例通过质谱检测和平行反应监测(PRM)验证了CAR-T治疗之后CD163表达和细胞因子释放综合症(CRS)变化趋势一致,并且在细胞因子释放综合症(CRS)重症患者中表达高于轻症,在炎症最重时的第七天,CD163表达到达峰值并且重轻症差异最明显。
以上实施例仅用以说明本发明的技术方案,而非对其限制,尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 一种用于监测CAR-T治疗之后CRS进程的临床标志物及其应用
- 白头翁皂苷组合物在制备治疗CAR-T疗法引起CRS的药物中的应用
