一种呋喃香豆素类化合物及其制备方法和应用
文献发布时间:2024-04-18 19:58:26
技术领域
本发明属于生物医药技术领域,具体涉及一种呋喃香豆素类化合物及其制备方法和应用。
背景技术
羌活为伞形科植物羌活Notopterygium incisum Ting ex H.T.Chang或宽叶羌活Notopterygium franchetii H.de Boiss.的干燥根和根茎。化学成分是中药起作用的物质基础也是质量控制的重要指标。目前已经从羌活中分离得到的近五百多种成分,结构复杂。具体可分为挥发油、香豆素、烯炔、倍半萜、有机酸及有机酸酯、黄酮、甾类和其他类[1]。香豆素是羌活中主要有效成分,在羌活中含量较高,有研究表明,香豆素类化合物具有广泛的药理活性,如抗炎、抗氧化、抗病毒、抗肿瘤、抗凝血、抗菌、增强免疫功能等作用[2-3],且关于香豆素类化合物抗炎活性的基础研究较多。
发明内容
本申请的主要目的为提供一种呋喃香豆素类化合物及其制备方法和应用,所述的化合物能够减少脂多糖(LPS)诱导的RAW264.7巨噬细胞产生的炎症反应,可以减少LPS诱导的RAW264.7巨噬细胞NO产生,可显著性抑制TNF-α、白细胞介素-6(IL-6)、白细胞介素1β(IL-1β)等炎症因子的产生。
为了实现上述目的,本发明提供如下技术方案:
一种呋喃香豆素类化合物,所述呋喃香豆素类化合物的结构式为:
上述一种呋喃香豆素类化合物,作为一种优选的实施方案,所述呋喃香豆素类化合物从羌活中提取。
本申请的第二方面,提供一种呋喃香豆素类化合物的制备方法,包括以下步骤:
(1)采用乙醇回流提取羌活,浓缩提取液,并进行流浸膏处理得流浸膏剂;
(2)将步骤(1)所得流浸膏剂用蒸馏水分散,上D101吸附树脂进行纯化,并采用甲醇-蒸馏水洗脱液进行梯度洗脱;
(3)将步骤(2)所得产物采用硅胶柱色谱纯化,并采用石油醚-丙酮进行梯度洗脱;
(4)将步骤(3)所得产物采用轴向压缩柱进行纯化,并采用甲醇-蒸馏水进行洗脱,对洗脱产物进行处理得呋喃香豆素类化合物。
上述一种呋喃香豆素类化合物的制备方法,作为一种优选的实施方案,步骤(1)中,将羌活进行粉碎采用8倍量95%乙醇回流提取;所述流浸膏处理为:采用蒸馏水分散浓缩液,并将分散液用透析袋盛装、蒸馏水浸泡12天,每天换水2次,待浸泡完毕浓缩透析液,得流浸膏剂。
上述一种呋喃香豆素类化合物的制备方法,作为一种优选的实施方案,步骤(2)中,所述甲醇-蒸馏水梯度洗脱为:
洗脱时间0-40个小时,洗脱液为蒸馏水,洗脱液流速为5ml/min;
洗脱时间40-80个小时,洗脱液为体积比为30:70的甲醇-蒸馏水,洗脱液流速为5ml/min,得30%甲醇洗脱产物;
洗脱时间80-120个小时,洗脱液为体积比为60:40的甲醇-蒸馏水,洗脱液流速为5ml/min,得60%甲醇洗脱产物;
洗脱时间120-160个小时,洗脱液为体积比为90:10的甲醇-蒸馏水,洗脱液流速为5ml/min,得90%甲醇洗脱产物。
上述一种呋喃香豆素类化合物的制备方法,作为一种优选的实施方案,步骤(3)中,将步骤(2)所得30%甲醇洗脱产物采用硅胶柱色谱纯化,所述石油醚-丙酮进行梯度洗脱为:
洗脱时间0-20个小时,洗脱液为体积比为30:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间20-40个小时,洗脱液为体积比为25:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间40-60个小时,洗脱液为体积比为20:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间60-80个小时,洗脱液为体积比为15:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间80-100个小时,洗脱液为体积比为10:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间100-120个小时,洗脱液为体积比为5:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间120-140个小时,洗脱液为体积比为1:1的石油醚-丙酮,洗脱液流速为5ml/min。
上述一种呋喃香豆素类化合物的制备方法,作为一种优选的实施方案,步骤(4)中,对体积比为1:1的石油醚-丙酮洗脱液洗脱产物采用轴向压缩柱进行纯化;
优选地,步骤(4)中,采用甲醇-蒸馏水进行洗脱时甲醇-蒸馏水的体积比为65:35;运用轴向压缩柱将洗脱部分分为8段,便于后续过正向硅胶柱和制备液相,保留时间为20min;
进一步优选地,步骤(4)中,将洗脱产物通过半制备液相处理得呋喃香豆素类化合物。
上述一种呋喃香豆素类化合物的制备方法,作为一种优选的实施方案,半制备液相的流动相为体积比为7:13的乙腈和水的混合物,流速为3ml/min,检测波长为254nm,柱温为30℃。
本申请的第三方面,提供一种上述呋喃香豆素类化合物或其药学上可接受的盐在制备抗炎药物中的应用。
优选地,所述抗炎药物还包括药学上可接受的载体或赋形剂。
本发明的有益效果为:本发明所述呋喃香豆素类化合物能够减少脂多糖(LPS)诱导的RAW264.7巨噬细胞产生的炎症反应,可以减少LPS诱导的RAW264.7巨噬细胞NO产生,可显著性抑制TNF-α、白细胞介素-6(IL-6)、白细胞介素1β(IL-1β)等炎症因子的产生。
附图说明
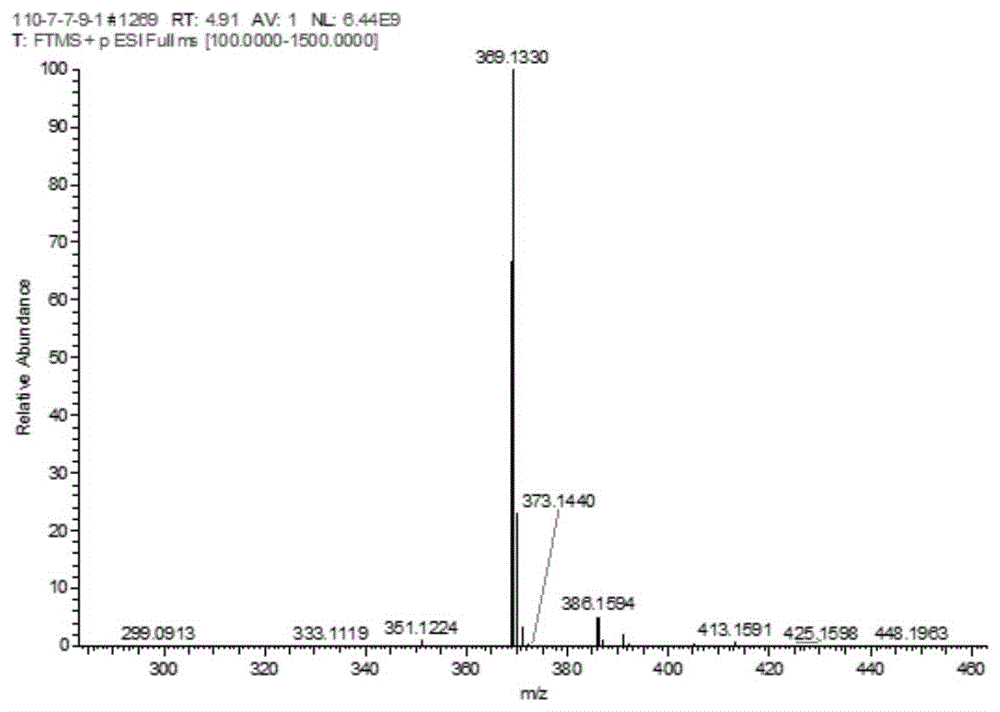
图1为本申请所述呋喃香豆素类化合物的ESI-MS谱图;
图2为本申请所述呋喃香豆素类化合物在MeOH中的紫外光谱图;
图3为本申请所述呋喃香豆素类化合物在MeOH中的红外光谱图;
图4为本申请所述呋喃香豆素类化合物在CDCl
图5为本申请所述呋喃香豆素类化合物在CDCl
图6为本申请所述呋喃香豆素类化合物在CDCl
图7为本申请所述呋喃香豆素类化合物在CDCl
图8为本申请所述呋喃香豆素类化合物在CDCl
图9为本申请所述呋喃香豆素类化合物在CDCl
图10为本申请所述呋喃香豆素类化合物在MeOH中的计算和实验ECD谱图;
图11用离散傅立叶变换(DFT)计算出在甲醇中最稳定的5s-1构象WB97XD/DGDZVP水平图;
图12为CCK-8法检测RAW264.7巨噬细胞的活力;
图13为本申请所述呋喃香豆素类化合物对lps刺激巨噬细胞NO生成的影响;
图14为本申请所述呋喃香豆素类化合物对lps刺激巨噬细胞mRNA产生的影响。
具体实施方式
为了使本技术领域的人员更好地理解本申请方案,下面将结合案例对本申请实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本申请一部分的实施例,而不是全部的实施例。基于本申请中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本申请保护的范围。
本申请实施例所采用的实验仪器如表1所示:
表1
本申请实施例所采用的材料和试剂如表2所示:
表2
本申请所述呋喃香豆素类化合物从羌活中分离得到,利用核磁共振、电喷雾质谱(ESIMS)、计算核磁、CD等对该新化合物的结构进行了表征。本申请所述化合物通过减少炎症因子如NO、TNF-α、IL-1β和IL-6的产生,能够抑制LPS诱导的RAW264.7巨噬细胞的炎症因子TNF-α、IL-1β、IL-6的mRNA表达,在体外表现出抗炎特性。
实施例1
一种呋喃香豆素类化合物,其结构式为:
本实施例所述呋喃香豆素类化合物从羌活中提取。
具体提取方法为:
(1)将100kg羌活粉碎经8倍量95%乙醇回流提取后,浓缩到无醇味,采用蒸馏水分散浓缩液,并将分散液用透析袋盛装,蒸馏水浸泡12天,每天换水2次,待浸泡完毕浓缩透析液,得1kg流浸膏剂;
(2)将步骤(1)所得流浸膏剂用蒸馏水分散,上样至D101大孔吸附树脂,并采用甲醇-蒸馏水洗脱液进行梯度洗脱:
甲醇-蒸馏水的具体洗脱方式为:
洗脱时间0-40个小时,洗脱液为蒸馏水,洗脱液流速为5ml/min;
洗脱时间40-80个小时,洗脱液为体积比为30:70的甲醇-蒸馏水,洗脱液流速为5ml/min,得30%甲醇洗脱产物;
洗脱时间80-120个小时,洗脱液为体积比为60:40的甲醇-蒸馏水,洗脱液流速为5ml/min,得60%甲醇洗脱产物;
洗脱时间120-160个小时,洗脱液为体积比为90:10的甲醇-蒸馏水,洗脱液流速为5ml/min,得90%甲醇洗脱产物;
(3)将步骤(2)所得30%甲醇洗脱产物采用硅胶柱色谱纯化,并采用石油醚-丙酮进行梯度洗脱;
石油醚-丙酮梯度洗脱方法为:
洗脱时间0-20个小时,洗脱液为体积比为30:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间20-40个小时,洗脱液为体积比为25:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间40-60个小时,洗脱液为体积比为20:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间60-80个小时,洗脱液为体积比为15:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间80-100个小时,洗脱液为体积比为10:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间100-120个小时,洗脱液为体积比为5:1的石油醚-丙酮,洗脱液流速为5ml/min;
洗脱时间120-140个小时,洗脱液为体积比为1:1的石油醚-丙酮,洗脱液流速为5ml/min;
(4)将体积比为1:1的石油醚-丙酮洗脱液洗脱产物采用轴向压缩柱进行纯化,并采用体积比为65:35的甲醇-蒸馏水进行洗脱,将洗脱产物通过半制备液相处理得呋喃香豆素类化合物;
半制备液相的流动相为体积比为7:13的乙腈和水的混合物,流速为3ml/min,检测波长为254nm,柱温为30℃。
本申请实施例1所得呋喃香豆素类化合物的波谱数据
采用高斯函数161进行实施例1所述呋喃香豆素类化合物的理论计算:首先使用Conflex 8进行构象分析,通过Boltzman Jump生成构象,然后使用Smart Minimizer利用MMFF分子力学力场最小化构象。
在B3LYP/6-31G(d,p)气体和WB97XD/DGDZVP甲醇中,所有相对能量为0-5.0kcal/mol的几何形状都被用于优化。根据玻尔兹曼分布规律计算室温平衡总体。在甲醇中CAM-B3LYP/DGDZVP水平上使用TD-DFT进行ECD的理论计算。通过对各几何构象的玻尔兹曼分布率进行加权得到ECD谱。利用SpecDis 1.712对单张CD光谱进行玻尔兹曼统计加权后求和,生成高斯曲线(o=0.2eV),并与实验数据进行比较,结果如图10和图11所示。
黄色粉末状:C
ESIHRMS m/z 369.1330[M+H]
1、CCK-8法检测细胞活力
取对数生长期RAW264.7巨噬细胞,以1×10
检测结果如图12所示:
从图12可以看出:本申请所述呋喃香豆素类化合物在不同浓度下对于巨噬细胞无毒性作用。
2、NO生成量的测定
取对数生长期RAW264.7巨噬细胞以2×10
测试结果如图13所示:从图13中可以看出,本申请所述呋喃香豆素类化合物能够呈浓度依赖抑制LPS诱导的RAW264.7巨噬细胞中NO的产生。(****P<0.0001;***P<0.001;**P<0.01;*P<0.05与LPS组比较)。
3、逆转录-聚合酶链式反应(RT-PCR)分析
取对数生长期RAW264.7巨噬细胞以2×10
表3
从图14中可以看出,本申请所述呋喃香豆素类化合物显著抑制了LPS诱导的RAW264.7巨噬细胞中炎症因子TNF-α、IL-1β和IL-6mRNA的表达(****P<0.0001;***P<0.001;**P<0.01;*P<0.05与LPS组比较)。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
- 一种香豆素类化合物及其制备方法与应用
- 一种含有异香豆素并吡咯并香豆素结构的OLED材料、制备方法及其应用
- 一种呋喃香豆素类化合物及其制备方法和应用
- 一种线型呋喃香豆素类化合物及其制备方法和应用
