一种制备氰胺和硫醇的方法
文献发布时间:2024-04-18 19:58:26
技术领域
本发明属于有机化学合成领域,具体涉及一种一锅法制备氰胺和硫醇的合成方法。
背景技术
氰胺(cyanamide)是含有N-CN官能团的化合物,氰胺化合物中含有亲核的氮原子,以及与该氮原子相连的亲电的氰基官能团,具有独特的化学性质。因此,这类化合物在有机合成上可以进一步转化为结构多样性的含氮化合物。氰胺在药物化学和配位化学中均有重要应用。
对于取代氰胺的制备,人们使用溴化氰(BrCN)等N-亲电氰化试剂对胺进行氰基化,广泛应用于制备取代氰胺。但是,溴化氰是一种剧毒化学品,其蒸气可以通过呼吸道进入人体,或者进过皮肤吸收导致痉挛或死亡。因此,通过原位制备溴化氰并直接发生氰基化,可以降低该危险化学品对人体的毒害作用。也可以开发一些安全的亲电氰基化试剂,有效地的获得取代氰胺。还可以使用亲核试剂对氰胺进行亲核取代,也是制备取代氰胺的有效方法。上述方法,都需要氰基源(亲电的氰基试剂,或者含有氰胺基团的底物),因此限制了该类型底物的多样化。
Patel等人(A one-pot preparation of cyanamide from dithiocarbamateusing molecular iodine,Green Chem.,2009,11,1503-1506)公开了一种使用碘对二硫代氨基甲酸盐进行脱硫反应,制备氰胺衍生物,收率中等至优秀,所制备的均为N-芳基氰胺。但是,该反应操作上较为繁琐,需要经过减压除去第一步过量的NH3,然后再进行第二步反应。一锅两步法的操作,使得该方法不够简便,也不便于放大生产。Doris等人(Triphenylbismuth Dichloride-Mediated Conversion of Thioamides to Nitriles,Eur.J.Org.Chem.2019,4043-4045)研究了一种使用三苯基二氯化铋辅助脱硫的方法,可以将硫代酰胺转化为氰化物,也可以将硫脲转化为氰胺。然而,三苯基二氯化铋用量为底物的1.2当量,极大地增加了成本,并且不利于后续的处理纯化。
含硫化合物在有机化学和药物化学中也有着重要的应用。目前,硫醇的制备方法报道并不多。
总体而言,现有技术中,虽然有一些制备氰胺的方法,仍然存在许多安全性和环保性的问题,并且使用贵金属等试剂,这导致成本高,同时废弃物料的增加带来严峻的环境问题。
因此,以简便易得的化合物为底物,发展操作简单、条件温和的合成方法构建结构多样化的取代氰胺仍然是极具挑战性的研究课题。
发明内容
为了克服现有技术的缺点和不足,本发明的目的在于提供了一种同时制备氰胺和硫醇的方法。本发明采用一锅法,以芳基硫脲为氰基和巯基源底物,通过与卤代烃反应,获得结构多样性的取代氰胺和硫醇。该方法操作简便,条件温和,官能团兼容性高,为具有潜在生物和药理活性的氰胺和硫醇的高效合成提供重要的技术支撑。
本发明是通过以下技术方案实现:
一种制备氰胺和硫醇的方法,包括以下步骤:
以非质子性有机溶剂为反应介质,芳基硫脲与卤代烃在碱或碱和铜盐作用下反应,获得氰胺和硫醇;
芳基硫脲的结构为式Ⅳ:
卤代烃的结构为式Ⅴ:
所述氰胺的结构为式I:
所述硫醇的结构为式II:
各式中,R
所述卤代烃中X为Cl、Br、I,其中,R
当卤代烃的结构为
所述取代的苯基包括含有卤素、烷基、烷氧基、三氟甲基、乙酰基中的一种或多种取代的苯基;所述取代的苄基是指苯环上的氢被卤素、烷基中一种或多种取代。
所述芳基硫脲和卤代烃的摩尔比为1:2~3,优选后为1:2.1~2.5,进一步优选为1:2.4~2.5。
所述碱为无机碱,在本发明中,所述碱包括:叔丁醇锂,叔丁醇钠,叔丁醇钾,甲醇锂,甲醇钠,甲醇钾,氢氧化锂,氢氧化钠,氢氧化钾,碳酸锂,碳酸钠,碳酸钾,碳酸铯,碳酸氢钠、碳酸氢钾,碳酸氢铯中的一种或几种;优选为碳酸氢钠,碳酸氢钾,碳酸钠,碳酸钾和碳酸铯中一种以上;进一步优选为碳酸钠和碳酸钾中一种以上。
所述芳基硫脲与碱的摩尔比例为1:2~4,优选后为1:2.4~3,进一步优选为1:2.5。
所述铜盐包括CuCl,CuI,CuBr,CuCl
所述铜盐和芳基硫脲的摩尔比例为1:1~100,进一步优选为1:10~100,再进一步优选为1:10~20;
所述非质子性有机溶剂包括为乙腈(MeCN)、甲苯(Toluene)、二甲基亚砜(DMSO)、六甲基磷酰三胺(HMPA)、二甲基甲酰胺(DMF)、N,N-二甲基乙酰胺(DMAc)、四氢呋喃(THF)、1,4-二氧六环(dioxane)、丙酮中一种以上,进一步优选为二甲基亚砜、二甲基甲酰胺、二甲基乙酰胺、1,4-二氧六环中一种以上,再进一步优选为二甲基亚砜、二甲基甲酰胺中一种以上。
所述反应可以在空气的氛围下进行。所述反应温度为80~150℃,进一步优选为90~130℃,再进一步优选为110-125℃。反应完后,加入稀盐酸,用乙酸乙酯萃取,合并有机相,干燥,过滤,减压浓缩,再通过柱层析分离纯化。
所述芳基硫脲IV的制备:芳胺III与硫氰酸铵混合均匀,加入稀盐酸,加热回流,冷却后加水析出固体,过滤后,烘干固体,即可获得芳基硫脲IV,该化合物无需进一步纯化,可直接用于后续反应。
芳胺III的结构为
所述芳胺III与硫氰酸铵摩尔比例为1:(1.5~2.5);所述芳胺III与盐酸摩尔比为1:2~4;所述反应温度为95~105℃;所述反应时间1-15小时;所述稀盐酸的浓度为1.5~2.5M。本发明的方法的反应方程式:
与现有技术相比,本发明具有以下有益效果和优点:
(1)本发明提供的一种利用芳基硫脲和卤代烃合成取代氰胺化合物的方法,所需原料易得,反应原子经济性高,对官能团适应性好和底物适用范围广;
(2)本发明方法操作简单、安全、成本低廉同时转化率和选择性都极高,具有较高的工业化价值。
附图说明
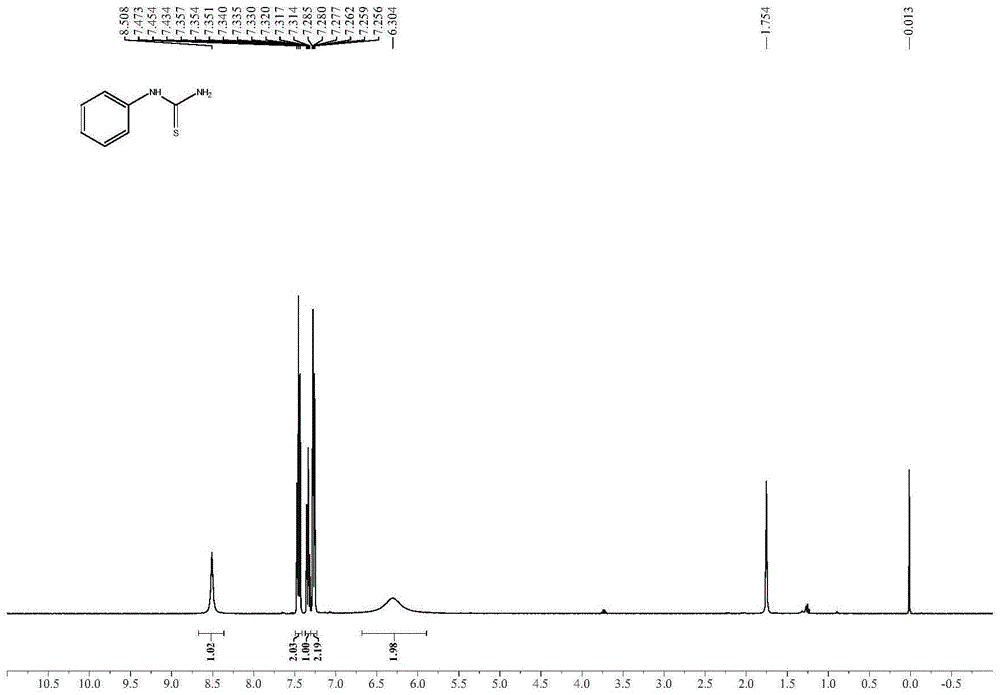
图1和图2分别是实施例1所得产物的核磁氢谱图和核磁碳谱图;
图3和图4分别是实施例5-10所得产物3aa的核磁氢谱图和核磁碳谱图;
图5和图6分别是实施例5-10所得产物4a的核磁氢谱图和核磁碳谱图;
图7和图8分别是实施例11所得产物3ab的核磁氢谱图和核磁碳谱图;
图9和图10分别是实施例11所得产物4b的核磁氢谱图和核磁碳谱图;
图11和图12分别是实施例15所得产物3af的核磁氢谱图和核磁碳谱图;
图13和图14分别是实施例15所得产物4f的核磁氢谱图和核磁碳谱图;
图15和图16分别是实施例27所得产物3ha的核磁氢谱图和核磁碳谱图;
图17、图18和图19分别是实施例29所得产物3ja的核磁氢谱、碳谱和氟谱。
具体实施方式
下面结合实施例对本发明作进一步地详细说明,但本发明的实施方式和保护不限于此。实施例1-4为芳基硫脲的合成方法示例;实施例5-36为一锅法同时制备氰胺和硫醇示例。
实施例1:苯基硫脲的制备
在含有聚四氟乙烯包裹的磁力搅拌子的50mL圆底烧瓶中,依次加入1.0g(10.74mmol)苯胺、1.63g(21.48mmol)硫氰酸铵和11mL稀盐酸(2.0M),加热回流12小时,冷却至室温后,加水稀释,过滤收集生成的白色固体,烘干后,即可获得所需苯基硫脲1.50g(92%)。
实施例2:3,5-二甲基苯基硫脲的制备
在含有聚四氟乙烯包裹的磁力搅拌子的50mL圆底烧瓶中,依次加入1.0g(8.25mmol)3,5-二甲基苯胺、1.26g(16.50mmol)硫氰酸铵和10mL稀盐酸(2.0M),加热回流12小时,冷却至室温后,加水稀释,过滤收集生成的白色固体,烘干后,即可获得所需3,5-二甲基苯硫脲1.350g(87%)。
1
实施例3:2,4-二氯苯基硫脲的制备
在含有聚四氟乙烯包裹的磁力搅拌子的50mL圆底烧瓶中,依次加入1.0g(6.17mmol)2,4-二氯苯胺、0.940g(12.34mmol)硫氰酸铵和7mL稀盐酸(2.0M),加热回流12小时,冷却至室温后,加水稀释,过滤收集生成的白色固体,烘干后,即可获得所需2,4-二l氯苯基硫脲1.20g(88%)。
1
实施例4:2,5-二甲氧基苯基硫脲的制备
在含有聚四氟乙烯包裹的磁力搅拌子的50mL反应容器中,依次加入1.0g(6.53mmol)2,5-二甲氧基苯胺、0.993g(13.06mmol)硫氰酸铵和7mL稀盐酸(2.0M),加热回流12小时,冷却至室温后,加水稀释,过滤收集生成的白色固体,烘干后,即可获得所需2,5-二甲氧基苯基硫脲1.12g(81%)。
1
实施例5
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、2-氯乙基苯2a(67.5mg,0.48mmol)、碳酸钠(69.1mg,0.5mmol)、Cu(OH)
3aa:
4a:
实施例6
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、2-氯乙基苯2a(67.5mg,0.48mmol)、碳酸钾(0.5mmol)、Cu(OH)
3aa:
4a:
实施例7
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、2-氯乙基苯2a(67.5mg,0.48mmol)、碳酸铯(0.5mmol)、Cu(OH)
3aa:
4a:
实施例8
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、2-氯乙基苯2a(67.5mg,0.48mmol)、碳酸氢钾(0.5mmol)、Cu(OH)
3aa:
4a:
实施例9
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、2-氯乙基苯2a(67.5mg,0.48mmol)、碳酸氢钠(0.5mmol)、Cu(OH)
3aa:
4a:
实施例10
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、2-氯乙基苯2a(67.5mg,0.48mmol)、氢氧化锂(0.5mmol)、Cu(OH)
3aa:
4a:
图3和图4分别是实施例5-10所得产物3aa的核磁氢谱图和核磁碳谱图;图5和图6分别是实施例5-10所得产物4a的核磁氢谱图和核磁碳谱图。
实施例11
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、1-氯-4-(2-氯乙基)苯2b(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ab:
4b:
图7和图8分别是实施例11所得产物3ab的核磁氢谱图和核磁碳谱图;图9和图10分别是实施例11所得产物4b的核磁氢谱图和核磁碳谱图。
实施例12
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、1-氟-4-(2-氯乙基)苯2c(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ac:
4c:
实施例13
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、4-氟丁基苯2d(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ad:
4d:
实施例14
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、氯化苄2e(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ae:
4e:
实施例15
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、1,3-二氯-2-氯甲基苯2f(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3af:
4f:
图11和图12分别是实施例15所得产物3af的核磁氢谱图和核磁碳谱图;图13和图14分别是实施例15所得产物4f的核磁氢谱图和核磁碳谱图。
实施例16
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、肉桂基氯2g(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ag:
4g:
实施例17
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、化合物2h(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ah:
4h:
实施例18
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、溴化苄2i(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ai:
4i:
实施例19
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、碘甲烷2j(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3aj:
实施例20
在反应管中加入苯基硫脲1a(30.4mg,0.2mmol)、1-碘丙烷2k(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ak:
实施例21
在反应管中加入1-(2’-甲基苯基)硫脲1b(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ba:
实施例22
在反应管中加入1-(2’-氯苯基)硫脲1c(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ca:
实施例23
在反应管中加入1-(3’-甲基苯基)硫脲1d(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3da:
实施例24
在反应管中加入1-(4’-甲基苯基)硫脲1e(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ea:
实施例25
在反应管中加入1-(4’-苯基苯基)硫脲1f(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3fa:
实施例26
在反应管中加入1-(4’-甲氧基苯基)硫脲1g(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ga:
实施例27
在反应管中加入1-(4’-溴苯基)硫脲1h(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ha:
图15和图16分别是实施例27所得产物3ha的核磁氢谱图和核磁碳谱图。
实施例28
在反应管中加入1-(4’-乙酰基苯基)硫脲1i(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ia:
实施例29
在反应管中加入1-(4’-三氟甲基苯基)硫脲1j(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ja:
图17、图18和图19分别是实施例29所得产物3ja的核磁氢谱、碳谱和氟谱。
实施例30
在反应管中加入1-(2’-甲基-4’-甲氧基苯基)硫脲1k(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ka:
实施例31
在反应管中加入1-(2’,4’-二氯苯基)硫脲1l(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3la:
实施例32
在反应管中加入1-(2’,6’-二甲基苯基)硫脲1m(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3ma:
实施例33
在反应管中加入1-(2’,6’-二氟苯基)硫脲1n(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3na:
实施例34
在反应管中加入1-(3’,4’-二甲基苯基)硫脲1o(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3oa:
实施例35
在反应管中加入1-(3’,5’-二甲基苯基)硫脲1p(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3pa:
实施例36
在反应管中加入1-(3’,5’-二氯苯基)硫脲1q(0.2mmol)、2-氯乙基苯2a(0.48mmol)、碳酸钠(0.5mmol)、Cu(OH)
3qa:
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其它的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 一种利用氰胺化钙制备的掺氮中孔炭及其制备方法和应用
- 一种纤维素/三聚氰胺甲醛复合树脂及其制备方法
- 一种银-三聚氰胺配合物纳米纤维及链状银纳米材料的制备方法
- 一种尿素和三聚氰胺增强增韧氧化石墨烯改性酚醛树脂泡沫及其制备方法
- 一种用于三聚氰胺检测的溶胶凝胶分子印迹微球的制备方法
- 酰化三聚氰胺及其制备方法、酰化三聚氰胺树脂及其制备方法和应用
- 一种水溶性三聚氰胺树脂的合成方法及所制备的水溶性三聚氰胺树脂
