一种青蒿琥酯基-二苯基脲衍生物ARS-DPU及其制备方法与应用
文献发布时间:2023-06-19 11:34:14
技术领域
本发明涉及肿瘤治疗技术,尤其是可逆转膀胱癌耐药的逆转剂,具体是一种青蒿琥酯基-二苯基脲衍生物ARS-DPU及其制备方法与应用。
背景技术
在恶性肿瘤治疗中,寻找有效的治疗方案,增强肿瘤细胞对化疗药物的敏感性,以及克服肿瘤的耐药性是研究人员和临床实践人员长期以来的目标。膀胱癌是泌尿生殖系统中常见的肿瘤,每年大约43万新增病例,在我国居男性泌尿生殖系统恶性肿瘤发病率第1位(Antoni S,Ferlay J,Soerjomataram I,Znaor A,Jemal A,Bray F.Bladder cancerincidence and mortality:a global overview and recent trends.Eur Urol,2017,71(1):96–108.)。膀胱癌主要分为非肌层浸润性膀胱癌(Non-Muscleinvasive BladderCancer,NMIBC)和肌层浸润性膀胱癌(Muscleinvasive Bladder Cancer,MIBC)。膀胱癌的最典型特征是易复发、转移,患者易对药物产生抵抗。目前对于NMIBC的手术治疗技术已十分成熟,术后定期膀胱灌注化疗药物以预防膀胱癌复发,一线的化疗方案包括甲氨蝶呤+多柔比星+长春新碱+顺铂(MAVC)、吉西他滨+顺铂(GC)(Nadal R,Bellmunt J.Management ofmetastatic bladder cancer.Cancer Treat Rev,2019,76:10–21.)。即便如此,仍有50%以上的患者会复发,另外约30%的患者会进展为MIBC(Smith AB,Deal AM,Woods ME,etal.Muscleinvasive bladder cancer:evaluating treatment and survival in theNational Cancer Data Base.BJU Int,2014,114(5):719–726.)。较NMIBC,MIBC的恶性程度更高,复发、转移及死亡率很高(Kamat AM,Hahn NM,Efstathiou JA,et al.Bladdercancer.Lancet,2016,388:2796–2810.)。膀胱癌复发的重要原因之一是癌细胞对化疗药物产生耐药性,因此寻找合适的耐药逆转剂,提高膀胱癌细胞对化疗剂的敏感度,降低化疗剂的使用剂量,从而降低其毒副作用已成为膀胱癌临床治疗的关键。
青蒿琥酯(Artesunate,ARS)系具有倍半萜内酯结构青蒿素(Artemisinin,ART)的衍生物,化学名二氢青蒿素-1,2-α-琥珀酸单酯。青蒿琥酯是一种常用的抗寄生虫药,其抗疟活性比青蒿素强,已成为临床上治疗疟疾的一线药物。有报道认为,青蒿琥酯主要作用于疟原虫的膜系结构:首先作用于食物泡、表膜、线粒体,其次是核膜、内质网、核内染色物质等。由于干扰原虫表膜——线粒体的功能,阻止原虫消化酶解宿主的血红蛋白成为氨基酸,使疟原虫无法得到自身蛋白质的原料,很快产生氨基酸饥饿,形成自噬泡,并不断排出虫体外,使疟原虫损失大量胞浆,导致虫体瓦解、死亡。青蒿琥酯对疟原虫的无性体有较强的杀灭作用,起效快,能迅速控制疟疾发作,对脑型疟、恶性疟和间日疟都有较好的疗效,对恶性疟的耐氯喹株同样有效。除了抗疟疾作用,其作为化疗增敏剂或逆转剂的作用更是引起人们的广泛关注(向敏,林芳.青蒿琥酯抗肿瘤多耐药的作用及其研究进展.海峡药学,2020,32(3):5–7.)。公开号为CN101125142的专利申请文献中提供了青蒿琥酯在制备作为长春新碱抗肿瘤增效剂药物中的应用。实验表明:青蒿琥酯与长春新碱配伍后,能明显增敏长春新碱,对KBv
发明内容
本发明的目的是针对现有技术的不足,提供一种青蒿琥酯基-二苯基脲衍生物及其制备方法与应用。这种衍生物的制备合成方法简单、反应条件温和、后处理简便,所制备的衍生物应用于逆转现有分子靶向药物肿瘤治疗中的耐药性,尤其是所制备的衍生物与瑞戈非尼或索拉非尼联合使用能逆转膀胱癌细胞株对瑞戈非尼、索拉非尼的耐药性,可进一步拓展瑞戈非尼、索拉非尼的临床应用范围。
实现本发明目的的技术方案是:
一种青蒿琥酯基-二苯基脲衍生物ARS-DPU,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU的化学结构如(I)所示:
制备上述青蒿琥酯基-二苯基脲衍生物ARS-DPU的方法,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的合成路线如Scheme 1所示,包括如下步骤:
1)酰胺化:氮气保护下,青蒿琥酯的二氯甲烷溶液中加入3-氨基苄胺、N,N'-二异丙基碳二亚胺DIC和4-二甲氨基吡啶DMAP,待溶解后,室温下搅拌,TLC监测反应进程,待反应结束,加入饱和食盐水,然后用有机溶剂萃取,保留有机相,减压除去溶剂得到固体,再向得到的固体中加入石油醚、过滤,滤渣交替用石油醚和甲醇洗涤,继而在低于35℃下真空干燥,得到高纯度白色固体产物,即中间体(2);
2)青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的合成:氮气保护下,将步骤1)得到的中间体(2)溶于DMF溶液、加入三乙胺,缓慢滴加4-氯-3-三氟甲基苯基异氰酸酯的DMF溶液,室温下搅拌,减压除去低沸点溶剂和三乙胺,加入蒸馏水,二氯甲烷萃取3次,合并有机相,饱和食盐水洗涤,无水硫酸镁干燥,减压除去溶剂,得粗品,粗品经硅胶柱层析分离,得白色固体,即产品ARS-DPU(I)。
步骤1)中所述青蒿琥酯∶3-氨基苄胺∶DIC:DMAP的摩尔比为1∶1.2-2∶1-2∶0.8-1。
步骤1)中所述的有机溶剂为二氯甲烷、氯仿、四氢呋喃、乙腈、1,4-二氧六环中的一种或他们的混合物。
步骤2)中所述的中间体(2)∶4-氯-3-三氟甲基苯基异氰酸酯的摩尔比为1∶1.2-2。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)用于于逆转肿瘤细胞对化疗剂的耐药性。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)与化疗剂联合使用。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的应用,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)与化疗剂联合使用时的化疗剂为索拉非尼或瑞戈非尼。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的应用,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)应用于逆转现有分子靶向药物肿瘤治疗中的耐药性时,肿瘤细胞株为膀胱癌细胞株,膀胱癌细胞株为人膀胱癌T24细胞株。
本技术方案中的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)与现有技术中的青蒿琥酯的衍生物结构完全不同。
这种衍生物的制备合成方法简单、反应条件温和、后处理简便,所制备的衍生物应用于逆转现有分子靶向药物肿瘤治疗中的耐药性,尤其是所制备的衍生物与瑞戈非尼或索拉非尼联合使用能逆转膀胱癌细胞株对瑞戈非尼、索拉非尼的耐药性,可进一步拓展瑞戈非尼、索拉非尼的临床应用范围。
附图说明
图1为实施例中中间体(2)的
图2为实施例中中间体(2)的
图3为实施例中中间体(2)的的ESI-HRMS图谱;
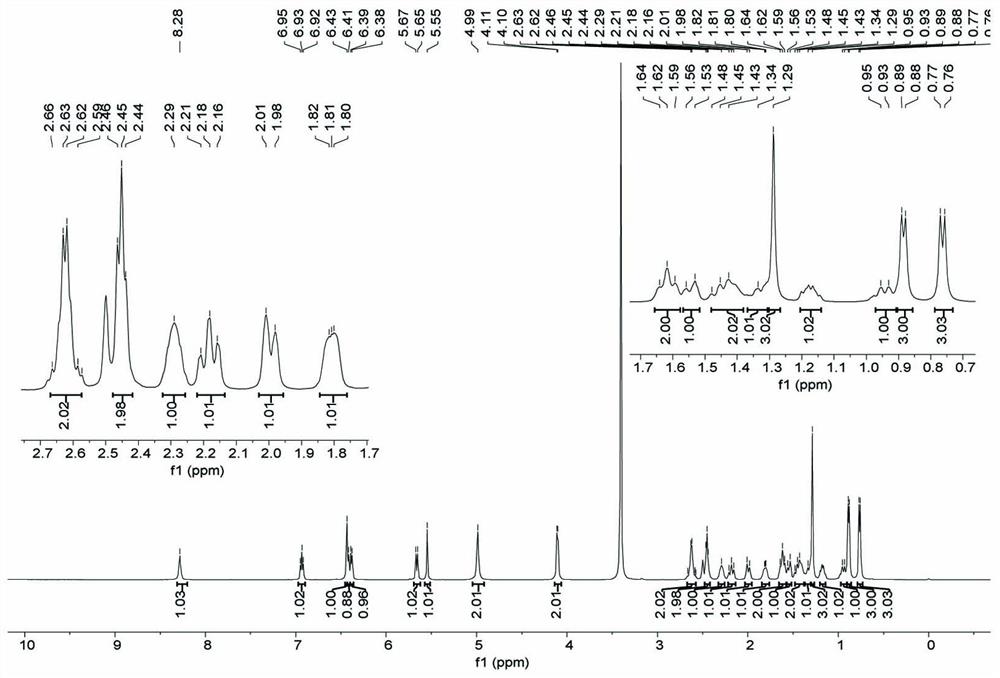
图4为实施例中化合物ARS-DPU的
图5为实施例中化合物ARS-DPU的
图6为实施例中化合物ARS-DPU的ESI-HRMS图谱;
图7为实施例中化合物ARS-DPU加入前后T24/Reg耐药细胞内铁死亡相关蛋白的表达变化图;
图8亲本T24与耐药T24/Sor和T24/Reg细胞内铁死亡相关蛋白表达差异以及化合物ARS-DPU对相关蛋白的影响图。
具体实施方式
下面结合附图和具体实施例对本发明内容作进一步的详述,但不是对本发明的限定。
实施例:
一种青蒿琥酯基-二苯基脲衍生物ARS-DPU,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU的化学结构如(I)所示:
制备上述青蒿琥酯基-二苯基脲衍生物ARS-DPU的方法,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的合成路线如Scheme 1所示,包括如下步骤:
1)酰胺化:氮气保护下,青蒿琥酯的二氯甲烷溶液中加入3-氨基苄胺、N,N'-二异丙基碳二亚胺DIC和4-二甲氨基吡啶DMAP,待溶解后,室温下搅拌,TLC监测反应进程,待反应结束,加入饱和食盐水,然后用有机溶剂萃取,保留有机相,减压除去溶剂得到固体,再向得到的固体中加入石油醚、过滤,滤渣交替用石油醚和甲醇洗涤,继而在低于35℃下真空干燥,得到高纯度白色固体产物,即中间体(2);
2)青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的合成:氮气保护下,将步骤1)得到的中间体(2)溶于DMF溶液、加入三乙胺,缓慢滴加4-氯-3-三氟甲基苯基异氰酸酯的DMF溶液,室温下搅拌,减压除去低沸点溶剂和三乙胺,加入蒸馏水,二氯甲烷萃取3次,合并有机相,饱和食盐水洗涤,无水硫酸镁干燥,减压除去溶剂,得粗品,粗品经硅胶柱层析分离,得白色固体,即产品ARS-DPU(I)。
步骤1)中所述青蒿琥酯∶3-氨基苄胺∶DIC:DMAP的摩尔比为1∶1.2-2∶1-2∶0.8-1。
步骤1)中所述的有机溶剂为二氯甲烷、氯仿、四氢呋喃、乙腈、1,4-二氧六环中的一种或他们的混合物。
步骤2)中所述的中间体(2)∶4-氯-3-三氟甲基苯基异氰酸酯的摩尔比为1∶1.2-2。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)用于逆转肿瘤细胞对化疗剂的耐药性。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)与化疗剂联合使用。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的应用,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)与化疗剂联合使用时的化疗剂为索拉非尼或瑞戈非尼。
上述制备方法制备的青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的应用,所述青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)应用于逆转现有分子靶向药物肿瘤治疗中的耐药性时,肿瘤细胞株为膀胱癌细胞株,膀胱癌细胞株为人膀胱癌T24细胞株。
具体地:
实施例1:
中间体(2)的合成及产物表征:
中间体(2)的合成如式(3)所示,包括如下步骤:
氮气保护下,100mL三口瓶中依次加入3.84g青蒿琥酯的二氯甲烷溶液50mL、3-氨基苄胺1.83g、N,N'-二异丙基碳二亚胺DIC1.89g和4-二甲氨基吡啶DMAP1.03g,待溶解后,室温下搅拌2h,反应结束后加入30ml饱和食盐水,用有机溶剂萃取,保留有机相,减压除去溶剂得到固体,再向得到的固体中加入石油醚、过滤,滤渣交替用石油醚和甲醇洗涤,继而在低于35℃下真空干燥,得到高纯度白色固体产物4.21g,即中间体(2),产率86.2%,中间体(2)的原始图谱如图1、图2、图3所示,产物表征为:
m.p.170.6–171.8℃.
实施例2:
青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的合成及产物表征:
青蒿琥酯基-二苯基脲衍生物ARS-DPU(I)的合成如式(4)所示,包括如下步骤:
氮气保护下,将实施例1制备的中间体(2)2.44g溶于DMF溶液20mL,加入三乙胺3mL,缓慢滴加4-氯-3-三氟甲基苯基异氰酸酯1.33g的DMF溶液10mL,室温下搅拌2h,减压除去低沸点溶剂和三乙胺,加入15mL蒸馏水,二氯甲烷萃取3次,每次45mL,合并有机相,用饱和食盐水洗涤、无水硫酸镁干燥,减压除去溶剂,得粗品,粗品经硅胶柱层析分离,得白色固体,即产品ARS-DPU(I),产率60.5%,化合物ARS-DPU的原始图谱如图4、图5、图6所示,产物表征为:
m.p.159.8–160.6℃.
实施例3:
前期研究发现:膀胱癌细胞株T24对两种已上市药物瑞戈非尼(Regorafenib,Reg)和索拉非尼(Sorafenib,Sor)均耐药,采用体外低浓度梯度递增联合大剂量间断冲击方法,建立两种耐药细胞株:T24/Reg和T24/Sor,具体方案如下:其中,瑞戈非尼和索拉非尼的化学结构式如下所示:
将对数生长期的T24细胞按每个孔5×10
表1:
实施例4:
ARS-DPU对耐药细胞株T24/Sor和T24/Reg的逆转活性评价:
取对数生长期的耐药细胞株T24/Sor(或T24/Reg)接种于96孔板中,分别加入索拉非尼(Sor),瑞戈非尼(Reg),并以化合物ARS-DPU为耐药逆转剂,青蒿琥酯(Artesunate,ARS)、维拉帕米(Verapamil,Ver)为逆转剂阳性参照,T24为亲本细胞株,ARS-DPU、ARS、Ver的终浓度分别为0、4、8、12.5、15、20、25、30、37.5、40、50μM,Reg(或Sor)的终浓度分别为0、2、4、6、7、8、10、12μM,其它条件以及检测方法同实施例3,实验结果如表2、表3所示,增殖抑制活性部分数据列于表4中,按照上述方法,检测化合物ARS-DPU、ARS和Ver对其它几种细胞株(包括正常细胞株和肿瘤细胞株)的增殖抑制活性,半数抑制浓度(IC
1)化合物ARS-DPU可分别逆转索拉非尼、瑞戈非尼的耐药性,其效果明显优于常用的耐药逆转剂维拉帕米;
2)化合物ARS-DPU对膀胱癌细胞株的增殖抑制活性很低:其对T24、EJ和5637细胞株的IC
3)在Sor+ARS-DPU组合中,索拉非尼和ARS-DPU的浓度分别为7.12,25μM,此时对T24/Sor逆转耐药的效果最佳,逆转倍数为3.25,青蒿琥酯在相同浓度下几乎不能逆转索拉非尼的耐药性,维拉帕米甚至在50μM的浓度下亦不能;
4)较组合Sor+ARS-DPU,组合Reg+ARS-DPU逆转耐药的效果更佳,即化合物ARS-DPU逆转瑞戈非尼耐药的效果优于索拉非尼,该组合中,瑞戈非尼和ARS-DPU的浓度分别为8.02,25μM时逆转耐药的效果最佳,逆转倍数为11.04;
5)当逆转剂浓度固定为25μM,ARS-DPU能显著逆转索拉非尼、瑞戈非尼的耐药性,但是相同浓度下维拉帕米几乎不能逆转T24/Sor细胞株对索拉非尼的耐药性,仅对瑞戈非尼显示较弱的逆转活性;
6)为了便于计算,后续实验组合Sor+ARS-DPU中索拉非尼和ARS-DPU的浓度分别选取7,25μM;组合Reg+ARS-DPU中瑞戈非尼和ARS-DPU的浓度分别选取8,25μM。
表2 ARS-DPU及其组合(Sor+ARS-DPU)对膀胱癌亲本和耐药细胞株的增殖抑制活性:
表3 ARS-DPU及其组合(Reg+ARS-DPU)对耐药细胞株T24/Reg的增殖抑制活性:
表4不同浓度化合物ARS-DPU及其组合对膀胱癌亲本和耐药细胞株的增殖抑制活性(孵育时间:48h):
表5化合物ARS-DPU、青蒿琥酯和维拉帕米和对其它数种肿瘤和正常细胞株的增殖抑制活性:
实例5:
亲本和耐药细胞株胞内铁死亡相关蛋白的检测:
现有技术中,死亡不仅是所有细胞的最终命运,而且它与细胞分裂、增殖一样,在整个机体的生长、发育中具有不可替代的作用,目前认为除了坏死外,细胞死亡方式分为程序性细胞死亡(programmed cell death,PCD),包括凋亡(apoptosis)、铁死亡(ferroptosis)和自噬(autophagy),以及非程序性细胞死亡(non-programmed celldeath,NPCD),包括副凋亡(paraptosis)、细胞有丝分裂灾难(mitotic catastrophe)和胀亡(oncosis)等(Tang D,Kang R,Berghe TV,et al.The molecular machinery ofregulated cell death.Cell Res,2019,29(5):347–364.)。2012年Dixon等(Dixon SJ,Lemberg KM,Lamprecht MR,et al.Ferroptosis:an iron-dependent form ofnonapoptotic cell death.Cell,2012,149(5):1060–1072.)提出了一种铁依赖的细胞死亡方式,称为铁死亡。铁死亡在形态、生物化学和基因水平上,均不同于目前已知的细胞凋亡、自噬、坏死等其他形式的细胞死亡,与肿瘤、神经系统和缺血再灌注损伤等多种临床疾病密切相关。胱氨酸/谷氨酸逆向转运体System Xc
由于ARS-DPU对瑞戈非尼耐药细胞株T24/Reg的逆转效果更佳,选取该耐药细胞株进行深入的研究,组合Reg+ARS-DPU中瑞戈非尼和化合物ARS-DPU的浓度分别选取8,25μM,T24/Reg细胞接种于9cm培养皿,以Ver为逆转剂阳性参照,未加入任何逆转剂、ARS-DPU(或药物)的为空白对照组。各组孵育16h后,收集细胞,加入蛋白裂解液后提取总蛋白,以BCA试剂盒测定蛋白浓度,根据结果调整各组蛋白,使之含量相同,以十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)试剂盒,根据说明书配方配制适宜浓度的SDS-PAGE胶,取20μg蛋白在电泳仪中进行电泳,转移目的蛋白至硝酸纤维膜上,加入5%的脱脂奶粉,室温下封闭2h,分别加入适宜浓度的兔源GAPDH、以及铁死亡相关蛋白(如xCT、GPx4、TFR1、DMT1、p62、Keap1、Nrf2、HO-1等)对应的一抗,4℃条件下孵育过夜,TBST洗膜后加入适宜浓度的二抗,4℃条件下孵育2h,以化学发光试剂显色,采用Image Lab软件分析蛋白条带得出蛋白的相对表达量,实验重复3次,如图7所示,实验结果表明:在图7(A)中,每个条带共7个泳道,各泳道对应的分组及浓度如下,(1)—空白对照组;(2)—Reg(8μM);(3)—Reg(16μM);
(4)—Reg(8μM)+ARS-DPU(25μM);(5)--Reg(8μM)+Ver(25μM);(6)--ARS-DPU(25μM);(7)--Ver(25μM).在图7(B)和7(C)中,与空白对照组相比,*p<0.05,**p<0.01,***p<0.001。较空白对照组,组合Reg(8μM)+ARS-DPU(25μM)能明显下调T24/Reg耐药细胞内xCT,GPx4,Nrf2和HO-1的表达,同时能上调p62,Keap1的表达。
为了进一步验证化合物ARS-DPU在诱导铁死亡中的作用,按照上述操作,比较T24亲本细胞株与耐药细胞株T24/Sor和T24/Reg胞内铁死亡相关蛋白表达的差异,结果如图8所示,结果表明:1)3株细胞(T24,T24/Sor和T24/Reg)内TFR1和FTL蛋白表达没有明显变化;
2)在细胞培养时发现两株耐药细胞的生长速度比亲本细胞慢,这可能是由于耐药细胞通过降低代谢速率来规避药物对自己的损伤,较T24亲本细胞株,耐药细胞株T24/Sor和T24/Reg胞内关键蛋白GPx4的表达明显上调,且Keap1蛋白表达下调,Nrf2蛋白上调,暗示T24/Sor和T24/Reg可通过抑制铁死亡机制产生耐药性,其耐药机制与Keap1-Nrf2通路相关。
在图8中也显示了化合物ARS-DPU在12h时对T24细胞内铁死亡相关蛋白的影响,基于ARS-DPU对IRP2、HO-1、GPx4等蛋白表达量的影响结果,ARS-DPU极可能经下调IRP2、HO-1蛋白表达,进而干预细胞内铁代谢过程,并通过下调GPx4蛋白的表达,最终诱导细胞发生铁死亡。
研究结果表明:低毒性的化合物ARS-DPU通过诱导膀胱癌耐药细胞株发生铁死亡,增强化疗剂瑞戈非尼、索拉非尼对膀胱癌耐药细胞株的敏感性,逆转耐药细胞株对上述两种化疗剂的耐药性。
综上的结果说明:
1)化合物ARS-DPU可能是膀胱癌亲本T24,以及耐药细胞株(T24/Sor和T24/Reg)的铁死亡诱导剂;
2)化合物ARS-DPU通过诱导铁死亡,增强化疗剂瑞戈非尼、索拉非尼对耐药细胞株的敏感性,逆转两种耐药细胞株T24/Reg和T24/Sor的耐药性。
试验表明:ARS-DPU与瑞戈非尼(或索拉非尼)两者配伍使用,可有效逆转膀胱癌细胞株对瑞哥非尼(或索拉非尼)的耐药性,可进一步拓展上述两种化疗剂的临床应用范围。
- 一种青蒿琥酯基-二苯基脲衍生物ARS-DPU及其制备方法与应用
- 一种青蒿琥酯基-二苯基脲衍生物ARS-DPU及其制备方法与应用
