浙麦冬来源化合物及其应用、药物组合物
文献发布时间:2023-06-19 11:40:48
技术领域
本发明涉及一种化合物及其医药用途,还涉及包含该化合物在药物组合物。
背景技术
恶性肿瘤是危害人类健康的三大疾病之一,具有较高的发病率和死亡率。现代西医治疗主要以化疗为主,毒副作用较大,患者生存期质量明显下降。中医药在抗癌防癌、减少不良反应等方面发挥了独特优势,是研发新型抗肿瘤药物的宝库。目前来源于中草药的抗癌制剂,占总抗癌药30%以上,如紫杉类、喜树碱、长春新碱等已经作为对抗抗肿瘤的首选药。
然而为了寻找更理想的抗癌化合物,人们并未停止寻找植物来源的具有抗癌活性的化合物的步伐。
浙麦冬(Ophiopogon japonicus(Thunb.)Ker-Gawl),为百合科沿阶草属多年生常绿草本植物。其须根较粗壮,根的顶端或中部常膨大成为纺锤状肉质小块,是一种中药材。中医认为,浙麦冬微苦,微寒。归心、肺、胃经。具有养阴生津,润肺清心。用于肺燥干咳,虚痨咳嗽,津伤口渴,心烦失眠,内热消渴,肠燥便秘,咽白喉。同时用于肺胃阴虚之津少口渴、干咳咯血;心阴不足之心悸易惊及热病后期热伤津液等证。
本发明的目的在于,从浙麦冬来源的天然化合物中,筛选抗肿瘤活性的先导化合物,从而为新型抗癌药物的研发和制备提供了新的选择。
发明内容
为了进一步寻找更多的植物来源的具有抗癌活性的化合物,本发明的发明人对中药浙麦冬的化学成分进行了深入的研究,结果从中分离出了一种麦冬黄酮类新化合物,其结构式如式(I)所示:
根据化合物的骨架分类,此化合物应该属于高异黄酮类化合物,这是黄酮化合物中特殊的一类,其母体结构中竟然比异黄酮多一个碳原子,因此生源合成途径是特异的,在自然界发现的很少,只存在于少数的植物中。本发明的高异黄酮具体为甲基高异黄酮,也称为麦冬黄酮类(Ophiopogonone)化合物。
本发明的式(I)所示化合物按照一般的天然产物中黄酮类的系统编号的化学式如下所示:
据发明人考证,至今为止,骨架6,8位存在甲基化并且在3为存在OH取代的化合物尚无从天然产物界获得该化合物的报道,也并无人合成该化合物,确定该化合物是首次发现的化合物。
本发明的化合物在天然药材中含量比较低,按照发明人的推算,在干药材中其含量大概是1.2ppm这样的数量级,天然药材的相关活性不可能与该化合物的活性直接相关。
然而,更为令人意外的发现是,上述式(I)所述的新颖结构化合物在抗癌活性测试中显示了明显的抗癌活性。迄今为止报道的有抗癌活性潜力的来源于浙麦冬的化合物与本发明上述式(I)所述化合物的在结构上差别较大,因此,该活性效果是令人意想不到的新发现,为新型抗癌药物的研发和制备提供了新的选择。
具体而言,本发明提供了以下的技术方案:
本发明提供一种化合物,其结构如式(I)所示:
本发明中,若无特别说明,化学元素通常包含化学性质相同的同位素的概念,例如“氢”的表述,也包括化学性质相同的“氘”、“氚”的概念,碳(C)则包括
本发明的化合物或其生理上可以接受的盐由于展示了抗癌的活性(参见具体实施方式),因此能够在在制备治疗癌症药物中应用,这里的所述治疗癌症药物优选的是治疗血癌、肝癌、乳腺癌、结肠癌的药物,但是并不限于这些抗癌药物,优选为治疗血癌的药物。
另外,本发明还提供一种医药组合物,其包含上述式(I)所述化合物和药学上可接受的载体。所述药学上可接受的载体,是指本发明的化合物制成制剂时,可以配合药学上可以接受的辅料一起使用,这些辅料可例举包括药学领域常规的溶剂(如水、乙醇、丙二醇、注射用油等)、稀释剂(如淀粉、糖粉、糊精、乳糖、预胶化淀粉、微晶纤维、无机钙盐(如硫酸钙、磷酸氢钙、药用碳酸钙等)、甘露醇等、植物油、聚乙二醇等)、粘合剂(如水、乙醇、淀粉浆、羧甲基纤维素钠、羟丙基纤维素、甲基纤维素和乙基纤维素、羟丙甲纤维素等)、崩解剂(如干淀粉、羧甲基淀粉钠、低取代羟丙基纤维素、交联聚乙烯吡咯烷酮、交联羧甲基纤维素钠等)、润滑剂(如硬脂酸镁、微粉硅胶、滑石粉、氢化植物油、聚乙二醇类、月桂醇硫酸镁等)、吸收促进剂(如表面活性剂、Azone(月桂氮卓酮)、EDTA、水杨酸、氨基酸乙胺衍生物、乙酰醋酸酯类、β-二羧酸酯、芳香族酸性化合物、脂肪族酸等)、防腐剂(如苯甲酸、羟丙丁酯、羟丙甲酯、苯酚、间甲酚等)、矫味剂(如蔗糖、甜菊素等)等。但并不限于这些。
本发明的医药组合物可以是各种剂型使用,即可以通过常规的制剂方法给药,例如制成选自片剂、胶囊剂、滴丸剂、颗粒剂、粉剂、口腔膜剂和口服液,或者制成注射剂、膏剂、霜剂、栓剂等,但并不限于这些。从治疗目的和简便程度看,优选将本发明的化合物制成口服制剂。
本发明的化合物可以从浙麦冬中药材的根皮中提取。本发明还提供其提取制备方法,其特征在于,包括以下步骤:
富集步骤,将浙麦冬的干燥块根粉末用85~98%乙醇提取,将提取液浓缩残渣溶于水中,用二氯甲烷进行萃取,得到二氯甲烷馏分;
粗分离步骤,将上述步骤得到的二氯甲烷馏分经过正相硅胶柱层析,采用石油醚-二氯甲烷梯度溶剂体系进行梯度洗脱,溶剂比例变化为石油醚:二氯甲烷以体积比计由10:1变化至1:1,获得相应的组分;
精分离步骤,将上述精分离步骤分离得到的组分再次经过正相硅胶柱层析,用二氯甲烷-甲醇进行梯度,溶剂比例变化为二氯甲烷:甲醇以体积比计由60:1变化至5:1,洗脱,获得相应的组分;
纯化步骤,将上述精分离步骤分离得到的组分在反相硅胶柱色谱上层析,获得目标化合物。
本发明当然也可以根据全合成或者半合成的方式获得,这些可以根据在本领域中公知的有机合成方法获得。
附图说明
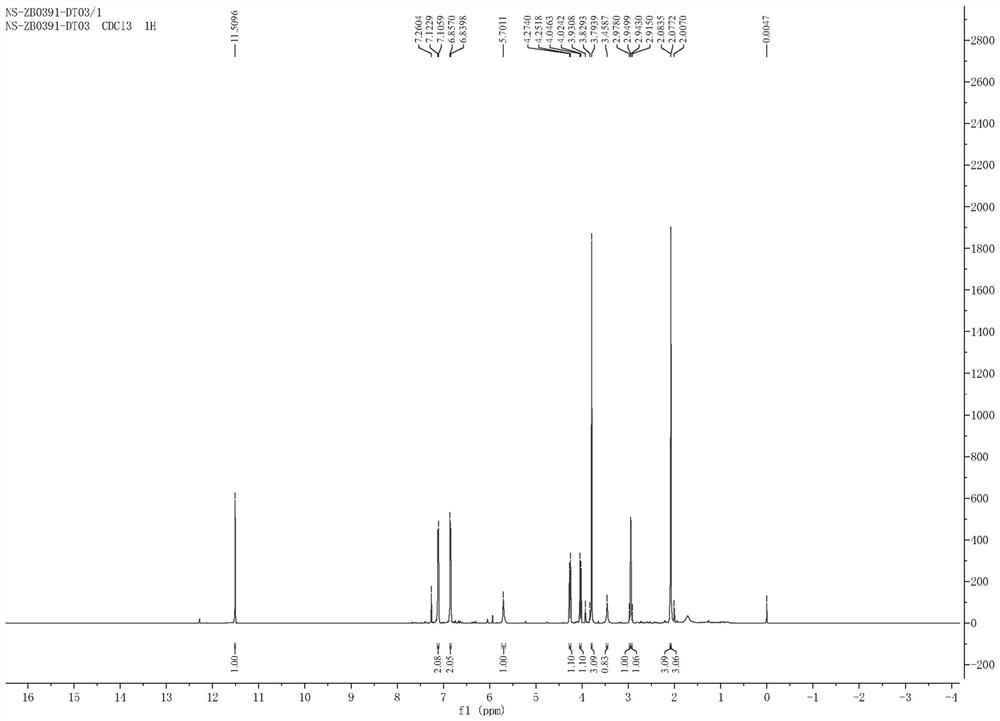
图1为本发明化合物的
图2为本发明化合物的
图3为本发明化合物的
图4为本发明化合物的HSQC谱图;
图5为本发明化合物的HMBC谱图;
图6为本发明化合物的NOESY谱图;
图7为本发明化合物的高分辨率质谱图;
图8为本发明化合物的HPLC谱图;
图9为本发明化合物的紫外谱图。
具体实施方式
以下记载本发明式(I)所示化合物(也简称“本发明化合物”)如何获得的方法。还具体披露了式(I)所示化合物抗癌活性的具体实验方法。
下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的原料、试剂材料等,如无特殊说明,均为市售购买产品。
本发明化合物的提取分离流程具体如下:
①本发明所用的浙麦冬药材采购自浙江慈溪,产品包装带有农产品地理标志登记证书,经形态学鉴别为浙麦冬。
以20kg麦冬的干燥块根粉末为原料,用95%乙醇在室温下提取3次,每次4小时。减压浓缩除去溶剂,残渣(1960克)溶解于水中,并依次用石油醚(3×5L)、二氯甲烷(3×5L)和乙酸乙酯(3×5L)进行萃取分离。将二氯甲烷萃取部位产物(180g)以硅胶柱层析分离,用石油醚-二氯甲烷(10:1–1:1v/v)梯度洗脱得到八个部分(Fr.A–Fr.H)。
②将步骤①二氯甲烷萃取部位产物(180g)以硅胶柱层析分离,用石油醚-二氯甲烷(10:1–1:1v/v)梯度洗脱得到八个部分(Fr.A–Fr.H)。
③对步骤②获得的Fr.C部分(25g)进行硅胶柱层析,用二氯甲烷-甲醇进行梯度(60:1;40:1;20:1;10:1;5:1v/v)洗脱,得到六个部分(Fr.1–6)。
④对Fr.2部分用制备型HPLC制备,使用YMC Pack ODS-A(50*250mm,7um)色谱柱,以甲醇-水(80:20,v/v)洗脱,通过制备,得到本发明式(1)表示的化合物(24.5mg,tR=10.72min)。
对实施例得到的新化合物进行产品分析;本发明化合物的
另外,本发明图8的HPLC检测条件如下:
色谱柱:Agilent SB-C18(4.6×250mm,5μm)
洗脱剂:乙腈(A):水(B)
梯度条件:0→15→23→24→50min;8%→20%→28%→65%→70%(A)
检测器:296nm紫外检测器
柱温:30℃
流速:1ml/min
本发明化合物的紫外光谱参见图9
通过对其高分辨MS(m/s 343.1170[M-H]
核磁共振图谱的解析参考以下解说:在
具体核磁数据归属如表1所示:
表1.
细胞毒活性实验方法(初筛):
肿瘤的产生是丧失细胞功能调控的结果,生长信号异常和细胞周期调控异常会导致细胞增殖的异常,最终产生恶性克隆。所以癌细胞的特征之一就是异常增殖。抑制癌细胞的增殖是治疗癌症的重要途径之一,也是抗肿瘤药物的基本要求。将新化合物分别作用于白血病HL-60、肺癌A549、肝癌SMMC-7721、乳腺癌MCF-7、结肠癌SW480上24小时后,通过CCK-8法在450nm波长处测定吸光度值来检测癌细胞增殖抑制作用。
将HL-60、A549、SMMC-7721、MCF-7以及SW480细胞以1×10
抑制率(%)=[(对照组OD450nm-给药组OD450nm)/((对照组OD450nm-空白组OD450nm)]×100
具体实验结果,见表2:
本次实验对麦冬黄酮类新化合物对肿瘤细胞增殖抑制活性进行评价,结果显示在40μmol/L浓度下,化合物对人白血病HL-60细胞、人肝癌细胞SMMC-7721、乳腺癌MCF-7及结肠癌SW480均有较好的增殖抑制作用,说明该化合物对于以上癌细胞具有选择性增殖抑制作用。尤其是对于人白血病HL-60细胞抑制率均在80%以上,效果明显,是理想的候选先导化合物。
细胞毒活性实验方法(复筛):
1.接种细胞(cell系HL-60,SMMC-7721,和MCF-7):用含10%胎牛血清的培养液(DMEM)配成单个细胞悬液,以每孔3000~15000个细胞接种到96孔板,每孔体积100μl,细胞提前12~24小时接种培养。
2.加入待测化合物溶液:化合物用DMSO溶解,分别配置以下5浓度0.064、0.32、1.6、8、以及40μM,每孔终体积200μl,每种处理均设3个复孔。
3.显色:37摄氏度培养48小时后,贴壁细胞弃孔内培养液,每孔加MTS溶液20μl和培养液100μl;悬浮细胞HL-60弃100μl培养上清液,每孔加20μl的MTS溶液;设3个空白复孔(MTS溶液20μl和培养液100μl的混合液),继续孵育2~4小时,使反应充分进行后测定光吸收值。
4.比色:选择492nm波长,多功能酶标仪读取各孔光吸收值,记录结果,数据处理后以化合物编号为横坐标,细胞抑制率为纵坐标绘制细胞的抑制率图。
5.阳性对照化合物:每次实验均设顺铂阳性化合物,以浓度为横坐标,细胞存活率为纵坐标绘制细胞生长曲线,应用两点法(Reed and Muench法)计算化合物的IC50值。结果如表3所示。
表3体外活性筛选(复筛)
本发明对于人白血病细胞HL-60的IC50值为14.42μM,肿瘤抑制活性优异。
以上所述的实施例仅是对本发明的优选实施方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
- 来源于浙麦冬的化合物、其应用和药物组合物
- 雷公藤来源化合物及其应用和制备方法、药物组合物、杀虫剂
