一种利用天然低共熔溶剂提取落新妇苷的方法及应用
文献发布时间:2024-04-18 19:58:26
技术领域
本发明属于生物化学和保健食品领域,具体涉及一种利用天然低共熔溶剂提取落新妇苷的方法及应用。
背景技术
现有研究表明,消化酶中的α-葡萄糖苷酶有较高活性,可促进肠道对碳水化合物的消化吸收,使血浆中葡萄糖水平升高,通过抑制α-葡萄糖苷酶的活性,可延缓对碳水化合物吸收,并增加胰岛素分泌,使糖尿病患者餐后血浆中葡萄糖维持在较低水平。因此,通过抑制α-葡萄糖苷酶的活性可缓解糖尿病,对糖尿病有治疗作用,市面上大多糖尿病药物都属于该酶抑制剂;或通过对α-淀粉酶的抑制来阻断淀粉转化为糖类,从而降低血浆中葡萄糖水平,用于血糖的控制。
落新妇苷(Astilbin)是一种天然的膳食黄酮,能发挥多种显著的生物活性,包括选择性免疫抑制、消炎、抗氧化、调节脂肪及血糖等作用。受其疏水性的影响,一般获得落新妇苷的方式为甲醇或乙醇提取,提取率低,既不符合食品开发的安全性要求,又污染环境。天然低共熔溶剂(NaDES)是用食品级原料制备的,近年来已被证明是提取多酚黄酮等活性成分的有效溶剂,并可获得现成的提取物直接运用于食品,但目前还没有应用于落新妇苷的提取。
CN116270772A公开了一种天然低共熔溶剂(氯化胆碱-乳酸)超声提取沙棘黄酮类成分的方法-异鼠李素、山奈酚和槲皮素。CN115925602A公开了一种利用低共熔溶剂(氯化胆碱-乳酸)提取万寿菊中叶黄素的方法。CN106565804A公开了一种黄杞叶落新妇苷的提取工艺,采用乙醇提取落新妇苷。落新妇苷具有低溶解度、低稳定性和低生物可及性的特点。
发明内容
为了得到一种生物可及性高、抗氧化强的落新妇苷提取物,本发明采用天然原料制备绿色环保的天然低共熔容溶剂(氯化胆碱-乳酸),用于提取土茯苓中的落新妇苷,获得了落新妇苷含量高于70%乙醇提取物2倍的天然低共熔溶剂提取物。
本发明通过体外模拟消化系统,分析了落新妇苷的天然低共熔溶剂提取物在消化各阶段的生物利用度和抗氧化能力的变化情况,确定了落新妇苷的天然低共熔溶剂提取物中落新妇苷的生物利用度和抗氧化能力显著高于70%乙醇提取物。
制备天然低共熔溶剂所用的原料(氯化胆碱和乳酸)存在于机体细胞和组织中。其中氯化胆碱可作为维生素类产品,广泛地应用于药品、保健品以及食品营养添加;乳酸常作为食品原料和添加剂。因此落新妇苷的天然低共熔溶剂提取物可以直接用于食品或药品中。
本发明的有益效果:
基于氯化胆碱-乳酸(CHCL-LAC)的NaDES不仅是一种环保的植物化学物质提取溶剂,而且可以作为一种即食载体,用于提高类黄酮等生物活性化合物的生物可及性。因此,新型绿色溶剂的选择解决了提取过程中的环境污染问题,组分的可食用性解决了后期分离的问题;天然低共熔溶剂在模拟消化中存在的保护作用,解决了天然低共熔溶剂提高消化各阶段活性成分生物利用率低的问题。
本发明采用新型环保溶剂天然低共熔溶剂(氯化胆碱-乳酸)提取落新妇苷,获得了高于采用乙醇提取两倍的落新妇苷提取率;采用分子动力学模拟技术,获得了天然低共熔溶剂提取落新妇苷的机制;采用模拟消化体系,获得了比乙醇提取物中落新妇苷生物利用度高84.1%、抗氧化能力高5倍的落新妇苷天然低共熔溶剂提取物。
附图说明
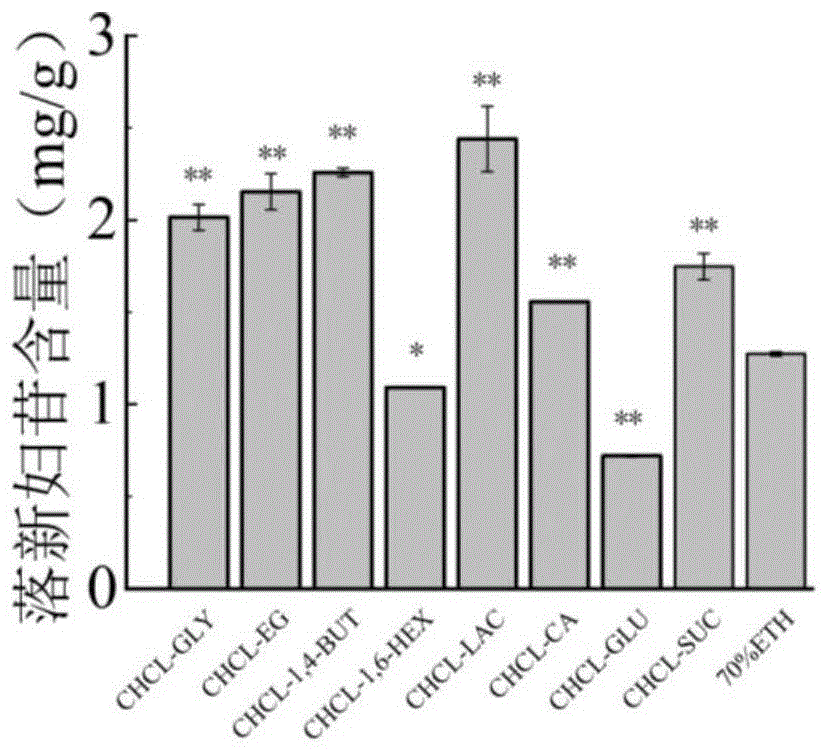
图1NaDES溶剂组分筛选;
图2CHCL-LAC摩尔比筛选;
图3料液比(A)、水分(B)、时间(c)含量三因素之间的交互作用对落新妇苷得率的影;
图4CHCL-LAC提取落新妇苷的最佳条件验证;
图5分子动力学模拟分析:0ns和20ns里,溶解在不同溶剂体系(70%乙醇(v/v)和CHCL-LAC)中的落新妇苷的分布图(A);不同溶剂体系中落新妇苷的平均非共价相互作用(ANI)分析和热波动指数(TFI)分析(B);0ns和20ns里,不同溶剂与落新妇苷间的可及表面积(SASA)(C)、相互作用能(D)、氢键结合数量和氢键寿命(E);
图6不同提取物在体外模拟胃肠道消化过程中落新妇苷生物可及性(A)DPPH抗氧化能力(B)和ORAC抗氧化能力(C)的变化,CHCL-LAC提取物(D)和70%乙醇提取物(E)中落新妇苷与抗氧化能力的相关性分析;
图7落新妇苷CHCL-LAC提取物对α-淀粉酶和α-葡萄糖苷酶的抑制作用结果图。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
1、天然低共熔溶剂制备
将氢键供体(HBDs)和氢键受体(HBA)组成的两种组分混合物置于磁搅拌器上的反应烧瓶中,温度为85℃,时间为60至120分钟,不断搅拌以形成粘性均质液体。NaDES由氯化胆碱(CHCL)与8种不同的HBDs混合组成,包括乳酸(LAC)、柠檬酸(CA)、葡萄糖(GLU)、蔗糖(SUC)、1,6-己二醇(1,6-HEX)、1,4-丁二醇(1,4-BUT)、乙二醇(EG)、甘油(GLY),含水量为20%。
2、天然低共熔溶剂筛选
(1)溶剂种类筛选
以氯化胆碱为氢键受体(HBA),分别以乳酸(LAC)、柠檬酸(CA)、蔗糖(SO)、葡萄糖(G)、1,6-己二醇(HDO)、1,4-丁二醇(BDO)和乙二醇(EG)、丙三醇(GLY)为氢供体(HBD)(表1所示),保持体系含水量20%,以不同的氢键HBD和HBA的摩尔比配制NADES,土茯苓(SGR)粉末以1:20(w/v)的料液比加入不同的NaDES溶剂,50℃超声水浴下提取40分钟;同时对比研究常用的70%乙醇落新妇苷提取法(提取时间90min,料液比10mL/g)。最后采用HPLC测定提取物中的落新妇苷含量,图1显示不同类型的NaDES提取得到的落新妇苷得率。显然,在设计参数下,CHCL-LAC提取得到的的落新妇苷得率(2.44mg/g)最高,显著高于70%乙醇的落新妇苷得率(1.27mg/g)。
表1不同的NaDES体系(含水20%)
(2)摩尔比筛选
最佳溶剂(氯化胆碱-乳酸)进行摩尔比优化,HBA:HBD的摩尔比分别为1:1、1:2、1:3和1:4,以加热搅拌的方式制备NaDES溶剂备用。精密称取60目的SGR过筛粉末0.25g于10mL试管中,分别将上述4种配比的NADES溶剂添加于试管中,充分混匀。于超声仪中设置温度50℃、超声时间40min、功率100W提取,每组重复三次。提取液经沉淀、12000rpm离心10min。采用高效液相色谱测定,并对比不同配比下NaDES提取的落新妇苷含量。
天然低共熔溶剂的摩尔比筛选结果如图2所示。摩尔比为1:1和1:2时,落新妇苷的得率分别为2.25mg/g和2.44mg/g,显著高于摩尔比为1:3(0.12mg/g)和1:4(0.11mg/g)的落新妇苷得率。
3、天然低共熔溶剂提取落新妇苷条件优化
(1)响应面优化
采用三级Box-Behnke响应面设计,研究了料液比(A)、超声辅助时间(B)和水分(C)对NaDES法从SGR中提取落新妇苷含量的影响(表2)。根据Box-Behnken设计,通过改变操作参数对变量进行优化,并根据实验数据进行回归分析。随后,进行了额外的验证性实验,以确认统计实验策略的有效性。采用DesignExpertVer.8.0.6软件对数据进行分析,采用三维响应图对提取效果进行分析。
表2Box-Benhnken试验水平和因素
进一步采用RSM法研究了提取条件对得率的影响,以落新妇苷得率(Y)为因变量,料液比(A)、水分(B)、提取时间(C)为自变量,得到提取的拟合方程为:Y=2.33-0.022a+0.0421B+0.0217C-0.0486AB-0.0037AC-0.0085BC0.1138A2-0.1154B2+0.0484C2。在模型项中,线性项和二次项(A2、B2、C2)的p值均小于0.05,说明它们对落新妇苷的提取有显著影响。三维响应面图(图3)显示了料液比与水分(AB)、水分与时间(BC)、料液比与时间(AC)对落新妇苷得率(Y)的交互影响。当料液比(15mL/g)和水分(30%)分别提高时,可提高落新妇苷的得率,而进一步增加这两个参数可使落新妇苷的得率适度降低。此外,落新妇苷得率受料液比(A)和水分(B)的线性项以及料液比(A2)、水分(B2)和提取时间(C2)的二次项影响明显。在料液比22.87mL/g、水分28.72%、45.07min条件下,土茯苓中落新妇苷的最高得率可达到2.45mg/g。为验证该工艺优化试验的可靠性,考虑到操作的可行性,实际提取结果与工艺优化的预期结果非常接近,显著高于70%乙醇的落新妇苷得率(1.27mg/g)2倍(表3、表4、图4)。
表3响应面实验设计和结果
表4响应面实验回归模拟ANOVA
注:*表示差异显著(p<0.05)
为了揭示CHCL-LAC相对于其他溶剂高得率的机理,采用溶剂体系(CHCL-LAC-70%乙醇(v/v))和落新妇苷进行了分子动力学模拟。如图5A所示,在70%乙醇(v/v)中,从0ns到20ns形成团簇,分子在CHCL-LAC中保持均匀分布,说明在CHCL-LAC中,落新妇苷比乙醇更易溶解。ANI的可视化以及与溶剂分子间相应的TFI列于图5B。与乙醇体系相比,CHCL-LAC中氯阴离子的结构可以连接落新妇苷上羟基的H原子与溶剂分子上其他羟基的H原子,有助于形成更多的氢键,避免碰撞。在ANI分析的基础上,用TFI表示相互作用的稳定性。结果表明,在CHCL-LAC中,落新妇苷的红色区域比在乙醇中要小得多(红色表示相互作用较弱)。表明CHCL-LAC与落新妇苷的相互作用更加稳定,形成了稳定的落新妇苷-CHCL-LAC氢键基超分子。
溶剂可及表面积(SASA)是分子与溶剂接触面积的量度。在CHCL-LAC溶剂中,SASA值保持在260nm
落新妇苷与溶剂分子之间的氢键数和平均寿命如图5E所示。与CHCL-LAC的平均氢键数为660.84,远高于乙醇(543.78个氢键)(图5E)。在CHCL-LAC体系中,落新妇苷的氢键平均寿命为12ps,远高于乙醇体系中的8.5ps(图5E),说明在CHCL-LAC体系中形成的落新妇苷氢键比在70%乙醇体系中形成的落新妇苷氢键具有更高的稳定性,这也使得用CHCL-LAC体系提取落新妇苷的得率高于乙醇。分子动力学模拟结果表明,落新妇苷与CHCL-LAC之间可能形成稳定的基于氢键的超分子,具有分布更广、SASA更高、相互作用更紧密、相互作用能更低、氢键平均寿命更长等特点。
(2)HPLC测定落新妇苷含量
以95%纯度的落新妇苷为标准品,制备标准液,绘制标准曲线,测定提取物中的落新妇苷含量,色谱条件如下:
色谱柱:WAT054275Symmetry C18(4.6mm×250mm,5μm),流速1.0mL/min,柱温30℃,检测波长291nm,进样量10μL,流动相为甲醇:水(30:70,v/v)
4、提取机制研究
分子动力学模拟(MD)分析采用GROMACS2019.6包,采用Amber(99SB-ildn)力场进行。MD仿真在NPT内进行1ns,2fs步长,每500帧保存一次轨迹坐标,共1000帧。结合Multiwfn3.8(dev)计算平均非共价相互作用(ANI)和热涨落指数(TFI)。采用高斯16编码和6-31+g(d,p)基函数计算落新妇苷、乙醇、氯化胆碱和乳酸分子的部分电荷。利用OPLSS-AA力场和MKTOP对所有原子进行参数化,如键参数、角参数和二面角等。采用分子动力学(MD)模拟方法研究了落新妇苷在乙醇和DES中的分布。水分子的模型为TIP3P。经过20ns的MD模拟,分析了落新妇苷与70%乙醇/NaDES之间的氢键数量、氢键寿命、相互作用能和溶剂可达表面积(SSA)。
5、NaDES提取物的体外消化
(1)生物利用度评价
分别将5毫升CHCL-LAC提取物、70%乙醇提取物(在PBS中重新溶解)和纯落新妇苷(在PBS中溶解)混合到模拟胃液(SGF)中。再加入猪胃蛋白酶(0.8mL,12500U/mL)和氯化钙(2.5μL,0.3M),pH调至2±0.2。每个样品的最终重量加水达到10g。然后,将混合物置于37℃、150rpm水浴中孵育30、60、90、120min。胃消化后,用1M NaOH调整全胃食糜pH值至6.8,进行随后的肠道消化,并与4.4mL模拟肠液、1mL胰酶(800U/mL)、16μL氯化钙(0.3M)和1mL胆盐(10mM)混合。最后将pH调至7±0.2,37℃继续孵育60、90、120、180min。在每个消化点,测量消化液的质量,并对消化液进行HPLC分析。按(1)计算落落新妇苷的生物可及性(%)
落新妇苷的生物利用度(%)=(特定消化阶段的落新妇苷含量/初始的落新妇苷含量)×100%(1)
(2)抗氧化能力测定
DPPH指标测定:准确称取Trolox(98%)标准品,采用无水乙醇溶解得到1000μM的标准品母液,无水乙醇梯度稀释为0、50、100、200、300、400、500μM标准品溶液。使用无水乙醇制备浓度为0.50mmol/l的DPPH溶液。将上述不同阶段的样品消化液各取50μL,加入150μL的DPPH溶液,混合均匀后充分震荡,在室温下避光放置反应30min,采用酶标仪于波长517nm处测定吸光光度值记为Asample。以无水乙醇代替DPPH溶液与样品溶液按比例混合均匀做对照,去除样品溶液颜色干扰,测定吸光值记为Acontrol。空白组以无水乙醇代替样品溶液与DPPH溶液按比例混匀,测定吸光值记为Ablank。以Trolox(水溶性VE)溶液作为阳性对照。每次测定设置三个平行,以其平均值计算DPPH自由基清除率,计算公式(2)如下:
DPPH自由基清除率(%)=【1-{(A
ORAC反应体系应在37℃下,PBS溶液中进行。测定前先进行酶标仪预热,读板前确认仪器加热到37℃,向黑色96孔的酶标板各微孔中分别加入不同浓度的待测样品溶液(需用PBS溶液溶解)、PBS(空白组)、标准溶液25μL,加入荧光素钠溶液150μL,盖上酶标板盖于仪器中孵育30min。后用多道移液器迅速在各微孔中加入现配好的AAPH溶液启动反应,将酶标板置于酶标仪,以激发波长485nm,发射波长518nm进行连续测定荧光强度。每2min采集一次各微孔荧光强度信号,测定时间设定在其荧光衰减呈基线后为止,每个样品分别作3次平行测定。样品溶液的抗氧化能力用Trolox当量(Trolox equivalent)表示。
CHCL-LAC提取物及70%乙醇提取物体外模拟胃肠消化过程中,落新妇苷的生物可及性和抗氧化能力结果见表5-7和图5。
胃消化和肠消化阶段的液体中落新妇苷残留量如图6所示。胃消化2h后,液体中落新妇苷有少量损失,残留量均大于90%,说明胃消化过程中落新妇苷是稳定的。肠道消化中,两种提取物中的落新妇苷均有明显的降解,其中70%乙醇提取物的落新妇苷降解程度最大,并发现其异构化和分解。这与落新妇苷在碱性溶液中不稳定有关。最终的消化液中,CHCL-LAC提取物的落新妇苷的回收率为84.1%,明显高于70%乙醇提取物(图6A和表5)
CHCL-LAC提取物和70%乙醇提取物的DPPH自由基清除能力和ORAC抗氧化能力如图6B和图6C所示。在胃消化过程中,DPPH抗氧化能力明显降低,而ORAC抗氧化活性相对稳定。经过肠道消化3h后,DPPH和ORAC的抗氧化能力分别保持在75.7%和57.7%,明显高于70%乙醇提取物(13.6% DPPH,21.4% ORAC)(图6B、6C和表6、表7),表明CHCL-LAC比70%乙醇保留了更高的抗氧化能力。相关性分析显示,ORAC抗氧化能力与消化过程中落新妇苷含量的变化尤其相关(图6D和6E),表明落新妇苷是ORAC抗氧化能力最有效的贡献者。
落新妇苷CHCL-LAC提取物对α-淀粉酶和α-葡萄糖苷酶的抑制作用见图7。随着CHCL-LAC提取物浓度的增加,酶的抑制率增加。提取物浓度越高(0.99g/L),其抑制α-淀粉酶的IC50值为0.67g/L(图7A),而提取物对α-葡萄糖苷酶的抑制作用更强,IC50值为0.64g/L(图7B)。
表5体外模拟胃肠消化过程中落新妇苷的生物可及性
表6不同提取物在体外模拟胃肠消化过程中DPPH抗氧化能力变化
表7不同提取物在体外模拟胃肠道消化过程中ORAC抗氧化能力
- 一种利用脯氨酸-山梨醇低共熔溶剂提取赤芍中单萜苷的方法
- 一种利用天然低共熔溶剂提取葛根素的方法
