滇重楼葡甘聚糖及其制备方法和应用
文献发布时间:2024-04-18 20:00:50
技术领域
本申请涉及化妆品和医药技术的领域,具体涉及一种滇重楼葡甘聚糖及其制备方法和应用。
背景技术
重楼是黑药花科重楼属植物的统称,药用历史悠久,一般以根茎入药,具有清热解毒、消肿止痛、凉肝定惊等功效,主治疔疮痈肿,咽喉肿痛,蛇虫咬伤,跌扑伤痛,惊风抽搐。滇重楼(Paris polyphylla Smith var.yunnanensis)又称云南重楼,是黑药花科(Melanthiaceae)重楼属(Paris L.)多年生草本植物,收录于《中华人民共和国药典》(2020版)。
滇重楼主要含有甾体皂苷类、黄酮类、三萜类等化学成分,其中甾体皂苷类化合物是滇重楼中化合物种类、含量高的一类重要天然有机化合物,具有较好的生物活性。然而,滇重楼作为民族特色的药用植物在使用频率高,其传统功效的物质基础研究仍有待挖掘,尤其对重楼属植物多糖亟需深入研究。
发明内容
针对现在技术中存在的问题,本申请实施例提供一种滇重楼葡甘聚糖及其制备方法与应用。
第一方面,本申请实施例提供一种滇重楼葡甘聚糖,所述滇重楼葡甘聚糖具有如下式I所示的结构:
式I中,m和n表示重复单元数,且均为自然数,m独立地为1或2,30≤n≤40。
本申请实施例中提供的结构新颖的滇重楼葡甘聚糖,其以β(1→4)甘露糖为主链,多糖链中含有葡萄糖和乙酰化甘露糖。本申请发明人经药理学研究发现,该结构新颖的滇重楼葡甘聚糖可以显著促进巨噬细胞RAW264.7分泌细胞因子IL-10和TNF-α,具有明显的机体免疫调节能力。而且,发明人经过进一步深入研究发现,该滇重楼葡甘聚糖能够显著降低过氧化氢损伤的皮肤成纤维细胞的细胞死亡率,具有显著的防止自由基细胞损伤的活性,可以起到防止紫外线氧化损伤皮肤组织的作用。
在本申请的一些实施例中,所述滇重楼葡聚糖的重均分子量为50kDa~100kDa。
在本申请的一些实施例中,所述滇重楼葡甘聚糖的单糖组成包括葡萄糖和甘露糖,葡萄糖相对于总单糖的摩尔占比为6.5%~9%。
在本申请的一些实施例中,所述甘露糖包括糖环上2位或3位被乙酰基取代的乙酰化甘露糖,所述乙酰化甘露糖占总单糖的摩尔比为27.5%~30%。
在本申请的一些实施例中,所述滇重楼葡甘聚糖的纯度不低于95%。
第二方面,本申请实施例提供了一种滇重楼葡甘聚糖的制备方法,包括:
从滇重楼地下根茎提取粗多糖;
提取所述粗多糖中重均分子量为50kDa~100kDa的组分,以得到滇重楼葡甘聚糖。
在本申请的一些实施例中,所述从滇重楼地下根茎提取粗多糖包括:将所述滇重楼地下根茎粉碎,温水或热水提取,得到所述粗多糖的溶液。
在本申请的一些实施例中,所述提取所述粗多糖中重均分子量为50kDa~100kDa的组分包括:
酶解所述粗多糖,分级醇沉,得到粗滇重楼葡甘聚糖;
精制所述粗滇重楼葡甘聚糖中重均分子量为50kDa~100kDa的组分,得到所述滇重楼葡甘聚糖。
在本申请的一些实施例中,所述酶解所述粗多糖,分级醇沉包括:将所述粗多糖用淀粉酶酶解,煮沸灭酶,取清液分级醇沉,收集沉淀。
在本申请的一些实施例中,所述精制的方法包括分级醇沉法、阴离子交换层析法、凝胶排阻色谱法、透析法和超滤法中的一种或多种。
在本申请的一些实施例中,所述淀粉酶的体积浓度为0.1%~0.5%。
在本申请的一些实施例中,所述酶解的温度为60~80℃。
在本申请的一些实施例中,所述酶解的时间为1~3h。
在本申请的一些实施例中,所述煮沸灭酶的时间为10~15min。
在本申请的一些实施例中,所述分级醇沉包括:取清液分级醇沉,使醇浓度分别达到35%~45%、55%~65%、75%~85%,收集沉淀。
第三方面,本申请实施例提供了一种化妆品或药物组合物,所述组合物包括有效量的本申请第一方面实施例提供的滇重楼葡甘聚糖以及化妆品或药学中可接受的辅料。
第四方面,本申请实施例提供了本申请第一方面实施例提供的滇重楼葡甘聚糖在化妆品中的应用。
第五方面,本申请实施例提供了本申请第一方面实施例提供的滇重楼葡甘聚糖在制备免疫活性调节的食品和/或药品中的应用。
附图说明
为了更清楚地说明本申请实施例的技术方案,下面将对本申请实施例中所需要使用的附图作简单的介绍,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
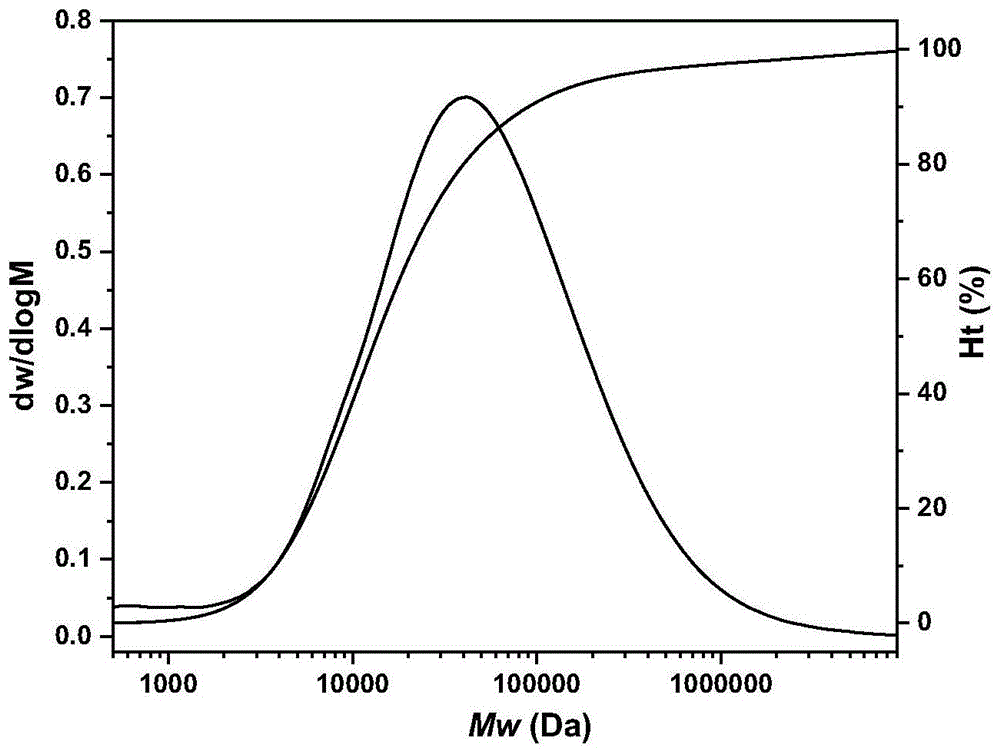
图1为本申请实施例中滇重楼葡甘聚糖分子量分布曲线图;
图2为本申请实施例中滇重楼葡甘聚糖单糖组成的液相色谱(HPLC)图;
图3为本申请实施例中滇重楼葡甘聚糖的甲基化总离子流图;
图4为本申请实施例中滇重楼葡甘聚糖的红外(IR)谱图;
图5为本申请实施例中滇重楼葡甘聚糖核磁共振(NMR)谱图,其中,A为
图6示出了本申请实施例中滇重楼葡甘聚糖对RAW264.7细胞增殖与细胞因子释放的影响,其中,A为滇重楼葡甘聚糖对巨噬细胞增殖的影响,B为滇重楼葡甘聚糖对RAW264.4细胞分泌NO的影响,C为滇重楼葡甘聚糖对RAW264.7细胞分泌IL-10的影响,D为滇重楼葡甘聚糖对RAW264.7细胞分泌TNF-α的影响(n=3,“*”表示与空白组相比具有显著性,*代表p<0.05,**代表p<0.01,***代表p<0.001);
图7示出了滇重楼葡甘聚糖对L929细胞增殖与对氧化损伤的L929细胞的保护作用,其中,A为滇重楼葡甘聚糖对L929细胞增殖的影响,B为滇重楼葡甘聚糖对过氧化氢诱导的L929细胞活率的影响(n=3,“#”表示与空白组相比具有显著性,“*”表示与模型组相比具有显著性,#或*代表p<0.05,##或**代表p<0.01,###或***代表p<0.001)。
具体实施方式
下面将详细描述本申请的各个方面的特征和示例性实施例。在下面的详细描述中,提出了许多具体细节,以便提供对本申请的全面理解。但是,对于本领域技术人员来说很明显的是,本申请可以在不需要这些具体细节中的一些细节的情况下实施。下面对实施例的描述仅仅是为了通过示出本申请的示例来提供对本申请的更好的理解。在附图和下面的描述中,至少部分的公知结构和技术没有被示出,以便避免对本申请造成不必要的模糊;并且,为了清晰,可能夸大了部分结构的尺寸。此外,下文中所描述的特征、结构或特性可以以任何合适的方式结合在一个或更多实施例中。
需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。在本申请的描述中,需要说明的是,除非另有说明,“多个”的含义是两个以上。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括……”限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
重楼是黑药花科(Melanthiaceae)重楼属(Paris L.)植物的统称,其药用历史悠久,自汉代以来,在本草古籍中多有记载。重楼属植物药用历史悠久,一般以根茎入药,最早以“蚤休”记录于《神农本草经》中,主治惊痫、癫疾、痈疮、去蛇毒,我国自1977年开始,将重楼的根茎载入《中国药典》,并规定云南重楼或七叶一枝花为重楼药材的基原植物,具有清热解毒、消肿止痛、凉肝定惊功效,用于疔疮痈肿、咽喉肿痛、蛇虫咬伤、跌扑伤痛、惊风抽搐。
滇重楼(Paris polyphylla var.yunnanensis(Franch.)Hand.-Mzt.)又称云南重楼,收录于《中华人民共和国药典》(2020版)。滇重楼一般以根茎入药,具有清热解毒,消肿止痛,凉肝定惊等功效。用于咽喉肿痛,蛇虫咬伤,惊风抽搐,功能性子宫出血,神经炎,外科炎性反应等疾病,且疗效显著,是重楼解毒酊、宫血宁胶囊、云南白药、散结止痛膏等中成药的主要成分。
滇重楼主要含有甾体皂苷类、黄酮类、三萜类等化学成分,其中甾体皂苷类化合物是滇重楼中化合物种类、含量高的一类重要天然有机化合物,具有较好的生物活性。然而,滇重楼作为民族特色的药用植物在使用频率高,其传统功效的物质基础研究仍有待挖掘,尤其对重楼属植物多糖亟需深入研究。因此,从资源开发利用的角度,尚需对其他成分开展研究。
基于此,本申请发明人对滇重楼的多糖进行了系统的化学与药理学研究,首次报道了一种结构新颖的滇重楼葡甘聚糖,并探究了其在化妆品以及药物制剂和食品领域的应用。
滇重楼葡甘聚糖
本申请第一方面的实施例提供一种滇重楼葡甘聚糖,具有如下式I所示的结构:
式I中,m和n表示重复单元数,且均为自然数,m独立地为1或2,30≤n≤40。
本申请发明人对滇重楼经过深入的研究惊奇地发现,从滇重楼的地下根茎中应用创新的方法提取纯化可获得一种结构新颖的滇重楼葡甘聚糖,发明人经过活性筛选研究发现,该结构新颖的滇重楼葡甘聚糖能够显著促进巨噬细胞RAW264.7分泌细胞因子IL-10和TNF-α,因而该滇重楼葡甘聚糖具有明显的机体免疫调节能力,因此该滇重楼葡甘聚糖具有用于制备提高机体免疫力的药物和/或保健食品的用途。发明人经进一步深入的药理学研究发现,该滇重楼葡聚糖能够显著降低过氧化氢损伤的皮肤成纤维细胞的细胞死亡率,具有显著的防止自由基细胞损伤的活性,对氧化损伤的皮肤具有显著的防护效果,因此,该滇重楼葡甘聚糖具有用于防止皮肤氧化损伤的化妆品的用途。
在一些实施例中,滇重楼葡甘聚糖的重均分子量为50kDa~100kDa。
在一些实施例中,滇重楼葡甘聚糖的单糖组成包括葡萄糖和甘露糖,葡萄糖占总单糖的摩尔占比为6.5%~9%。
在一些实施例中,甘露糖包括糖环上2位或3位被乙酰基取代的乙酰化甘露糖,所述乙酰化甘露糖占总单糖的摩尔比为27.5%~30%。
在一些实施例中,滇重楼葡甘聚糖的纯度不低于95%。
根据本申请实施例,上述结构新颖的滇重楼葡甘聚糖的重均分子量为50kDa~100kDa,其以β(1→4)甘露糖为主链,多糖链中含有葡萄糖,葡萄糖占总单糖的摩尔比为6.5%~9%,而甘露糖的糖环上的2或3位部分被乙酰基取代,乙酰化甘露糖占总单糖的摩尔比为27.5%~30%。
滇重楼葡甘聚糖的制备方法
本申请第二方面的实施例提供一种滇重楼葡甘聚糖的制备方法,包括以下步骤S100至S200:
S100、从滇重楼地下根茎提取粗多糖;
S200、提取粗多糖中重均分子量为50kDa~100kDa的组分,以得到滇重楼葡甘聚糖。
根据本申请实施例,通过上述制备方法可以得到一种结构新颖、活性突出的滇重楼葡甘聚糖,该滇重楼葡甘聚糖的重均分子量为50kDa~100kDa,以β(1→4)甘露糖为主链,该滇重楼葡甘聚糖中含有葡萄糖,葡萄糖占总单糖的摩尔比为6.5%~9%,而甘露糖的糖环上2位或3位部分被乙酰基取代成为乙酰化甘露糖,乙酰化甘露糖占总单糖的摩尔比为27.5%~30%,因此,本申请第二方面实施例提供的制备方法可以用来制备本申请实施例第一方面的滇重楼葡甘聚糖。
本申请实施例中,滇重楼地下根茎可以是滇重楼地下根茎块,也可以是将滇重楼地下根茎块粉碎后得到的粉末。
一些实施例中,滇重楼地下根茎为将滇重楼地下根茎块粉碎得到的粉末,具体获取方式为:取干燥后的滇重楼地下根茎粉碎成粉末,将滇重楼地下根茎的粉末用90%~100%乙醇以1:(8~12)的料液比,在60~80℃、1~4h提取1~2次以去除脂溶性物质,趁热过滤,收集滤饼,挥干滤饼中残留的乙醇,得到脱脂与脱色素的滇重楼地下根茎的残渣。
具体地,乙醇的浓度优选为95%,料液比优选为1:10,温度优选为70℃,提取时间优选为2h,提取次数优选为2次。
在一些实施例中,从滇重楼地下根茎提取粗多糖包括:将脱脂的滇重楼地下根茎的残渣用热水或温水提取,得到粗多糖的溶液。
具体地,提取水温为75~85℃,提取的料液比为1:(8~12),可选为1:10;提取时间为2~4h,提取次数为1~2次,可选为2次。
在一些实施例中,提取粗多糖中重均分子量为50kDa~100kDa的组分包括以下的步骤S210至S220:
S210、酶解粗多糖,分级醇沉,得到粗滇重楼葡甘聚糖。
本申请实施例中,酶解粗多糖包括:将粗多糖的溶液用淀粉酶酶解以去除其中的淀粉类多糖。
具体地,酶解温度为60~80℃,酶解时间为1~3h,淀粉酶的浓度为0.1%~0.5%(v/v),可选为0.2%。
本申请实施例中,分级醇沉包括:将酶解后的粗多糖溶液煮沸灭酶,离心,取清液分级醇沉,收集沉淀。
具体地,取清液分级醇沉包括以下步骤S211至S214:
S211、向灭酶后清液搅拌下加入95%乙醇至醇终浓度为35%~45%,离心,得35%~45%醇沉物和35%~45%醇沉上清液;
S212、向上述35%~45%醇沉上清液搅拌下加入95%乙醇至醇终浓度为55%~65%,离心,得55%~65%醇沉物和55%~65%醇沉上清液,用95%的乙醇洗涤55%~65%醇沉物3~5次,加水复溶后冻干;
S213、向上述55%~65%醇沉上清液搅拌下加入95%乙醇至醇终浓度为75%~85%,离心,得75%~85%醇沉物和醇沉上清液,用95%乙醇洗涤75%~85%醇沉物3~5次,加水复溶后冻干;
S214、合并两次冻干后产物,得到粗滇重楼葡甘聚糖。
具体地,步骤S211中醇终浓度可选为40%,步骤S212中醇终浓度可选为60%,步骤S213中醇终浓度可选为80%。
S220、精制粗滇重楼葡甘聚糖中重均分子量为50kDa~100kDa的组分,得到滇重楼葡甘聚糖。
本申请实施例中,精制粗滇重楼葡甘聚糖的方法包括阴离子交换柱层析法、凝胶排阻层析法、透析法、超滤法中的一种或多种组合。
具体地,可将粗滇重楼葡甘聚糖加去离子水复溶后,离心去除不溶物,任选醇沉分级、凝胶排阻层析法、透析法或超滤法进行纯化,收集含有滇重楼葡甘聚糖的流份或截留液或透过液,若含有盐需脱盐后,直接真空冷冻干燥或减压浓缩后醇沉减压干燥,即得纯化的滇重楼葡甘聚糖。
本领域技术人员可以理解的是,对于凝胶排阻层析法,是根据滇重楼葡甘聚糖的多糖组分中葡甘聚糖物质的分子量,合理选择凝胶材料,例如葡聚糖凝胶Sephadex系列、琼脂糖凝胶Sepharose系列、聚丙烯酰胺Bio-Gel P系列以及它们相互交联形成的凝胶填料,然后按照各个填料的实际性能进行装柱、上样以及用含盐或不含盐洗脱溶液依次洗脱并收集流份。合并各个流出峰,流出液可浓缩或不需要浓缩,装入透析袋透析或超滤膜包透析或超滤脱盐,收集脱盐后的截留液,经真空冷冻干燥或真空减压干燥,即得纯化的滇重楼葡甘聚糖。或者采用透析法或超滤法等方法进行纯化滇重楼多糖组分时,选择适当分子量的超滤膜包进行切向流超滤截留处理。例如,滇重楼多糖组分水溶液先经一个小于滇重楼葡甘聚糖分子量的超滤膜包充分超滤,收集透过液,除去小分子量的物质,然后再经大于滇重楼葡甘聚糖分子量的透析袋或超滤膜包充分透析或超滤,收集截留液,浓缩后经真空冷冻干燥或真空减压干燥,即得精制的滇重楼葡甘聚糖。
化妆品或药物组合物
本申请三方面的实施例提供一种化妆品或药物组合物,该组合物包括有效量的滇重楼葡甘聚糖和化妆品或药学可接受的辅料,滇重楼葡甘聚糖包括根据本申请第一方面实施例的滇重楼葡甘聚糖或根据本申请第二方面实施例的制备方法得到的滇重楼葡甘聚糖。
在一些实施例中,化妆品中滇重楼葡甘聚糖的有效量为0.01%~10%。
在一些实施例中,药物组合物中滇重楼葡甘聚糖的有效量为0.01%~10%。
在一些实施例中,辅料包括赋形剂、载体、稀释剂、成膜剂中的一种或多种。
可选地,赋形剂包括淀粉、卡波姆、甘油、羟苯乙酯、三乙醇胺、聚山梨酯80、丙二醇中的一种或多种组合。
可选地,载体包括胶囊、水凝胶贴剂、纯净水中的一种或多种组合。
可选地,稀释剂包括甘油、丙二醇、丁二醇、纯净水中的一种或多种组合。
可选地,成膜剂包括聚乙烯基吡咯烷酮、三甲基硅氧基硅酸酯、聚乙烯吡咯烷酮类、聚乙烯醇、丙烯酸共聚物中的一种或多种组合。
在一些实施例中,化妆品的剂型包括面膜、霜剂、软膏剂、隔离剂。
在一些实施例中,药物组合物的剂型包括冻干粉、口服液、胶囊、微丸、片剂。
滇重楼葡甘聚糖在化妆品中的应用
本申请第四方面的实施例提供一种滇重楼葡甘聚糖在化妆品中的应用。
根据本申请实施例,滇重楼葡甘聚糖具有降低氧化损伤的小鼠皮肤成纤维细胞死亡,可以达到保护紫外线氧化损伤皮肤的效果。因此,滇重楼葡甘聚糖可以应用于具有防止紫外线氧化损伤功效的化妆品中。
滇重楼葡甘聚糖在制备免疫活性调节的食品和/或药品中的应用
本申请第五方面的实施例提供一种滇重楼葡甘聚糖在制备免疫活性调节的食品和/或药品的应用。
根据本申请实施例,滇重楼葡甘聚糖可以激活巨噬细胞,刺激巨噬细胞释放细胞免疫因子IL-10、TNF-α等免疫相关活性物质,具有显著的免疫调节活性,因此,滇重楼葡甘聚糖可以应用于制备免疫活性调节的食品和/或药品。
本申请实施例还提供了上述滇重楼葡甘聚糖的结构解析方法,包括:
(1)分子量测定:取滇重楼葡甘聚糖样品,采用高效凝胶排阻色谱-示差检测器检测法测定。
(2)单糖组成分析:取滇重楼葡甘聚糖样品,酸水解为单糖,经1-苯基-3-甲基-5-吡唑啉酮(PMP)衍生化后,用十八烷基硅烷键合硅胶作为填充剂的色谱柱,经高效液相色谱仪分析滇重楼葡甘聚糖的单糖组成。
(3)甲基化分析:取滇重楼葡甘聚糖样品,用碘甲烷等卤代甲烷试剂在碱性条件下进行多糖甲基化,在碱性条件下水解后用硼氢化钠还原,用酸酐对甲基化糖醇进行乙酰化,萃取后进行气相色谱仪连用质谱仪(GC-MS)分析,判断滇重楼葡甘聚糖的糖苷键连接方式。
(4)红外光谱分析:取滇重楼葡甘聚糖样品,充分干燥后,采用固体溴化钾压片法,在红外光谱仪上测定样品的红外光谱。
(5)核磁共振分析:取滇重楼葡甘聚糖样品溶解于重水中,真空冷冻干燥,重复三次重水交换后,溶解到重水中,检测样品的核磁共振谱包括一维
(6)综合数据解析:综合分析上述步骤的分析数据,解析滇重楼葡甘聚糖的化学结构。
按照上述结构解析方法,对本申请实施例提供的滇重楼葡甘聚糖进行结构分析,结果显示,该滇重楼葡甘聚糖在HPGPC凝胶色谱上只显示一个色谱峰,重均分子量约为50kDa~100kDa,单糖组成显示该滇重楼葡甘聚糖由甘露糖或含有少量葡萄糖组成;甲基化分析显示,该滇重楼葡甘聚糖存在β(1→4)糖苷键;红外光谱分析显示,乙酰基的羰基吸收峰,糖环上的羟基吸收峰,指纹图谱区有吡喃糖吸收信号峰都符合葡甘聚糖的吸收峰;根据核磁共振谱数据,可以清晰地归属重楼葡甘聚糖的
综合上述数据,本申请实施例中提供的重楼葡甘聚糖具有如下通式I所示的结构特征:以甘露糖β(1→4)糖苷键为主,部分甘露糖上伴随有2或3位乙酰化。
式I中,m和n表示糖重复单元数,且均为自然数,m独立地为1或2,30≤n≤40。
实施例
以下列举具体实施例对本发明进行说明。需要指出的是,下面描述的实施例是示例性的,仅用于解释本申请,而不能理解为对本申请的限制。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
实施例1:制取滇重楼葡甘聚糖
滇重楼粗多糖的提取
S10、称取干燥粉碎后的滇重楼地下根茎粉末300g,加入3L 95%乙醇在80℃提取2次,每次2h,趁热过滤,收集滤饼,挥干滤饼中残留的乙醇;
S20、向滤饼加入3L去离子水80℃提取2h,提取结束后4000rpm离心15min,取上清;滤渣重复提取一次,合并上清;
S30、上清液中加入0.2%(v/v)的α-淀粉酶,70℃酶解2h,I
S40、上清液加入95%乙醇至醇终浓度为40%,4000rpm离心15min,的40%醇沉物和40%醇沉上清液;向40%醇沉上清液中搅拌下加入95%乙醇至醇终浓度为60%,4000rpm离心15min,得60%醇沉物和60%醇沉上清液,用95%乙醇洗涤60%醇沉物3次,加水复溶后冻干;向60%醇沉上清液中搅拌下加入95%乙醇至醇终浓度为80%,4000rpm离心15min,得80%醇沉物和80%醇沉上清液,用95%乙醇洗涤80%醇沉物3次,加水复溶后冻干;
S50、合并两次冻干的醇沉物,得滇重楼粗多糖,冻干后总计5.27g;
精制滇重楼葡甘聚糖
S60、称取滇重楼粗多糖400mg,加入10mL去离子水溶解,4000rpm离心15min,取上清液经0.45μm的滤膜过滤后缓慢均匀注入到DEAE52纤维素层析柱的顶端,依次用水、0.1MNaCl溶液、0.3M NaCl溶液、0.5MNaCl溶液洗脱,控制流速为1mL/min,每管收集5mL,用苯酚-硫酸法对其多糖含量进行检测。以吸光值为纵坐标,管数为横坐标,绘制多糖组分的洗脱曲线。合并属于同一洗脱峰的洗脱液,收集洗脱曲线最大面积的样品,手机水洗部分的多糖,减压浓缩,真空冷冻干燥,得精制的滇重楼葡甘聚糖300mg。
实施例2:滇重楼葡甘聚糖的结构解析
试验方法
1.分子量及其分布
采用高效凝胶排阻色谱-示差检测器检测法(HPGPC-RID)分析实施例1制备的滇重楼葡甘聚糖的分子量及其分布。
色谱仪器:Agilent technologies 1260series高效液相色谱仪;
色谱条件:Shodex OHpak SB-804HQ(8mm×300mm)柱,柱温为35℃,示差检测器,流动相为0.1M NaCl,流速0.5mL/min;
测定过程:各取5mg滇重楼葡甘聚糖样品或已知分子量的右旋糖酐对照品加流动相配制为5mg/mL的溶液,过0.2μm微孔滤膜,滤过液30μL进高效液相色谱仪分析,记录色谱图。数据采用GPC软件处理,绘制标准曲线,将数据代入方程,计算分子量。
2.单糖组成分析
取单糖标准品溶液、样品溶液1mL,置于水解管中,加入4M的三氟乙酸溶液1mL,混匀,于110℃烘箱水解4h。水解反应结束后,将水解液使用旋转蒸发浓缩仪旋蒸干燥,确保TFA的完全去除。干燥完成后,加入200μL去离子水溶解,然后依次加入0.6M的NaOH溶液200μL、0.5M的PMP-甲醇溶液400μL,均匀混合,于70℃烘箱中衍生化反应1h,冷却至室温,加0.6M的盐酸200μL中和,再加氯仿充分萃取3次(每次2mL),水相离心(10000rpm,10min)后经0.2μm的微孔滤膜过滤后供液相色谱分析。
色谱条件:
色谱仪:Agilent technologies 1260series高效液相色谱仪;
色谱柱:Hadesil C18-Bio(250mm×4.6mm,id.5μm);柱温:25℃;
流动相:A:0.1M磷酸盐缓冲液;B:乙腈,A/B=82/18;
洗 脱:流速1mL/min,进样量10μL,时间60min;
检 测:DAD检测器,波长250nm。
3.甲基化分析
甲基化反应:取干燥氢氧化钠粉末120mg,加无水DMSO 1mL充分溶解氢氧化钠,得到120mg/mL的碱性DMSO溶液。称取滇重楼葡甘聚糖3~5mg,置于10mL螺旋管中,加入DMSO溶液1mL溶解多糖样品,待样品溶解后,加入1mL NaOH/DMSO溶液,密封超声10min,然后加入碘甲烷200μL,超声避光反应10min,再次加入碘甲烷200μL,反应10min,最后加入碘甲烷400μL,反应30min。待反应结束后,加入1mL去离子水淬灭反应,按体积1:1加氯仿萃取3次后,合并有机相,有机相使用去离子水洗3遍,最后将有机相减压干燥。
酸水解:向上述干燥后样品中加入2mL 2M的TFA溶液,封管120℃下酸水解2h。
还原:将上述水解液旋干,溶于1mL 2M的NH
乙酰化:上述样品中加入1mL吡啶和1mL乙酸酐于试管中,100℃封管反应1.5h。冷却后,加入1mL水终止反应,用3mL二氯甲烷萃取3次,有机相水洗3次,最后将有机相旋干,加入1mL色谱级氯仿溶解过膜,进行GC-MS分析。
GC条件:DB-5MS石英毛细管柱(30m×0.25mm×0.25μm);柱温:起始温度80℃,保持1min,程序升温5℃/min至250℃,保持5min;柱流量为1.5mL/min;进样口温度270℃;分流比为10:1;载气为高纯氦气,进样量1μL。
MS条件:电离方式EI;电子能量70eV;传输线温度290℃;离子源温度230℃;四极杆温度150℃;质量范围50~600;与CCRC光谱数据库进行对比,从而判断糖苷键类型。
4.红外光谱分析
按照2020版《中国药典》第四部分采用固体压片法:取2mg样品经40℃真空干燥24h,采用KBr压片法,使用Tensor 27傅立叶变换中红外光谱仪对样品进行4000~400cm
5.核磁共振分析
取滇重楼葡甘聚糖样品20mg溶于0.5mL D
实验结果
本申请实施例的滇重楼葡甘聚糖的性状为:白色或类白色固体,无味,有引湿性。
分子量及其分布分析结果如图1,高效凝胶排阻色谱法分析结果表明,从滇重楼根茎中提取纯化的滇重楼葡甘聚糖仅有一个色谱峰,其重均分子量为92kDa,多分散系数为6.85;经多批次样品分析,滇重楼葡甘聚糖的重均分子量为50kDa~100kDa。
单糖组成分析结果如图2,结果表明,滇重楼葡甘聚糖经PMP柱前衍生后的HPLC图显示滇重楼葡甘聚糖含有甘露糖和少量葡萄糖的峰,说明所述滇重楼葡甘聚糖主要由甘露糖组成,并带有少量的葡萄糖,经多批次分析葡萄糖占总单糖的摩尔比为6.5%~9%。
甲基化分析结果如图3,结果表明,滇重楼葡甘聚糖存在β(1→4)甘露糖糖苷键、少量的β(1→4)葡萄糖糖苷键、β(1→)甘露糖糖苷键和β(1→)葡萄糖糖苷键。
红外光谱分析结果如图4,结果表明,3400~3430cm
核磁共振(NMR)检测结果如图5,详细的
核磁共振结果表明,在NMR
1,4-β-D-甘露糖(A/E残基)的4位质子信号为3.83ppm以及其对应的C-4的化学位移为79.4/80.3ppm,相对于无取代甘露糖的相应的化学位移显著向低场移动,说明甘露糖基A/E的1位和4位上的羟基有取代,A与E残基虽同为1,4-β-D-甘露糖,但E残基的C-4化学位移(高于A残基)与H-1化学位移(低于A残基)与A残基相比略有不同,这可能是由于E残基与含乙酰基的B和C残基相连导致。2位含有乙酰基的1,4-β-D-甘露糖(残基B)的2位质子信号为5.52ppm,4位质子信号为3.82ppm,其对应的C-2化学位移为74.5ppm,C-4化学位移为79.5ppm,相对于无取代甘露糖的2位和4位碳化学位移显著向低场移动,结合以前的文献,表明甘露糖基B的2位羟基被乙酰基取代,4位羟基与其他残基相连。3位含有乙酰基的1,4-β-D-甘露糖的3位质子信号为5.11ppm,4位质子信号为4.04ppm以及其对应的C-3与C-4的化学位移均为76.3ppm,相对于无取代甘露糖3位和4位的氢碳化学位移均显著向低场移动,说明甘露糖基C的3位羟基被乙酰基取代,4位羟基与其他残基相连。
1
综合上述数据可知,该结果新颖的滇重楼葡甘聚糖的化学结构如下通式I所示:
式I中,m和n表示糖重复单元数,且均为自然数,m独立地为1或2,30≤n≤40。
其结构特征为:(1)该滇重楼葡甘聚糖是从滇重楼的根茎提取的结构新颖的葡甘聚糖;(2)该滇重楼葡甘聚糖的单糖连接方式为:以β(1→4)甘露糖糖苷键为主链。
表1:滇重楼葡甘聚糖的
实施例3:滇重楼葡甘聚糖的免疫调节试验
受试品、试剂
滇重楼葡甘聚糖(PMM):按照实施例1制备的滇重楼葡甘聚糖;
DMEM高糖培养基、0.25%胰酶EDTA溶液:上海源培生物科技股份有限公司;
青霉素、链霉素、胎牛血清:Biological Industries公司;
磷酸缓冲盐溶液PBS:武汉塞维尔生物科技有限公司;
细菌脂多糖(LPS):美国Sigma公司;
一氧化氮检测试剂盒:碧云天生物技术;
TNF-α、IL-10检测试剂盒:欣博胜科技有限公司;
灭菌水:实验室自制。
小鼠巨噬细胞系RAW264.7,购买于中国科学院生命科学研究院细胞资源中心。
实验方法
1.溶液配制
样品母液:称取滇重楼葡甘聚糖10mg,用灭菌水溶解至10mg/mL,4℃保存,临用前用细胞培养基稀释至终浓度200μg/mL,0.2μm微孔滤膜过滤除菌备用。
脂多糖LPS:用无菌PBS配制成1mg/mL母液,4℃保存,实验前用细胞培养基稀释至终浓度1μg/mL,0.22μm微孔滤膜过滤。
2.RAW264.7细胞培养与传代
细胞复苏:将冻存于液氮中的巨噬细胞RAW264.7取出并迅速置于37℃恒温水浴锅中,使细胞在短时间内完全解冻。将解冻的细胞转移至含有8mL DMEM培养基的15mL离心管中,800rpm离心5min,弃去上清液。离心管中加入含1%(v/v)青霉素-链霉素双抗和10%(v/v)胎牛血清的DMEM培养基2mL,轻轻吹打沉淀细胞至完全悬浮得到细胞悬液,将细胞悬液转移至T25培养瓶中,用4mL培养基洗涤离心管确保沉淀细胞全部转移至T25培养瓶中,保持培养瓶中培养基约6mL,在倒置显微镜下观察细胞密度,放入CO
细胞传代:细胞复苏培养后,待细胞生长到90%融合(培养瓶表面90%面积被细胞覆盖)时进行细胞传代培养,弃去旧培养基,无菌PBS洗涤2遍,加入DMEM培养基2mL,轻轻吹打细胞并使贴壁细胞完全悬浮后接种至新的培养瓶中(一般以1:2比例传代),保持培养瓶中培养基约6mL,在倒置显微镜下观察细胞密度。培养条件:5% CO
需要说明的是,在后续的细胞实验中,均以此复苏细胞RAW264.7为实验对象,未作明确说明时培养条件均为5% CO
3.对RAW264.7细胞增殖的影响
将RAW264.7细胞以1×10
4.对RAW264.7细胞释放NO的影响
取对数生长期的RAW264.7细胞以2×10
5.ELISA法检测对巨噬细胞细胞因子分泌水平的影响
取对数生长期的RAW264.7细胞以2×10
实验结果
1.对巨噬细胞增殖的影响
参照图6-A,与正常对照组相比,滇重楼葡甘聚糖在10~160μg/mL的浓度下能够显著促进RAW264.7细胞增殖,浓度为160μg/mL时细胞增殖最为显著,浓度在320~640μg/mL之间对细胞增殖不具备促进效果。
2.对巨噬细胞NO释放的影响
参照图6-B,与正常对照组相比,滇重楼葡甘聚糖能够显著促进巨噬细胞NO释放,促进NO释放量与滇重楼葡甘聚糖的浓度呈正相关,说明滇重楼葡甘聚糖具有较好的免疫活性,且呈剂量依赖性。
3.对巨噬细胞分泌TNF-α、IL-10的影响
参照图6-C,滇重楼葡甘聚糖对巨噬细胞分泌IL-10具有显著的促进作用,量效关系明显,随着滇重楼葡甘聚糖的浓度增加,其促进巨噬细胞分泌IL-10的能力越强,当浓度达到200μg/mL时,巨噬细胞分泌IL-10的量最多。如图6-D所示,滇重楼葡甘聚糖对巨噬细胞分泌TNF-α具有显著促进作用,随着滇重楼葡甘聚糖的浓度增加,其促进巨噬细胞分泌TNF-α的能力越强,提示滇重楼葡甘聚糖具有免疫增强活性。
实施例4:滇重楼葡甘聚糖对氧化损伤的皮肤成纤维细胞活率的影响
滇重楼葡甘聚糖(PMM):按照实施例1制备的滇重楼葡甘聚糖;
DMEM高糖培养基、0.25%胰酶EDTA溶液:上海源培生物科技股份有限公司;
青霉素、链霉素、胎牛血清:Biological Industries公司;
磷酸缓冲盐溶液PBS:武汉塞维尔生物科技有限公司;
噻唑蓝(MTT):北京索莱宝科技有限公司;
灭菌水:实验室自制;
小鼠皮肤成纤维细胞L929:购买于中国科学院生命科学研究院细胞资源中心。
实验方法
1.溶液配制
样品母液:称取滇重楼葡甘聚糖10mg,用灭菌水溶解至10mg/mL,过0.22μm微孔滤膜过滤除菌,4℃保存备用。
MTT母液:用无菌PBS配制成5mg/mL母液,-20℃避光保存,实验前用无血清细胞培养基稀释至终浓度0.5mg/mL,0.22μm微孔滤膜过滤。
2.细胞培养与传代
细胞复苏:将冻存于液氮中的小鼠成纤维细胞L929取出并迅速置于37℃恒温水浴锅中,使细胞在短时间内完全解冻。将解冻的细胞转移至含有4mL DMEM培养基的15mL离心管中,1000rpm离心5min,弃去上清液。离心管中加入含1%(v/v)青霉素-链霉素双抗和10%(v/v)胎牛血清的DMEM培养基2mL,轻轻吹打沉淀细胞至完全悬浮得到细胞悬液。将细胞悬液转移至10cm培养皿中,用2mL培养基洗涤离心管确保沉淀细胞全部转移至培养皿中,保持培养皿中培养基约10mL,在倒置显微镜下观察细胞密度,放入CO
细胞传代:细胞复苏培养后,待细胞生长到90%融合(培养瓶表面90%面积被细胞覆盖)时进行细胞传代培养,弃去旧培养基,无菌PBS洗涤2遍,加入DMEM培养基2mL,轻轻吹打细胞并使贴壁细胞完全悬浮后接种至新的培养瓶中,保持培养皿中培养基约10mL,在倒置显微镜下观察细胞密度。
3.对L929细胞增殖的影响
将L929细胞以2×10
4.对H
96孔板每孔细胞接种20000个,培养24h后,加入100μg/mL、200μg/mL、500μg/mL的滇重楼葡甘聚糖样品处理24h,不吸出培养液,加入每孔终浓度为800μM的过氧化氢溶液作用2h,吸出过氧化氢溶液,加入无血清溶液稀释的MTT(0.5mg/mL)溶液作用4h后,490nm测定细胞存活率。以不加过氧化氢溶液的细胞作为对照组,只加过氧化氢溶液作为模型组,加过氧化氢和多糖的作为实验组,每组3个重复平行。
实验结果
1.对L929细胞增殖的影响
参照图7-A,与正常对照组相比,滇重楼葡甘聚糖对L929细胞没有显著增殖或抑制增殖作用,说明滇重楼葡甘聚糖在50~500μg/mL浓度下为安全剂量。
2.对H
参照图7-B,与正常对照组相比,经过过氧化氢诱导的模型组细胞存活率极显著降低,仅有25%左右,说明过氧化氢能够使L929细胞出现严重氧化损伤。与模型组相比,滇重楼葡甘聚糖组能够极显著的增加细胞存活率,这提示滇重楼葡甘聚糖可以保护氧化损伤的皮肤组织。
实施例6:滇重楼葡甘聚糖冻干粉针的制备
1.材料
按照实施例1制备的滇重楼葡甘聚糖、药用级氯化钠。
2.处方
3.制备工艺
称取处方量的滇重楼葡甘聚糖和氯化钠加注射用水至全量,搅拌使溶解完全,间歇式热压法灭菌。加入0.3%的药用活性炭,搅拌20min,使用布氏漏斗及3.0μm微孔滤膜脱炭过滤除去热源。含量合格后用0.22μm的微孔滤膜过滤,分装于管制西林瓶中,每瓶0.5mL,半压塞,置冷冻干燥箱内,按设定的冻干曲线进行冻干,压塞,出箱,轧盖,目检合格,包装得成品。
冻干过程:将样品进箱,降隔板温至-40℃,保持4h;冷阱降至-50℃,开始抽真空至250μbar。开始升华:1h匀速升温至-20℃,保持3h;3h匀速升温至-10℃,保持8h,真空保持100~250μbar;再进行干燥:2h升温至-5℃,保持2h,真空保持150~200μbar;0.5h升温至10℃,保持2h,真空保持80~100μbar;0.5h升温至40℃,保持4h,真空抽至最低。
实施例7:滇重楼葡甘聚糖胶囊剂的制备
1.材料
按照实施例1制备的滇重楼葡甘聚糖、食品或药品级淀粉。
2.处方
3.制备工艺
称取处方量的滇重楼葡甘聚糖和淀粉,搅拌使混合完全,加入适量滑石粉,用乙醇湿法制粒,过筛干燥后,装入2号胶囊壳中,每个胶囊体装填20mg的滇重楼葡甘聚糖,制得滇重楼葡甘聚糖胶囊。
实施例8:滇重楼葡甘聚糖口服液的制备
1.材料
根据实施例1的方法得到滇重楼葡甘聚糖、食品或药品级矫味剂为焦糖香精。
2.处方
3.制备工艺
称取处方量的滇重楼葡甘聚糖、蔗糖和焦糖香精,加纯化水完全溶解后,0.22μm的微孔滤膜过滤,滤液按每瓶2mL的量,经口服液罐装机灌装,封口后灭菌,即得。
实施例9:滇重楼葡甘聚糖凝胶的制备
1.材料
按照实施例1制备的滇重楼葡甘聚糖、化妆品级或食品级原料。
2.处方
3.制备工艺
称取配方量的滇重楼葡甘聚糖加入5L水溶解备用;将处方量的卡波姆940粉末均匀的撒于甘油表面,使卡波姆充分润湿后,加入4L水使卡波姆充分溶胀,再加入提前溶解好的多糖溶液,搅拌混合均匀后得混合液Ⅰ;将羟苯乙酯溶于丙二醇后,缓慢加入混合液Ⅰ中,得混合液Ⅱ;再将处方量的聚山梨酯80和三乙醇胺溶于1L水中,在搅拌条件下加入混合液Ⅱ中,搅拌均匀后,罐装即得滇重楼葡甘聚糖凝胶。
实施例10:滇重楼葡甘聚糖洁面乳的制备
1.材料
按照实施例1制备的滇重楼葡甘聚糖、其他化妆品级别或食品级原料。
2.配方
滇重楼葡甘聚糖0.5g、甘油3.0g、丁二醇3.0g、丙二醇0.6g、EDTA钠0.1g、瓜尔胶0.3g、二氧化锌2.0g、C
3.制备工艺
称取配方量的滇重楼葡甘聚糖,加纯化水完全溶解;取甘油、丁二醇、丙二醇、EDTA钠、瓜尔胶、二氧化锌、硬脂酸钠、C
实施例11:滇重楼葡甘聚糖面膜的制备
1.材料
按照实施例1制备的滇重楼葡甘聚糖、其他化妆品级或食品级的原料。
2.配方
滇重楼葡甘聚糖5.0g、黄原胶3.0g、透明质酸钠3.0g、丙二醇0.3g、卡波姆0.5g、尼泊金酯0.1g、PPG-10甲基葡糖醚0.25g、甘油葡糖苷1.0g、去离子水200g。
3.制备工艺
S10:取去离子水、黄原胶、透明质酸钠、丙二醇、卡波姆、尼泊金酯加入乳化锅内,一边搅拌一边加热至70℃,达到温度以后保温并继续搅拌直至溶液呈透明均一,然后保温20分钟后,降温至40℃。
S20:调节pH=7.4±0.2。
S30:继续降温至35℃,加入PPG-10甲基葡糖醚、滇重楼葡甘聚糖、甘油葡糖苷,继续搅拌均匀,检验合格后即可出料。以无纺布底材进行涂布,即得。
虽然已经参考优选实施例对本申请进行了描述,但在不脱离本申请的范围的情况下,可以对其进行各种改进并且可以用等效物替换其中的部件。尤其是,只要不存在结构冲突,各个实施例中所提到的各项技术特征均可以任意方式组合起来。本申请并不局限于文中公开的特定实施例,而是包括落入权利要求的范围内的所有技术方案。
- 一种AOI缺陷检测系统的性能调节方法
- 一种AOI自动检测设备
- 一种高电位晶闸管的检测装置的供能装置及检测系统
- 一种扩散板AOI检测装置
- 一种扩散板AOI检测装置
