一种YAP-TEAD抑制多肽及其用途
文献发布时间:2024-04-18 20:00:50
技术领域
本发明涉及一种YAP-TEAD抑制多肽及其用途,属于肿瘤治疗技术领域。
背景技术
鼻咽癌是我国南方地区高发的头颈部肿瘤,其发病率和死亡率远高世界平均水平,分别占全球的38.29%和40.14%
一方面,靶向药物作用于特定靶点,特异性强,对正常组织的损伤小,与化疗药物的作用机制不同,开展二者联用治疗鼻咽癌的临床研究,有望减少药物不良反应,提高生存率,改善生活质量。
目前针对鼻咽癌的靶向治疗药物主要包括表皮生长因子受体(EGFR)、血管生成因子(VEGF)和血管生成因子受体(VEGFR)抑制剂。西妥昔单抗作为首个应用于临床的EGFR抑制剂,其为单克隆抗体,与顺铂合用可以提高化疗后复发或转移的鼻咽癌患者病情的缓解率和稳定率贝伐单抗是抗血管生成因子单克隆抗体,其可缓解局部晚期鼻咽癌患者的病情进展,但是治疗效果也不明显。同样,寻找安全有效的靶向药物,逆转耐药性对鼻咽癌的临床研究具有重要意义,其为鼻咽癌个体化治疗的重要组成部分。
另一方面,YAP蛋白是一种在Hippo信号通路中的核心效应因子,是一种多功能的细胞内连接蛋白和转录共激活因子,在正常机体细胞内发挥信号转导和基因转录调节的作用,已有研究表明YAP参与肿瘤发生的发展,在机体中扮演致癌基因的角色,可以影响肿瘤细胞的生长,已有研究表明YAP蛋白在人的肝细胞癌、胃癌等肿瘤疾病中有明显发达,在多种实体肿瘤中过度表达,也表明其表达的程度与临床具有密切相关性。目前还没有文献报道关于YAP表达与鼻咽癌之间作用关系,研究YAP表达在治疗鼻咽癌中的应用具有重要意义。
发明内容
本发明针对以上现有技术中存在的缺陷,提供一种YAP-TEAD抑制多肽及其用途,解决的问题是提供新的治疗鼻咽癌的靶向功能的多肽,能够抑制YAP与TEAD的结合能力。
本发明的目的之一是通过以下技术方案得以实现的,一种YAP-TEAD抑制多肽,其特征在于,所述多肽通过对YAP氨基酸序列的85-98氨基酸片段突变后进行内环化设计,所述多肽包含PS-2(cyc87,96)或PS-2(cyc86,95),所述PS-2(cyc87,96)的氨基酸序列如下:
所述PS-2(cyc86,95)的氨基酸序列如下:
本发明通过对基于YAP氨基酸序列中的85-98范围的氨基酸片段的多肽结构进行改善,对YAP85-98氨基酸片段进行内环化设计。具体来说,通过在YAP的85-98氨基酸片段中进行点位突变,使在YAP的85-98氨基酸片段范围内突变位点87和96是的氨基酸,将对应的位置突变为C(半胱氨酸),再利用两个半胱氨酸形成二硫键进行内环化形成上述的PS-2(cyc87,96),或者通过在在YAP的85-98氨基酸片段范围内突变位点85和95,将对应的位置突变为C(半胱氨酸),再利用两个半胱氨酸形成二硫键进行内环化形成上述的PS-2(cyc86,95);获得以上两个经过突变且内环化后的PS-2(cyc87,96)或PS-2(cyc86,95)的YAP-TEAD抑制多肽。通过突变内环化后形成的多肽,能够提升该多肽与TEAD的亲和力,从而有效实现阻断YAP和TEAD的结合,使YAP不会被共沉淀,而本发明突变后内环化设计的多肽PS-2(cyc87,96)或PS-2(cyc86,95)与TEAD的之间具有极强的亲和力,从而具有优异的抑制活性,使在抗肿瘤性能方面具有活性,能够抑制YAP与TEAD的结合能力,使本发明的上述多肽能成为新的治疗鼻咽癌的靶向药物。通过在细胞和动物水平对新型YAP/TEAD抑制多肽对顺铂耐药鼻咽癌细胞株的药效进行评价,并深入探索其逆转顺铂耐药的分子机制,从而进一步开发靶向治疗策略,有望应用在鼻咽癌的治疗或预防等药物上,使晚期鼻咽癌患者获益。
在上述YAP-TEAD抑制多肽中,作为优选,所述多肽的C端增加穿膜CPP序列,所述CPP序列为:GRKKRRQRRR。为了改善多肽PS-2(cyc87,96)或PS-2(cyc86,95)通过细胞膜的能力,通过在其C端增加穿膜CPP序列,能够有效的使多肽大量进入而分布于细胞核,更好的显示出抑制CNE2和cDDP-CNE2功能(IC50),其细胞水平药效得到明显提升。
在上述YAP-TEAD抑制多肽中,作为优选,所述多肽具有YAP活性抑制功能。通过将上述YAP的85-98氨基酸片段的相应位点进行突变且内环化处理,能够提升其与TEAD的亲和力,从而也就阻断了YAP与TEAD的结合力,有效的抑制YAP的活性,抑制其与TEAD的结合,有效实现该多肽的整体抗肿瘤活性能力,尤其是在抗鼻咽癌的能力得到有效提升。作为进一步的优选,所述多肽抑制YAP与TEAD蛋白结合。
本发明的目的之二是通过以下技术方案来实现的,一种YAP-TEAD抑制多肽的用途,上述多肽用于制备预防、缓解和/或治疗鼻咽癌的药物。上述的多肽通过对YAP氨基酸序列85-98氨基酸片段进行突变后且内环化设计,所述多肽包含PS-2(cyc87,96)或PS-2(cyc86,95)所示的氨基酸片段。上述的药物利用YAP-TEAD抑制多肽作为预防、缓解和/或治疗鼻咽癌的药物的活性成分,利用其能够阻断YAP与TEAD的结合力,能够有效的缓解鼻咽癌疼痛;或抑制炎症细胞因子浸润;还能够有效的缓解鼻咽癌耐药性;本发明的药物利用上述多肽得到的药物能够有效的降低IL-1、IL-6、IL-17、IFN-γ或TNF-α的表达,具有优异的治疗效果。
在上述YAP-TEAD抑制多肽的用途中,作为优选,所述药物的制剂剂型选自片剂、胶囊剂、注射剂、颗粒剂、喷雾剂或冻干剂。具体的剂型可以根据需要进行加工,根据药物的活性添加上述多肽的有效量,使能达到治疗有效性均可。
综上所述,本发明与现有技术相比,具有以下优点:
通过对野生YAP的85-98氨基酸片段进行突变后且内环化设计,对应点位突变为C(半胱氨酸),利用两个半胱氨酸形成二硫键进行内环化,能够提升该多肽与TEAD的亲和力,从而有效实现阻断YAP和TEAD的结合,使YAP不会被共沉淀,具有优异的抑制活性,使在抗肿瘤性能方面具有活性,能够抑制YAP与TEAD的结合能力,使本发明的上述多肽能成为新的治疗鼻咽癌的靶向药物。
附图说明
图1是本发明的YAP结合关键氨基酸分析图。
图2是本发明的YAP多肽结构预测分析图。
图3是本发明的YAP-TEAD多肽抑制剂的分子水平评价分析图。
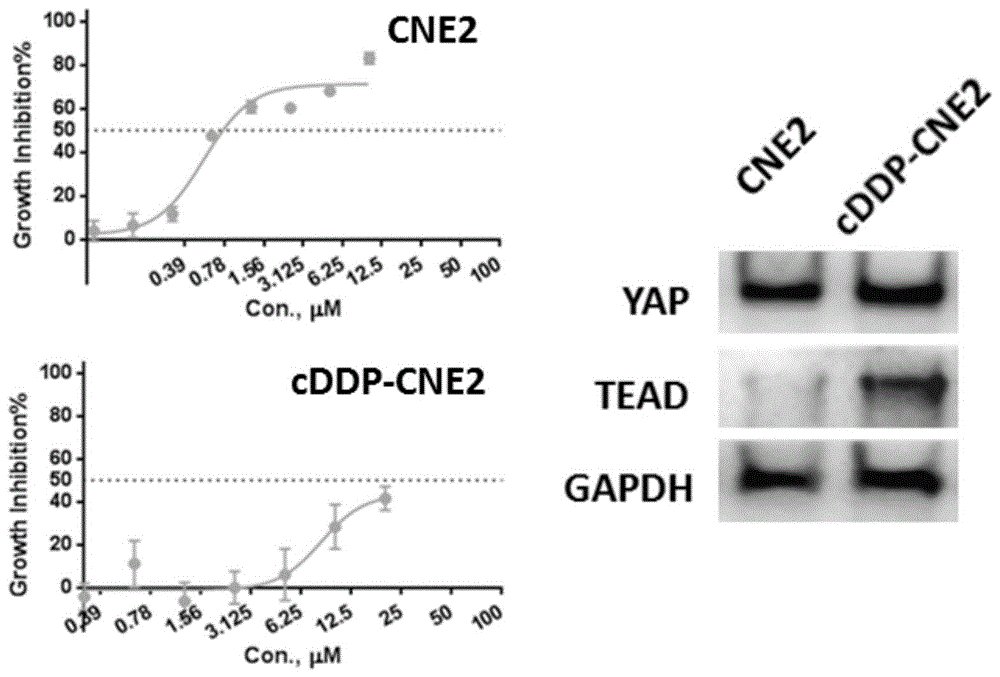
图4是本发明的CNE2顺铂耐药株构建图。
图5是本发明的YAP-TEAD抑制多肽的胞定位图。
具体实施方式
下面通过具体实施例和附图,对本发明的技术方案作进一步具体的说明,但是本发明并不限于这些实施例。
1.YAP-TEAD抑制多肽的生物信息学手段优化改造
为了得到YAP结合TEAD的关键区域,首先通过构建YAP-TEAD的复合物结构模型,这里的模型构建采用一般的构建方法均可,通过该模型,比较分析YAP-TEAD的相互作用力(如氢键、范德华力、静电吸引、去溶剂化效应和熵惩罚等),计算得到YAP结合关键区域中各氨基酸残基对相互作用的贡献度,具体如图1所示,结果显示YAP蛋白的63-73以及85-98氨基酸序列是YAP结合TEAD的关键区域。
本发明人通过对基于YAP 63-73或85-98氨基酸片段的多肽的结构进行预测,如图2所示,结果表明与YAP该区域不同,多肽的结构以无规卷曲为主,确认以YAP的85-98氨基酸片段进行突出且内环化设计。
为了改善多肽与TEAD的亲和力,本发明通过对YAP 85-98氨基酸片段(或表述为YAP位置aa85-98,aa表示氨基酸序列)进行突出后并进行内环化设计,即将YAP 85-98氨基酸片段上的87和96位突变为C(半胱氨酸),相当于对应YAP氨基酸序列的85-98氨基酸片段上的突变点位为87和96位;或者将YAP 85-98氨基酸片段上的86和95位突变为C(半胱氨酸),相当于对应YAP氨基酸序列85-98的氨基酸片段上的突变点位为86和95位,然后,利用两个突变点位上对应的两个半胱氨酸形成二硫键进行内环化,获得2个内环化多肽生物,即对应YAP-TEAD抑制多肽PS-2(cyc87,96)和PS-2(cyc86,95)。发明人经过初步分析比较了这2个内环化多肽与TEAD的结合自由能,结果显示经过突变且内环化改造后的内环化多肽的理论亲和能力明显提升。具体分析结果如以下表1所示:
表1:
表1中的PS-2(cyc87,96)和PS-2(cyc86,95)中氨基酸序列(Sepuence)是对应各自位置上突出为C后的两个C(半胱氨酸)形成二硫键进行环化后的多肽,即形成如下的内环化特性:
所述PS-2(cyc87,96)的氨基酸序列如下:
所述PS-2(cyc86,95)的氨基酸序列如下:
上述的YAP(即野生的YAP1)是现有的氨基酸序列,YAP的蛋白质序列号为P46937,是现有的序列,YAP整个蛋白的氨基酸序列号为P46937,利用该序列号P46937,可以在美国UniProt数据库上可获得。
上述两个PS-2(cyc87,96)和PS-2(cyc86,95)多肽的氨基酸序列相当于是在上述野生的YAP原序列(P46937)中的85-98氨基酸片段上对应的点位进行人工突变为半胱氨酸后进行内环化而成,对于具体的突变手段可采用常规的基团工程进行即可。
2.YAP-TEAD抑制多肽(或YAP-TEAD多肽抑制剂)的分子水平评价
本发明通过大肠杆菌原核表达和亲和层析纯化,得到高纯度的单体YAP和TEAD蛋白,构建免疫共沉淀体系,具体构建采用常规方法即可。结果显示对TEAD进行免疫沉淀,YAP会被共沉淀,利用本发明的YAP-TEAD抑制多肽PS-2(cyc87,96)和PS-2(cyc86,95),能够有效阻断YAP和TEAD的结合,导致YAP不会被共沉淀,而没有经过突变且内环化处理的PS-1和PS-2对YAP共沉淀的影响较小,进一步采用SPR对PS-2(cyc87,96)与TEAD的结合能力进行验证,结果表明其与TEAD有极强的亲和力,KD=1.2nM,也说明本发明通过对YAP85-98氨基酸片段的相应点位进行突变后并进行内环化处理,相比于PS-1和PS-2具有显著的优异表现。
3.YAP-TEAD抑制多肽(或YAP-TEAD多肽抑制剂)的细胞水平评价
本发明采用低浓度逐步加量诱导法构建了CNE2顺铂鼻咽癌耐药株cDDP-CNE2,如图4所示,检测结果显示顺铂抑制CNE2和cDDP-CNE2的IC50分别为0.54μM和8.2μM,耐药指数为15.2,Western Blot的结果显示顺铂耐药株中YAP和TEAD的表达上调,这也表明YAP-TEAD与鼻咽癌的顺铂耐药机制相关。表明本发明的YAP-TEAD抑制多肽对鼻咽癌具有抑制活性,能够用于制备预防、缓解和/或治疗鼻咽癌的药物。对于具体的药物的制剂剂型可以根据不同剂型的需求选自片剂、胶囊剂、注射剂、颗粒剂、喷雾剂或冻干剂。
作为另一优选的方案,为了改善PS-2(cyc87,96)通过细胞膜的能力,通过在本发明的YAP-TEAD抑制多肽PS-2(cyc87,96)的C-端增加穿膜CPP序列(GRKKRRQRRR)。结合图5所示,是本发明的YAP-TEAD抑制多肽PS-2(cyc87,96)的C-端增加穿膜CPP序列(GRKKRRQRRR)后和YAP-TEAD抑制多肽PS-2(cyc87,96)对应的细胞定位图,从图5的数据结果显示,其中PS-2(cyc87,96)主要分布于细胞膜表面,而增加CPP序列后多肽大量进入分布于细胞核,得到的PS-2(cyc87,96)CPP抑制cDDP-CNE2的IC50为3.1μM,其细胞水平药效得到明显提升。也表明通过在C端增加穿膜CPP序列(GRKKRRQRRR)能够更有效的提升其进入细胞核内的能力水平。当然也可对YAP-TEAD抑制多肽PS-2(cyc86,95)的C-端增加穿膜CPP序列(GRKKRRQRRR)。
本发明中所描述的具体实施例仅是对本发明精神作举例说明。本发明所属技术领域的技术人员可以对所描述的具体实施例做各种各样的修改或补充或采用类似的方式替代,但并不会偏离本发明的精神或者超越所附权利要求书所定义的范围。
尽管对本发明已作出了详细的说明并引证了一些具体实施例,但是对本领域熟练技术人员来说,只要不离开本发明的精神和范围可作各种变化或修正是显然的。
