一种酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂、其制备方法及应用
文献发布时间:2024-04-18 20:01:30
技术领域
本发明涉及一种酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂,以及该抑制剂的制备方法和应用。
背景技术
酪氨酸酶是黑色素生成的关键酶,能够催化酪氨酸或多巴酸转化为多巴醌,最终生成黑色素。酪氨酸酶的异常活性增强,会导致黑色素的过度沉着,从而影响皮肤美观,如炎症后黑皮病、痤疮后色素沉着、黄褐斑、雀斑、老年斑等黑色素沉着症,抑制酪氨酸酶的活性能够抑制黑色素的合成,降低黑色素的过度沉着,达到美白效果。另外,炎症后黑皮病、痤疮后色素沉着问题还涉及到5-脂氧合酶(5-lipoxygenase,5-LO)的异常活性增强。5-LO能够催化花生四烯酸变成5-羟过氧化二十碳四烯酸进而被氧化成白三烯(leukotriene,LT)。LT是皮炎等多种慢性炎症性疾病相关的促炎性脂质介质。炎症能够导致酪氨酸酶的异常活性增强,诱发黑色素细胞内黑色素的过量合成并引起色斑、色素沉着等问题,包括如前所述的炎症后黑皮病、痤疮后色素沉着。5-脂氧合酶激活蛋白(5-Lipoxygenase-activatingProtein,FLAP)调控5-LO的活性,抑制FLAP的活性可以抑制5-脂氧合酶的活性,降低白三烯的生物合成,以阻断后续炎症反应的发生,降低皮肤红斑,并抑制由炎症导致的酪氨酸酶活性异常增强,降低黑色素过度沉着。
解决黑色素沉着问题多应用酪氨酸酶抑制剂,例如曲酸、熊果苷、氢醌及重金属铅和汞离子等,该类酪氨酸酶抑制剂活性较低、安全性较差,例如细胞毒性、致癌性、导致皮炎、神经退行性症状、过敏、白斑病、褐黄病(Bioorganic&Medicinal Chemistry,2017,25(5):1687-1695)等,氢醌及重金属铅和汞离子禁止应用于化妆品中,曲酸、熊果苷、氢醌在医药领域和食品工业的应用也受到限制。
发明内容
本发明的目的是提供一种安全性好、稳定性强、抑制活性高的酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂,并为该抑制剂提供一种制备方法和用途。
针对上述目的,本发明提供的酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂的结构通式如下所示:
式中R
上述结构通式中,优选R
上述结构通式中,还可优选R
上述酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂的制备方法由下述步骤组成:
步骤1:将活泼金属加入干燥的四氢呋喃中,在氮气保护及加热回流下,滴加溴代烷烃R
式中R
步骤2:在氮气保护下,将钯催化剂、碱、化合物I和化合物II加入溶剂A中,于50~80℃搅拌反应2~6小时,加盐酸调pH值至1~3,继续反应1~4小时,加氢氧化钠调pH值至9~13,搅拌0.5~2小时,二氯甲烷萃取,硅胶柱色谱分离,得到式III所示酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂;
或者进一步将上述化合物III加入溶剂B中,并加酸调节pH为1~3,在室温下反应0.5~2小时,浓缩,2~8℃静置20~24小时,过滤取固体,得到式IV所示酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂;
上述酸为HCl、HBr、H
上述步骤1中,所述活泼金属优选镁或锂;所述溴代烷烃为碳原子数2~20的溴代烷烃;所述溴代烷烃与活泼金属、2,2-二甲基-1,3-二噁烷-5-酮、磺酰氯的摩尔比1:1~1.2:0.9~1.0:0.9~1.0。
上述步骤2中,优选所述化合物I和化合物II、钯催化剂、碱的摩尔比为1:2.5~4:0.04~0.06:1~1.2。其中,所述钯催化剂为乙酸钯、氯化钯、钯碳、硝酸钯、四(三苯基膦)钯、乙二胺氯化钯、双(三苯膦基)氯化钯、双(三苯膦基)醋酸钯、双(吡啶)二氯化钯、双(二亚芐基丙酮)钯中任意一种,所述碱为氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、三乙胺、N,N-二异丙基乙胺、1,8-二氮杂双环[5.4.0]十一碳-7-烯、左旋咪唑中任意一种,所述溶剂A为甲醇、乙醇、N,N-二甲基甲酰胺、二甲亚砜、乙二醇、四氢呋喃、1,4-二氧六环中任意一种;所述溶剂B为甲醇、乙醇、乙醚、四氢呋喃、二氯甲烷、蒸馏水中任意一种。
本发明所述酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂可用于制备治疗黑色素过度沉着的药物。
本发明的有益效果如下:
1、本发明提供的抑制剂结构新颖,总合成路线短,环境友好,原料来源广,成本低,可行性高,所有目标化合物易纯化,纯度均在99.5%以上。
2、本发明合成方法中的化合物I经一锅法合成,缩短了合成路线,简化了反应后处理,提高了生产效率。
3、本发明化合物对5-脂氧合酶激活蛋白和酪氨酸酶的活性具有明显的抑制作用,对酪氨酸酶的IC
附图说明
图1是化合物I-1的碳谱图。
图2是化合物I-1的氢谱图。
图3是化合物I-1的氟谱图。
图4是化合物III-1的氢谱图。
图5是化合物III-1的碳谱图。
图6是化合物III-2的氢谱图。
图7是化合物III-2的碳谱图。
图8是化合物III-3的氢谱图。
图9是化合物III-3的碳谱图。
图10是化合物III-4的氢谱图。
图11是化合物III-4的碳谱图。
图12是化合物III-5的氢谱图。
图13是化合物III-5的碳谱图。
图14是化合物III-6的氢谱图。
图15是化合物III-6的碳谱图。
图16是化合物III-7的氢谱图。
图17是化合物III-7的碳谱图。
图18是化合物IV-1的氢谱图。
图19是化合物IV-1的碳谱图。
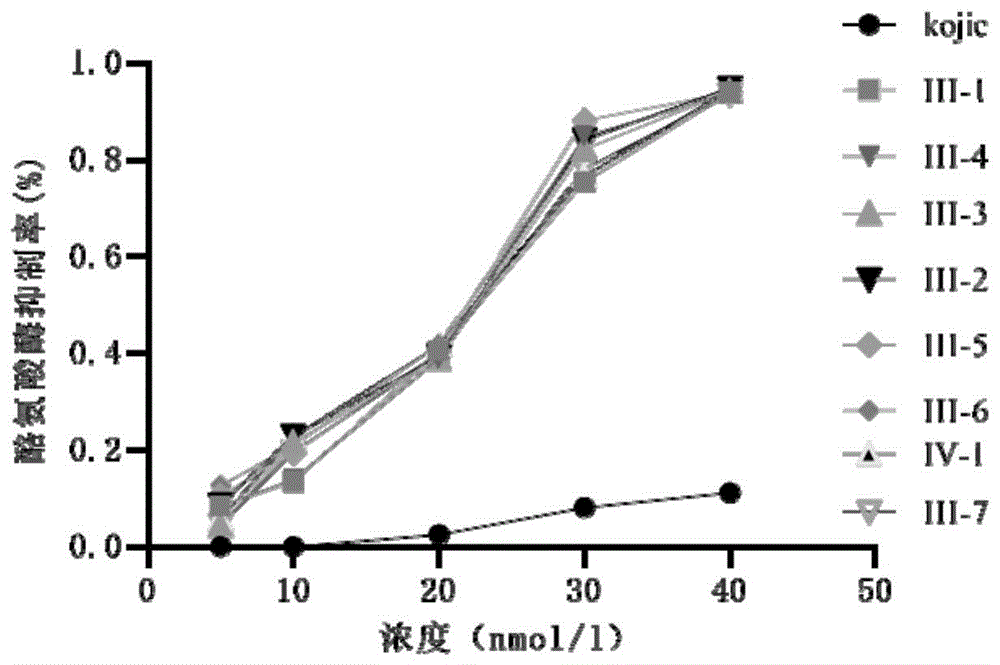
图20是化合物III-1~III-7及化合物IV-1对酪氨酸酶的体外抑制曲线图。
下面结合附图和实施例对本发明进一步详细说明,但本发明的保护范围不仅限于这些实施例。
实施例1
步骤1:在氮气保护下,将2.64g(0.11mol)镁粉和50mL干燥的四氢呋喃加入到500mL安装有搅拌器、冷凝管、恒压漏斗的三口瓶中,恒压漏斗中先加入50mL含33.30g(0.10mol)溴代十八烷的四氢呋喃溶液,升温至回流,滴加少量溴代十八烷的四氢呋喃溶液,待反应引发后,关闭加热,缓慢滴加剩余溶液。滴加完毕后升温至回流,反应2小时后,关闭加热降至室温,向反应体系中滴加13.00g(0.10mol)2,2-二甲基-1,3-二噁烷-5-酮,滴加完毕后回流反应2小时,继续滴加50mL含16.80g(0.10mmol)三氟甲磺酰氯的四氢呋喃溶液,继续回流反应4小时,降至室温,回收四氢呋喃,剩余物过硅胶色谱柱,以石油醚为洗脱剂洗脱,得到白色固体化合物I-1,即2,2-二甲基-5-十八烷基-1,3-二噁烷-5-三氟甲磺酸酯,纯度99.5%,收率60%。
化合物I-1的表征结果见图1~3:
步骤2:在氮气保护下,将20mL二甲基亚砜、1.40g(0.01mol)碳酸钾、113mg(0.5mmol)乙酸钯、5.20g(0.01mol)化合物I-1和3.63g(0.03mol)式II-1所示的2-苯乙胺加入到100mL安装有搅拌器、导气管的三口瓶中,于60℃油浴中搅拌反应6小时,反应过程中薄层色谱监测反应,反应完毕滴加盐酸调pH值为1,继续反应4小时,加氢氧化钠调pH值至13,搅拌0.5小时,二氯甲烷萃取,经硅胶柱色谱分离,以二氯甲烷与甲醇、氨水体积比为5:1:0.01的混合液洗脱,得到结构式如下的白色固体化合物III-1,即酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂,其化学命名为2-十八烷基-N-(2′-苯乙基)-1,3-二羟基-2-胺,液相纯度99.50%,收率70%。
化合物III-1的表征结果见图4~5:
实施例2
本实施例中,用等摩尔2-(2-甲氧基)苯乙胺替换实施例1中的2-苯乙胺,其他步骤与实施例1相同,得到结构式如下的白色固体化合物III-2,总收率45%。
化合物III-2的表征结果见图6~7:
实施例3
本实施例中,用等摩尔2-(4-氟)苯乙胺替换实施例1中的2-苯乙胺,其他步骤与实施例1相同,得到结构式如下的白色固体化合物III-3,总收率43%。
化合物III-3的表征结果见图8~9:
实施例4
本实施例中,用等摩尔2-(4-甲基)苯乙胺替换实施例1中的2-苯乙胺,其他步骤与实施例1相同,得到结构式如下的白色固体化合物III-4,总收率40%。
化合物III-4的表征结果见图10~11:
实施例5
本实施例中,用等摩尔2-(3-甲氧基)苯乙胺替换实施例1中的2-苯乙胺,其他步骤与实施例1相同,得到结构式如下的白色固体化合物III-5,总收率49%。
化合物III-5的表征结果见图12~13:
实施例6
本实施例中,用等摩尔2-(4-甲氧基)苯乙胺替换实施例1中的2-苯乙胺,其他步骤与实施例1相同,得到结构式如下的白色固体化合物III-6,总收率43%。
化合物III-6的表征结果见图14~15:
实施例7
本实施例中,用等摩尔3-甲氧基苄胺替换实施例1中的2-苯乙胺,其他步骤与实施例1相同,得到结构式如下的白色固体化合物III-7,总收率44%。
化合物III-7的表征结果见图16~17:
实施例8
本实施例中,用等摩尔2-(2-氟)-苯基乙胺替换实施例1中的2-苯乙胺,其他步骤与实施例1相同,得到式III-8所示的白色固体化合物。将4.66g(0.01mol)III-8所示的白色固体化合物加入20mL二氯甲烷中,并加入甲酸调节pH为2,在室温下反应0.5小时,浓缩至总体积10mL,5℃静置24小时,过滤取固体,得到结构式如下的白色固体化合物IV-1,即酪氨酸酶和5-脂氧合酶激活蛋白双靶点抑制剂,总收率37%。
化合物IV-1的表征结果见图18~19:1HNMR(CDCl
实施例9
实施例1~8制备的化合物在制备治疗黑色素过度沉着的药物中的应用
1、5-脂氧合酶激活蛋白抑制活性
对上述实施例1~8制备的化合物进行5-脂氧合酶激活蛋白(FLAP)抑制率测定,采用酶联免疫双抗夹心法,测定浓度为20nmol/L时对FLAP的抑制率,结果见表1。
同时与授权专利CN 112480062 B(一种5-脂氧合酶激活蛋白活性抑制剂及其制备方法)中公开的下列化合物1、3、5、6、7、9、10、11,在浓度为20nmol/L时时测定其对FLAP的抑制率,进行对比实验,结果见表1。
表1不同化合物对5-脂氧合酶激活蛋白的抑制活性(20nmol/L)
表1的5-脂氧合酶激活蛋白抑制活性结果显示,本发明的化合物III-1~III-7以及IV-1对于5-脂氧合酶激活蛋白(FLAP)的抑制率虽然没有化合物1、3、5、6、7、10、11的高,但也具有较好的抑制作用。
2、酪氨酸酶抑制活性
在96孔板中依次加入100μL蘑菇酪氨酸酶(终浓度:66.6U·mL
同时在浓度为1mmol/L时测定上述化合物1、3、5、6、7、9、10、11对蘑菇酪氨酸酶的活性,进行对比实验,结果见表3。
表2实施例1~8化合物对酪氨酸酶的抑制活性(IC
表3化合物1、3、5、6、7、10对酪氨酸酶的抑制活性(1mmol/L)
图20的酪氨酸酶的体外抑制结果显示,浓度为40nmol/L时,本发明化合物III-1~III-7及IV-1对酪氨酸酶的抑制率均在90%以上,曲酸对酪氨酸酶的抑制率仅为11%,表2显示化合物III-1~III-67及IV-1的IC
3、细胞毒性
以B16F10细胞系为对象,采用MTT法测定化合物III-1~III-7的细胞毒性,样品浓度为0.25mmol/L,作用于细胞时间为24小时,采用曲酸为阳性对照药,实验结果见表4。
表4细胞毒性实验
表4的细胞活力结果显示,浓度为0.25mmol/l时,与曲酸相比,本发明化合物III-1~III-7对B16F10细胞未表现出明显的毒性作用。
综合实验结果可见,本发明化合物对5-脂氧合酶激活蛋白和酪氨酸酶活性均具有明显的抑制作用,且安全无毒,可用于制备治疗黑色素过度沉着的药物中。
