一种化合物、发光层染料材料和有机电致发光器件
文献发布时间:2023-06-19 09:24:30
技术领域
本发明涉及有机发光显示技术领域,具体涉及一种化合物、发光层染料材料和有机电致发光器件。
背景技术
电致发光(electroluminescence,EL)是指发光材料在电场作用下,受到电流和电场的激发而发光的现象,它是一个将电能直接转化为光能的一种发光过程。有机电致发光显示器(以下简称OLED)具有自主发光、低电压直流驱动、全固化、视角宽、重量轻、组成和工艺简单等一系列的优点,与液晶显示器相比,有机电致发光显示器不需要背光源,且视角大、功率低,其响应速度可达液晶显示器的1000倍,其制造成本却低于同等分辨率的液晶显示器。因此,有机电致发光器件具有十分广阔的应用前景。
随着OLED技术在照明和显示两大领域的不断推进,人们对于影响OLED器件性能的高效有机材料的研究更加关注,一个效率好寿命长的有机电致发光器件通常是器件结构与各种有机材料的优化搭配的结果,这就为化学家们设计开发各种结构的功能化材料提供了极大的机遇和挑战。
相对于无机发光材料,有机电致发光材料具有很多优点,比如:加工性能好,可以通过蒸镀或者旋涂的方法在任何基板上成膜,可以实现柔性显示和大面积显示;可以通过改变分子的结构,调节材料的光学性能、电学性能和稳定性等,材料的选择具有很大的空间。在最常见的OLED器件结构里,通常包括以下种类的有机材料:空穴注入材料、空穴传输材料、电子传输材料,以及各色的发光材料(染料或者掺杂客体材料)和相应的主体材料等。
发明内容
本发明实施例的目的在于提供一种发光层染料材料,实现有机电致发光器件工作效率的提高和使用寿命的延长。
本发明的第一方面提供一种通式(I)的化合物:
其中,
X选自O、S或CRaRb,Ra、Rb彼此独立地选自C
R
R
所述杂芳基上的杂原子彼此独立地选自O、S、N;
所述Rc彼此独立地选自氘、卤素、硝基、氰基、C
本发明第二方面提供了一种发光层染料材料,其包含本发明提供的化合物中的至少一种。
本发明第三方面提供一种有机电致发光器件,其包含本发明提供的发光层染料材料中的至少一种。
本发明第四方面提供一种显示装置,其包含本发明提供的有机电致发光器件。
本发明公开的化合物,具有多元化稠环的母体结构,原子间的键能高,具有良好的热稳定性,并有利于分子间的固态堆积,同时带宽很大,发光区域位于蓝光区,发光强度很高,用作发光层染料材料,能有效降低器件电压,提高材料的发光效率和寿命。
本发明提供的多元化稠环的衍生物,在发光层中应用,与相邻层级间具有合适的能级水平,有利于激子的注入和迁移,能够有效降低驱动电压,同时较高的激子迁移速率,能够在器件中实现良好的发光效率。本发明化合物,具备较大的共轭平面,有利于分子堆积,表现出良好的热力学稳定性,在器件中表现为长寿命。
同时,本发明所述衍生物的制备工艺简单易行,原料易得,适合于工业化生产。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一种实施方式,对于本领域普通技术人员来讲,还可以根据这些附图获得其他的实施方式。
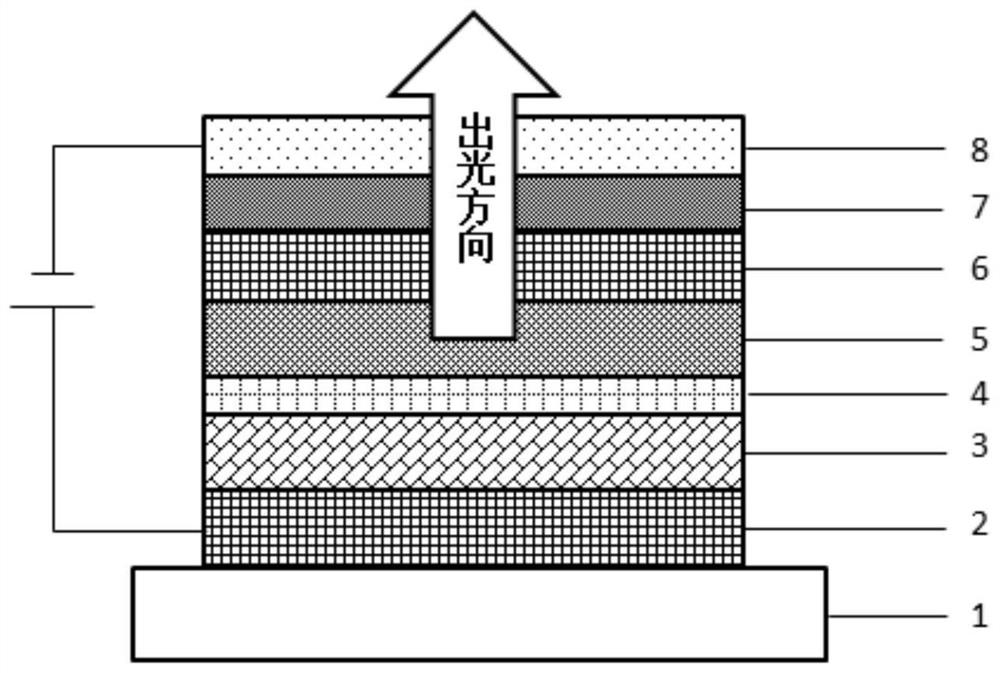
图1为一种典型的有机电致发光器件的结构示意图。
具体实施方式
下面将结合附图,对本发明中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。本领域普通技术人员基于本发明中的实施例所获得的所有其他实施例,都属于本发明保护的范围。
本发明的第一方面提供一种通式(Ⅰ)的化合物:
其中,
X选自O、S或CRaRb,Ra、Rb彼此独立地选自C
R
R
所述杂芳基上的杂原子彼此独立地选自O、S、N;
所述Rc彼此独立地选自氘、卤素、硝基、氰基、C
优选地,Ra和Rb彼此独立地选自C
优选地,R
优选地,R
更优选地,所述Ra和Rb彼此独立地选自甲基、乙基、环戊基、环己基、未取代或被Rc取代的以下基团:苯基、联苯基、三联苯基、萘基、菲基、三亚苯基、芴基、吡啶基、哒嗪基、嘧啶基、吡嗪基、喹啉基、异喹啉基、喹唑啉基、喹喔啉基、噌啉基、萘啶基、三嗪基、吡啶并吡嗪基、呋喃基、苯并呋喃基、二苯并呋喃基、氮杂-二苯并呋喃基、噻吩基、苯并噻吩基、二苯并噻吩基、氮杂-二苯并噻吩基、9,9-二甲基芴基、螺芴基、芳胺基、咔唑基。
更优选地,所述R
更优选地,所述R
例如,所述通式(I)的化合物选自以下化合物:
本发明第二方面提供一种发光层染料材料,其包含本发明提供的化合物中的至少一种。
图1示出了一种典型的有机电致发光器件的示意图,其中,从下到上,依次设置基板1、反射阳极电极2、空穴注入层3、空穴传输层4、发光层5、电子传输层6、电子注入层7、阴极电极8。
可以理解,图1仅示意性地示出了一种典型的有机电致发光器件的结构,本发明并不限于这种结构,本发明的发光层染料材料可以用于任何类型的有机电致发光器件。例如,有机电致发光器件还可以包括电子阻挡层、空穴阻挡层、光提取层等,实际应用时,可以根据具体情况增加或省略这些层。
本发明第三方面提供一种有机电致发光器件,其包含本发明提供的发光层染料材料中的至少一种。
在本发明中,对于有机电致发光器件的种类和结构没有特别限制,只要可以使用本发明提供的发光层染料材料即可。
本发明的有机电致发光器件,可以是顶部发光结构的发光器件,例如,在基板上依次包含阳极、空穴注入层、空穴传输层、发光层、电子传输层、电子注入层、透明或半透明阴极。
本发明的有机电致发光器件,还可以是底部发光结构的发光器件,例如,在基板上依次包含透明或半透明阳极、空穴注入层、空穴传输层、发光层、电子传输层、电子注入层及阴极结构。
本发明的有机电致发光器件,还可以是双侧发光结构的发光器件,例如,在基板上依次包含透明或半透明阳极、空穴注入层、空穴传输层、发光层、电子传输层、电子注入层及透明或半透明阴极结构。
在本发明的有机电致发光器件中,除了所述发光层包含本发明提供的发光层染料材料外,其它层均可以使用现有技术中用于所述层的任何材料。
为了方便起见,以下参照图1对本发明的有机电致发光器件进行说明,但这不意味着对本发明的保护范围的任何限定。可以理解,所有能够使用本发明的发光层染料材料的有机电致发光器件都在本发明的保护范围内。
在本发明中,所述基板1没有特别限制,可以使用现有技术中有机电致发光器件所用的常规基板,例如,玻璃、聚合物材料以及带有TFT元器件的玻璃和聚合物材料等。
在本发明中,所述反射阳极电极2的材料没有特别限制,可以选自现有技术中已知的铟锡氧(ITO)、铟锌氧(IZO)、二氧化锡(SnO
在本发明中,所述空穴注入层3的材料没有特别限制,可以使用本领域公知的空穴注入层材料制成,例如选用空穴传输材料(HTM)作为空穴注入材料。
在本发明中,所述空穴传输层4没有特别限制,可以选用本领域公知的空穴传输材料(HTM)中的至少一种。
例如,用于空穴注入层主体的材料和用于空穴传输层的材料可以选自以下HT-1至HT-31化合物中的至少一种:
在本发明中,所述发光层5包含主体材料和染料材料。其中,主体材料没有特别限制,可以使用本领域技术人员公知的任何主体材料,例如,已知的发光层主体材料可以选自以下BH-1至BH-10化合物中的至少一种:
在本发明中,发光层5中的染料材料包含本发明的发光层染料材料中的至少一种。发光层5中的染料材料也可以包含本发明的发光层染料材料中的至少一种与已知的染料材料的任意组合。目前已知的染料材料可以选自以下BD-1至BD-9化合物中的至少一种,但不局限于列举的化合物。
在本发明中,所述发光层5中染料材料的用量没有特别限制,可以为本领域技术人员公知的用量。
在本发明中,所述电子传输层6的材料没有特别限制,可以使用本领域公知的电子传输材料制成。例如,所述电子传输层材料可以选自以下ET-1至ET-57化合物中的至少一种:
在本发明中,所述电子注入层7的材料没有特别限制,可以使用本领域公知的电子注入材料,例如,可以包括但不限于现有技术中LiQ、LiF、NaCl、CsF、Li
在本发明中,所述阴极电极8的材料没有特别限制,例如,可以选自但不限于镁银混合物、LiF/Al、ITO、Al等金属、金属混合物、氧化物等。
本发明第四方面提供一种显示装置,其中包含本发明提供的有机电致发光器件。所述显示装置包括但不限于显示器、电视、平板电脑、移动通信终端等。
制备本发明的有机电致发光器件的方法没有特别限制,可以采用本领域公知的任何方法,例如,本发明可以采用如下制备方法制备:
(1)清洗顶发光用OLED器件基板1上的反射阳极电极2,在清洗机中分别通过药洗、水洗、毛刷、高压水洗、风刀等步骤,然后再加热处理;
(2)在反射阳极电极2上真空蒸镀空穴注入材料作为空穴注入层3;
(3)在空穴注入层3上真空蒸镀空穴传输材料作为空穴传输层4;
(4)在空穴传输层4上真空蒸镀发光层5,发光层5中包含主体材料和染料材料;
(5)在发光层5上真空蒸镀电子传输材料作为电子传输层6;
(6)在电子传输层6上真空蒸镀电子注入材料作为电子注入层7,电子注入材料选自LiQ、LiF、NaCl、CsF、Li
(7)在电子注入层7上真空蒸镀阴极材料作为阴极电极8。
以上仅描述一种典型的有机电致发光器件的结构及其制备方法,应当理解,本发明并不限于这种结构。本发明的发光层染料材料可以用于任何结构的有机电致发光器件,并且可以采用本领域公知的任何制备方法制备所述有机电致发光器件。
本发明的化合物的合成方法没有特别限制,可以采用本领域技术人员公知的任何方法进行合成。以下举例说明本发明化合物的合成过程。
合成实施例
合成实施例1:化合物A1的合成
在反应瓶中加入100mmol的10-溴-12,12-二甲基-12H-芴并[1,2-b]苯并呋喃、100mmol的2-溴-5-氯苯硼酯、41.4g碳酸钾(300mmol)、800ml四氢呋喃(THF)和200ml水,并加入1mol%的四(三苯基膦)钯(Pd(PPh
将100mmol的M1、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol的甲基溴化镁,0℃保温1h,升至室温反应6h,薄层色谱分析(TLC)监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M2。
将100mmol的M2、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M3。
在反应瓶中加入100mmol的M3、105mmol的双(4-叔丁基苯胺)、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的二苄基丙酮钯(Pd(dba))、2mol%的三叔丁基膦。在120℃下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末A1。其中,Pd(dba)的加入量为M3的1mol%,三叔丁基膦的加入量为M3的2mol%。
M/Z:实验值,679.2;理论值,679.4。
合成实施例2:化合物A4的合成
在反应瓶中加入100mmol的10-溴-12,12-二甲基-12H-芴并[1,2-b]苯并噻吩、100mmol的2-溴-5-氯苯硼酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M1、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol的甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M2。
将100mmol的M2、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M3。
在反应瓶中加入100mmol的M3、105mmol的2-二苯并呋喃-(2-甲基苯胺)、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的Pd(dba),2mol%的三叔丁基膦。在120℃下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末A4。其中,Pd(dba)的加入量为M3的1mol%,三叔丁基膦的加入量为M3的2mol%。
M/Z:实验值,687.4;理论值,687.2。
合成实施例3:化合物A6的合成
在反应瓶中加入100mmol的2-氯-12,12-二甲基-12H-芴并[1,2-b]苯并呋喃和500ml的THF,降温至-78℃,滴加入110mmol的正丁基锂,-78℃保温1h,滴加120mmol的硼酸三甲酯,自然升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得白色固体M1。
在反应瓶中加入100mmol的M1、100mmol的2-溴苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M2、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol的甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M3。
将100mmol的M3、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M4。
在反应瓶中加入100mmol的M4、105mmol的2,4,6-三甲基苯-苯胺、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的Pd(dba),2mol%的三叔丁基膦。在120℃下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末A6。其中,Pd(dba)的加入量为M4的1mol%,三叔丁基膦的加入量为M4的2mol%。
M/Z:实验值,608.7;理论值,609.3。
合成实施例4:化合物A8的合成
在反应瓶中加入100mmol的2-氯-11,11,12,12-四甲基-芴并[1,2-b]芴和500ml的THF,降温至-78℃,滴加入110mmol的正丁基锂,-78℃保温1h,滴加硼酸三甲酯120mmol,自然升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得白色固体M1。
在反应瓶中加入100mmol的M1、100mmol的2-溴苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M2、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M3。
将100mmol的M3、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M4。
在反应瓶中加入100mmol的M4、105mmol的4-二苯并呋喃-苯胺、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的Pd(dba),2mol%的三叔丁基膦。在120摄氏度下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末A8。其中,Pd(dba)的加入量为M4的1mol%,三叔丁基膦的加入量为M4的2mol%。
M/Z:实验值,682.9;理论值,683.3。
合成实施例5:化合物A14的合成
在反应瓶中加入100mmol的2-苯并萘并噻吩-硼酯、100mmol的2-溴苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M1、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M2。
将100mmol的M2、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M3。
在反应瓶中加入100mmol的M3和500ml的THF,降温至-78℃,滴加入110mmol正丁基锂,-78℃保温1h,滴加120mmol硼酸三甲酯,自然升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得白色固体M4。
在反应瓶中加入100mmol的M4、100mmol的2-溴-5-氯苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M5、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M6。
将100mmol的M6、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M7。
在反应瓶中加入100mmol的M7、105mmol的2-二苯并呋喃-苯胺、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的Pd(dba),2mol%的三叔丁基膦。在120℃下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末A14。其中,Pd(dba)的加入量为M7的1mol%,三叔丁基膦的加入量为M7的2mol%。
M/Z:实验值,723.3;理论值,723.2。
合成实施例6:化合物A15的合成
在反应瓶中加入100mmol的5-溴-二萘并[2,1-b:1',2'-d]呋喃、100mmol的2-硼酸苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M1、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M2。
将100mmol的M2、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M3。
在反应瓶中加入100mmol的M3和500ml的THF,降温至-78℃,滴加入110mmol正丁基锂,-78℃保温1h,滴加120mmol硼酸三甲酯,自然升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得白色固体M4。
在反应瓶中加入100mmol的M4、100mmol的2-溴-6-氯苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M5、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M6。
将100mmol的M6、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M7。
在反应瓶中加入100mmol的M7、105mmol的二苯胺、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的Pd(dba),2mol%的三叔丁基膦。在120℃下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末A15。其中,Pd(dba)的加入量为M7的1mol%,三叔丁基膦的加入量为M7的2mol%。
M/Z:实验值,666.8;理论值,667.2。
合成实施例7:化合物A19的合成
在反应瓶中加入100mmol的3-溴螺二芴并[1,2-b]苯并呋喃、105mmol的二苯胺、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的二苄基丙酮钯(Pd(dba))、2mol%的三叔丁基膦。在120℃下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末M1。其中,Pd(dba)的加入量为3-溴螺二芴并[1,2-b]苯并呋喃的1mol%,三叔丁基膦的加入量为3-溴螺二芴并[1,2-b]苯并呋喃的2mol%。
将100mmol的M1、500ml的THF加入到单口瓶中,降温至-78℃,滴加入110mmol的正丁基锂,-78℃保温1h,滴加二溴乙烷110mmol,自然升至室温反应12h,薄层色谱分析(TLC)监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M2。
在反应瓶中加入100mmol的M2、100mmol的1-甲酸甲酯-2-萘硼酯、41.4g碳酸钾(300mmol)、800ml四氢呋喃(THF)和200ml水,并加入1mol%的四(三苯基膦)钯(Pd(PPh
将100mmol的M3、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol的甲基溴化镁,0℃保温1h,升至室温反应6h,薄层色谱分析(TLC)监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M4。
将100mmol的M4、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体,重结晶得到A19。
合成实施例8:化合物A26的合成
在反应瓶中加入100mmol的2-苯并萘并呋喃-硼酯、100mmol的2-溴-5-氯苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M1、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol的甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M2。
将100mmol的M2、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M3。
在反应瓶中加入100mmol的M3和500ml的THF,降温至-78℃,滴加入110mmol正丁基锂,-78℃保温1h,滴加120mmol硼酸三甲酯,自然升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得白色固体M4。
在反应瓶中加入100mmol的M4、100mmol的2-溴-5-氯苯甲酸甲酯、41.4g碳酸钾(300mmol)、800ml的THF和200ml水,并加入1mol%的Pd(PPh
将100mmol的M5、500ml的THF加入到单口瓶中,降温至0℃,滴加入220mmol甲基溴化镁,0℃保温1h,升至室温反应6h,TLC监测原料消失。反应液中加水,乙酸乙酯萃取,有机相浓缩,得棕色固体M6。
将100mmol的M6、500ml三氟甲磺酸酐加入到单口瓶中,加热至120℃,反应6h,TLC监测原料消失。反应液中加水,过滤,滤饼用水和乙醇淋洗,洗至滤液为无色清液,得棕色固体M7。
在反应瓶中加入100mmol的M7、210mmol的二苯胺、28.83g叔丁醇钠(300mmol)、800ml二甲苯,并加入1mol%的Pd(dba),2mol%的三叔丁基膦。在120℃下反应12h。反应完毕后停止反应,并将反应物冷却至室温,加水,分离有机相,浓缩,柱层析,所得到的固体用甲苯进行重结晶纯化,得到白色粉末A26。其中,Pd(dba)的加入量为M7的2mol%,三叔丁基膦的加入量为M7的4mol%。
M/Z:实验值,784.1;理论值,784.3。
本发明的其他化合物均可按照上述实施例1-8的思路选择合适的原料进行合成,也可以选择任何其他合适的方法和原料进行合成。
实施例1
将涂布了ITO透明导电层的玻璃板在商用清洗剂中超声处理,在去离子水中冲洗,在丙酮-乙醇混合溶剂中超声除油,在洁净环境下烘烤至完全除去水份,用紫外光和臭氧清洗,并用低能阳离子束轰击表面;
然后,把上述带有阳极的玻璃基片置于真空腔内,抽真空至小于10
然后,在空穴注入层之上真空蒸镀空穴传输材料HT-5作为空穴传输层,其中,蒸镀速率为0.1nm/s,蒸镀膜厚为80nm;
然后,在空穴传输层之上真空蒸镀发光层,发光层包括主体材料BH-1和染料材料A1,利用多源共蒸的方法进行蒸镀,调节主体材料BH-1的蒸镀速率为0.1nm/s,染料材料A1蒸镀速率为主体材料蒸镀速率的3%,蒸镀总膜厚为30nm;
然后,在发光层之上真空蒸镀电子传输材料ET-42作为电子传输层,其中,蒸镀速率为0.1nm/s,蒸镀膜厚为30nm;
然后,在电子传输层(ETL)上真空蒸镀LiF作为电子注入层,其中,蒸镀速率为0.1nm/s,蒸镀膜厚为0.5nm;
然后,在电子注入层之上真空蒸镀铝层作为器件的阴极电极,其中,蒸镀速率为0.1nm/s,蒸镀膜厚为150nm。
实施例2-8
除了分别用A4、A6、A8、A14、A15、A19、A26代替A1以外,其余与实施例1相同。测试结果见表1。
对比例1
除了用BD-1替换A1以外,其余与实施例1相同。测试结果见表1。
对由上述过程制备的有机电致发光器件进行如下性能测定:
在同样亮度下,使用数字源表及亮度计测定实施例以及对比例制备得到的有机电致发光器件的驱动电压和电流效率以及器件的寿命,具体而言,以每秒0.1V的速率提升电压,测定当有机电致发光器件的亮度达到1000cd/m
表1有机电致发光器件性能结果
从表1可以看出,本发明制得的化合物用于有机电致发光器件发光层染料材料,可以有效的降低驱动电压,提高电流效率,延长器件寿命,是性能良好的蓝光染料材料。
以上所述仅为本发明的较佳实施例,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内所作的任何修改、等同替换、改进等,均包含在本发明的保护范围内。
- 一种化合物、发光层染料材料和有机电致发光器件
- 一种有机化合物,包含该化合物的有机电致发光器件材料及包含该材料的有机电致发光器件
