一种术后风险预测模型的建立方法及装置
文献发布时间:2023-06-19 12:21:13
技术领域
本发明涉及医学软件技术领域,尤其涉及一种术后风险预测模型的建立方法及装置。
背景技术
Stanford A型主动脉夹层(stanford type A aortic dissection,TAAD)是一种极为凶险的是主动脉疾病,自然预后极差,院内死亡率约10.3%,若未得到及时的处理,每小时死亡率可提升1-2%,通过外科手术修复仍然是TAAD的主要治疗方法,但患者手术风险较大,若能及时识别高危患者,进行早期干预,降低术后不良事件的发生率可能是帮助患者改善预后的有效方法,目前国际上应用最多的心血管手术评分系统是更新后的欧洲心脏手术风险评估系统(EuroSCORE-II),其具有更强的鉴别能力,模型校准度较好,然而,EuroSCORE-Ⅱ评分系统对于主动脉夹层手术的预测效能并不高,且我国TAAD患者的平均发病年龄较西方国家低,从发病到手术治疗的时间却比发达国家要长,导致患者术后差异较大。
发明内容
本发明目的在于,提供一种术后风险预测模型的建立方法及装置,以解决现有紧急Stanford A型主动脉夹层术后风险预测效率低的问题。
为实现上述目的,本发明提供一种术后风险预测模型的建立方法,包括:
根据确定符合预设入组条件的患者数据纳入多元回归分析模型,获取多元回归分析结果;
根据所述多元回归分析结果,建立术后风险评估预测模型。
优选地,所述根据确定符合预设入组条件的患者数据纳入多元回归分析模型,获取多元回归分析结果,包括:
将所述患者数据进行单因素分析,获取预设范围内的第一变量;
根据所述第一变量的逐步逻辑回归多变量分析确定预设范围内的第二变量;
将所述第二变量纳入多元回归分析模型,获取多元回归分析结果。
优选地,所述多元回归分析模型,包括:
logit P=ln[P/(1-P)]=B
其中,表示术后不良事件发生的概率,B表示与风险因数相关的常数,X表示给定患者的危险因数的状态。
优选地,所述根据所述多元回归分析结果,建立术后风险评估预测模型,包括:
W=-4.0.43+0.033×a+1.5109×b+1.0603×c+0.9455×d+0.7008×e+1.6092×f;
其中,w表示术后风险评估预测模型,a表示患者的年龄,若患者术前谷丙氨酸氨基转移酶水平变量大于或等于120U/L,b=1否则b=0,若室内隔离厚度大于或等于12mm,c=1否则c=0,d表示患者是否同时进行冠状动脉旁路移植术,若是,d=1否则d=0,若患者体外循环时间大于或等于250分钟,e=1否则e=0,若患者延迟关胸,f=1否则f=0。
本发明还提供一种术后风险预测模型的建立装置,包括:
分析模块,用于根据确定符合预设入组条件的患者数据纳入多元回归分析模型,获取多元回归分析结果;
建模模块,用于根据所述多元回归分析结果,建立术后风险评估预测模型。
优选地,所述分析模块,还用于:
将所述患者数据进行单因素分析,获取预设范围内的第一变量;
根据所述第一变量的逐步逻辑回归多变量分析确定预设范围内的第二变量;
将所述第二变量纳入多元回归分析模型,获取多元回归分析结果。
优选地,所述分析模块,还用于:
logit P=ln[P/(1-P)]=B
其中,表示术后不良事件发生的概率,B表示与风险因数相关的常数,X表示给定患者的危险因数的状态。
优选地,所述建模模块,还用于:
W=-4.0.43+0.033×a+1.5109×b+1.0603×c+0.9455×d+0.7008×e+1.6092×f;
其中,w表示术后风险评估预测模型,a表示患者的年龄,若患者术前谷丙氨酸氨基转移酶水平变量大于或等于120U/L,b=1否则b=0,若室内隔离厚度大于或等于12mm,c=1否则c=0,d表示患者是否同时进行冠状动脉旁路移植术,若是,d=1否则d=0,若患者体外循环时间大于或等于250分钟,e=1否则e=0,若患者延迟关胸,f=1否则f=0。
本发明还提供一种计算机终端设备,包括一个或多个处理器和存储器。存储器与所述处理器耦接,用于存储一个或多个程序;当所述一个或多个程序被所述一个或多个处理器执行,使得所述一个或多个处理器实现如上述任一实施例所述的术后风险预测模型的建立方法。
本发明还提供一种计算机可读存储介质,其上存储有计算机程序,其特征在于,所述计算机程序被处理器执行时实现如上述任一实施例所述的术后风险预测模型的建立方法。
本发明根据确定符合预设入组条件的患者数据纳入多元回归分析模型,获取多元回归分析结果,根据多元回归分析结果,建立术后风险评估预测模型,构建术后风险评估预测模型,评估Stanford A型主动脉夹层术后发生不良事件发生风险,提高患者的存活率且降低并发症发生率。
附图说明
为了更清楚地说明本发明的技术方案,下面将对实施方式中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
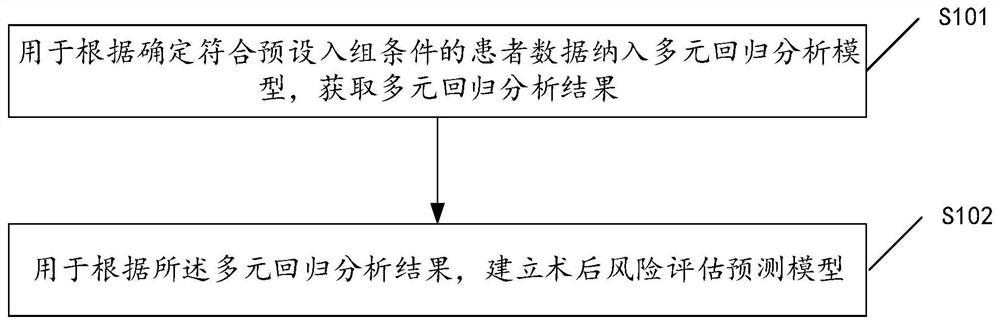
图1是本发明某一实施例提供的术后风险预测模型的建立方法的流程示意图;
图2是本发明另一实施例提供的建模组术后不良事件发生风险评估模型的ROC曲线图;
图3是本发明某一实施例提供的术后风险预测模型的建立装置的结构示意图;
具体实施方式
下面将结合本发明中的附图,对本发明中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
应当理解,文中所使用的步骤编号仅是为了方便描述,不作为对步骤执行先后顺序的限定。
应当理解,在本发明说明书中所使用的术语仅仅是出于描述特定实施例的目的而并不意在限制本发明。如在本发明说明书和所附权利要求书中所使用的那样,除非上下文清楚地指明其它情况,否则单数形式的“一”、“一个”及“该”意在包括复数形式。
术语“包括”和“包含”指示所描述特征、整体、步骤、操作、元素和/或组件的存在,但并不排除一个或多个其它特征、整体、步骤、操作、元素、组件和/或其集合的存在或添加。
术语“和/或”是指相关联列出的项中的一个或多个的任何组合以及所有可能组合,并且包括这些组合。
请参阅图1,本发明提供一种术后风险预测模型的建立方法,包括:
S101、根据确定符合预设入组条件的患者数据纳入多元回归分析模型,获取多元回归分析结果。
具体的,患者的数据收集首先采用广东省人民医院的患者资料,若部分患者从外地转院到该医院,因病情危重未能在该医院进行检验或TTE或CTA等检查,则收集外院的检查资料,患者资料包括基本情况、临床表现、病史、体格检查、实验室检查、影像学检查6方面,各方面的具体收集内容如下:
(1)基本情况
包括年龄、性别、身高、体重、BMI、心率、呼吸频率、体温、四肢血压等。
(2)临床表现
包括疼痛的发生部位(胸部、背部、腹部、腰部)和疼痛性质(撕裂样、烧灼样、刺痛)、放射痛、肢端缺血症状(肢端麻木、肢端发冷)、头颈部缺血症状(头晕、头痛)、脏器缺血症状(腹痛、少尿、无尿)、少见症状(大汗淋漓、恶心、呕吐)等。
(3)病史
包括主诉、发病时间、基础病史(高血压、糖尿病、冠心病、高脂血症)、重要器官病史(COPD、慢性肝肾病、神经系统病史)、心血管病史(主动脉病变病史、瓣膜病病史、心律失常病史)、心血管手术史、特殊药物服用史(抗凝药物、抗血小板药物)、正性肌力药物的使用(肾上腺素、多巴胺)、遗传病史(高血压、马凡综合征、主动脉夹层)、妊娠、烟酒嗜好、转归(术前死亡、外科手术、存活)、气管插管、心肺复苏等。
(4)体格检查
包括神志(清醒、嗜睡、昏迷)、四肢活动(自如、乏力、瘫痪)、肠鸣音、心肺听诊(心脏瓣膜杂音、心律、肺干湿啰音)、颈动脉搏动(正常、减弱、消失)等。
(5)实验室检查
包括血常规(白细胞、中性粒比、血小板、血红蛋白)、凝血功能(APTT、PTA、INR、D-二聚体)、肝肾功能及生化(ALT、AST、CREA、ALB、空腹血糖、尿素)、动脉血气分析(PH、PAO2、PACO2、SAO2、BE、LAC)、心功能(CKMB、CTNT、BNP、LDH)、感染指标(CRP、PCT)、血型等。
(6)影像学检查的记录与测量
包括TTE(LVEF、主动脉窦内径、主动脉根部内径、左室舒张末内径、左室收缩末内径、室间隔厚度、左室后壁厚度、瓣膜返流与缩窄、肺动脉压力及分级、左室舒张功能、心包积液分度)、主动脉CTA(主动脉窦直径、窦管结合部直径、升主动脉真假腔内径及病理分型、主动脉弓真假腔内径及病理分型、胸主动脉上中下段真假腔内径及病理分型、降主动脉上下端真假腔内径及病理分型、近端内膜破口大小与位置、头臂干与左颈总动脉的距离、左颈总与左锁骨下动脉的距离、是否累及重要血管分支、主动脉及分支的闭塞与狭窄、主动脉的变异与位置、合并胸腹主动脉瘤、胸腔积液)、心电图(左右冠脉的心肌缺血表现)等。
将符合入组标准的患者分为发生组和未发生组,终点事件为术后30天内发生不良反应的事件,计数资料比较采用χ
将患者数据进行单因素分析,获取预设范围内的第一变量,根据第一变量的逐步逻辑回归多变量分析确定预设范围内的第二变量,第二变量包括年龄,将第二变量纳入多元回归分析模型,获取多元回归分析结果。
具体的,通过单因素分析,获得P<0.05为差异有统计学意义,将P<0.05的第一变量输入逐步逻辑回归多变量分析确定P<0.05的第二变量,将第二变量纳入多元回归分析模型,获取多元回归分析结果,如下:
logit P=ln[P/(1-P)]=B
其中,表示术后不良事件发生的概率,B表示与风险因数相关的常数,X表示给定患者的危险因数的状态。最终模型中的独立风险因素以比值比表示,受试者工作特征曲线(receiver operating characteristic curve,ROC),检测观测值和预测值的差异采用Hosmer-Lemeshow拟合优度检验,年龄和性别均强制进入模型,利用SPSS 25.0软件处理,排除资料缺失>20%的病例。
本发明模型入组标准为2017年9月至2020年3月连续就诊于广东省人民医院且由主动脉全程增强CT确诊为TAAD并行外科手术治疗的患者,采用本发明模型所得到的预测结果能评估TAAD患者的术后不良事件发生风险,简单、易用、可靠,协助外科医师对高危患者进行早期干预,以提高患者的存活率及降低并发症发生率。
S102、根据所述多元回归分析结果,建立术后风险评估预测模型。
具体的,在多元回归分析结果上,建立了风险评分模型,紧急Stanford A型主动脉夹层术后不良事件风险评估预测模型w,如下:
W=-4.0.43+0.033×a+1.5109×b+1.0603×c+0.9455×d+0.7008×e+1.6092×f;
其中,w表示术后风险评估预测模型,a表示患者的年龄,若患者术前谷丙氨酸氨基转移酶水平变量大于或等于120U/L,b=1否则b=0,若室内隔离厚度大于或等于12mm,c=1否则c=0,d表示患者是否同时进行冠状动脉旁路移植术,若是,d=1否则d=0,若患者体外循环时间大于或等于250分钟,e=1否则e=0,若患者延迟关胸,f=1否则f=0。
请参照图2,通过Hosmer-Lemeshow检验发现,观测值和预测值的分离度差异无统计学意义(χ
请参照图2,采用内部验证并通过10倍交叉验证,将数据集随机分为10个大小相等的样本,将模型重新拟合到包含90%数据的10个集合中的每一个,计算每个情况下未使用的10%的ROC曲线下的面积,并对10个ROC曲线下的面积进行平均见表1,验证集的Hosmer-Lemeshow检验发现,观测值和预测值的分离度差异无统计学意义(χ
表1术后不良事件风险预测模型的10倍交叉验证数据
本发明模型入组标准为2017年9月至2020年3月连续就诊于广东省人民医院且由主动脉全程增强CT确诊为TAAD并行外科手术治疗的患者,根据确定符合预设入组条件的患者数据纳入多元回归分析模型,获取多元回归分析结果,根据多元回归分析结果,建立术后风险评估预测模型,构建术后风险评估预测模型,评估Stanford A型主动脉夹层术后发生不良事件发生风险,采用本发明模型所得到的预测结果能评估TAAD患者的术后不良事件发生风险,简单、易用、可靠,协助外科医师对高危患者进行早期干预,以提高患者的存活率及降低并发症发生率。
本发明提供的术后风险预测模型应用于医疗中,以下是实施示例:
患者男,69岁,主诉为颜面部、颈前、胸部浮肿皮疹6小时。到我院急诊后根据外院检查结果考虑诊断为主动脉夹层(Stanford A型),采集患者基本信息、围术期各项指标。实验室检查发现患者术前门冬氨酸氨基转移酶为13U/L;我院心脏彩超提示室间隔厚度为10mm。患者术中体外循环时间410分钟,未合并冠脉搭桥手术,但考虑到术区创面渗血严重,遂决定行延迟关胸术。将患者资料带入模型公式得到术后不良事件发生率为63.27%,属于高风险人群。实际上,患者术后感染较重、急性肾衰竭并发生右侧大脑半球大面积脑梗死导致脑疝形成,经抢救无效死亡。
患者男,39岁,主诉为胸痛5小时。到我院急诊后根据外院检查结果考虑诊断为主动脉夹层(Stanford A型),采集患者基本信息、围术期各项指标。实验室检查发现患者术前门冬氨酸氨基转移酶为37U/L;我院心脏彩超提示室间隔厚度为16mm。患者术中体外循环时间198分钟,未合并冠脉搭桥手术及延迟关胸术。将患者资料带入模型公式得到术后不良事件发生率为15.50%,属于中风险人群。实际上,患者术后虽出现低氧血症但经重症监护室监护治疗后恢复良好,顺利出院。
作为示例性的,术后风险评估模型评分分数参考判断结果如下:
1、p(>60%),为极高风险;
2、p(30%-60%),为高风险;
3、p(10%-29%),为中风险;
4、p(<10%),为低风险。
请参照表2、表3和表4,相关统计结果,分别为单因素分析结果,多因素分析结果,参数估计,如下:
表2单因素分析结果
其中,表2加粗字体为通过单因素分析得到具有统计学意义的变量,即P<0.05。将单因素分析得到的变量纳入多变量分析,得到具有统计学差异的建模变量,如下:
表3多因素分析
表4参数估计
请参阅图3,本发明提供一种术后风险预测模型的建立装置,包括:
分析模块11,用于根据确定符合预设入组条件的患者数据纳入多元回归分析模型,获取多元回归分析结果。
建模模块12,用于根据所述多元回归分析结果,建立术后风险评估预测模型。
关于术后风险预测模型的建立装置的具体限定可以参见上文中对于的限定,在此不再赘述。上述术后风险预测模型的建立装置中的各个模块可全部或部分通过软件、硬件及其组合来实现。上述各模块可以硬件形式内嵌于或独立于计算机设备中的处理器中,也可以以软件形式存储于计算机设备中的存储器中,以便于处理器调用执行以上各个模块对应的操作。
本发明提供一种计算机终端设备,包括一个或多个处理器和存储器。存储器与所述处理器耦接,用于存储一个或多个程序,当所述一个或多个程序被所述一个或多个处理器执行,使得所述一个或多个处理器实现如上述任意一个实施例中的术后风险预测模型的建立方法。
处理器用于控制该计算机终端设备的整体操作,以完成上述的术后风险预测模型的建立方法的全部或部分步骤。存储器用于存储各种类型的数据以支持在该计算机终端设备的操作,这些数据例如可以包括用于在该计算机终端设备上操作的任何应用程序或方法的指令,以及应用程序相关的数据。该存储器可以由任何类型的易失性或非易失性存储设备或者它们的组合实现,例如静态随机存取存储器(Static Random Access Memory,简称SRAM),电可擦除可编程只读存储器(Electrically Erasable Programmable Read-OnlyMemory,简称EEPROM),可擦除可编程只读存储器(Erasable Programmable Read-OnlyMemory,简称EPROM),可编程只读存储器(Programmable Read-Only Memory,简称PROM),只读存储器(Read-Only Memory,简称ROM),磁存储器,快闪存储器,磁盘或光盘。
在一示例性实施例中,计算机终端设备可以被一个或多个应用专用集成电路(Application Specific 1ntegrated Circuit,简称AS1C)、数字信号处理器(DigitalSignal Processor,简称DSP)、数字信号处理设备(Digital Signal Processing Device,简称DSPD)、可编程逻辑器件(Programmable Logic Device,简称PLD)、现场可编程门阵列(Field Programmable Gate Array,简称FPGA)、控制器、微控制器、微处理器或其他电子元件实现,用于执行上述的术后风险预测模型的建立方法,并达到如上述方法一致的技术效果。
在另一示例性实施例中,还提供了一种包括程序指令的计算机可读存储介质,该程序指令被处理器执行时实现上述任意一个实施例中的术后风险预测模型的建立方法的步骤。例如,该计算机可读存储介质可以为上述包括程序指令的存储器,上述程序指令可由计算机终端设备的处理器执行以完成上述的术后风险预测模型的建立方法,并达到如上述方法一致的技术效果。
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
- 一种术后风险预测模型的建立方法及装置
- 一种TAPVC心上术后再狭窄的风险预测模型的构建方法及装置
