一种肉鸡饲料有效磷的仿生消化测定试剂盒和测定方法
文献发布时间:2024-04-18 19:59:31
技术领域
本发明属于农业领域,涉及一种肉鸡饲料有效磷的测定技术,具体涉及一种肉鸡饲料有效磷的仿生消化测定试剂盒和测定方法。
背景技术
磷元素是肉鸡必需的营养素,在骨骼健康、核酸合成、细胞能量传递、信号传导等生命基本活动中发挥着必不可少的作用。肉鸡饲料中磷主要来源于磷酸氢钙等矿物质添加剂和动植物性原料中的无机磷和植酸,是肉鸡饲料中第三昂贵的营养素。然而,植酸形式存在的磷以及未溶解含磷矿物质并不能被机体吸收利用,随粪便排出体外造成环境富营养化污染。因此,准确测定肉鸡饲料中有效磷对于维持肉鸡基础生命活动和健康、确定畜禽合理的磷的需要量、减少磷排放维持生态环境等方面,都具有极其重要意义;对肉鸡养殖生产效益提高、节本增效有着重要的经济价值。
饲料中“有效磷”指能够被畜禽消化道吸收和利用的磷,主要以磷酸根离子(PO
因此,根据肉鸡的体内消化条件建立体外消化过程的新方法,实现磷的释放过程逼近体内过程,解决释放无机磷的定量等问题,是对肉鸡饲料原料和配合饲料中有效磷快速、准确测定的基础,对解决行业重大技术需求势在必行。
发明内容
为了解决上述问题,本发明的目的在于建立一种肉鸡饲料有效磷的仿生消化测定试剂盒,该试剂盒适配单胃动物仿生消化系统可以实现肉鸡饲料的原料和配合饲料中有效磷的快速准确测定。
本发明的另一目的在于提供一种肉鸡饲料有效磷的仿生测定方法,实现肉鸡饲料有效磷的快速准确测定。
为了实现上述目的,本发明提供一种肉鸡饲料有效磷的仿生消化测定试剂盒,包括如下组成:
缓冲液I粉末:无水乙酸钠4.101 g;氯化钾2.01 g;
消化酶I:胃蛋白酶114400 U;
缓冲液II粉末:无水乙酸钠4.101 g;
消化酶II:淀粉酶67860 U;胰蛋白酶12870 U;糜蛋白酶6450U;
标准品:磷酸二氢钾0.2195 g;
显色剂:偏钒酸铵1.25 g;钼酸铵25 g;
C18色谱柱 10个;
0.22 μm针头滤器10个。
如上所述地,所述消化酶II提取自肉鸡空肠末端食糜。
上述试剂盒可供测定10份样品,样品可为不同样品或重复样品。
为了实现上述目的,本发明提供一种快速、准确测定肉鸡饲料有效磷的仿生消化方法,包括如下步骤:
1)模拟消化液、缓冲液的制备
胃缓冲液的制备:将上述的仿生消化测定试剂盒中的缓冲液I粉末溶解于450 mL去离子水中,用6 mol/L的盐酸在41℃下调节溶液的pH至4.35,冷却后定容至500 mL制成胃缓冲液;
模拟胃液的制备:将上述的仿生消化测定试剂盒中的消化酶I溶解于41℃下pH4.35的200 mL胃缓冲液中,缓慢搅拌30分钟制成模拟胃液;
小肠缓冲液的制备:将上述的仿生消化测定试剂盒中的缓冲液II粉末溶解于450mL去离子水中,用氢氧化钠溶液调节pH至12.2,定容至500 mL制成小肠缓冲液;
浓缩模拟小肠液的制备:将上述的仿生消化测定试剂盒中的消化酶II溶解于30mL去离子水中,制成浓缩模拟小肠液;
2)预热、上样
采用单胃动物仿生消化系统,其包括立式模拟消化器、配套搅拌装置、立式固定架、消化液试剂瓶、缓冲液试剂瓶、去离子水试剂瓶、废液收容瓶;将步骤1)制备的模拟胃液、模拟小肠液放入该单胃动物仿生消化系统的消化液试剂瓶中;将步骤1)中制备的小肠缓冲液和去离子水放入该单胃动物仿生消化系统的缓冲液控温室;在该单胃动物仿生消化系统中,41℃预热时间为60分钟后,将准确称取0.5 g粉碎后过60目标准筛的鸡饲料样品置于该单胃动物仿生消化系统的玻璃模拟消化器中;将配套搅拌装置与玻璃模拟消化器连接,并固定到该单胃动物仿生消化系统的固定架的夹具上;每个样品测定5重复,每个重复使用1根模拟消化器;
3)胃模拟消化:
将装置好的立式固定架置于该单胃动物仿生消化系统中,按照立式模拟消化器外管下端进水,上端出水的原则,接好管路,再通过消化液加液管将每管根立式模拟消化器内管与相连;15 mL胃模拟消化液泵入各立式模拟消化器,通过搅拌器旋转提供胃液与饲料样品的混合动力,进行胃的模拟消化;
4)小肠模拟消化:
将5 mL小肠缓冲液泵入立式模拟消化器中,以使立式模拟消化器溶液的pH由胃的消化环境自动切换为小肠的消化环境,再将3 mL浓缩模拟小肠液泵入立式模拟消化器中,通过搅拌器旋转提供小肠液与饲料样品的混合动力,进行小肠的模拟消化;
5)消化产物的去蛋白预处理
量取5 mL色谱级甲醇于固相萃取仪上活化C18色谱柱,用10 mL超纯水清洗C18色谱柱;将步骤4)中消化液和消化残渣无损失地转移到50 mL容量瓶中,用去离子水准确定容至刻度,摇匀;取20 mL溶液10000转离心10分钟后,取上清并通过0.22 μm针头滤器过滤;取9.2 mL滤液加入10.8 mL的浓度为0.34 mol/L的高氯酸溶液,混合均匀,10000转离心10分钟后,取上清通过C18色谱柱,再用20 mL去离子水清洗,将滤液用去离子水定容到50 mL,制备去蛋白消化液待测;
6)磷标准贮备液和显色液制备
磷标准贮备液的制备:将上述的仿生消化测定试剂盒中的标准品溶解于900 mL去离子水中,加入3 mL硝酸,定容至1000 mL制成50 μg/mL磷标准贮备液;
显色液的制备:将上述的仿生消化测定试剂盒中的显色剂中的偏钒酸铵溶解于200 mL沸水,冷却后加入250 mL硝酸,再将钼酸铵溶解于沸水中,冷却后把溶液混合,定容至1000mL制成显色液;
7)磷标准曲线的制作
分别取步骤6)制备的磷标准贮备液0.0, 1.0, 2.0, 4.0, 8.0, 16.0 mL置于50mL容量瓶中制成浓度分别为0.0, 1.0, 2.0, 4.0, 8.0, 16.0 μg/mL的磷标准液,分别加入步骤6)制备的显色剂10 mL,用水定容至刻度,摇匀,室温下放置10分钟以上,以0.0 ml溶液作为参比溶液,用1cm比色皿在波长400 nm处读取吸光值;以吸光值为横坐标,磷含量为纵坐标,绘制标准曲线;
8)消化产物中游离磷含量的测定
取步骤5)处理好的去蛋白消化液4 mL,加入步骤6)制备的显色剂1 mL,摇匀,室温下放置15分钟以上,用1cm比色皿在波长400 nm处读取吸光值,带入步骤7)的标准曲线,获得去蛋白消化液的磷含量;
9)计算饲料有效磷
饲料有效磷AP
AP
式中:AP
如上所述地,所述步骤3)胃模拟消化中:混合频率,180转/分钟;胃模拟消化时间,1小时。
如上所述地,所述步骤4)小肠模拟消化中:混合频率,180转/分钟;小肠模拟消化时间,5小时。
如上所述地,所述肉鸡饲料为肉鸡饲料的原料或肉鸡饲料的配合饲料。
与现有技术相比,本发明具有如下优点:
1、在胃消化中,本发明模拟胃液的蛋白酶活性、pH、消化时间与肉鸡肌胃胃液中胃蛋白酶活性、pH和消化时间保持一致。与透析袋法仅用盐酸调节胃液pH相比,采用乙酸钠缓冲液配制模拟胃液,能够保证消化过程中pH稳定地维持在生理范围。文献中报道的柠檬酸缓冲液可以完全溶解磷酸氢钙,此时磷酸氢钙的消化率为100%,与畜禽体内磷酸氢钙的消化率仅为70~80%相比,严重高估了磷酸氢钙中有效磷含量。而本发明采用乙酸钠缓冲液体系配制模拟胃液,磷酸氢钙溶解度在70~80%左右,与体内磷酸氢钙消化过程接近,而且乙酸钠缓冲液的缓冲作用有效地解决了肉鸡饲料中石粉等原料吸附氢质子而导致胃液pH升高的问题,从而提高了饲料中蛋白质和植酸磷水解效率。因此,本发明不仅能够准确测定动植物性饲料原料中的有效磷,也适用于含磷矿物质、以及添加有含磷矿物质、石粉等配合饲料中有效磷的测定。
2、在小肠消化中,本发明的浓缩模拟小肠液使用肉鸡内源性消化酶进行制备,浓缩模拟小肠液的淀粉酶、胰蛋白酶、糜蛋白酶、pH与肉鸡空肠液中对应酶活性、pH保持一致,本发明与透析袋法仅模拟饲料蛋白质消化释放无机磷不同,还模拟淀粉消化过程以释放碳水化合物结合的无机磷,消化时间参考肉鸡体内消化时间设定。由于消化酶的酶学特性和酶的活性存在种属差异,采用肉鸡内源性消化酶与其他体外消化方法所使用的商品酶相比,本发明的浓缩模拟小肠液的酶学特性和酶活与体内完全一致。因此小肠模拟消化过程中磷的释放率更加接近肉鸡体内情况。
3、在体外模拟消化过程中,温度、混合频率、浓缩模拟小肠液的泵入、胃和小肠消化时间、全部通过在单胃动物仿生消化系统设置相应的参数进行自动化控制,从而实现全自动模拟肉鸡体内消化测定饲料中有效磷含量。
4、消化产物中无机磷全部被收集,不需要进一步分离消化产物无机磷与有机磷,通过直接定量释放的无机磷来计算饲料中有效磷含量。与通常采用的“透析分离消化产物中的无机磷,再测定透析液中总磷”的技术路径相比,本发明避免了透析方法无法分离无机磷与有机磷的重大问题,也解决了由于透析时长、透析袋内外两侧磷离子平衡等造成消化产物无机磷不能完全被收集的关键问题。本发明检测了所有释放的无机磷,简化了消化产物分离和消解步骤,减少了定量误差,提高了测试的准确性。
5、消化产物中无机磷通过与偏钒酸铵、钼酸铵结合形成黄色的磷钒钼酸而被直接测定,且不与有机磷反应。但是消化产物中蛋白质和小肽与偏钒酸铵、钼酸铵会形成絮状不溶物使吸光值偏高,导致消化产物中无机磷含量测值虚高。传统方法采用硝酸-高氯酸消解水解产物中的蛋白去除蛋白的干扰,但也导致消化产物中有机磷同时被强酸氧化形成无机磷,因而测定的为消化产物中的总磷,而不是无机磷。本发明通过高氯酸沉淀蛋白、C18色谱柱吸附小肽两个步骤去除消化产物中可溶性蛋白质和小肽,而消化产物中溶解的有机磷和无机磷不会被沉淀和吸附,不仅克服了无机磷定量过程中蛋白质和小肽的干扰,也解决了有机磷氧化分解成无机磷,实现对消化产物中释放的无机磷准确测定。
6、本发明以消化酶的比活性组成、缓冲液及电解质的离子浓度定义模拟胃液、浓缩模拟小肠液和浓缩模拟大肠液,确保了不同批次配制的模拟消化液的消化能力高度可重复,可以形成标准化的模拟消化液试剂盒产品,有利于实现用户间测定数据的比对。
7、由于消化酶中本身也还有一定磷元素,无论生物学法还是体外消化法测定有效磷含量时,均需要设定无磷饲料或者空白对照组测定内源无机磷,对有效磷进行校正。本发明得益于试剂盒的标准化,试剂中内源无机磷含量稳定,为1331 μg,无需设置空白对照组测定试剂内源无机磷,可直接通过1331μg进行校正,进一步简化了饲料中有效磷测定步骤和计算过程。
本发明的有益效果在于:
本发明提供的一种肉鸡饲料中有效磷的仿生消化测定试剂盒及方法。该试剂盒采用肉鸡内源性消化酶制备模拟消化液,根据肉鸡体内消化液组成参数配制模拟消化液,在消化酶的酶学特性和活性、消化时间、消化液pH与肉鸡体内逼近,保证了消化液的消化能力与肉鸡体内胃液和小肠液一致,从而实现准确模拟体内有机磷的释放。同时,胃和小肠阶段采用了乙酸钠缓冲液体系模拟磷酸氢钙等含磷矿物质溶解和消化,维持仿生消化过程中pH的稳定性,解决了肉鸡饲料中石粉等原料中和pH,导致植酸酶活性降低、磷酸氢钙溶解性降低,因此,该方法不仅适用于肉鸡动植物性饲料原料中有效磷的测定,也可准确测定含磷矿物质和配合饲料中的有效磷。通过高氯酸沉淀蛋白和C18色谱柱吸附小肽两个步骤解决了消化产物蛋白质对无机磷测定的干扰,直接定量消化过程中释放的所有无机磷,无需进行无机磷和有机磷的分离,减少了操作步骤,还杜绝了有机磷的干扰。本发明提供的方法解决了模拟磷酸氢钙等体内消化过程、饲料原料对消化液pH干扰、消化产物中有机磷和蛋白质对释放的无机磷测定干扰等问题,去除了无机磷与植酸磷的分离步骤,克服了体外消化测定饲料中有效磷低于生物学法测定的问题,实现了方法的标准化、自动化。同时,传统生物学法测定饲料中有效磷的过程需要8天,而本发明提供的方法测定饲料中有效磷的过程仅需要8个小时。因此本发明提供的方法具有节资降耗、重复性高、准确、快速的优点。
附图说明
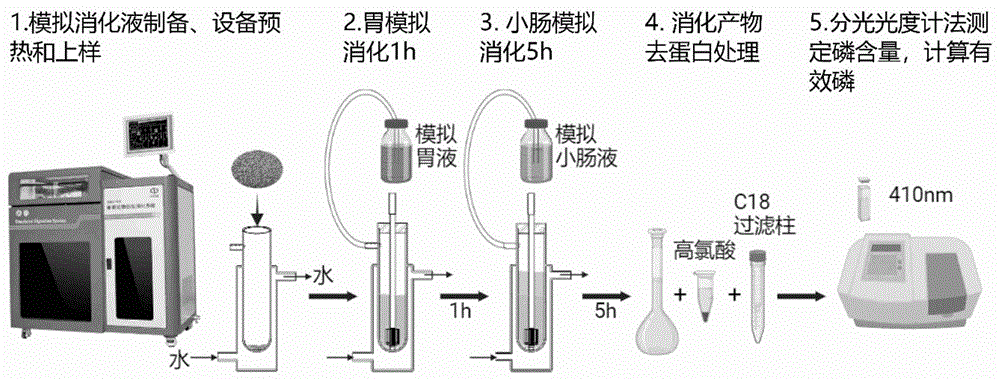
图1为本发明提供的肉鸡饲料有效磷的仿生消化测定方法的流程图。
图2为本发明提供的肉鸡饲料有效磷的仿生消化测定方法和现有生物学法测定肉鸡饲料有效磷的比较图。
图3 为肉鸡饲料磷消化率对体外仿生测定磷的回归模型。
具体实施方式
下面将对本发明的实施例进行详细、完善的描述,以使本发明的优点和特征能更易于被本领域技术人员理解,从而对本发明的保护范围做出更为清楚明确的界定。
本发明中“有效磷”指饲料中可被畜禽吸收利用的磷的总称,包括溶解的无机磷以及有机磷水解释放的无机磷的总量。
本发明中“饲料”是指来源于动物、植物、或者矿物质,用于加工制作配合饲料但不属于饲料添加剂的饲用物质。
本发明中“配合饲料”是指根据动物营养需要,按科学配方把多种不同来源的饲料,如玉米、豆粕等动植物性原料,还有磷酸氢钙、石粉等原料以及饲料添加剂依一定比例均匀混合生产的饲料。
现有的饲料中有效磷体外消化测定方法中仅模拟了蛋白质消化,没有模拟淀粉和矿物质的溶解和消化过程,忽略了消化过程中饲料原料对消化液pH的干扰,导致饲料中磷酸氢钙溶解率、蛋白酶、植酸酶水解效率降低,无法应用于配合饲料中有效磷的测定;透析袋法无法有效地分离植酸磷和水解释放的无机磷、透析液中蛋白质和小肽干扰无机磷的测定;以上导致了饲料中有效磷体外消化测定方法无法准确测定饲料原料和配合饲料中有效磷,不能在饲料生产和肉鸡养殖中使用。本发明通过建立胃、小肠两种消化缓冲体系缓冲饲料原料对pH干扰,利用蛋白酶和淀粉酶配伍提高水解效率,建立消化产物去蛋白的前处理技术直接测定释放的无机磷,从而与饲料中磷在肉鸡体内消化率保持一致,实现对饲料原料和配合饲料中有效磷的准确测定。
仪器与设备
植物样品粉碎机或研钵;试验筛:孔径0.3 mm(60目);分析天平:分度值0.0001 g;pH计:分度值0.01;单胃动物仿生消化系统(型号:SDS-3,湖南中本智能科技发展有限公司);分光光度计;干燥器:无水氯化钙或变色硅胶为干燥剂;漩涡振荡器;可调温电炉;SHB-3循环水式多用真空泵;固相萃取仪。
试剂与材料
除特别注明者外,所有试剂均为分析纯。
实验室用水符合GB/T 6682-2008中三级水的规格。
肉鸡饲料中有效磷的仿生消化测定试剂盒:
缓冲液I粉末:无水乙酸钠4.101 g;氯化钾2.01 g;
消化酶I:胃蛋白酶114400 U;
缓冲液II粉末:无水乙酸钠4.101 g;
消化酶II:淀粉酶67860 U;胰蛋白酶12870 U;糜蛋白酶6450U;
标准品:磷酸二氢钾0.2195 g;
显色剂:偏钒酸铵1.25 g;钼酸铵25 g;
C18色谱柱10个;
0.22 μm针头滤器10个。
其他试剂:盐酸(HCl)、氢氧化钠(NaOH),碳酸氢钠(NaHCO
胃缓冲液:将缓冲液I粉末溶解于450 mL去离子水中,用6 mol/L的盐酸在41℃下调节溶液的pH至4.35,冷却后定容至500 mL。
模拟胃液:将消化酶I溶解于41℃下pH 4.35的200 mL胃缓冲液中,缓慢搅拌30分钟制成模拟胃液。勿在加热板上加热,或配制时过热。临用前配制。
小肠缓冲液的制备:将缓冲液II粉末溶解于450 mL去离子水中,用氢氧化钠溶液调节pH至12.2,用去离子水定容至500 mL。
浓缩模拟小肠液:将消化酶II溶解于30 mL去离子水中,快速涡旋溶解2分钟,临用前配制;
磷标准贮备液:将标准品溶解于900 mL去离子水中,加入3 mL硝酸,定容至1000mL制成50 μg/mL磷标准液;
显色液:将偏钒酸铵溶解于200 mL沸水,冷却后加入250 mL硝酸,再将钼酸铵溶解于沸水中,冷却后把溶液混合,定容至1000 mL,避光保存,若生成沉淀,则不能继续使用。
立式模拟消化器购买自湖南中本智能科技发展有限公司,产品型号:DT-V。
单胃动物仿生消化系统购买自湖南中本智能科技发展有限公司,产品型号:SDS-3。
消化酶I中的胃蛋白酶购买自Sigma,商品编号为P7000。
消化酶II的制备方法为:
1)从若干鸡的小肠中采集空肠食糜并将其混合均匀,然后将混合后的肠道食糜进行离心,条件为4 ℃、10000 g下离心10分钟,收集上清液1;
该上清液1为含有淀粉酶、胰蛋白酶和糜蛋白酶的小肠液;
2)对上清液1进行蒸发浓缩,得浓缩肠液;将浓缩肠液进行离心,条件为在4 ℃、10000 g下离心10分钟,收集上清液2;
步骤2)中,所述蒸发浓缩在旋转蒸发仪上进行,蒸发浓缩的条件为:在蒸馏瓶水浴温度59 ℃、旋转速度80转/分钟、真空度为0的条件下,蒸发15分钟;
3)将上清液2转移到置于冰水浴的容器中,并向其中加入甘露醇,每100 mL上清液2中加入1.5 g,搅拌溶解后,按照100 mL所述的上清液2再加入350 mL的95%乙醇溶液,搅拌均匀后在-10 ℃静置12 h;然后进行离心,条件为:在4 ℃、10000 g下离心10分钟,收集沉淀;
4)向沉淀中加入去离子水,并进行搅拌和超声溶解,然后进行离心,条件为:4 ℃、10000 g下离心10分钟,收集上清液3;将所述上清液3进行冷冻干燥,即得所述鸡小肠消化酶粉剂。
根据测算肉鸡小肠消化酶中淀粉酶的活性为280.4U/mL,胰蛋白酶的活性为53.2U/mL,糜蛋白酶的活性为26.7U/mL,由于试剂盒中可测试10个样品,并且由于体外环境会影响消化酶活性,因此增加大约5%的消化酶含量以抵消上机操作过程中消化酶配制的浓缩模拟小肠液体积损失。
实施例1肉鸡饲料中有效磷测定试剂盒中内源磷的含量测定
由肉鸡空肠末端小肠消化酶制备高水溶性小肠消化酶,用来提供有效磷测定试剂盒中的模拟小肠液的消化酶II。由于肉鸡消化液中存在磷酸盐,在制备高水溶性小肠消化酶粉剂中也有磷酸盐,因此需要确定肉鸡饲料中有效磷测定试剂盒中内源磷含量,以减少其对饲料原料和配合饲料中有效磷测定的干扰。
1 材料与方法
1.1试验设计
采用双因素完全随机设计,进行5个批次试验,每批次随机选择2台单胃动物仿生消化系统进行实验。
1.2仿生消化方法测定试剂盒内源磷的含量的过程,如图1所示。
1.2.1 模拟消化液及缓冲液:
胃缓冲液:将缓冲液I粉末溶解于450 mL去离子水中,用6 mol/L的盐酸在41℃下调节溶液的pH至4.35,冷却后定容至500 mL。
模拟胃液:将消化酶I溶解于41℃下pH 4.35的200 mL胃缓冲液中,缓慢搅拌30分钟制成模拟胃液。勿在加热板上加热,或配制时过热。临用前配制。
小肠缓冲液的制备:将缓冲液II粉末溶解于450 mL去离子水中,用氢氧化钠溶液调节pH至12.2,用去离子水定容至500 mL。
模拟小肠液:将消化酶II溶解于30 mL去离子水中,快速涡旋溶解2分钟,现配现用。
1.2.2 预热、上样
将制备的模拟胃液、模拟小肠液放入该单胃动物仿生消化系统的消化液试剂瓶中;将制备的小肠缓冲液和去离子水放入该单胃动物仿生消化系统的缓冲液控温室;在该单胃动物仿生消化系统,41℃预热时间为60分钟后,将配套搅拌装置与玻璃模拟消化器连接,并固定到该单胃动物仿生消化系统的固定架的夹具上;每个样品测定5重复,每个重复使用1根模拟消化器。
1.2.3胃模拟消化:
将装置好的立式固定架置于该单胃动物仿生消化系统中,按照立式模拟消化器外管下端进水,上端出水的原则,接好管路,再通过消化液加液管将每管根立式模拟消化器内管与相连;15 mL胃模拟消化液泵入各立式模拟消化器,通过搅拌器旋转提供胃液与饲料样品的混合动力,进行胃的模拟消化。
1.2.4 小肠模拟消化:
将5 mL小肠缓冲液泵入立式模拟消化器中,以使立式模拟消化器溶液的pH由胃的消化环境自动切换为小肠的消化环境,再将3 mL浓缩模拟小肠液泵入立式模拟消化器中,通过搅拌器旋转提供小肠液与饲料样品的混合动力,进行小肠的模拟消化。
1.2.5消化产物的处理
量取5 mL色谱级甲醇于固相萃取仪上活化C18色谱柱,用10 mL超纯水清洗C18色谱柱;将步骤4)中消化液和消化残渣无损失地转移到50 mL容量瓶中,用去离子水准确定容至刻度,摇匀;取20 mL溶液10000转离心10分钟后,取上清并通过0.22 μm针头滤器过滤;取9.2 mL滤液加入10.8 mL的高氯酸溶液,混合均匀,10000转离心10分钟后,取上清通过C18色谱柱,再用20 mL去离子水清洗,将滤液用去离子水定容到50 mL,待测。
1.2.6 磷标准贮备液和显色液制备
磷标准贮备液的制备:将仿生消化测定试剂盒中的标准品溶解于900 mL去离子水中,加入3 mL硝酸,定容至1000 mL制成50 μg/mL磷标准液;
显色液的制备:将仿生消化测定试剂盒中的显色剂中的偏钒酸铵溶解于200 mL沸水,冷却后加入250 mL硝酸,再将钼酸铵溶解于沸水中,冷却后把溶液混合,定容至1000 mL制成显色液。
1.2.7 磷标准曲线的制作
分别取磷标准贮备液0.0, 1.0, 2.0, 4.0, 8.0, 16.0 mL置于50mL容量瓶中制成浓度分别为0.0, 1.0, 2.0, 4.0, 8.0, 16.0 μg/mL的磷标准液,分别加入显色剂10mL,用水定容至刻度,摇匀,室温下放置10分钟以上,以0.0 ml溶液作为参比溶液,用1 cm比色皿在波长400 nm处读取吸光值;以吸光值为横坐标,磷含量(μg/mL)为纵坐标,绘制标准曲线,获得标准曲线的回归系数a和常数b。
1.2.8 消化产物中游离磷含量的测定
取消化液滤液4 mL,加入显色剂1 mL,摇匀,室温下放置15分钟以上,用1 cm比色皿在波长400 nm处读取吸光值。
1.3 数据计算和统计分析
P
式中:
P
OD为测定空白消化液的吸光度;
a为磷标准曲线的回归系数;
b为磷标准曲线的常数;
采用SAS 9.4的MEANS模块进行基本统计量分析。用GLM模块对批次、机器的效应进行差异显著性检验。当
2 测试结果
测试结果如表1所示,对内源磷的方差分析结果如表2所示。
表1 有效磷测试试剂盒内源磷测定结果(单位:μg)
表2 有效磷测试试剂盒内源磷方差分析结果(单位:μg)
如表1和表2所示,通过仿生消化法对肉鸡饲料中有效磷测定试剂盒中内源磷的释放率进行分析,结果表明内源磷的释放量稳定,不同批次、不同机器间测定的试剂盒内源磷的量均无显著差异,平均值为1331μg,可作为试剂盒中内源磷含量直接作为背景进行扣除。
实施例2通过仿生消化法估测肉鸡饲料中有效磷的含量
1 材料与方法
1.1试验设计和饲料的配制
采用2×2×3两因素完全随机设计,根据14~21日龄、22~30日龄的肉鸡营养需要,配制玉米-豆粕型、玉米-碎米-杂粕型2个类型饲料,以植酸酶与磷酸氢钙配伍设2个处理水平,分别为不添加植酸酶时添加推荐水平的磷酸氢钙(饲料1、3、5、7)、添加150 mg/kg植酸酶时减少约8 g/kg磷酸氢钙用量(饲料2、4、6、8),结果如表3所示。
表3试验饲料组成及化学成分含量(风干基础,%)
1.2试验动物及管理
384只0日龄沃德168肉鸡雏鸡,随机分别8个处理组,每个处理组设6个重复,每个重复8只鸡。0~14日龄,所有鸡只饲喂相同饲料;15~21日龄,处理组1~4分别饲喂试验饲料1~4,处理组5~6和7~8在15~21日龄分别饲喂饲料1和饲料3;22~30日龄,处理组5~8分别饲喂饲料5~8。
1.3生物学测定磷的表观消化率
分别在21、30日龄采用屠宰法测定处理1~4和处理5~8磷的标准回肠消化率。肉鸡标准回肠磷消化率的测定参考Babatunde et al. (2020)的方法进行测定。各试验单元肉鸡经二氧化碳(处置浓度≥45%)致死后,打开腹腔,将卵黄囊憩室至距离回盲结2cm处的肠段取出,将后1/2长段的食糜用去离子水冲洗至培养皿中,于-20℃保存。根据《饲料中总磷的测定 分光光度法》(GB/T 6437-2018)测定饲料和回肠食糜中总磷的含量;根据Myers WDet al. (2004)的方法测定饲料和回肠食糜中TiO
1.4仿生消化方法测定磷的消化率,过程如图1所示。
1.4.1 模拟消化液及缓冲液:
胃缓冲液:将缓冲液I粉末溶解于450 mL去离子水中,用6 mol/L的盐酸在41℃下调节溶液的pH至4.35,冷却后定容至500 mL。
模拟胃液:将消化酶I溶解于41℃下pH 4.35的200 mL胃缓冲液中,缓慢搅拌30分钟制成模拟胃液。勿在加热板上加热,或配制时过热。临用前配制。
小肠缓冲液的制备:将缓冲液II粉末溶解于450 mL去离子水中,用氢氧化钠溶液调节pH至12.2,用去离子水定容至500 mL。
模拟小肠液:将消化酶II溶解于30 mL去离子水中,快速涡旋溶解2分钟,现配现用。
1.4.2 预热、上样
将制备的模拟胃液、模拟小肠液放入该单胃动物仿生消化系统的消化液试剂瓶中;将制备的小肠缓冲液和去离子水放入该单胃动物仿生消化系统的缓冲液控温室;在该单胃动物仿生消化系统,41℃预热时间为60分钟后,将准确称取0.5 g粉碎后过60目标准筛的鸡饲料样品置于该单胃动物仿生消化系统的玻璃模拟消化器中;将配套搅拌装置与玻璃模拟消化器连接,并固定到该单胃动物仿生消化系统的固定架的夹具上;每个样品测定5重复,每个重复使用1根模拟消化器。
1.4.3胃模拟消化:
将装置好的立式固定架置于该单胃动物仿生消化系统中,按照立式模拟消化器外管下端进水,上端出水的原则,接好管路,再通过消化液加液管将每管根立式模拟消化器内管与相连;15 mL胃模拟消化液泵入各立式模拟消化器,通过搅拌器旋转提供胃液与饲料样品的混合动力,进行胃的模拟消化。
1.4.4 小肠模拟消化:
将5 mL小肠缓冲液泵入立式模拟消化器中,以使立式模拟消化器溶液的pH由胃的消化环境自动切换为小肠的消化环境,再将3 mL浓缩模拟小肠液泵入立式模拟消化器中,通过搅拌器旋转提供小肠液与饲料样品的混合动力,进行小肠的模拟消化。
1.4.5消化产物的处理
量取5 mL色谱级甲醇于固相萃取仪上活化C18色谱柱,用10 mL超纯水清洗C18色谱柱;将步骤4)中消化液和消化残渣无损失地转移到50 mL容量瓶中,用去离子水准确定容至刻度,摇匀;取20 mL溶液10000转离心10分钟后,取上清并通过0.22 μm针头滤器过滤;取9.2 mL滤液加入10.8 mL的高氯酸溶液,混合均匀,10000转离心10分钟后,取上清通过C18色谱柱,再用20 mL去离子水清洗,将滤液用去离子水定容到50 mL,待测。
1.4.6 磷标准贮备液和显色液制备
磷标准贮备液的制备:将仿生消化测定试剂盒中的标准品溶解于900 mL去离子水中,加入3 mL硝酸,定容至1000 mL制成50 μg/mL磷标准液;
显色液的制备:将仿生消化测定试剂盒中的显色剂中的偏钒酸铵溶解于200 mL沸水,冷却后加入250 mL硝酸,再将钼酸铵溶解于沸水中,冷却后把溶液混合,定容至1000mL制成显色液。
1.4.7 磷标准曲线的制作
分别取磷标准贮备液0.0, 1.0, 2.0, 4.0, 8.0, 16.0 mL置于50mL容量瓶中制成浓度分别为0.0, 1.0, 2.0, 4.0, 8.0, 16.0 μg/mL的磷标准液,分别加入显色剂10mL,用水定容至刻度,摇匀,室温下放置10分钟以上,以0.0 ml溶液作为参比溶液,用1 cm比色皿在波长400 nm处读取吸光值;以吸光值为横坐标,磷含量(μg/mL)为纵坐标,绘制标准曲线。
1.4.8 消化产物中游离磷含量的测定
取消化液滤液4 mL,加入显色剂1 mL,摇匀,室温下放置15分钟以上,用1 cm比色皿在波长400 nm处读取吸光值,带入标准曲线计算去蛋白消化液的磷含量。
1.5 数据计算和统计分析
1.5.1 生物学法测定的饲料有效磷(AP
AP
式中:
AP
P
P
T
T
1.5.2 体外法测定的饲料有效磷(AP
AP
式中:
AP
P为去蛋白消化液的磷含量;
P
m为饲料样品重量,g;
DM为饲料样品的干物质含量。
采用SAS 9.4的MEANS模块进行基本统计量分析。用PROC TTEST模块对AP
2 测试结果
如图2所示,对配对T检验结果表明,在8个饲料有效磷体外法测值与生物学法测值无显著差异(
从上述实施例可以看出,本发明提供的肉鸡饲料中有效磷的仿生测定试剂盒及测定方法在充分解析肉鸡体内消化参数的基础上,利用蛋白酶和淀粉酶配伍在体外模拟消化过程、胃-小肠阶段缓冲体系,使得消化液pH、酶活、消化水解效率与肉鸡体内一致、在整个消化过程中的稳定;解决了消化产物中蛋白质和有机磷对释放的无机磷测定的干扰问题,实现了消化产物中无机磷和植酸磷的准确分离;基于商业化的全自动单胃动物仿生消化系统实现测定方法的标准化、自动化,从而解决基于透析袋的体外消化方法存在的测定的结果偏低、难以标准化、自动化的技术缺陷,并且将检测时间从8天缩减到8个小时,大大节省了检测时间。
以上所述实施例仅表达了本发明的实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 一种振膜的制备方法和发声装置
- 振膜的制备方法以及发声装置
- 一种硅胶振膜及其发声装置
- 声学连接件及其制备方法和修复方法、发声装置
- 音圈辅助支撑部制备方法、音圈辅助支撑部及发声装置单体
- 用于发声装置的振膜、振膜的制备方法以及发声装置
- 用于发声装置的振膜、振膜的制备方法以及发声装置
