一种快速检测鲤春病毒血症病毒的方法
文献发布时间:2023-06-19 11:42:32
技术领域
本发明属于病毒检测领域,具体涉及一种快速检测鲤春病毒血症病毒的方法。
背景技术
鲤春病毒血症病毒(Spring viremia of carp virus,SVCV)属水泡病毒属(Vesiculovirus),是一种弹状病毒,主要流行于欧洲、中东和俄罗斯,近几年蔓延至美洲和亚洲。SVCV宿主范围非常广泛,四大淡水鱼类均能被感染,其中最易感的为鲤科鱼类,尤其仔鱼,一旦感染死亡率可达70%。它可以引起鱼类大规模暴发鲤春病毒血症(SVC),是世界动物卫生组织(OIE)必须通报的动物疾病,也是《中华人民共和国进境动物一、二类传染病、寄生虫病名录》中的一类动物疫病,是淡水鱼养殖场重点防控疫病。为预防该病暴发,在目前无疫苗使用的情况下,因此需要精准而有简便的检测技术对鲤春病毒血症病毒进行定期检测。目前的常用的检测手段为实时荧光PCR技术,但其检测过程和检测周期长,需要复杂的检测设备,检测成本高,很难全面推广应用。
近几年新发展的重组酶聚合酶扩增技术(recombinase polymeraseamplification,RPA)是一种等温核酸扩增技术。该技术的显著特点是在接近室温(37-42℃)的条件下,10-40min就能完成扩增反应,具有操作简单、快速、准确、灵敏度高、特异性强、检测时间短、结果读取多元化、不需要专业的操作人员操作、不需要昂贵的精密仪器等特点。只需在室外使用简单的加温设备即可完成反应,可以真正实现使用便携式的方法快速进行核酸检测,是目前可用于POCT最方便快捷的核酸检测方法之一。
但是RPA技术受蛋白质干扰大,而且分离提取SVCV的RNA时造成该RNA不同程度的产量和质量的损失,在待测样本中SVCV的含量较低时,由于分离提取不当,使大部分的SVCV核酸不能通过聚合酶链式反应扩增,检出限高。
发明内容
为了克服现有技术的不足,本发明的目的在于提供一种快速检测鲤春病毒血症病毒的方法,能提高SVCV的核酸产量,降低裂解物的干扰,降低检出限,操作简便,可现场进行快速检测。
本发明的目的采用如下技术方案实现:
一种快速检测鲤春病毒血症病毒的方法,包括以下步骤:
S1,取待测样本,加入释放剂,置于焦点区域并传输1-80MHz的聚焦声能装置中,3-10min后,得到核酸液;
S2,向核酸液中加入逆转录酶浓缩缓冲液、dNTP、随机引物、RNA酶抑制剂、AMV逆转录酶,40℃-42℃反应20-40min,合成cDNA模板;
S3,通过cDNA模板建立RT-RPA反应体系,得到扩增产物;
S4,将扩增产物进行稀释5-10倍,并通过胶体金试纸条进行检测。
进一步地,步骤S1中,温度为40-60℃,释放剂的pH值为6-9。
进一步地,所述释放剂包括洗涤剂5-30%、缓冲液30-120mM、离液剂5-20M、螯合剂20-100mM;
所述缓冲液为HEPES、TRIS、MOPS、PIPES、SSC、MES和磷酸盐的一种或多种的组合物;
所述离液剂为硫氰酸胍盐、异硫氰酸胍盐、盐酸胍盐、甲酰胺、高氯酸锂、三氯乙酸钠、尿素的一种或两种以上的组合物;
所述螯合剂为EDTA、DTPA、EDDS、NTA和膦酸盐的一种或两种以上的组合物;
所述洗涤剂包含为N-月桂酰基肌氨酸、十二烷基硫酸钠、Triton-X-100,N-辛基--D-吡喃葡萄糖苷、CHAPS、N-辛基--D-吡喃麦芽糖苷,N-辛基--D-硫代吡喃葡萄糖苷和Tween20的一种或两种以上的组合物。
进一步地,所述释放剂还包括蛋白水解酶0.1-2mg/mL和金属盐1-20mM,所述金属盐为氯化钾或氯化钠。
进一步地,所述释放剂包括以下组分:N-月桂酰基肌氨酸1-10%(v/v),Tween205-20%(v/v),TRIS 30-120mM,EDTA 30-100mM,蛋白水解酶0.1-2mg/mL、氯化钠5-15mM、硫氰酸胍盐2-10M、尿素3-10M。
进一步地,所述聚焦声能装置为便携式装置,所述聚焦声能装置单次可处理50-100μL溶液;所述聚焦声能的峰值强度功率为100-300W,周期为100-300。
进一步地,步骤S3中,RT-RPA反应体系包括噬菌体重组酶、DNA聚合酶、单链DNA结合蛋白、引物和探针。
进一步地,所述引物序列如下:
SVCV-RPA-F1:5'-biotin-GTCTTGTCGAATGAAATTCTGTAATAAAGATGG-3',SVCV-RPA-R1:5'-biotin-CTTTTAGTCCCCTCACACAAAGTATATTCTACC-3'。
进一步地,所述探针序列如下:
5'-FITC-GGTAGAAAAAACAGCTGGAACATTGACGAATA-FAM-dT-THF-BHQ1-dT-ATGCAAATATACCTGAA-C3-3';
其中,FAM-dT:携带荧光素的胸腺嘧啶核苷酸;THF:四氢呋喃残基;BHQ1-dT:携带淬灭基团的胸腺嘧啶核苷酸;C3:阻断物。
进一步地,步骤S4中,所述胶体金试纸条包括PVC背板、样品垫、金标垫、硝酸纤维素膜、吸水纸,样品垫、金标垫、吸水纸依次粘贴到PVC背板的相应位置,所述硝酸纤维素膜上喷涂有检测线和质控线,所述金标垫上喷涂金标抗FITC抗体,所述检测线喷涂avidin蛋白,所述质控线喷涂抗兔抗体。
相比现有技术,本发明的有益效果在于:
本发明的检测方法简单,产业现场能够完成整个过程,无需大型设备,无需特殊温度条件,全部为试管和试纸条反应,用时不超过40分钟。通过释放剂与聚焦声能结合,提高分离提取效率,降低检出限,释放剂能与干扰元素形成更稳定的化合物而释放SVCV核酸,在聚焦声能的协同作用下,能明显提高裂解液中SVCV核酸的产量,且核酸的质量高,大部分可用于反应扩增。利用重组酶聚合酶扩增技术(RPA),该技术的显著特点是在接近室温(37-42℃)的条件下,10-40min就能完成扩增反应,具有操作简单、快速、准确、灵敏度高、特异性强、检测时间短、结果读取多元化、不需要专业的操作人员操作、不需要昂贵的精密仪器等特点;通过RPA技术与胶体金试纸条配合,只需在室外使用简单的加温设备即可完成反应,胶体金试纸条法约需要10min即可判定结果,可以真正实现使用便携式的方法快速进行产业现场核酸检测。
附图说明
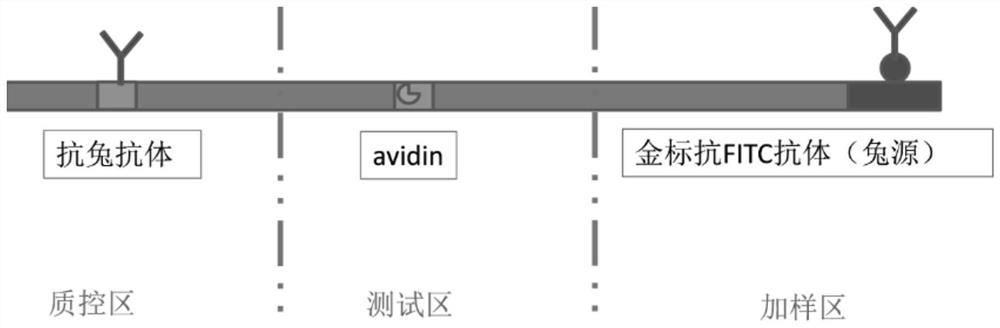
图1是本发明的胶体金试纸条的结构示意图。
图2是本发明的胶体金试纸条的检测原理图。
图3是本发明的胶体金试纸条的反应结果图。
具体实施方式
下面,结合具体实施方式,对本发明做进一步描述,需要说明的是,在不相冲突的前提下,以下描述的各实施例之间或各技术特征之间可以任意组合形成新的实施例。
一种快速检测鲤春病毒血症病毒的方法,包括以下步骤:
S1,取待测样本,加入释放剂,置于焦点区域并传输1-80MHz的聚焦声能装置中,3-10min后,得到核酸液;
S2,向核酸液中加入逆转录酶浓缩缓冲液、dNTP、随机引物、RNA酶抑制剂、AMV逆转录酶,40℃-42℃反应20-40min,合成cDNA模板;
S3,通过cDNA模板建立RT-RPA反应体系,得到扩增产物;
S4,将扩增产物进行稀释5-10倍,并通过胶体金试纸条进行检测。对扩增产物进行适当的稀释,有利于减少蛋白的干扰。
进一步地,步骤S1中,温度为40-60℃,释放剂的pH值为6-9。
进一步地,所述释放剂包括洗涤剂5-30%、缓冲液30-120mM、离液剂5-20M、螯合剂20-100mM;离液剂用于变性裂解细胞,溶解蛋白质,释放核酸;加入离液剂的缺点是核酸在较长的保持时间内沉淀,而且沉淀的核酸可能不可逆地粘附在包含样品的容器的壁上,这显著地降低了核酸产量。在再悬浮样品中掺入螯合剂显著地减少了沉淀物的形成,并且进一步地,防止了沉淀物粘附到包含再悬浮样品的容器壁上,所述再悬浮样品包含离液剂;洗涤剂与样品中所含细胞的裂解,并与释放的核酸形成复合物;缓冲液能为核酸提供保护的环境;
所述缓冲液为HEPES、TRIS、MOPS、PIPES、SSC、MES和磷酸盐的一种或多种的组合物;
所述离液剂为硫氰酸胍盐、异硫氰酸胍盐、盐酸胍盐、甲酰胺、高氯酸锂、三氯乙酸钠、尿素的一种或多种的组合物;
所述螯合剂为EDTA、DTPA、EDDS、NTA和膦酸盐的一种或多种的组合物;
所述洗涤剂包含为N-月桂酰基肌氨酸、十二烷基硫酸钠、Triton-X-100,N-辛基--D-吡喃葡萄糖苷、CHAPS、N-辛基--D-吡喃麦芽糖苷,N-辛基--D-硫代吡喃葡萄糖苷和Tween20的一种或多种的组合物。
进一步地,所述释放剂还包括蛋白水解酶0.1-2mg/mL和金属盐1-20mM,所述金属盐为氯化钾或氯化钠。蛋白水解酶能一方面协助细胞的裂解从细胞中分离核酸,另一方面降解裂解物中的蛋白,使降解物与螯合剂结合形成温度的结合物,减少对后续检测的干扰;金属盐能促进核酸的分离。
进一步地,所述释放剂包括以下组分:N-月桂酰基肌氨酸1-10%(v/v),Tween205-20%(v/v),TRIS 30-120mM,EDTA 30-100mM,蛋白水解酶0.1-2mg/mL、氯化钠5-15mM、硫氰酸胍盐2-10M、尿素3-10M。
进一步地,所述聚焦声能装置为便携式装置,所述聚焦声能装置单次可处理50-100μL溶液;所述聚焦声能的峰值强度功率为100-300W,周期为100-300。
进一步地,步骤S3中,RT-RPA反应体系包括噬菌体重组酶、DNA聚合酶、单链DNA结合蛋白、引物和探针。
进一步地,所述引物序列如下:
SVCV-RPA-F1:5'-biotin-GTCTTGTCGAATGAAATTCTGTAATAAAGATGG-3',SVCV-RPA-R1:5'-biotin-CTTTTAGTCCCCTCACACAAAGTATATTCTACC-3'。
进一步地,所述探针序列如下:
5'-FITC-GGTAGAAAAAACAGCTGGAACATTGACGAATA-FAM-dT-THF-BHQ1-dT-ATGCAAATATACCTGAA-C3-3';
其中,FAM-dT:携带荧光素的胸腺嘧啶核苷酸;THF:四氢呋喃残基;BHQ1-dT:携带淬灭基团的胸腺嘧啶核苷酸;C3:阻断物。
进一步地,步骤S4中,所述胶体金试纸条包括PVC背板、样品垫、金标垫、硝酸纤维素膜、吸水纸,样品垫、金标垫、吸水纸依次粘贴到PVC背板的相应位置,所述硝酸纤维素膜上喷涂有检测线和质控线,所述金标垫上喷涂金标抗FITC抗体,所述检测线喷涂avidin蛋白,所述质控线喷涂抗兔抗体。
实施例1
一种快速检测鲤春病毒血症病毒的方法,包括以下步骤:
S1,抽提核酸;取100μL血液样品,加入释放剂,温度为40-60℃,释放剂的pH值为6-9,将溶液置于3-5cm的焦点区域并传输1-80MHz的聚焦声能,所述聚焦声能的峰值强度功率为100-300W,周期为100-300,聚焦声能处理5min后,得到核酸液;
释放剂中各组分的浓度为:N-月桂酰基肌氨酸3%(v/v),Tween20 8%(v/v),TRIS缓冲液50mM,EDTA 60mM,蛋白水解酶1.2mg/mL、氯化钠10mM、硫氰酸胍盐4M、尿素5M。
S2,制备核酸模板;取10μL RNA溶液,加5倍逆转录酶浓缩缓冲液4μL、dNTP 1μL、随机引物1μL、RNA酶抑制剂1μL、AMV逆转录酶2μL,使用不含RNA酶的去离子水补足20μL,42℃反应30min,合成cDNA模板,保存于-20℃备用。
S3,建立RT-RPA反应体系;以制备的cDNA为模板,做RT-RPA,优化反应条件,确定反应体系、各种组分的浓度和反应条件,推荐反应程序如下:
如表1所示,将
表1:50μL反应体系的RT-RPA反应的反应体系组成
所述引物序列如下:
SVCV-RPA-F1:5'-biotin-GTCTTGTCGAATGAAATTCTGTAATAAAGATGG-3',
SVCV-RPA-R1:5'-biotin-CTTTTAGTCCCCTCACACAAAGTATATTCTACC-3'。
所述探针序列如下:
5'-FITC-GGTAGAAAAAACAGCTGGAACATTGACGAATA-FAM-dT-THF-BHQ1-dT-ATGCAAATATACCTGAA-C3-3';
其中,FAM-dT:携带荧光素的胸腺嘧啶核苷酸;THF:四氢呋喃残基;BHQ1-dT:携带淬灭基团的胸腺嘧啶核苷酸;C3:阻断物。
S4,将扩增产物进行稀释,并通过胶体金试纸条进行检测;
胶体金试纸条的构成为:
(1)加样区,含有兔源金标抗FITC抗体;
(2)测试区,含有亲和素(avidin);
(3)质控区,含有抗兔抗体。
试纸条用来测试扩增产物中是否含有目的序列,首先在引物上标记生物素,经扩增的产物就被生物素标记,被标记的核酸能够被测试区的亲和素结合而捕获;在特异性探针上标记FITC,被标记的探针能够与加样区的兔源金标抗FITC抗体结合成免疫复合物。
如图1-2所示,将试纸条的加样区插入待测溶液中,探针携带FITC标记基团,可以与加样区的金标抗FITC抗体结合;扩增产物随着流动相到达测试区时,能够被亲和素捕获,如果FITC标记探针与兔源金标抗FITC抗体形成的免疫复合物中的探针序列与扩增引物序列匹配,将被滞留在测试区,探针携带的金标抗FITC抗体聚集而显色,在测试区形成肉眼可见的检测带(胶体金形成);如果免疫复合物中的探针序列与扩增引物序列不匹配,则含兔源的免疫复合物随着流动相移动到质控区与抗兔抗体结合,滞留在质控区,形成肉眼可见的质控条带。
如图3所示,试纸条的加样区插入待测溶液后5-15min,取出试纸条,观察结果,结果判断:
阳性:质控线和测试线均显色;
可疑:质控线显色,测试线颜色较浅;
阴性:只有质控线显色,测试线不显色。
试纸条的制备:
(1)试纸条的基质材料为吸水滤纸,加样区、测试区和质控区为硝酸纤维素膜。
(2)将购置的兔源金标抗FITC抗体0.5g溶于5mL含0.1%BSA(wt)的0.001mol/L磷酸盐缓冲液稀中,得到1:10(mg/mL)比例的释胶体金标记的抗FITC抗体,将上述稀释后的金标抗体液按50uL/cm
(3)将浓度为1mg/mL的亲和素蛋白溶液按1uL/cm的速度喷于检测层上作为检测区,将包被浓度为0.5mg/mL的鼠抗兔IgG的二抗按1uL/cm的速度喷于质控区的检测层上作为质控线,37℃下干燥30min,从而制备得到检测区和质控区。
上述实施方式仅为本发明的优选实施方式,不能以此来限定本发明保护的范围,本领域的技术人员在本发明的基础上所做的任何非实质性的变化及替换均属于本发明所要求保护的范围。
- 一种快速检测鲤春病毒血症病毒的RPA-LFD引物、方法和试剂盒
- 一种快速检测鲤春病毒血症病毒的RPA-LFD引物、方法和试剂盒
